二苯胺与邻氨基酚共聚的原位紫外-可见光谱电化学研究
袁文娟,张 雷
(上海师范大学 生命与环境科学学院 化学系,上海 200234)
聚苯胺(PAN)由于具有许多独特的物理学、化学、电学及光学性质而成为多年来的研究热点,其广泛应用于充电电池的电池材料[1]和化学及电化学传感器的制备[2]。与苯胺相比,苯胺的衍生物以其能提供更多的修饰基团而引起了人们广泛的兴趣。二苯胺(DPA)是一种N-取代苯胺衍生物,其聚合物是一种介于PAN和聚对苯的聚合物。Athawale等[3]在乙腈中运用恒电流法氧化DPA制备了聚二苯胺(PDPA),并用紫外-可见光谱法研究其相关性质。与PAN相比,PDPA不仅具有更好的溶解性,而且其电化学稳定性也得到了提高。邻氨基酚(OAP)是苯胺的另一衍生物,由于其分子结构中具有含氧的羟基官能团,对开发新型的电聚合材料有着特殊意义[4]。因此,聚邻氨基酚(POAP)的制备与结构[5]、电化学性质[6]及其在传感器中的应用[7]等方面已引起人们的关注。
光谱电化学是通过结合光谱技术和电化学方法,在一个电解池内进行同步测量而同时获得多种信息,为研究电极过程机理及电极表面特性提供分子水平信息的技术。紫外-可见光谱电化学技术在鉴别反应产物,特别是反应的瞬间态和中间体方面具有独到的优越性。因此,该方法已成为检测苯胺及其衍生物聚合过程中生成的中间体、研究聚合机理及电极上聚合物膜电化学性质的强有力手段[8]。Zhang等[9]采用原位紫外-可见光谱法对甲苯胺和邻苯二胺的共聚过程进行了研究。结果表明,在电化学氧化过程中生成了胺阳离子中间体。Wen等[10]采用原位光谱电化学技术研究了DPA和4-磺酸基二苯胺的共聚过程,并检测到在共聚过程中生成的头-尾相接的二聚物中间体。Shah等[11]对苯胺和OAP的共聚进行了光谱研究,也证实了在共聚过程中有中间体产生,同时还研究了共聚物的组成与溶液中苯胺和OAP浓度的关系。这些研究表明,在苯胺及其衍生物聚合的初始阶段,首先生成苯胺及其衍生物的自由基中间体,之后,这些中间体与溶液中的苯胺及其衍生物单体和/或中间体进一步发生反应,生成稳定的聚合物。
本实验以氧化铟锡(ITO)导电玻璃作为工作电极,采用原位紫外-可见光谱法对DPA、OAP及不同浓度比DPA和OAP的混合液在恒电位氧化过程中阳离子自由基的产生、二聚体的生成进行了研究,讨论了DPA和OAP的共聚机理,并从光谱学的角度研究了溶液中DPA和OAP的浓度对共聚过程的影响。
1 实验部分
1.1 仪器与试剂
CHI 660B电化学工作站(上海辰华公司);三电极体系:工作电极为ITO玻璃电极(表面电阻为10 Ω/cm2),参比电极为Ag/AgCl电极,盘状铂丝为对电极;UV-1800紫外-可见分光光度计(日本岛津公司)。
DPA(纯度99.5%,北京化学试剂有限公司);OAP(Sigma公司);4 mol/L H2SO4溶液作为支持电解质。所用试剂皆为分析纯,实验用水为18 MΩ超纯水。
1.2 实验方法
以石英比色皿为光谱电化学池,ITO导电玻璃为工作电极(垂直于光路放置在比色皿中),盘状铂丝为对电极,Ag/AgCl为参比电极,在0.8 V电位下分别聚合DPA、OAP和不同浓度比的DPA与OAP混合液。同时在波长300~800 nm范围内检测在电化学聚合过程中吸光度随时间的变化情况。每次实验前,ITO玻璃电极均依次用丙酮和超纯水冲洗干净。
2 结果与讨论
2.1 电化学自聚与共聚
为了研究DPA和OAP的电化学自聚和共聚行为,用循环伏安法(CV)以100 mV/s的扫速在4 mol/L H2SO4溶液中于-0.2~1.2 V循环扫描20圈,分别记录DPA和OAP单独聚合及浓度比(R)分别为1∶2、1∶1和2∶1的DPA和OAP混合液共聚过程的CV图,见图1~2。
图1A为0.01 mol/L的OAP在4 mol/L H2SO4溶液中的CV图。由图1A可知,在第1圈扫描时,于0.78 V处出现1个氧化峰。此氧化峰是由OAP上氨基电氧化生成的阳离子自由基(OAPCR)造成的,此OAPCR将作为聚合单体引发OAP的聚合。随着反应的进行,此阳极峰随着扫描圈数的增加峰电流逐渐减弱。这是由于在聚合过程中溶液中的OAPCR发生相互反应或与溶液中的OAP单体反应,从而使OAPCR的量不断减少所致。在随后的扫描中,在0.67 V和0.31 V处出现了另1对氧化还原峰,并随着扫描的继续进行,该氧化还原峰逐渐负移至0.58 V和0.12 V。其中,位于0.67 V和0.31 V的氧化还原峰是由于OAP自由基发生氧化还原反应所致。而位于0.58 V和0.12 V的氧化还原峰可归因于溶液中的OAP二聚物/低聚物继续发生化学反应而生成POAP所致。此外,随着电氧化的继续进行,氧化还原峰电流不断增加,此为电活性聚合物不断生成的典型特征。上述研究说明在OAP的聚合过程中,OAP先被氧化成其阳离子自由基,之后,该自由基之间或与其单体发生化学反应产生OAP二聚物/低聚物,最后OAP二聚物/低聚物继续发生化学反应生成POAP。
图1B是0.02 mol/L的DPA在4 mol/L H2SO4溶液中的CV图。在扫描的第1圈,出现1个位于0.76 V处的氧化峰和位于0.53 V的还原峰。此处的氧化峰是由于DPA的电氧化而产生的DPA阳离子自由基(DPACR)所致,而还原峰是由于DPACR之间或与溶液中的DPA单体发生化学反应生成的聚合物的还原反应所致。在随后的连续扫描中,该对氧化还原峰消失,同时有另外两对新的氧化还原峰出现,峰电位分别为0.70/0.62 V和0.60/0.48 V。说明溶液中生成的DPACR很快发生化学反应被转换成聚合物。这两对氧化还原峰的电流响应值随着扫描的继续进行而不断增加,充分说明电极表面不仅有电活性物质生成,而且其在电极表面的量逐渐增加。这是电活性物质在电极表面发生聚合反应的典型特征。

图1 0.01 mol/L OAP(A)与0.02 mol/L DPA(B)电聚合的循环伏安图Fig.1 CVs of 0.01 mol/L OAP(A)and 0.02 mol/L DPA(B)in 4 mol/L H2SO4at 100 mV/s
图2A、B、C分别为不同浓度比(R)的DPA和OAP混合液在4 mol/L H2SO4中的CV图。对比图1和图2,可以发现DPA和OAP混合液的电化学行为和DPA及OAP单独聚合过程的电化学行为有明显的不同,这说明DPA和OAP确实发生了电化学共聚而生成了新的具有电化学活性的聚合物。对比图2A~C,可以看出不同浓度比的DPA和OAP混合液共聚的电化学行为有明显差异。图2B是浓度比为1∶1的DPA和OAP混合液进行共聚的CV图。由图可知,在电位扫描的第1圈,于0.79 V处出现1个阳极峰。这是由于DPA和OAP的氧化而形成了电活性物质,这些电活性物质最终会导致低聚物/聚合物的形成。在随后的扫描中,出现了两个分别位于0.53 V和0.74 V处的氧化峰。这明显不同于DPA和OAP浓度比为1∶2和2∶1的混合溶液共聚的CV图。在DPA和OAP浓度比为1∶2和2∶1的混合溶液共聚的CV图中,共出现3个氧化峰(图2A和C),分别位于0.53、0.76、1.0 V和0.54、0.74、1.0 V处。其中,位于0.74~0.76 V处的氧化峰是由于电活性物质上羟基的氧化产生的[12],而位于1.0 V处的氧化峰是由电活性物质上氨基的氧化产生的。图2中不同的氧化还原性质是由于DPA和OAP的浓度比不同所致,这在后续的光谱研究中也得到了证实。这些电化学性质不仅说明DPA和OAP发生了共聚,而且还表明共聚过程与溶液中DPA和OAP的浓度比有关。

图2 不同浓度比(R)的DPA和OAP共聚的循环伏安图Fig.2 CVs of the electrochemical copolymerization of DPA and OAP with different ratios in 4 mol/L H2SO4at 100 mV/s
2.2 原位紫外-可见光谱电化学研究
2.2.1 OAP的原位光谱电化学 在0.8 V电位下对0.01 mol/L OAP进行电聚合,并记录其紫外-可见吸收光谱(图3)。由图可知,在聚合初始,OAP分别在波长460、615、755 nm处呈现3个吸收峰。其中,位于460 nm处的吸收峰是由于OAP发生电氧化生成的OAPCR的吸收所致[13],并且随着电氧化的继续进行,溶液中OAPCR的浓度也逐渐增加,该峰的吸收强度逐渐增大。位于615 nm的吸收峰对应于OAP上羟基的氧化产生的醌式结构单元的特征吸收峰[13];然而,对于755 nm处的吸收峰目前还没有明确的归属[14]。从第7 min开始,位于460 nm处的吸收峰随着电解时间的增加逐渐发生蓝移,最后移至450 nm处。这是由以下两个原因造成的:①在电氧化过程中,OAPCR之间及其与溶液中的OAP单体之间发生交互反应生成OAP二聚物、三聚物等低聚物中间体,最后生成POAP;②这种蓝移现象也与羟基的空间位阻效应有关,聚合链上羟基的位阻效应可使苯环空间构象发生扭曲,从而使电子跃迁能隙增大,导致吸收峰蓝移。随着POAP链长的逐渐增加,羟基的空间位阻效应增强,其蓝移也逐渐加大。位于615 nm处的吸收峰随着反应的进行逐渐减弱并最后消失,这是由于在电聚合过程中,为数不多的醌式结构单元被氢解,参与聚合而形成OAP双阳离子自由基[15],同时在686 nm处出现了1个新吸收峰,随着反应的进行,溶液中OAP双阳离子自由基的浓度逐渐增加,该峰强度也逐渐增加。

图3 0.01 mol/L OAP在0.8 V恒电位聚合时的紫外-可见吸收光谱Fig.3 UV-Vis spectra of 0.01 mol/L OAP at different time intervals at 0.8 V
为了进一步证实以上结论,在OAP聚合一段时间后切断电压,继续记录其吸收光谱随时间的变化情况。结果表明,切断电压后,位于450 nm处吸收峰的强度随时间的增加逐渐减弱,表明OAPCR的量逐渐减少。这是由于切断电压后,OAP不再生成新的阳离子自由基,而随着溶液中OAPCR与其单体或自由基反应不断生成POAP,溶液中OAPCR的量逐渐减少所致。因此,基于文献[16]及图3中OAP电聚合的光谱特性可知,OAP的电聚合是一个两步反应。首先,OAP经电氧化生成其相应的阳离子自由基,对应于460 nm处的吸收峰;之后,OAP自由基之间及其与溶液中的OAP单体之间发生交互反应生成OAP二聚物、三聚物等低聚物中间体,最后生成稳定的POAP。
2.2.2 DPA的原位光谱电化学 在0.8 V电位下对0.02 mol/L DPA进行电聚合,并记录其紫外-可见吸收光谱(见图4)。由图可知,在DPA聚合初始,其吸收光谱呈现3个分别位于430、490、655 nm处的吸收峰。其中,430 nm处的吸收峰对应于苯胺类聚合物分子中的π-π*电子跃迁[11];490 nm处的吸收峰是由氧化初始阶段生成的DPACR所致[17];而655 nm处的吸收峰对应于氧化过程中生成的低聚物N’,N联苯类二阳离子自由基(DPB2+)[16]。随着电化学氧化的继续进行,位于430 nm处吸收峰的峰位置保持不变,而峰强度逐渐增大,这表示溶液中苯胺类聚合物的量越来越多;位于490 nm处吸收峰的峰位置和峰强度均发生了变化,其中,峰位置由初始的490 nm逐渐红移至500 nm,这是因为在聚合过程中,DPACR之间或与DPA单体之间发生交互反应生成了新物质二苯胺阳离子自由基或/和联苯类低聚物阳离子自由基(DPB+)[18];而峰强度的逐渐增大是由于随着聚合的进行,溶液中低聚物的量增多所致;随着反应的进行,位于655 nm处的吸收峰的峰位置发生红移,峰强度逐渐减弱直至消失。这是因为随着反应的进行,在聚合初始生成的DPB2+进一步聚合生成长链的高聚物,从而使溶液中DPB2+的量逐渐减少所致。
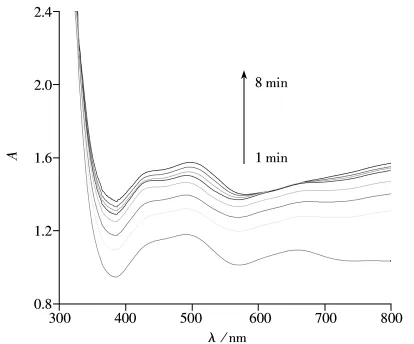
图4 0.02 mol/L的DPA在0.8 V进行恒电位聚合时的吸收光谱Fig.4 UV-Vis spectra of 0.02 mol/L DPA at different time intervals at 0.8 V
为了进一步证实上述中间体的生成,在DPA聚合一段时间后,切断电压并继续记录其吸收光谱。结果发现,切断电压后,位于430 nm和500 nm处吸收峰的强度均随时间的增加逐渐减弱,且位于500 nm处吸收峰的强度快速减弱。这是由于停止电解后,溶液中生成DPACR、DPB+及DPB2+的速度减弱,而溶液中原有的DPACR、DPB+及DPB2+的量随着聚合反应的进一步发生而逐渐减少所致。而430 nm处吸收峰的强度反而比500 nm处吸收峰的强度大,这是由于随着化学聚合反应的进行,溶液中PDPA的量逐渐增加,致使π-π*电子跃迁的强度增大所致。
2.2.3 DPA与OAP共聚的现场光谱电化学 将不同浓度比的DPA和OAP混合液在0.8 V电位下进行共聚合,同时记录其吸收光谱的变化情况。将获得的吸收光谱与DPA或OAP单独聚合时的吸收光谱相比较,结果发现,DPA与OAP共聚的光谱特征发生了很大变化。图5A~C分别为DPA与OAP的浓度比(R)为2∶1、1∶1和1∶2时的混合液在4 mol/L H2SO4中共聚的吸收光谱。由图5A可见,当R=2∶1时,其共聚吸收光谱在430 nm和490 nm处呈现2个吸收峰。由“2.2.2”讨论可知:430 nm处的吸收峰对应于苯胺类聚合物分子中的π-π*电子跃迁,而490 nm处的吸收峰是由在聚合过程中生成的DPACR和/或DPB+所致。另外,图5A还显示,聚合初始时这两个吸收峰的吸收强度随电解的进行快速增加,说明聚合反应进行较快。而在随后的聚合过程中,吸收强度增长较为缓慢,说明聚合反应稳定进行。而当R=1∶1时,其吸收光谱(图5B)与图5A有明显的不同:在聚合初始,其吸收光谱中只有一个波长位于460 nm的吸收峰,由“2.2.1”讨论可知该吸收峰是电氧化过程中生成的OAPCR的吸收。而随着电解的继续进行,又出现两个波长分别位于430 nm和508 nm的新吸收峰。由“2.2.2”讨论可知,430 nm处的吸收峰对应于苯胺类聚合物分子中的π-π*电子跃迁;而位于508 nm处的吸收峰在DPA和OAP单独聚合时获得的吸收光谱中均没有出现。初步推断此吸收峰是由DPA及OAP的阳离子自由基与溶液中的DPA和OAP单体或其自由基发生交互反应产生混合二聚物中间体所致。此外,由图5B还可以看到,随着电解的进行,这两个吸收峰的强度逐渐增加,表明溶液中聚合物的量不断增加。图5C为R=1∶2时的吸收光谱,其与图5B基本相似:在聚合初始,吸收光谱中只有1个位于460 nm处的吸收峰,该吸收峰对应于OAP氧化生成的OAPCR的吸收。随着反应的进行,该吸收峰消失,说明OAPCR进一步发生反应而被消耗。此时,在吸收光谱上又出现2个位于430 nm和508 nm处的新吸收峰。位于430 nm处的吸收峰对应于苯胺类聚合物分子中的π-π*电子跃迁,而位于508 nm处的吸收峰是由DPA及OAP的阳离子自由基与溶液中的DPA和OAP单体或其自由基发生交互反应产生混合二聚物中间体所致。随着反应的进行,这两个吸收峰的强度逐渐增大,说明随着共聚反应不断进行,生成越来越多的聚合物。

图5 不同浓度比的DPA和OAP在0.8 V恒电位共聚时的紫外-可见吸收光谱Fig.5 UV-Vis spectra for the copolymerization of DPA and OAP with different ratios at 0.8 V
对比图5中不同浓度比的DPA和OAP发生共聚时的不同光谱特性,可以发现:当溶液中DPA的浓度较大时(图5A,R=2∶1),光谱中只有对应于苯胺类聚合物分子中π-π*电子跃迁的430 nm处的吸收峰和对应于DPACR的位于490 nm处的吸收峰,而没有对应于OAPCR的位于460 nm处的吸收峰和生成的共聚物位于508 nm处的吸收峰。这是由于当溶液中DPA浓度较大时,DPA的氧化聚合占主导作用,抑制了OAP的氧化,使得OAPCR的量很少,从而使共聚反应难以发生。因此,几乎观察不到460 nm和508 nm处的吸收峰。当溶液中DPA的浓度逐渐减小,OAP浓度逐渐增大时,从图5B、C可以看到在聚合初始出现位于460 nm处的吸收峰,表明生成了OAPCR,并且在此吸收峰很快减弱并消失的同时,出现了2个分别位于430 nm和508 nm的新吸收峰,表明在溶液中发生了共聚反应。反应结束后,在电极上出现墨绿色的沉积物,说明有稳定的聚合物生成。
为了进一步证实上述推断,测定了DPA和OAP(R=1∶2)共聚10 min停止电位扫描后吸收光谱的变化情况。结果表明,位于430 nm和508 nm处吸收峰的吸收强度均随着时间的增加而逐渐减弱。这是因为在停止电位扫描后,生成OAPCR及DPACR的速度逐渐减弱,而与此同时,各种中间体继续发生聚合反应,使其浓度逐渐减小,从而导致其吸收强度也逐渐减小。
综上所述,在DPA和OAP的共聚过程中,DPA和OAP首先被氧化产生其阳离子自由基,然后,DPA与OAP的阳离子自由基与溶液中的DPA和OAP单体或其自由基发生交互反应产生混合二聚物中间体,在吸收光谱中对应于508 nm处的吸收峰。混合低聚物中间体继续发生反应,最终得到稳定的聚合物。另外,当混合液中DPA浓度较大时(图5A),DPA的氧化聚合占主导作用,抑制了OAP的氧化,从而阻碍了共聚反应的发生;当混合液中OAP的量逐渐增大时(图5B、C),DPA的抑制作用减弱,OAP的氧化明显,从而有共聚物生成。其共聚机制见图6。
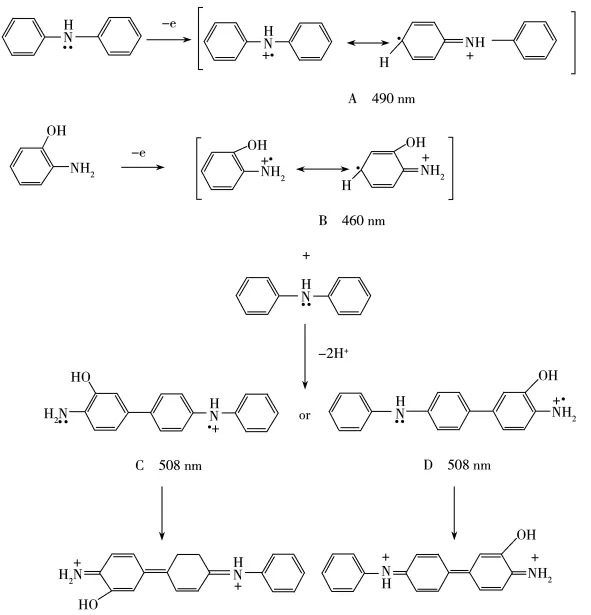
图6 DPA和OAP的共聚机制Fig.6 Copolymerization mechanism of DPA and OAP
3 结论
采用循环伏安法和原位紫外-可见吸收光谱法研究了DPA和OAP的单独聚合及共聚过程,初步探讨了两者的共聚机制。结果表明,在其共聚过程中,DPA和OAP首先被氧化产生各自的阳离子自由基,然后DPA和OAP的阳离子自由基与溶液中的DPA和OAP单体或与其自身发生交互反应,产生混合二聚物中间体,此混合二聚物中间体继续发生化学反应生成共聚物。另外,当混合液中DPA浓度较大时,DPA的氧化聚合占主导地位,对OAP的电氧化有抑制作用,使得共聚速度较慢。因此,从光谱学的角度说明,DPA与OAP的共聚过程与其浓度比有关,即共聚物的性质受溶液中DPA和OAP浓度的影响。
[1]Mu S L,Ye J H,Wang Y H.J.Power Sources,1993,45(2):153 -159.
[2]Bartett P N,Wallace E N K.Phys.Chem.Chem.Phys.,2001,3:1491-1496.
[3]Athawale A A,Deore B A,Chabukswar V V.Mater.Chem.Phys.,1999,58(1):94-100.
[4]Yamada K,Teshima K,Kobayashi N,Hirohashi R.J.Electroanal.Chem.,1995,394(1):71-79.
[5]Yong Y,Lin Z.Synth.Met.,1996,78(2):111-115.
[6]Tucceri R I.J.Electroanal.Chem.,2001,505(1):72 -84.
[7]Pang D W,Chen J H,Nie L H,Tao W Y,Yao S Z.Anal.Biochem.,2004,324(1):115-122.
[8]Lang Q H,Zhang L.J.Instrum.Anal.(郎秋华,张雷.分析测试学报),2010,29(8):761-766.
[9]Zhang G,Zhang A,Liu X,Zhao S,Zhang J,Lu J.J.Appl.Polym.Sci.,2010,115(5):2635 -2647.
[10]Wen T,Sivakumar C,Gopalan A.Spectrochim.Acta Part A,2002,58(1):167-177.
[11]Shah A A,Holze R.Electrochim.Acta,2006,52(3):1374-1382.
[12]Mu S L.Synth.Met.,2004,143(3):259-268.
[13]Zhang A,Cui C,Chen Y,Lee J Y.J.Electroanal.Chem.,1994,373(1/2):115-121.
[14]Shah A A,Holze R.Synth.Met.,2006,156(7/8):566-575.
[15]Bonello J M,Lambert R M.Surf.Sci.,2002,498(3):212-228.
[16]Chung C Y,Wen T C,Gopalan A.Electrochim.Acta,2001,47(3):423 -431.
[17]Thanneermalai M,Jeyaraman T,Sivakumar C,Gopalan A,Vasudevan T,Wen T C.Spectrochim.Acta Part A,2003,59(9):1937-1950.
[18]Ma X D,Qian X F,Yin J,Xi H A,Zhu Z K.J.Colloid Interface Sci.,2002,252(1):77-81.

