超高压液相色谱荧光检测法快速测定水中痕量苯胺与联苯胺
王 超,吕怡兵,滕恩江,加那尔别克·西里甫汗,许人骥
(1.中国环境监测总站,北京 100012;2.新疆环境监测总站,新疆自治区 乌鲁木齐 830011)
苯胺和联苯胺是化工、印染和制药等工业生产的重要原料,释放到环境中会通过皮肤、呼吸道和消化道进入人体,严重威胁人类健康。苯胺可造成急/慢性中毒,引起高铁血红蛋白症、神经衰弱、轻度贫血等;联苯胺可引起接触性皮炎、出血性膀胱炎和膀胱癌,被国际癌症研究机构(IARC)认定为1类致癌物质(对人类致癌性证据充分)[1-2]。因此,美国、日本等国将其列入主要监测项目或优先监测的污染物黑名单[3]。我国将苯胺和联苯胺列为环境重点污染物,并在《地表水环境质量标准》(GB 3838-2002)中规定苯胺和联苯胺的标准限值分别为100 μg/L和0.2 μg/L。因此开发一种高灵敏并且简单实用的方法,对于控制水体中苯胺和联苯胺的污染,保证人类用水安全,具有重要意义。
目前已开发基于不同检测原理的方法主要有萘乙二胺偶氮光度法(NEAP)[4]、液相色谱紫外吸收法(HPLC/UV)[5-6]、液相色谱电化学检测法(HPLC - EC)[7]、气相色谱质谱法(GC - MS)[8]、超临界流体色谱法[9]、电极法[10]、电化学发光猝灭法(ECIQ)[11]、直接电化学法[12]、毛细管电泳法(CE)[13]、共振光散射法(RLS)[14]、表面增强拉曼散射法(SERS)[15]。有文献报道[16-17]可采用液相色谱荧光检测法直接测定水中的苯胺,但分析时间较长且灵敏度不高。对于比苯胺的地表水环境质量规定浓度低500倍的痕量联苯胺,现有成熟的方法均需经过复杂的富集浓缩过程,才能满足水质监测需求。超高压液相色谱由于采用亚2 μm粒径填料的色谱柱,可得到比常规HPLC更快的分离速度和更高的灵敏度[18],近年来在环境监测、食品药品分析等领域得到越来越广泛的应用[19-20]。目前未见关于超高压液相色谱荧光检测法直接测定水中苯胺和联苯胺的报道。
本研究建立的直接进样/超高压液相色谱荧光检测法,具有操作方便、快速准确和灵敏度较高的优点,适用于水中痕量苯胺和联苯胺的快速测定。
1 实验部分
1.1 仪器、试剂与材料
UPLC H-class超高压液相色谱仪(美国Waters公司),S220pH仪(上海梅特勒-托利多公司),U-10电导率仪(日本Horiba公司)。苯胺(5.0 g/L,溶于甲醇)、联苯胺(2.0 g/L,溶于二氯甲烷)均为美国AccuStandard公司产品;乙腈(色谱级,美国Tedia公司),甲醇(色谱级,美国Kanglin公司),醋酸铵(纯度>97.0%,美国Alfa Aesar公司),实验用水均为二次去离子水。针式过滤器(0.22 μm,13 mm内径,材质分别为聚醚砜(PES)、尼龙(PA)和聚四氟乙烯(PTFE),上海安谱公司),针式过滤器(0.2 μm,13 mm内径,材质为聚丙烯(GHP),美国Waters公司)。
1.2 实验步骤
取1 mL水样,经针式过滤器过滤,收集到样品瓶中,待液相色谱分析。水样的pH值和电导率分别采用“1.1”所列pH仪和电导率仪测定。
1.3 实验条件
针式过滤器为聚四氟乙烯材质;色谱柱为ACQUITY UPLC BEH C18(2.1 mm×50 mm,1.7 μm);流动相为乙腈-3.85 g/L醋酸铵(25∶75);流速0.7 mL/min,进样量10 μL,柱温40℃;荧光检测器的激发和发射波长:苯胺为λex/λem=232 nm/329 nm,联苯胺为λex/λem=292 nm/383 nm。
2 结果与讨论
2.1 荧光检测条件的选择
采用液相色谱荧光检测器的光谱扫描技术,分别对苯胺和联苯胺标准溶液的激发光谱和发射光谱进行扫描。通过对光谱图进行分析,得到苯胺的发射波长为329 nm,激发波长在232 nm和292 nm各有1峰,其中232 nm处的激发能量最大;联苯胺的发射波长为383 nm,激发波长仅在292 nm有1峰。最终确定苯胺和联苯胺的激发/发射波长分别为232 nm/329 nm和292 nm/383 nm。
2.2 流动相条件的选择
分别选择甲醇-水、乙腈-水和乙腈-醋酸铵体系作为流动相,考察不同浓度有机相条件下,苯胺和联苯胺的分离效果。为减少苯胺和联苯胺的分析时间,结合仪器的最高耐压限制,选择流速为0.7 mL/min。对于乙腈-水和甲醇-水的流动相体系,确定最佳的流动相比例分别为25%乙腈和30%甲醇。图1比较了30%甲醇-70%水、25%乙腈-75%水和25%乙腈-75%醋酸铵的流动相条件下,苯胺和联苯胺的分离情况。结果显示,3种流动相条件下,苯胺和联苯胺均在1 min内达到基线分离;后两种乙腈流动相体系下,分析时间可缩短为0.8 min。对于联苯胺,有机相为乙腈的两种体系下,信号响应明显高于甲醇体系;对于苯胺,信号响应则略有提高。比较两种乙腈体系,对于联苯胺,25%乙腈-75%醋酸铵体系下的信号略高于25%乙腈-75%水体系,而对于苯胺,两种体系相差无几。
综上,乙腈作为流动相可以缩短分析时间,并且显著提高苯胺和联苯胺的荧光信号,因此本研究优先选择乙腈作为流动相中的有机相。由于采用直接进样法,未进行样品前处理,且苯胺和联苯胺是弱碱性物质,水样的pH值、电导率等因素很可能会影响苯胺和联苯胺荧光信号,所以需对两种乙腈流动相体系(25%乙腈-75%水和25%乙腈-75%醋酸铵)做进一步研究。
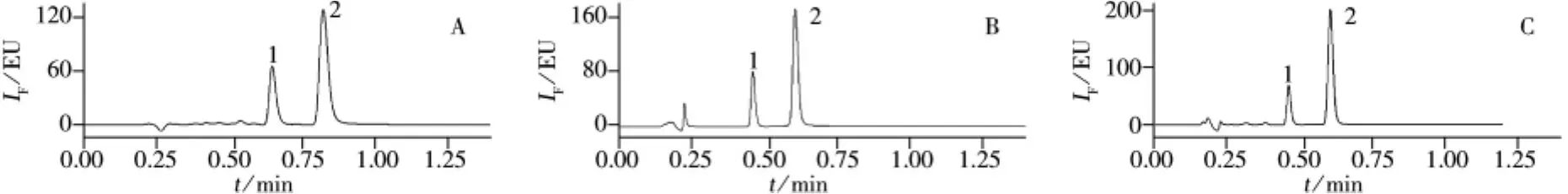
图1 不同流动相条件下苯胺和联苯胺的色谱图Fig.1 Chromatograms of aniline and benzidine obtained by using different mobile phases
2.3 水样pH值的影响
为了考察水样pH值对分析结果的影响,采用自来水(未检出苯胺和联苯胺)配制了质量浓度均为50 μg/L的水样。考察了25%乙腈-75%水(A)和25%乙腈-75%醋酸铵(B)的流动相体系下,不同水样pH值对苯胺和联苯胺回收率的影响(见图2)。从图2A可见,对于25%乙腈-75%水流动相体系,苯胺在pH 3.9~11.9的回收率为95%~104%;联苯胺在pH 3.9~10.0时的回收率为92%~100%,但在pH 11.1和pH 11.9时,其回收率分别达到144%和169%。从图2B可以得出,对于25%乙腈-75%醋酸铵流动相体系,在pH 3.9~11.9范围内,苯胺和联苯胺的回收率较高且稳定,分别在95%~103%和94%~100%之间。
由于苯胺和联苯胺的pKa值分别约为4.6[21]和4.3[22],在不同pH值的水溶液中,两种物质可分别以两种状态存在:分子状态和带正电荷的离子状态。对于苯胺,不同pH值的水样中,两种状态的荧光信号几乎无差别。而对于联苯胺,当水样pH值增加到一定数值后,相应的荧光信号不稳定,导致分析结果不稳定。通过在流动相中加入醋酸铵缓冲液,使联苯胺主要以离子状态稳定存在,克服由于水样pH值变化而引起荧光信号变化的问题,增强其荧光信号的稳定性,提高分析测试的可靠性和准确性。图2显示25%乙腈-75%醋酸铵的流动相具有良好的缓冲能力,对于一般的环境样品前处理,可不调pH值,以避免对苯胺和联苯胺的浓度产生影响,保证分析的准确度和重现性。
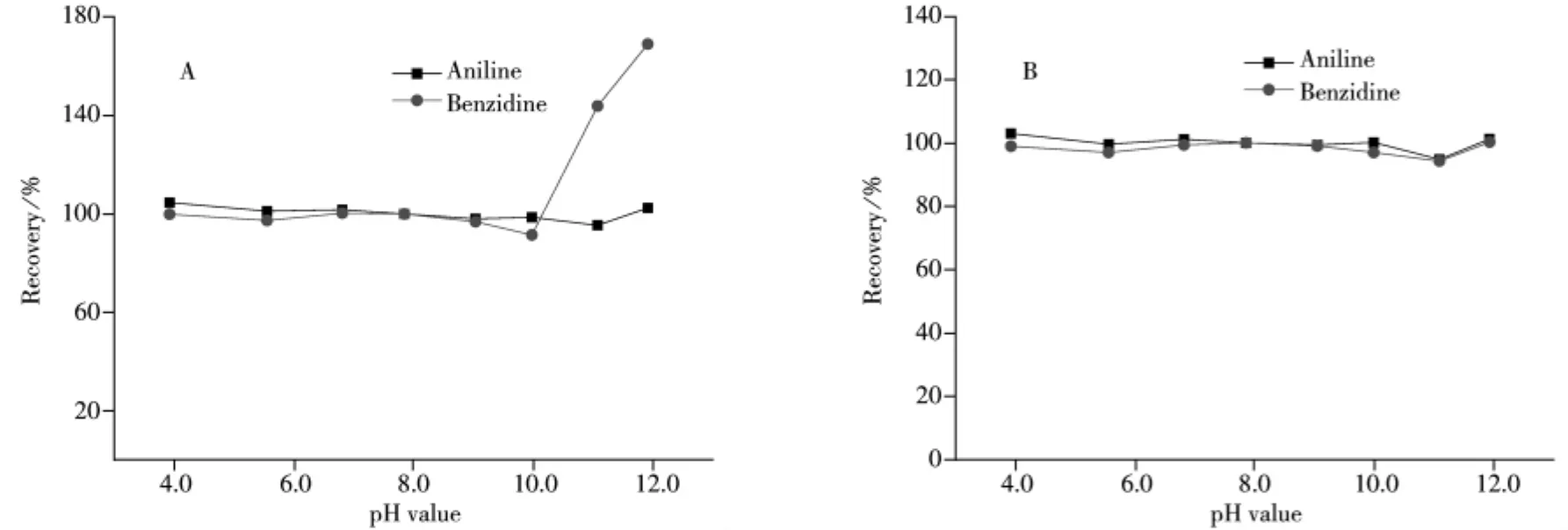
图2 不同pH值对苯胺和联苯胺回收率的影响Fig.2 Effect of different pH values on recoveries of aniline and benzidine mobile phase:A.25%acetonitrile -75%H2O,B.25%acetonitrile-75%ammonium acetate
2.4 水样电导率的影响
为了考察水样电导率对分析结果的影响,采用不同稀释倍数的自来水,配制了电导率不同但质量浓度均为100 μg/L的水样。25%乙腈-75%水(A)和25%乙腈-75%醋酸铵(B)的流动相体系下,水样不同电导率对苯胺和联苯胺回收率的影响见图3。从图3A可以得出,对于25%乙腈-75%水的流动相体系,在不同电导率条件下,苯胺具有良好的回收率(95%~103%);而对于联苯胺,随着电导率的增加,其回收率逐渐增加,电导率为0.315 mS/cm后,回收率稳定在97%~101%之间。从图3B可以得出,对于25%乙腈-75%醋酸铵的流动相体系,在不同电导率条件下,苯胺和联苯胺均具有良好的回收率,分别在100%~104%和99%~102%之间。这说明25%乙腈-75%醋酸铵具有较宽的电导率耐受范围,对于一般的环境样品前处理,水样的电导率对分析结果几乎无影响。因此,实验最终选用25%乙腈-75%醋酸铵为最佳流动相。
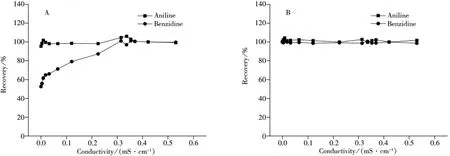
图3 不同电导率值对苯胺和联苯胺回收率的影响Fig.3 Effect of different conductivity values on recoveries of aniline and benzidine mobile phase:A.25%acetonitrile-75%H2O,B.25%acetonitrile-75%ammonium acetate
2.5 前处理方法的选择
用自来水和一定体积甲醇或乙腈配制100 μg/L的苯胺和联苯胺混合溶液,考察不同前处理方法的回收率。比较了4种膜材质(PES、PA、PTFE和GHP膜)针式过滤器过滤、5种溶剂(水、10%乙腈、20%乙腈、10%甲醇和20%甲醇)的效果,结果如图4所示。图4A显示,对于苯胺,3种膜材质(PA、PTFE和GHP膜)过滤器在5种溶剂下的回收率均较高,在90%~104%之间,能满足分析要求;而PES滤膜在含有机相的溶剂下的回收率异常升高,可能是由于溶剂中的有机成分(乙腈或甲醇)将PES膜上的一些组成物质溶解,该类物质对苯胺的荧光信号具有显著增强效应。图4B显示,对于联苯胺,2种膜材质(PA和PTFE膜)过滤器在5种溶剂下的回收率较高,在101%~116%之间,能满足分析要求;其余2种膜材质(PES和GHP膜)在5种溶剂下的回收率偏低,可能是由于膜上的吸附作用降低了联苯胺的回收率。另外,实验中发现PA膜过滤器有时会析出荧光杂质,对分析结果存在一定干扰。综合考虑,选择不向水样中加入任何有机溶剂,采用PTFE膜过滤器直接进行水样过滤。
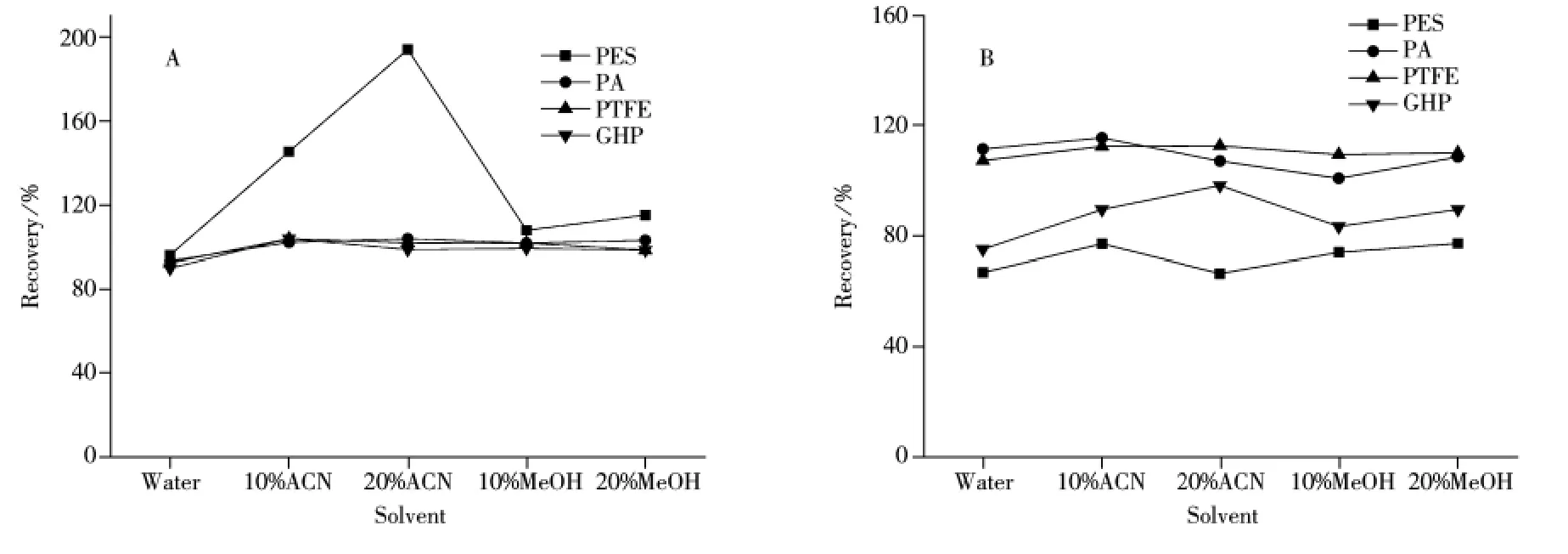
图4 采用4种膜材质过滤器和5种溶剂进行前处理时苯胺(A)和联苯胺(B)(浓度均为100 μg/L)的回收率Fig.4 Recoveries of added 100 μg/L aniline(A)and 100 μg/L benzidine(B)with four types of filters and five kinds of solvents in the pretreatment
2.6 标准曲线、灵敏度及精密度
以自来水(未检出苯胺和联苯胺)配制6个不同质量浓度(1.0、5.0、10.0、25.0、50.0、100.0 μg/L)的苯胺和联苯胺混合标准溶液,将荧光信号(峰面积)和质量浓度进行线性回归分析,得到标准曲线和线性系数(见表1)。结果表明,苯胺和联苯胺在1.0~100.0 μg/L质量浓度范围内线性关系良好,线性系数(r)达到0.999以上。对10.0 μg/L的混合标准溶液,在相同条件下连续分析10次,苯胺和联苯胺峰面积的RSD分别为0.4%和0.5%,满足仪器精密度要求。
配制0.2 μg/L的混合标准溶液,按照本方法进行前处理和分析,分别以3倍和10倍信噪比(S/N)计算方法的检出限和定量下限。由表1可见,苯胺和联苯胺的检出限分别为0.023、0.024 μg/L,定量下限分别为0.078、0.079 μg/L,均低于GB 3838-2002规定的控制标准值,因此本方法可满足水质监测的分析要求。

表1 苯胺和联苯胺的标准曲线、线性系数、线性范围、检出限及定量下限Table 1 Standard curves,correlation coefficients(r),linear ranges,detection limits and quantitative limits of aniline and benzidine
2.7 方法的加标回收率
采用某饮用水水源地(未检出苯胺和联苯胺)的水样分别配制不同浓度的苯胺和联苯胺溶液,考察实际水样中方法的加标回收率。苯胺和联苯胺的加标浓度、实测值和回收率如表2所示。由表2可见,4种加标浓度下,苯胺和联苯胺的回收率在86%~106%之间,说明方法有较好的回收率,可满足分析检测的要求。

表2 水样中苯胺和联苯胺的分析结果和回收率Table 2 Analysis results and recovery rate of aniline and benzidine in water
2.8 方法的优越性与局限性
本方法无需繁琐的前处理过程,即取得较高的灵敏度,而且分析时间仅为0.8 min,可显著提高工作效率。与其他方法比较(如表3所示),本方法具有较明显的优势,如:NEAP法只能测定苯胺类化合物的总量,不能对单个苯胺类化合物进行定性和定量分析;HPLC/UV、HPLC/EC、GC-MS和SFC-UV方法由于仪器灵敏度较低,均需对水样进行繁琐的富集浓缩过程。ECIQ法可直接检测水样,但其对联苯胺的检测灵敏度不能满足水质分析要求。电极法、EC、CE、RLS和SERS可直接分析水中的苯胺或联苯胺,且灵敏度较高,但由于对应的仪器方法并不常见,在水质分析部门的普及率较低,不利于方法推广与使用。与常规HPLC/FD相比,本方法扩展至联苯胺的分析,显著提高了灵敏度,而且流速低,可减少流动相的消耗。本方法的局限性在于:虽然苯胺类物质荧光信号的选择性和超高压液相色谱的强大分离能力,在较大程度上可将分析物和杂质分离,但仅靠保留时间定性,仍可能出现假阳性结果,此时需要采用不同色谱柱进一步加以确认。

表3 水中苯胺和联苯胺的分析方法比较Table 3 Comparison of various analysis methods of aniline and benzidine in water
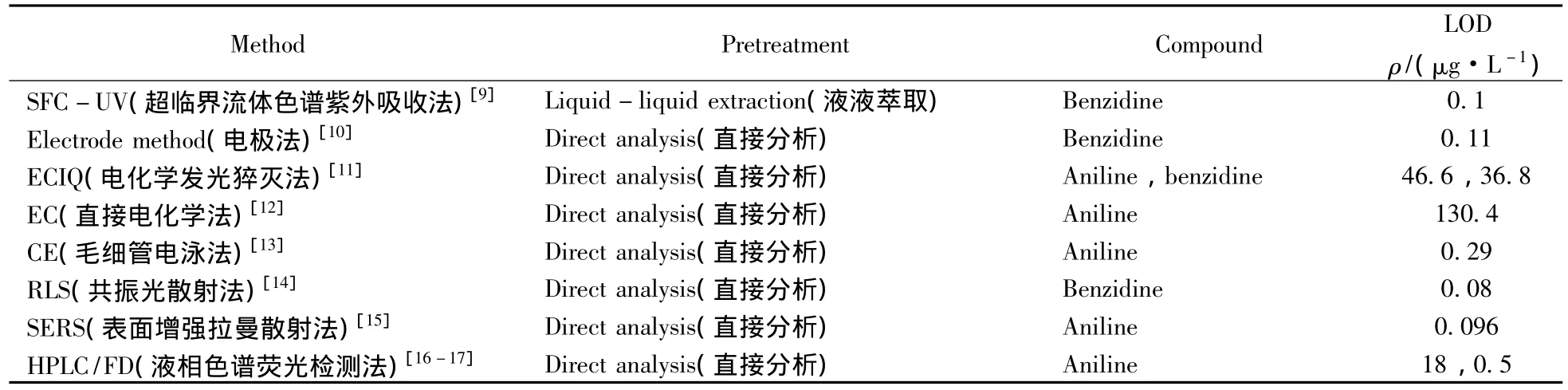
(续表3)
2.9 实际水样分析
采集某饮用水水源地、引水渠、淡水湖和咸水湖的水样,4个水样的pH值在7.7~8.9之间,除咸水湖水样的电导率较高(达18.1 mS/cm)外,其余水样的电导在0.324~0.477 mS/cm之间。按照本方法对4个水样进行分析,同时加入低浓度混合标准溶液(2.0 μg/L)进行加标分析。结果显示,4种不同类型水样中均未检出苯胺和联苯胺,对应的低浓度加标回收率较高,分别为苯胺88%~107%,联苯胺:90%~99%(见表4)。结果表明,本方法适用于多种类型地表水体中苯胺和联苯胺的快速检测。
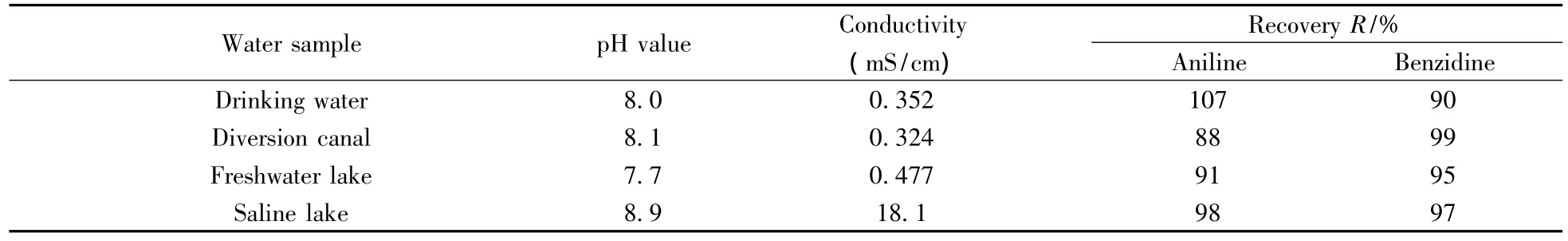
表4 4种水样的pH值、电导率以及在加标浓度为2.0 μg/L下苯胺和联苯胺的回收率Table 4 pH values,conductivity values and recoveries(spiked 2.0 μg/L)of aniline and benzidine in four kinds of water samples
3 结论
采用直接进样/超高压液相色谱荧光检测法,成功地进行了多种类型地表水体中苯胺和联苯胺的快速分析。该方法与已报道的方法相比,无需繁琐的前处理浓缩过程,具有操作简单、方法检出限低、分析速度快等优点,满足水质监测的需求。有望用于分析其他具有荧光信号的芳香胺类物质。
[1]Zhang Y D,Gao Y Z,Fu M Y.The Control of Aminobenzene and Nitrobenzene Intoxication.Beijing:Chemical Industry Press(张印德,高玉之,傅鸣远.苯的胺基、硝基化合物中毒的防治.北京:化学工业出版社),1982:46-64.
[2]Lakshmi V M,Hsu F F,Zenser T V.Chem.Res.Toxicol.,2003,16(3):367 -374.
[3]Zhou W M,Kou H R,Wang X J.Priority Pollutant.Beijing:China Environmental Science Press(周文敏,寇洪如,王湘君.环境优先污染物.北京:中国环境科学出版社),1989:114.
[4]Environmental Protection Bureau of China.Standard Methods for Examination of Water and Wastewater.4th ed.Beijing:China Environmental Science Press(国家环境保护总局《水和废水监测分析方法》编委会.水和废水监测分析方法.4版.北京:中国环境科学出版社),2002:515-517.
[5]Zhao S L,Wei F S,Zou H F,Xu X B.Chin.J.Chromatogr.(赵淑莉,魏复盛,邹汉法,徐晓白.色谱),1997,15(6):508-511.
[6]Bouzige M,Legeay P,Pichon V,Hennion M C.J.Chromatogr.A,1999,846(1/2):317-329.
[7]Vera-Avila L E,Garcia-Ac A,Covarrubias-Herrera R.J.Chromatogr.Sci.,2001,39(7):301-307.
[8]Shin H S,An H S.Chromatographia,2006,63(1/2):77 -84.
[9]Patel G,Agrawal Y K.J.Chromatogr.B,2003,795(2):157-165.
[10]Falciola L,Pifferi V,Mascheroni E.Electroanalysis,2012,24(4):767-775.
[11]Yi C Q,Li M J,Tao Y,Chen X.Chin.J.Anal.Chem.(易长青,李梅金,陶颖,陈曦.分析化学),2004,32(11):1421-1425.
[12]Seymour E H,Lawrence N S,Beckett E L,Davis J,Compton R G.Talanta,2002,57(2):233-242.
[13]Liu S H,Wang W J,Chen J,Sun J Z.Int.J.Mol.Sci.,2012,13(6):6863 -6872.
[14]Chen Z G,Zhang G M,Chen X,Peng Y R,Lin Y J,Lu S M.Anal.Methods,2011,3(8):1845-1850.
[15]Li D,Li D W,Fossey J S,Long Y T.Anal.Chem.,2010,82(22):9299-9305.
[16]Xue K S,Dong F X.Chin.J.Anal.Lab.(薛科社,董发昕.分析试验室),2004,23(8):36-38.
[17]Liu P,Zhang L Y,Jiao Y L,Liu N,Liu Y Y,Gao S.Chin.J.Anal.Chem.(刘鹏,张兰英,焦雁林,刘娜,刘莹莹,高松.分析化学),2009,37(5):741-744.
[18]Li D X,Tang T,Wang F Y,Li T,Zhang W B.Chin.J.Chromatogr.(李笃信,唐涛,王风云,李彤,张维冰.色谱),2008,26(1):105-109.
[19]Luo Y.Analysis Methods for Environmental Monitoring of Surface Water.Beijing:China Environmental Science Press(罗毅.地表水环境质量监测实用分析方法.北京:中国环境科学出版社),2009.
[20]Zhao J,Xue X F.Application of Ultra Performance Liquid Chromatography on the Analysis of Food and Drug.Beijing:China Light Industry Press(赵静,薛晓锋.超高效液相色谱技术在食品与药品分析中的应用.北京:中国轻工业出版社),2012.
[21]Brown H C.Determination of Organic Structures by Physical Methods.New York:Academic Press,1955.
[22]Benzidine - Chemical and Physical Information,Agency for Toxic Substances and Disease Registry.http://www.atsdr.cdc.gov/toxprofiles/tp62-c4.pdf.

