162例药品不良反应报告分析
李家田(江苏省丰县中医医院,江苏徐州 221700)
药品不良反应(ADR)监测工作的开展,可以加强药品管理,保障用药安全,有效减少药源性损害的发生;又可以促进临床安全、有效用药,提高临床用药水平。现对我院2011—2012年上报的162例ADR报告进行分析,探索我院ADR发生规律和特点,为临床合理用药提供参考。
1 资料与方法
资料来源于我院2011—2012年上报的有效ADR报表162份,按ADR级别、患者性别与年龄、使用药品、给药途径、引发ADR的药物种类及发生率、临床表现等项目进行统计、分析。
2 结果
2.1 ADR的级别
严格按照《药品不良反应报告和监测管理办法》附则中规定的新的ADR和严重的ADR的定义进行分级。162例ADR中,一般的ADR为146例,占90.12%;新的/严重的ADR为16例,占9.88%。
2.2 发生ADR患者的性别与年龄分布
162例ADR报告中,男性77例,女性85例;患者年龄最小1.5岁,最大95岁,见表1。
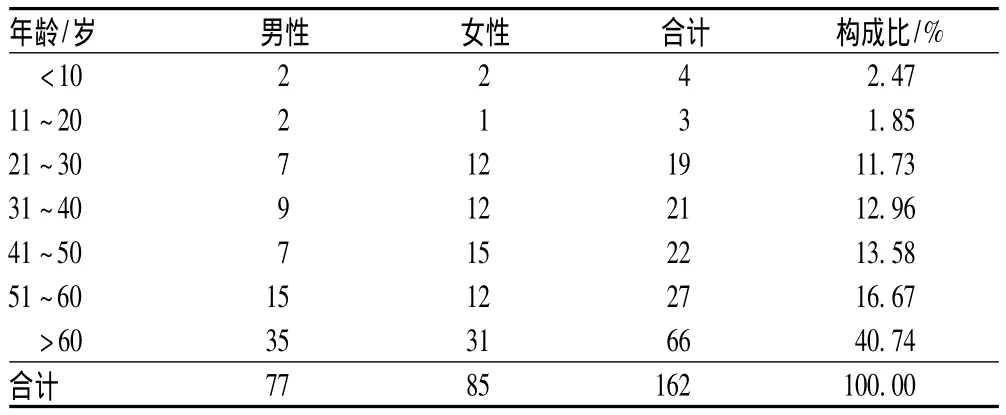
表1 发生ADR患者的性别与年龄分布(例)Tab 1 Distribution of age and sex of patients with ADR(cases)
2.3 引发ADR的给药途径分布
静脉给药致ADR居第1位,其次为口服给药,见表2。

表2 引发ADR的给药途径分布Tab 2 Distribution of route of administration of drugs that induced ADR
2.4 引发ADR的药物种类及构成比
按照《新编药物学》(17版)进行分类,我院2011—2012年上报的162份ADR报告共涉及药品12类73种,其中抗感染药最多,其次为中药制剂,见表3。
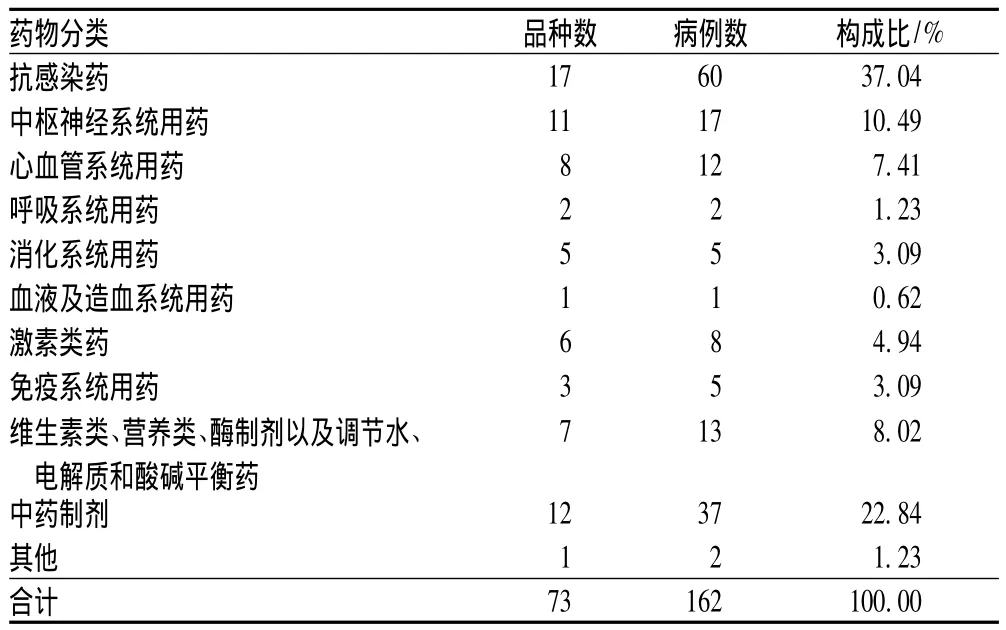
表3 引发ADR的药物种类及构成比Tab 3 Types of ADR-involved drugs and constituent ratio
2.5 引发ADR的抗感染药类别及构成比
162例ADR中,60例由17种抗感染药引起,在整个ADR中占比最多,为37.04%,而β-内酰胺类引起的ADR占抗感染药ADR的比例最大,见表4。
2.6 引发ADR的中药制剂及构成比
中药制剂引起的ADR为37例,占22.84%,其中中药注射剂占比最大,见表5。
2.7 ADR累及器官和(或)系统及临床表现
参照《WHO药品不良反应术语集》对ADR累及的器官和(或)系统进行分类,我院ADR以消化系统损害最多,其次是皮肤及其附件损害和心血管系统损害,见表6(由于部分ADR累及多个器官和(或)系统,故总的例次数>162例)。
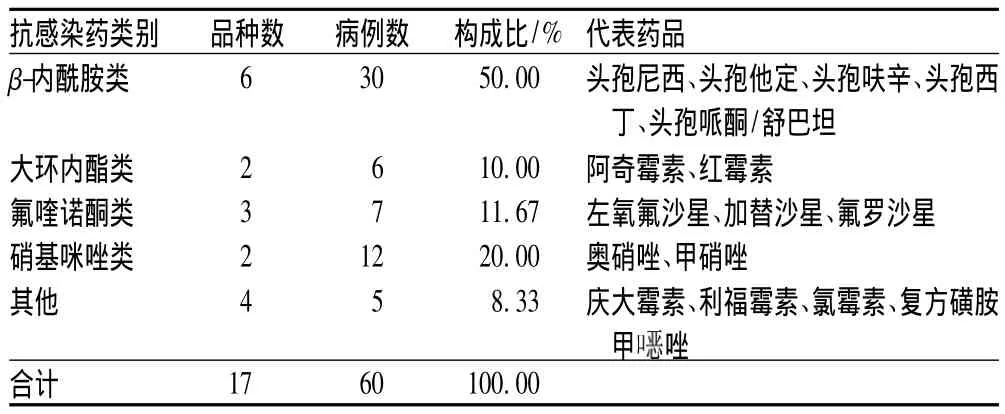
表4 引起ADR的抗感染药种类及构成比Tab 4 Types of ADR-involved anti-infective drugs and constituent ratio

表5 引起ADR的中药制剂及构成比Tab 5 Types of ADR-involved traditional Chinese medicine preparations and constituent ratio

表6 ADR累及器官和(或)系统及主要临床表现Tab 6 ADR-involved organs and(or)systems and chief clinical manifestations
2.8 ADR的转归
162例ADR在停用可疑药品或停用可疑药品并对症治疗后,治愈91例,占56.17%,好转71例,占43.83%。
3 讨论
3.1 增强责任心,强化ADR报表质量
我院162例 ADR报告中,新的/严重的报告仅占9.88%,远远低于世界卫生组织规定的能够起到有效预警30%的比例[1],其中已知的、一般的ADR报告占绝大多数,而有意义的、有价值的报告较少。因药品在上市销售前药物临床试验存在观察病例少、观察时间短、受试者入选条件局限等问题导致许多ADR未被发现[2],所以对药品上市后的临床广泛使用过程中进行ADR监测意义重大,应进一步加大宣传力度,完善相关制度,增强医务人员上报ADR的自觉性和责任心。对新发现的ADR及时准确上报,既能及时避免药品对更多人群的伤害,又能促进临床合理用药,为患者用药安全提供保障。
3.2 加强对老年人ADR的监测
本次调查的162例ADR报告中,女性多于男性,男女比例为1∶1.10,但基本平衡,表明ADR发生率在性别方面差异无统计学意义。由表1可知,ADR可发生于任何年龄组人群,但60岁以上高龄患者构成比明显高于其他年龄段,这可能与老年人的生理特性及用药频次有关。老年患者器官功能萎缩退化,从而影响药物在体内的代谢过程,而且老年患者往往有多种疾病,合并用药较普遍,ADR发生率较其他年龄段高。提示伴随我国人口老龄化趋势,对老年患者ADR的监测工作将成为研究领域的重点[3]。
3.3 选择合理给药途径,控制ADR的发生
由表2可以看出,ADR发生率最高的给药途径是静脉给药,为 135例,占 83.33%,其次为口服给药,为 17例,占10.49%,与国内相关报道相近[4]。静脉给药易发生ADR的原因主要是医院静脉用药占主导地位,住院患者静脉用药比例接近100%,门诊患者静脉用药比例高于30%。静脉给药直接进入人体循环,无吸收过程,静脉注射剂存在较多产生ADR的直接诱因如内毒素、pH值、为保持其稳定性需要加入的缓冲剂和其他添加剂,以及滴注速度与疗程等因素,特别是中药注射剂等。针对静脉给药ADR报告多的情况,在临床治疗过程中,医生应根据患者的病情、年龄、体质等情况考虑能口服给药尽量避免或减少静脉给药,减少ADR对患者的损害。此外,应积极开展临床药学服务,做好静脉滴注过程的监护工作,及早规避ADR的发生。
3.4 加强抗感染药的合理应用与管理,减少ADR的发生
由表3、4可见,抗感染药引起的ADR居首位,共60例,占37.04%,且用药起点较高。可能与我院抗感染药的使用频率较高有关。其中 β-内酰胺类发生 ADR的比例最高,为50.00%,其次为硝基咪唑类,占20.00%,氟喹诺酮类为11.67%,这与国内其他ADR报告文献有差异[1,5]。这可能与我院2011年以来认真开展卫生部关于抗菌药物的专项整治活动和贯彻落实《抗菌药物临床应用指导原则》、《卫生部办公厅关于抗菌药物临床应用管理有关问题通知》(卫办医政发[2009]38号文件,简称“38号文件”)精神,“38号文件”明确要求医疗机构严格控制氟喹诺酮类药的临床应用,以及严格控制氟喹诺酮类药作为外科围术期预防性用药,故氟喹诺酮类药应用受到一定限制有关。但β-内酰胺类药的应用依然居高不下,应进一步严格把握适应证,避免无指征用药、联合用药、超剂量用药、高起点用药以及疗程过长等不合理用药现象,减少ADR的发生。
3.5 加强用药监护与沟通
从表5中可以看出,ADR累及器官和(或)系统以消化系统损害最多,消化系统ADR主要表现为恶心、呕吐、腹痛等,其次为皮肤及其附件和心血管系统损害等,与国内相关报道略有不同[6-7]。分析其原因,在我院ADR涉及的抗感染药的占比中,硝基咪唑类占20.00%,氟喹诺酮类占11.67%、大环内酯类占10.00%,这些主要与引起消化系统不良反应有关。特别是大环内酯类药阿奇霉素引起的ADR较多,多以胃肠道反应[6]和静脉刺激为主,少见胸闷、憋气、呼吸困难等症状。主要原因为大环内酯类药在临床的广泛应用和本身特有的不良反应类型,调查分析表明患者在空腹、滴速快和溶剂量少的情况下更容易发生胃肠道反应和静脉刺激,提示临床在使用阿奇霉素时应注意溶剂、滴速和进食的问题,减少ADR的发生。临床对于易观察到的ADR上报较多,对难以观察、需临床检验数据的ADR上报很少,可能存在漏报现象,这与医师临床观察不细致、医患沟通不到位有关。
3.6 重点关注中药注射剂的合理应用
从表 3、5可以看出,中药制剂致 ADR为 37例,占22.84%,仅次于抗感染药,其中中药注射剂引发ADR的比例最高,占中药制剂ADR的83.78%,这与国内相关报道基本一致[8-9]。中药注射剂在临床应用越来越广泛,同时,中药注射剂的原料成分复杂、有效成分不明确、药材质量不稳定、提取制备工艺简单,造成中药注射剂的质量不稳定,中药注射液中的鞣质和不溶性微粒是发生不良反应的主要原因[10]。一种中药制剂常由多种组分组成,本身又多为大分子物质,如蛋白质、多肽、多糖等,在具有免疫原性的同时,又具有免疫反应性。还有许多未知成分,配制制剂时又加入一些辅助剂,这样有可能引起交叉感染[6],另外其pH、渗透压、微粒、内毒素等都可能成为不良反应的诱因。在我院应用较多的参麦注射液、银杏达莫注射液、丹红注射液等中药注射剂,多为60岁以上人群使用,老年患者往往有多种疾病,联合用药较普遍。因此,为减少中药制剂ADR的发生,中药注射剂最好单独使用。
3.7 积极开展合理用药宣传与临床药学服务工作
积极开展临床药学服务与合理用药宣传活动,要求临床医师在诊断明确的基础上对症下药,要对药物有全面的了解,特别是药物的不良反应及药物相互作用,对于长期使用或用量较大时更容易在患者身上出现毒性反应的药物,要全面掌握、充分考虑其作用的各种因素,制定合理的用药方案。应开展临床药学服务工作,定期深入临床开展ADR监测工作,确保患者用药安全、有效,提高医疗水平,使医院药学与临床密切结合,达到合理用药的目的。
3.8 充分发挥护理人员在ADR监测中的重要作用
把监测ADR作为护士的职责之一。护士对用药全过程进行观察,对及早发现ADR起着重要的作用。在执行医嘱、落实各治疗计划的过程中,护士是药物治疗的直接实施者。在用药中、用药后细心观察药物的不良反应和患者的病情变化是护士在药疗过程中的职责和必须坚持的原则。护士只要经常深入病房,观察、了解患者的生命体征、皮肤及黏膜等变化,重视患者的主诉,就可以通过病情变化,及时发现和协助医生处理ADR,避免产生严重后果和减少漏报现象的发生。
综上所述,ADR监测是一项重要的工作,医院药事管理与药物治疗学委员会应广泛开展ADR的宣传教育,完善和落实监测报告制度;强化对抗感染药、中药制剂、高危人群的不良反应监测;在增加报表数量的同时提高报表质量,特别是及时发现和上报新的/严重的ADR意义重大;通过对ADR的分析、评价,切实为临床用药提供参考,促进临床合理用药,为患者用药安全提供保障。
[1]张娟,熊永山,王登峰,等.武汉市2010年5252例药品不良反应报告分析[J].中国药房,2012,23(2):153-156.
[2]王宏源.我院193例药品不良反应报告回顾与分析[J].安徽医药,2011,15(4):122-124.
[3]王杰松,刘刚,吴久.药物临床试验的风险与管理[J].中国药房,2008,19(31):2406-2407.
[4]许书慧,林则彬.蒙脱石散与维生素B6联合应用减轻阿奇霉素胃肠道不良反应的临床随机对照研究[J].中国药房,2009,20(29):2295-2296.
[5]刑蓉,许健,师佩兰,等.蚌阜地区2009—2010年抗菌药物致不良反应报告分析[J].中国药房,2012,23(2):150-152.
[6]谢丽.179例药品不良反应报告分析[J].安徽医药,2010,14(03):116-117.
[7]李双.我院177例药品不良反应报告分析[J].中国新药杂志,2010,19(8):725-728.
[8]江亮,肖律.我院442例药品不良反应报告分析[J].中国药房,2012,23(2):156-158.
[9]唐智权,杨思芸.我院774例药品不良反应报告分析[J].中国药房,2012,23(26):2472-2474.
[10]阎爱荣,彭芳辰.10种中药注射液的不良反应及相关因素分析[J].中国医院药学杂志,2008,28(9):765-766.
——南方医科大学广东省中药制剂重点实验室团队介绍

