生理性和病理性心脏脂肪浸润的MSCT 表现
齐琳,毛定飚,李铭,陈阳,滑炎卿
生理性脂肪浸润是指出现在健康成人心肌中的脂肪成分,随年龄增长而增多,体现了心脏的正常老化退变过程,心功能正常。病理性脂肪浸润是指由于冠状动脉或心肌病变引发的心肌脂肪变性,其与心脏疾病相关,而与年龄无关,体现心脏的病理损害结果,常伴心功能的下降,病理性心脏脂肪浸润可能为患者猝死的重要病因。随年龄增长出现的生理性心肌脂肪浸润,常见于右心室流出道和游离壁,可伴或不伴室壁增厚,通常右室功能正常。病理性心肌脂肪浸润主要见于陈旧性心肌梗死、致心律失常性右室发育不全(arrhythmogenic right ventricular cardiomyopathy,ARVC)、病毒性心肌炎等,少数可见于心脏脂肪瘤、房间隔脂肪瘤样肥厚(lipomatous hypertrophy of the interatrial septum,LHIS)、结节性硬化症、扩张型心肌病、萎缩性心肌病等[1]。本文回顾性分析395例心脏脂肪浸润患者的临床和CT 表现,旨在探讨其在生理性和病理性心肌脂肪浸润鉴别诊断中的价值。
材料与方法
1.病例资料
搜集2008年6月-2011年10月在我院行冠状动脉CT成像的1515例患者,其中心肌或心腔脂肪浸润者392例,男206 例,女186 例,年龄46~78 岁,平均(61.0±5.3)岁,患者多有胸闷、胸疼及心电图异常,临床疑诊冠心病或为排除冠心病而行心脏MSCT检查。
2.检查方法
CT 扫描采用GE Light Speed VCT 或GE 750 HDCT 扫描仪,扫描范围自气管分叉下1cm 至膈下2cm,扫描方向为足向头。先平扫测定冠脉钙化积分,CTA 扫描前先于主动脉根部同层动态扫描测定对比剂峰值时间,然后根据时间-密度曲线确定延迟时间(22~36s),使用前瞻性或回顾性心电门控扫描采集数据。增强扫描采用非离子型碘对比剂(350mg I/mL),注射流率为4.0~5.0mL/s,剂量60~80mL 加生理盐水20mL,采用双筒高压注射器经肘正中静脉注入对比剂。扫描参数:管电压120~140kV,管电流350~750mA,层厚0.625mm,螺距0.26,旋转时间0.35s。
3.图像处理及分析
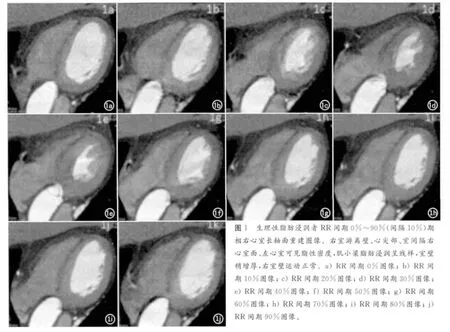
原始数据分别采用Detail、HD detail模式进行重建,常规默认心室舒张中末期(RR 间期75%)和收缩期(RR 间期45%)时相的数据,以病变区平扫CT 值<-20HU 为脂肪浸润的参照标准。脂肪浸润累及右心室壁者,于肺动脉环下方测量其在75%期相时室壁脂肪浸润厚度,若需观察室壁运动情况和分析心功能,则重建RR 间期0%~90%期相(间隔10%)。采用GE AW4.4工作站心脏分析软件进行后处理,以左右长轴、短轴、四腔心及左右心室流出道进行多平面重建(multiplanar reformation,MPR),曲面重组(curve planar reformation,CPR)、容积再现(volume rendering,VR)及最大密度投影(maximum intenisity projection,MIP)重建,VR 图像位置与DSA 常规位置吻合。心功能数据处理采用心功能分析软件包计算相关参数。
4.统计学分析
采用SPSS 17.0软件进行统计学分析,连续性变量采用均值±标准差(±s)表示,对右心室壁生理性脂肪沉积者年龄和脂肪浸润厚度行正态分布检验和相关分析,以P<0.05为差异有统计学意义。
结 果
生理性脂肪浸润:本组358 例,男186 例,女172例,平均年龄(64.0±4.2)岁,脂肪分布见表1。采用R-R 间期0%~90%重建并结合心脏彩色多普勒超声,结果显示右室壁运动、右心功能正常。累及右心室壁者,室壁平均厚度3.5mm(2.3~9.5mm),与年龄呈正相关(r=0.5870,P<0.05),无性别差异。心室壁厚度≤4mm 者185例(72.3%),>4mm 者80 例(27.7%)。累及左心室壁者,均未见局部室壁变薄,部分较邻近正常室壁稍增厚(图1)。
病理性脂肪浸润:本组34例(陈旧性心肌梗死28例,ARVC 3例,LHIS 3例)。陈旧性心肌梗死心脏脂肪浸润患者中男17例,女11例,平均年龄65岁,均有一支或两支冠状动脉粥样硬化斑块致管腔闭塞的心肌梗死病史,梗死时间均为半年以上(图3a、b)。脂肪浸润部位均位于心内膜下,呈细条状(78.6%,22/28)和斑块状(21.4%,6/28),其分布部位和病变血管见表2。19例(67.9%)梗死部位伴室壁变薄,4例(14.3%)伴室壁瘤形成,6 例(21.4%)有室壁钙化点。3 例ARVC患者中男2例,女1例,均有左心室传导阻滞、频发室性早搏病史,2 例为心功能不全II级(NYHA分级)行人工心脏起搏器安装术后,2例有明确家族史(1例其胞弟于30岁时猝死,图7a~c)。LHIS3例,其中男2例,女1例,平均年龄73岁,均为临床怀疑冠心病行冠状动脉CTA 检查时偶然发现,无相关临床症状,1例心电图ST 波低平(图8a~c)。
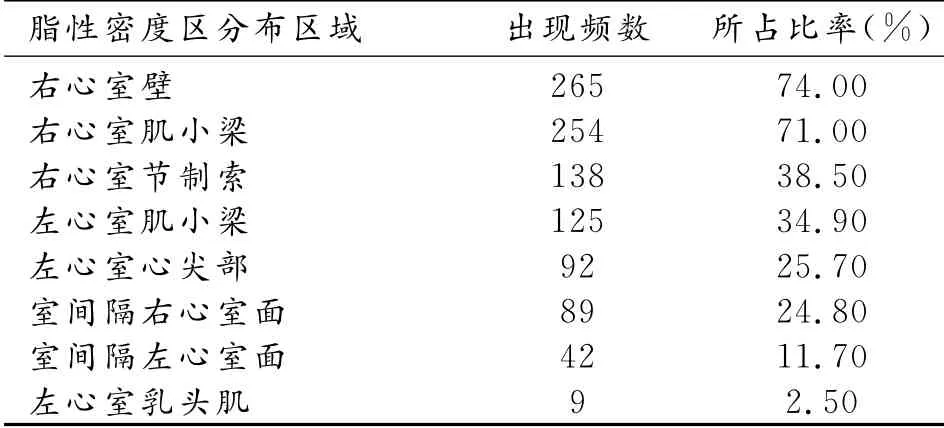
表1 生理性脂肪浸润的分布及所占比率
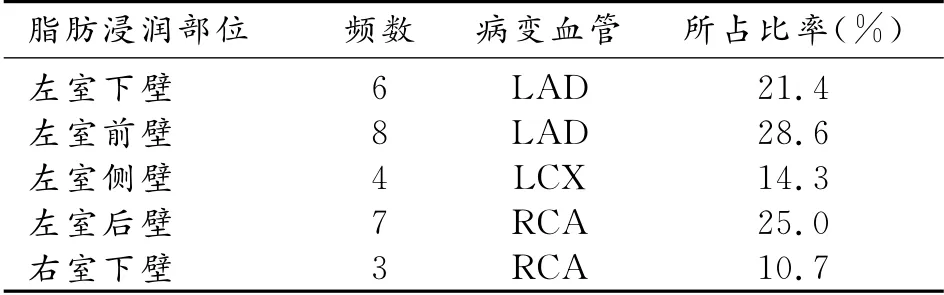
表2 陈旧性心肌梗死脂肪浸润部位
讨 论
心脏脂肪主要分布于心外膜下和冠状血管周围,其含量与年龄和营养状况有关,随年龄的增长而增多。Tansey等[2]对148例非心脏病死亡的尸检中发现,约85%的个体右室壁存在脂肪浸润,认为是心脏退变的表现。正常心壁内脂肪主要分布于右室壁的外1/3和心尖部,部分可浸润右室壁全层并延伸至心内膜和肌小梁[3]。在体脂较多的个体中,脂肪组织可沉积在肌束和/或心肌细胞之间,但不代替正常的心肌细胞,此时室壁厚度可增加[4]。
CT 的密度分辨力高,借CT 值的差异可较准确地区分脂肪和心肌组织。心脏脂肪浸润在MSCT 中主要表现为局部区域平扫时CT 值低于-20 HU。16%~43%的病例在MSCT 检查中可发现右心室壁脂肪浸润,其发现频率和程度随着年龄的增大而增加,与检查者性别、体重指数、肥胖程度的相关性尚不明确,有心肌脂肪浸润者与无脂肪浸润者心电图表现无显著差别[5]。
本研究中,无冠心病临床症状和病史者的脂肪浸润按发生频率依次为右心室壁、右心室肌小梁和节制索、左室肌小梁和心尖部、室间隔右心室面、室间隔左心室面。右心室壁CT 测量厚度较小(常<4mm),厚度超过4mm 者仅占27.7%,以致不能确定脂肪浸润是在心内膜下、中层还是心外膜下。因生理性脂肪浸润是心脏退变的表现,其程度可随年龄增长而累积增加,且其沉积在肌束和/或心肌细胞之间,不代替正常的心肌细胞,故浸润部位室壁可增厚,并随年龄增长而增加。
病理性心脏脂肪浸润可见于陈旧性心肌梗死、ARVC、LHIS等。
陈旧性心肌梗死:心肌梗死后,坏死心肌经历炎症反应、血管生成、成纤维细胞浸润和胶原沉积,最终形成瘢痕组织。心肌梗死后脂肪细胞在此聚集,可能与缺血的心肌细胞不能产生促进脂肪代谢必须的游离脂肪酸或与心肌收缩力减低不能消耗脂肪细胞内的能量有关,也可能与心肌再灌注治疗如经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)、搭桥手术促进瘢痕组织分化为脂肪细胞有关。脂肪组织在梗死区域的浸润无特定范围,局部脂肪含量一般低于75%[6],其分布与梗死范围、左心室射血分数、左心室收缩末期和舒张末期容积指数有关。有研究认为在心肌梗死后六周内梗死区无肉眼可见的脂性密度区,随着时间的推移梗死心肌处脂肪浸润增加,且与性别、年龄、冠心病危险因素、心电图异常及再灌注治疗无相关性[7]。本组28例陈旧性心梗(梗死时间超过半年)均可找到肇事血管,除梗死区脂肪浸润外,还可伴局部室壁变薄、室壁瘤形成、室壁钙化等表现,与生理性脂肪浸润鉴别不难。
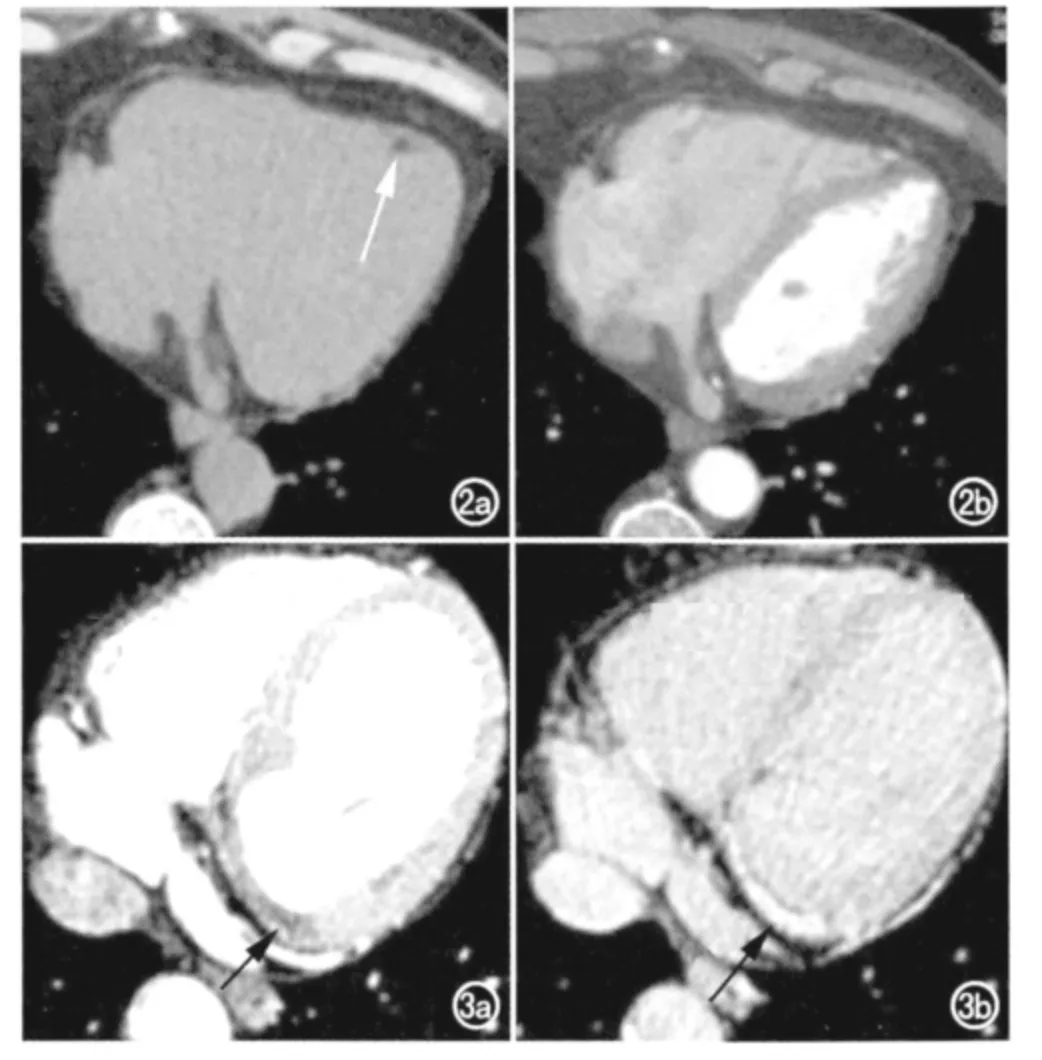
图2 a)健康成人体检的钙化积分扫描图像,室间隔心尖部右心室可见面块状脂性密度灶(箭);b)横轴面冠状动脉CT 增强扫描图像,脂性密度灶未见强化。 图3 左心室后壁急性心肌梗死6个月患者。a)冠状动脉CTA 图像示左心室下壁早期有灌注缺损(箭);b)增强扫描延迟期图像示原灌注缺损区完全强化。
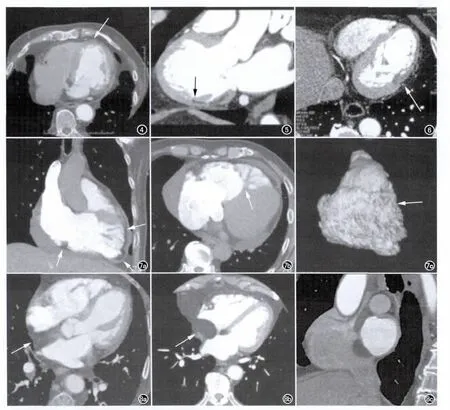
图4 陈旧性心肌梗死患者,冠状动脉造影图像示左心室心尖部弧线状脂性密度影(箭)。 图5 陈旧性心肌梗死患者,心肌梗死累及乳头及根部,脂肪浸润也呈弧线状(箭)。 图6 左心室侧壁陈旧性心肌梗死患者,局部心肌变薄、凹陷(箭)。图7 ARVC患者右心室CT 重建图像。a)MPR 图像示心肌脂性密度区呈带状分布于右心室“发育异常三角”(箭);b)横轴面图像示右心室节制索的结节状脂性密度浸润(箭),肌小梁结构紊乱、过度显影,游离壁膨胀呈扇贝状;c)VR 图像示紊乱的肌小梁(箭)。 图8 LHIS患者冠状动脉CT 扫描图像,a)房间隔上部层面横轴面图像示分隔左右心房的宽带状脂肪密度肿块(箭);b)房间隔中部层面横轴面图像示典型的跨越卵圆窝的哑铃状脂肪密度肿块(箭);c)矢状面图像示LHIS自上腔静脉口延伸至下腔静脉口。
CT 显示陈旧性心肌梗死引起的脂肪密度影较薄,呈斑块状或线状,位于肇事血管供应的坏死心肌的心内膜下,很少位于中层、心外膜下。本研究中脂肪密度累及心肌厚度均小于75%,单凭脂肪区域的形态特征与生理性脂肪浸润较难鉴别,需结合心肌梗死病史及间接征象方可得到正确诊断。心肌梗死的间接征象包括:供血动脉严重狭窄或闭塞,梗死区不成比例的心壁变薄、凹陷、室壁瘤、附壁血栓、心肌钙化,心功能不全致肺静脉淤血及肺水肿等。
致心律失常性右心室发育不全:ARVC 是一种与遗传因素和病毒感染有关的心肌疾病,主要累及右心室,病理上以心肌被纤维脂肪组织进行性替代为特征,主要临床表现为室性心律失常、难治性右心衰竭、猝死。尽管ARVC室壁厚度可能正常,但心肌组织的变性使其呈透明状外观,纤维脂肪组织从心外膜向心内膜呈波浪状推进,常位于心脏“发育异常三角”,即右心室流出道、三尖瓣后瓣下方的心室前壁、右心室近心尖部[8]。ARVC的CT 特征包括:右心室扩大(主要为右心室体部和流出道),心壁、肌小梁、节制索脂肪浸润,肌小梁过度显示,右心室游离壁呈“扇贝”状膨胀。在这些CT 表现中,肌小梁过度显示与组织学上小梁收缩和右心室壁存在较深的裂隙有关[9],右室游离壁的“扇贝”样改变和肿胀与组织学上右心室游离壁瘤有关。本组ARVC 病例只有3例,CT 表现与文献描述相近。
房间隔脂肪瘤样肥厚:LHIS 由无包膜的成熟脂肪细胞过度堆聚于房间隔内而形成,是一种少见的良性病变,CT 表现为房间隔增厚超过15mm 并呈脂肪密度,可从冠状窦延伸至主动脉根部。病灶多位于卵圆窝上部且突入右房,在房间隔上部层面呈分隔左右心房的宽带状脂肪密度区,在房间隔中部层面呈典型的跨越卵圆窝的哑铃状脂肪密度肿块,在心房底部层面呈包绕冠状窦的隧道状脂肪密度肿块或指状突起,常伴有心包或纵隔脂肪增多,增强后无强化[10]。本组LHIS患者只有3例,对其影像特点的认识尚待强化。
鉴别诊断:陈旧性心肌梗死脂肪浸润分布于心内膜下并与肇事血管供血范围一致,通常与生理性脂肪浸润较易鉴别,但当脂肪组织位于左心尖部时,与小范围的心肌梗死较难区分。另外,当右心室的生理性脂肪浸润沿右冠状动脉分布时,与心梗后脂肪浸润较难鉴别。ARVC患者右心室壁心肌组织由于纤维化和脂肪浸润而逐渐变薄,而生理性脂肪浸润室壁厚度正常或增厚;另外,ARVC 还常伴有右心室扩大、右心室游离壁变薄、右室壁运动异常等。LHIS与糖尿病、年龄增长有关,女性多见,一般无症状,常在心脏影像学检查、手术、活检时偶然发现,房间隔哑铃状脂肪密度影、增强扫描无强化是其特征性影像学表现。
总之,了解患者的年龄、心肌脂肪分布特征、室腔大小、有无室壁运动异常、临床病史和实验室检查有助于鉴别病理性和生理性脂肪浸润。
[1] Kimura F,Matsuo Y,Nakajima T,et al.Myocardial fat at cardiac imaging:how can we differentiate pathologic from physiologic fatty infiltration?[J].RadioGraphics,2010,30(6):1587-1602.
[2] Tansey DK,Aly Z,Sheppard MN.Fat in the right ventricle of the normal heart[J].Histopathology,2005,46(1):98-104.
[3] Basso C,Thiene G.Adipositas cordis,fatty infiltration of the right ventricle,and arrhythmogenic right ventricular cardiomyopathy.Just a matter of fat?[J].Cardiovasc Pathol,2005,14(1):37-41.
[4] Lorin DLGG,Le Bihan C,Durigon M.Assessment of right ventricular lipomatosis by histomorphometry in control adult autopsy cases[J].Int J Legal Med,2001,115(2):105-108.
[5] Imada M,Funabashi N,Asano M,et al.Epidemiology of fat replacement of the right ventricular myocardium determined by multislice computed tomography using a logistic regression model[J].Int J Cardiol,2007,119(3):410-413.
[6] Winer-Muram HT,Tann M,Aisen AM,et al.Computed tomography demonstration of lipomatous metaplasia of the left ventricle following myocardial infarction[J].J Comput Assist Tomogr,2004,28(4):455-458.
[7] Zafar HM,Litt HI,Torigian DA.CT imaging features and frequency of left ventricular myocardial fat in patients with CT findings of chronic left ventricular myocardial infarction[J].Clin Radiol,2008,63(3):256-262.
[8] Kawakubo M,Funabashi N,Takahashi M,et al.Relationship of natriuretic peptide and transthoracic echocardiographic findings in 135subjects with muscular dystrophy[J].Int J Cardiol,2010,145(3):506-514.
[9] Maksimovic R,Ekinci O,Reiner C,et al.The value of magnetic resonance imaging for the diagnosis of arrhythmogenic right ventricular cardiomyopathy[J].Eur Radiol,2006,16(3):560-568.
[10] 毛定飚,吴昊,葛虓俊,等.多层螺旋CT 诊断房间隔脂肪瘤样肥厚[J].临床放射学杂志,2010,9(7):902-904.

