3,4,5,6-四溴酚磺酞合成及纯化方法的改进
修志明,黄梦媛,胡 冰,雷莉妍,王丽萍
(吉林大学生命科学学院,长春130012)
酚磺酞类衍生物属于三苯甲烷类染料,是目前应用较广泛的一类酸碱指示剂[1-5].3,4,5,6-四溴酚磺酞作为酚磺酞类衍生物,是合成多种蛋白误差指示剂的原料,如四溴酚蓝和DIDNTB(5',5″-二硝基-3',3″-二碘-3,4,5,6-四溴酚磺酞)等作为检测尿液白蛋白已广泛用于临床早期肾病的诊断[6-8].3,4,5,6-四溴酚磺酞通常采用3,4,5,6-四溴-2-磺苯甲酸环酐与苯酚在无水四氯化锡催化条件下反应生成,并进一步用碱溶、酸沉法纯化后制得[9].Cihelnik 等[10]以 3,4,5,6-四溴-2-磺基苯甲酸环酐为原料,采用微波法合成了3,4,5,6-四溴酚磺酞.但上述两种方法制得的四溴酚磺酞纯度较低,同时原料四溴-2-磺基苯甲酸环酐不易购买,且价格昂贵.本文在文献[11-12]的基础上,以2-磺基苯甲酸环酐为原料,经溴代反应得到3,4,5,6-四溴-2-磺基苯甲酸环酐,再与苯酚反应合成了3,4,5,6-四溴酚磺酞,并改进了纯化方法.
1 材料与方法
1.1 试剂与仪器
2-磺基苯甲酸环酐(质量分数为98%,国产);3,4,5,6-四溴酚磺酞对照品(美国Sigma公司);发烟硫酸、液溴、碘、亚硫酸、苯酚、无水四氯化锡、乙酸乙酯和乙醚均为国产AR级.
液相色谱仪(LC-2010HT型,日本岛津公司);核磁共振仪(300 MHz,美国Varian公司);液质联用仪(1100型,美国Agilent公司).
1.2 方法
1.2.1 3,4,5,6-四溴酚磺酞的合成 3,4,5,6-四溴酚磺酞的合成路线如图1所示.
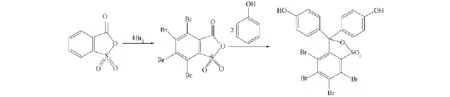
图1 3,4,5,6-四溴酚磺酞的合成Fig.1 Synthesis of 3,4,5,6-tetrabromophenolsulfonephthalein
1.2.1.1 3,4,5,6-四溴-2-磺基苯甲酸环酐的合成 将184.2 g(1 mol)2-磺基苯甲酸环酐置于900 mL发烟硫酸(含体积分数为50%的SO3)中,混合均匀后加入18.0 g碘.量取307 mL(1.5 mol)液溴,先滴加200 mL液溴,升温至80℃控温反应约3 h,再升温至100℃控温反应约3 h.反应冷却后,滴加70 mL液溴,升温至130℃反应1 h,直至液溴被完全吸收.反应冷却后滴加37 mL液溴,并升温至150℃控温反应30 min.反应冷却至室温后加入1.5 L水,用亚硫酸充分洗涤,除去过量的液溴,沉降,过滤,滤饼干燥后,用V(乙酸酐)∶V(冰醋酸)=1∶3重结晶即可制得产物.
1.2.1.2 3,4,5,6-四溴酚磺酞的合成 将117.6 g(1.25 mol)苯酚于120℃控温搅拌0.5 h,加入250.0 g(0.5 mol)四溴-2-磺基苯甲酸环酐,搅拌均匀后加入发烟四氯化锡93 mL(0.8 mol),将混合液升温至130℃,控温搅拌反应8 h,TLC监测反应(V(甲醇)∶V(乙酸乙酯)=1∶5,下同),反应完成后,趁热倒入10 L水中,沉降,倾去上清液;再加入5 L水,搅拌10 min,沉降,倾去上清液,过滤,滤饼于105℃烘干2 h,制得粗品,用HPLC检测纯度(检测波长:254 nm;色谱柱:C18(5 μm,4.6 mm×250 mm);流动相:含质量分数为0.1%TFA的V(乙腈)∶V(水)=35∶65溶液,下同).
1.2.2 3,4,5,6-四溴酚磺酞的纯化
1.2.2.1 溶剂抽提 取3,4,5,6-四溴酚磺酞粗品100.0 g,将w(粗品)∶V(乙酸乙酯)=1∶10混合,搅拌2 h,过滤,滤液浓缩至干,于105℃干燥1 h,制得抽提产物,用HPLC检测纯度.
1.2.2.2 重结晶 将w(抽提产物)∶V(乙醚)=1∶5混合,搅拌1 h,过滤,滤饼于105℃干燥1 h,制得3,4,5,6-四溴酚磺酞纯品,用HPLC检测纯度.
2 结果与讨论
2.1 反应温度对3,4,5,6-四溴酚磺酞合成的影响
按照方法1.2.1.1制得3,4,5,6-四溴-2-磺基苯甲酸环酐402.0 g,产物为白色晶体,收率80.4%;m.p.:217~219℃;质谱检测结果:MS(ESI):m/z 500.7[M+H]+,与目标化合物一致.
按照方法1.2.1.2,将苯酚、四溴-2-磺基苯甲酸环酐和无水四氯化锡依次投入反应器中,分别于120,130,140℃控温反应,TLC监测至原料反应完全,制得产物,用HPLC检测纯度,实验结果列于表1.

表1 反应温度对3,4,5,6-四溴酚磺酞合成的影响Table 1 Effect of reaction temperature on the synthesis of 3,4,5,6-tetrabromophenolsulfonephthalein
四溴-2-磺基苯甲酸环酐先与一分子苯酚发生加成反应,再与一分子苯酚缩合生成酚磺酞产物.当n(催化剂)∶n(底物)>1.6时,提高催化剂用量对产率影响较小;当反应温度较低时,需延长反应时间,但产率和纯度均较低;提高反应温度,产率增加,但温度过高在反应后期易使产物碳化;苯酚过量将导致产物产率和纯度均较低.
3,4,5,6-四溴酚磺酞产物分析结果:MS(ESI):m/z 670.5 [M+H]+;1H NMR(300 MHz,DMSO-d6),δ 7.13(d,J=9.0 Hz,4H),6.79(d,J=9.0 Hz,4H).与目标化合物一致.
2.2 抽提溶剂对3,4,5,6-四溴酚磺酞纯化的影响
取3份各50 g 3,4,5,6-四溴酚磺酞粗品按照1.2.2.1方法分别将该粗品与1 L的丙酮、乙腈和乙酸乙酯混合,制得抽提产物,用HPLC检测纯度,实验结果列于表2.

表2 抽提溶剂对3,4,5,6-四溴酚磺酞纯化的影响Table 2 Effect of extraction solvent on the purification of 3,4,5,6-tetrabromophenolsulfonephthalein
由于四溴酚磺酞、加成产物和苯酚均易溶于质子溶剂,且不易分离,因此抽提溶剂不能使用质子溶剂;四溴酚磺酞和苯酚可完全溶解于非质子极性溶剂中,而加成产物不易溶解,因此产物中含有微量加成产物杂质.由于非质子极性溶剂的极性越强,溶解度越大,产率越高,但纯度越低,因此,用乙酸乙酯做抽提溶剂所得产物纯度较高.
2.3 重结晶溶剂对3,4,5,6-四溴酚磺酞纯化的影响
取4份各50 g按照1.2.2.1方法制得的抽提产物,按照1.2.2.2方法分别将抽提产物与0.5 L苯、乙醚、石油醚和四氯化碳混合,制得产物,用HPLC检测纯度,实验结果列于表3.

表3 重结晶溶剂对3,4,5,6-四溴酚磺酞纯化的影响Table 3 Effect of recrystallization solvent on the purification of 3,4,5,6-tetrabromophenolsulfonephthalein
四溴酚磺酞在非质子非极性(或低极性)溶剂中难溶,而苯酚相对易溶,因此产物中仅含有微量苯酚杂质.由表3可见:选用苯或四氯化碳为重结晶溶剂,产物的产率低、纯度低,且溶剂的毒性较大;使用乙醚作为重结晶溶剂,产物的产率高、纯度高,效果较好.
图2为本文合成提纯的3,4,5,6-四溴酚磺酞与其对照品的薄层色谱.由图 2可见,3,4,5,6-四溴酚磺酞对照品主斑点(Rf=0.3)上方存在加成产物杂质斑点(Rf=0.5)和苯酚斑点(Rf=0.9),合成产物中未出现加成产物和苯酚杂质斑点.
图3为本文合成提纯的3,4,5,6-四溴酚磺酞与其对照品的液相色谱.由图3可见,3,4,5,6-四溴酚磺酞对照品在14.142 min和18.531 min处存在杂质峰,合成的3,4,5,6-四溴酚磺酞未出现杂质峰,因此纯化效果较好.
综上,本文以2-磺基苯甲酸环酐为原料,合成了3,4,5,6-四溴酚磺酞粗品,使用乙酸乙酯为抽提溶剂,制得了纯度较高的抽提产物;使用乙醚为重结晶溶剂,制备了纯度和收率均较高的终产物.

图2 3,4,5,6-四溴酚磺酞薄层色谱Fig.2 TLC of 3,4,5,6-Tetrabromophenolsulfonephthalein

图3 合成的3,4,5,6-四溴酚磺酞(A)及其对照品(B)的液相色谱Fig.3 HPLC of 3,4,5,6-tetrabromophenolsulfonephthalein samples samples(A)and reference substance(B)
[1]Rao G G,Viswanath S G.Some Triphenylmethane Dyes as Redox Indicators in the Titration of Antimony(Ⅲ)with Cerium(Ⅳ)Sulphate[J].Talanta,1977,24(5):323-324.
[2]Duxbury D F.The Photochemistry and Photophysics of Triphenylmethane Dyes in Solid and Liquid Media[J].Chem Rev,1993,93(1):381-433.
[3]Tamura Z,Maeda M.Differences between Phthaleins and Sulfonphthaleins [J].Yakugaku Zasshi,1997,117(10/11):764-770.
[4]Tamura Z.Studies on the Structures of Molecular Species of Phthaleins and Sulfonphthaleins[J].Bunseki,2005(10):557-562.
[5]Balderas-Hernández P,Ramírez-Silva M T,Romero-Romo M,et al.Experimental Correlation between the pka Value of Sulfonphthaleins with the Nature of the Substituents Groups[J].Spectrochim Acta a Molbiomol Spectrosc,2008,69(4):1235-1245.
[6]Pugia M J,Lott J A,Profitt J A,et al.High-Sensitivity Dye Binding Assay for Albumin in Urine[J].J Clin Lab Anal,1999,13(4):180-187.
[7]Sasaki M,Pugia M J,Parker D R,et al.Measurement of the Albumin Content of Urinary Protein Using Dipsticks[J].J Clin Lab Anal,1999,13(5):246-250.
[8]Wallace J F,Pugia M J,Lott J A,et al.Multisite Evaluation of a New Dipstick for Albumin,Protein,and Creatinine[J].J Clin Lab Anal,2001,15(5):231-235.
[9]Boyd W C,Rowe A W.A New Series of Halogenated Sulfonephthaleins[J].J Am Chem Soc,1930,52(12):4954-4959.
[10]Cihelnik S,Stibor I,Lhoták P.Solvent-Free Synthesis of Sulfonephthaleins,Sulfonefluoresceins and Fluoresceins under Microwave Irradiation[J].Collection of Czechoslovak Chemical Communications,2002,67(12):1779-1789.
[11]Kachur A V,Popov A V,Karp J S,et al.Direct Fluorination of Phenolsulfonphthalein:A Method for Synthesis of Positron-Emitting Indicators for in vivo PH Measurement[J].Cell Biochem Biophys,2013,66(1):1-5.
[12]ZHANG Cun-hua,FAN Xian-hong,WANG Zhi-gang,et al.Studies on Process of Reaction of Bromine with Benzene[J].Journal of Jilin University:Science Edition,2005,43(2):222-224.(张存华,范鲜红,王志刚,等.苯分子的溴代反应研究[J].吉林大学学报:理学版,2005,43(2):222-224.)

