HPLC法测定妇炎康复片中芍药苷的溶出度
王玉平,丁建伶,邢 婧,赵新红
承德医学院附属医院药剂科,承德 067000
妇炎康复片来源于临床经验处方,由赤芍、当归、黄柏等11味中药组成,具有清热解毒、除湿止带、消肿散结等功效,主要用于湿热下注、毒淤互阻所致带下病等。作为广泛应用临床多年的制剂,其良好的临床疗效得到广泛认可,然而对于其质量控制仅仅局限于薄层鉴别,质量控制仍需进一步加强。溶出度作为一种重要的固体制剂的质量控制方法,已在多国质量控制中收载,因此,为了进一步控制该制剂的质量,进而提高临床疗效,我们参考相关文献[1-3]中的含量测定方法,以方中君药赤芍的主要成分芍药苷为指标,HPLC法测定其体外溶出情况,以便于控制其内在质量。
1 仪器与材料
1.1 仪器
Waters e2695高效液相色谱仪(美国)、2998光电二极管阵列检测器、Empower 2软件;Sartorius CP225D分析天平(德国Sartorius公司);ZRS-8型智能溶出仪(天津大学无线电厂)。
1.2 试剂
芍药苷对照品(批号:201104,纯度大于98%,购于四川维克奇生物科技有限公司);妇炎康复片(自制,批号为 20110508、20110611、20110725);乙腈、甲醇、磷酸为色谱纯;水为重蒸水,其它试剂均为分析纯。
2 方法与结果
2.1 色谱条件
Agilent TC-C18色谱柱(4.6 mm ×250 mm,5 μm);流动相为乙腈-0.1%磷酸溶液(15∶85);流速1 mL/min;检测波长230 nm;柱温30℃;进样体积20 μL;理论塔板数按芍药苷峰计算应不低于4000。
2.2 方法学考察
2.2.1 标准曲线制备
精密称取芍药苷对照品3.68 mg,置于5 mL量瓶中,加甲醇至刻度线,摇匀。再精密吸取2 mL,置于10 mL量瓶中,加甲醇至刻度线,摇匀,即得147.2 μg/mL的对照品溶液。分别精密吸取该对照品溶液1、2、3、5、8、10 mL,置于 10 mL 量瓶中,加甲醇至刻度线,摇匀。按照已经确定的色谱条件,进样体积20 μL进行测定。以峰面积(Y)对浓度(X)进行线性回归,得到回归方程为Y=4932.21X-13548.77(R2=0.9998)。说明浓度在 14.72 ~147.2 μg/mL范围内,线性关系良好。
2.2.2 专属性考察
按照原工艺制备不含赤芍的阴性样品,并制备溶出2 h的溶出液,分别取对照品溶液、供试品溶出液、阴性样品溶出液进样测定,结果见图1。根据实验结果可知,供试品溶出液中芍药苷色谱峰与其他组分峰可达到基线分离,阴性样品无干扰。
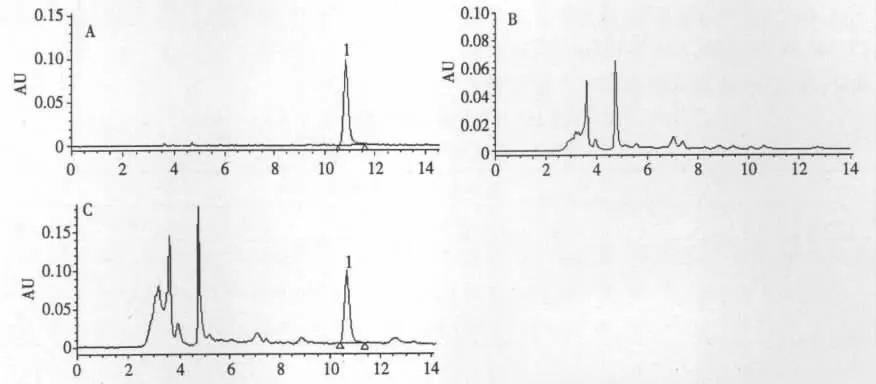
图1 芍药苷对照品溶液(A)、阴性样品溶液(B)和供试品溶液(C)的HPLC色谱图Fig.1 HPLC Chromatogram of paeoniflorin standard(A),blank(B)and sample(C)
2.2.3 稳定性试验
取供试品溶液,分别于 0、2、4、8、12、24 h 进样测定,记录峰面积,结果RSD为1.78%,表明供试品溶液在室温条件下放置24 h稳定性良好。
2.2.4 精密度试验
取取样时间为24 h的溶出液制备供试品溶液,重复进样测定6次,结果芍药苷峰面积的RSD为1.49%,说明本方法精密度良好。
2.2.5 重复性试验
取同一批次的样品,平行制备6份取样时间为4 h的溶出液,分别进样测定,记录峰面积,结果芍药苷峰面积的RSD为0.85%,表明本方法的重复性良好。
2.2.6 加样回收试验
取同一批次的样品,平行制备6份溶出液,精密吸取3 mL置于10 mL量瓶中,再精密吸取浓度为147.2 μg/mL的芍药苷对照品溶液置于上述溶出液中,加甲醇至刻度线,摇匀。按照已经确定的色谱条件,进样测定,根据标准曲线方程计算含量及回收率,结果见表1。根据实验结果可知:平均加样回收率及其RSD值分别为99.89%、2.76%,结果符合要求。

表1 芍药苷加样回收试验Table 1 The recovery rate of paeoniflorin

5 0.298 0.294 0.579 95.58 6 0.29 0.294 0.593 104.08
2.3 妇炎康复片中芍药苷溶出度测定
2.3.1 溶出度测定方法
精密量取已超声30 min进行脱气处理的水900 mL,加入溶出杯中,开启电源开关至(37±0.5℃)保温30 min,调整转速至100 rpm,称取妇炎康复片约10 g,精密称定,置于溶出杯中,分别在开启转桨后的 5、15、30、45、60、120、240、1440 min,迅速取样10 mL,补液,滤过,残渣加入溶出杯中。精密吸取滤液2 mL,置于5 mL量瓶中,加甲醇至刻度线,摇匀,进样,测定。
2.3.2 三批样品溶出度测定
取三批样品,每批样品平行称取6份,照溶出度测定方法下的操作,进行溶出度测定,计算每批样品的平均溶出度,结果显示了三品样品测定结果基本一致,结果见表2。
表2 3批妇炎康复片中芍药苷累积溶出度(n=6,±s,%)Table 2 Dissolution of paeoniflorin in Fuyan Kangfu tablets(n=6,±s,%)
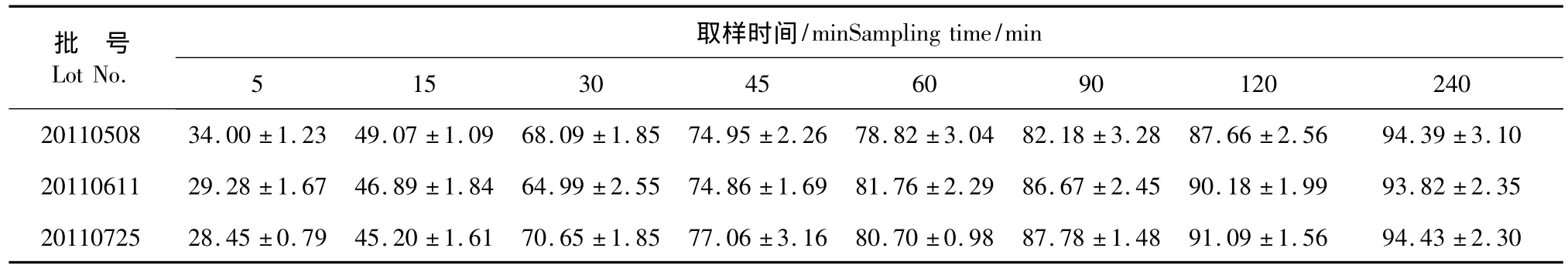
表2 3批妇炎康复片中芍药苷累积溶出度(n=6,±s,%)Table 2 Dissolution of paeoniflorin in Fuyan Kangfu tablets(n=6,±s,%)
批 号Lot No.取样时间/minSampling time/min 5 15 30 45 60 90 120 240 20110508 34.00±1.23 49.07±1.09 68.09±1.85 74.95±2.26 78.82±3.04 82.18±3.28 87.66±2.5694.39±3.10 20110611 29.28±1.67 46.89±1.84 64.99±2.55 74.86±1.69 81.76±2.29 86.67±2.45 90.18±1.99 93.82±2.35 20110725 28.45±0.79 45.20±1.61 70.65±1.85 77.06±3.16 80.70±0.98 87.78±1.48 91.09±1.5694.43±2.30
2.3.3 溶出参数提取
中的方法[4,5],选择 1stOpt软件进行威布尔溶出模型、零级速率模型、一级速率模型、Higuchi模型、Hixson-Crowell模型、Ritger-Peppas模型等6种溶出模型优选,结果最优模型为威布尔溶出模型。选择SAS软件实现溶出参数T50、Td提取,为了编写程序的简便,参考文献中的方法[6],设定威布尔溶出模型为y=1-exp(-b*(t-a)^m),实验结果见表3。
表3 溶出模型选择及溶出参数提取(n=6,±s)Table 3 Selection of dissolution models and parameters(n=6,±s)

表3 溶出模型选择及溶出参数提取(n=6,±s)Table 3 Selection of dissolution models and parameters(n=6,±s)
批号Lot No.最优模型The optimal dissolution model R2 T50/min Td /min 26.36±0.45 20110508 威布尔溶出模型/Weibull dissolution model 0.9900 13.00±1.16 20110611 威布尔溶出模型/Weibull dissolution model 0.9932 15.41±1.44 27.99±0.32 20110725 威布尔溶出模型/Weibull dissolution model 0.9843 14.82±1.3526.26±0.24
2.3.4 溶出参数方差分析
三批样品的溶出参数进行方差分析,结果表明三批样品的溶出参数 a、b、m、T50、Td无显著性差异(P <0.05)。
3 讨论
在进行溶出方法选择时,考虑到妇炎康复片中芍药苷的含量偏低,这不仅需要加大投药量才可以实现定量检测,同时,也给溶出方法选择带来一定难度。预实验中发现,选择转篮法进行取样测定时,篮内片剂装得较满,在溶出试验过程中仅转篮外层的片剂才能接触溶出介质,从而影响片剂实际溶出。因此,综合考虑选择桨法为溶出方法。
在溶出度模型优选中,百分之百溶出量的选择是其中的关键一步。既有选择“制备药粉的溶出24 h的量”为溶出百分之百,亦存在“直接测定药物中的含量”为溶出百分之百的计算方法[7]。本试验中,曾对上述两种方法进行比较,考虑到上述两种方法选择的水为提取溶剂时,测定结果不理想,最终选择以溶出取样时间为24h的累积溶出量作为溶出百分之百。
本试验所建立的妇炎康复片溶出度测定方法,存在操作简便易行,准确可靠等优点,在一定程度上可以达到控制其内在质量的目的。然而,本试验主要研究的是妇炎康复片中芍药苷的体外溶出度,对于体内吸收机制等有待于进一步深入研究。
参考文献
1 Lei DC(雷定超),E XH(鄂秀辉),Zhang LL(张兰兰),et al.Simultaneous determination of five components in Tangminlingwan by HPLC.China J Exp Tradit Med Form(中国实验方剂学),2012,18(13):70-73.
2 Feng Y(冯源),Wang Y(王胤),Zhou N(周浓),et al.Determination of paeoniflorin in different parts of Paeonia Delavayi var.lutea by HPLC.China J Exp Tradit Med Form(中国实验方剂学),2012,18:139-143.
3 Yang YF(杨燕飞).RP-HPLC determination of paeoniflorin,baicalin,palmatine hydrochloride and berberine Hydroc-Hloride in Kuntai capsules.Chin Tradit Med(中成药),2010,32:958.
4 Chen TC(陈天朝),Zhao XH(赵新红),Kang BY(康冰亚).Application of SAS in the choice of six dissolution models.Tradit Chin Med Res(中医研究),2012,25(4):68-71.
5 Yuan WP(袁伟萍),He ZX(何忠祥).Application of global optimization based on 1stopt in tractor's final transmission Design.Tractor Farm Trans(拖拉机与农用运输车),2010,37(6):28.
6 Pan YS(潘玉善),Li WQ(李文清),Wang W(王伟),et al.Calculation of Weibull'S distribution parameters for drug dissolution with SAS.J Guangdong Pharm Coll(广东药学院学报),2010,26:23-26.
7 Cheng HZ(程荷珍),Wang GH(王桂红),Wang P(王萍).The dissolution study of Liuweidihuang pill.Chin Tradit Med(中成药),2001,23:380-381.

