CTMAB催化增敏分光光度法测定食品中的己烯雌酚
陈荷莲,黄 璐,郑 琦
(江汉大学 化学与环境工程学院,湖北 武汉 430056)
己烯雌酚(DES)[1]是一种人工合成的非甾体雌激素类物质,药理性质与天然雌二醇相似,具有促进蛋白质合成,增加蛋白质沉积,减少脂肪沉积等功效;它能促进畜牧动物生长、增加瘦肉率、提高肉料比等。但实践表明,DES对人体具有很强的毒副作用,如改变机体遗传物质,导致基因突变,促使细胞癌变。因此,自1979年起包括我国在内的世界各国开始严格控制DES作为治疗药物的使用,并禁止用作动物饲料添加剂。但由于利益的驱动,一些不法商人仍然违规滥用。为保护人类健康,动物性食品中DES残留的检测显得尤为重要,文献报道的DES检测方法主要有:高效液相色谱法、气相色谱法、色谱-质谱联用法[2-4]、酶联免疫分析法、电化学法等[5],这些方法要么对仪器要求较高,要么对试剂要求较高,其推广和应用受到一定限制。笔者利用DES具有还原性特性,探索了由三甲基十六烷基溴化铵(CTMAB)、Fe(Ⅱ)、K3[Fe(CN)6]等组成的多元络合体系[6]为探针的用可见分光光度法测试DES的新方法。该方法所要求仪器普通,试剂常规,一般实验室条件都能满足。
1 材料与方法
1.1 材料与仪器
DES,阿拉丁试剂公司,99%标准品;乙腈,国药集团化学试剂有限公司,AR;HCl,信阳市化学试剂厂,AR;NaOH,天津市大陆化学试剂厂,AR;CTMAB,BDH Chemicals Ltd.Poole(Eng⁃land),98%标准品;K3[Fe(CN)6]、FeCl3,天津市福晨化学试剂厂,AR;配溶液所用水为二次蒸馏水;奶粉,购自超市。
BF-2000型N2吹干仪,北京八方世纪有限公司;UV-2550双光束紫外可见分光光度计,日本岛津公司;800型低速离心沉淀机、HH-2数显性恒温水浴锅,国华仪器;电子天平,赛多利斯科学仪器有限公司;Q-250超声波提取仪,昆山市超声仪器有限公司。
1.2 方法与步骤
1.2.1 溶液配制 DES储备液:电子天平准确称量0.0514 g的DES,用乙腈溶解并稀释至50 mL,得浓度为1.0177 mg/mL的标准储备液。实验时用乙腈稀释至8.14 μg/mL。
FeCl3溶液:准确称取1.0100 g FeCl3,蒸馏水溶解并稀释至250 mL,其间用浓HCl调溶液pH在1.0~1.5之间,得浓度为1.5×10-2mol/L储备液。实验时用蒸馏水稀释到所需浓度。
K3[Fe(CN)6]溶液:准确称取1.2300 g K3[Fe(CN)6],用蒸馏水溶解并稀释至250 mL,得浓度为1.5×10-2mol/L储备液。实验时用蒸馏水稀释到所需浓度。
CTMAB溶液:用电子天平准确称量0.1016 g CTMAB,用蒸馏水溶解并稀释至100 mL,得浓度为2.79×10-3mol/L CTMAB溶液。
1.2.2 实验方法 准确移取1.5×10-3mol/L FeCl3溶液2.0 mL和CTMAB 200 μL于10 mL比色管中,摇匀;在10 min内分批加入适量的DES标准溶液或试样溶液,用HCl调pH值到3.0,30℃下反应10 min;最后加入1.5×10-3mol/L K[3Fe(CN)6]溶液2.0 mL,摇匀,40℃下反应40 min;用二次蒸馏水定容到10 mL,摇匀,以试剂空白为参比,用2 cm的比色皿于736 nm处测定其吸光度[1]。
2 结果与分析
2.1 吸收光谱
按1.2.2实验方法配制溶液绘制其吸收光谱,以乙腈为参比测得DES溶液吸收光谱,以水为参比测得FeCl3溶液、K3[Fe(CN)6]溶液吸收光谱,以试剂空白为参比,测得反应生成的多元络合物的吸收光谱,扫描区间在300~900 nm(图1)。
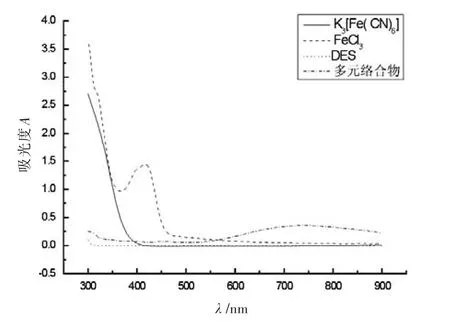
图1 物质吸收光谱
如图1所示,DES、FeCl3和K3[Fe(CN)6]在可见光区几乎没有吸收,反应生成的多元络合体系在700~800 nm范围内有明显吸收,体系的最大吸收波长在736 nm处,故选择测定吸光度的波长为736 nm。
2.2 条件的选择
2.2.1 酸碱度的影响 按实验1.2.2的方法,在加入DES后调节体系的pH值分别为1.0、2.0、3.0、5.0、7.0、9.0,试剂空白做参比,测吸光度值(表1)。
由表1可知,pH值为3.0时有最大的吸光度值,故加入DES后调整体系pH值为3.0。分析原因:当体系pH值超过3.0时,溶液中的Fe(Ⅲ)以Fe(OH)3沉淀析出,残存于体系中Fe(Ⅲ)太少,影响了与DES的反应,pH值为3.0时能保证体系中的Fe(Ⅲ)浓度最高,与DES的相互作用更充分、完全,为后续的络合体系提供更多Fe(Ⅱ)。
2.2.2 反应时间 依据1.2.2的实验步骤,FeCl3溶液中加入一定量DES后,控制反应时间分别为10、20、30、50 min,然后加入K[3Fe(CN)6]溶液,反应40 min,试剂空白做参比,测吸光度(图2)。
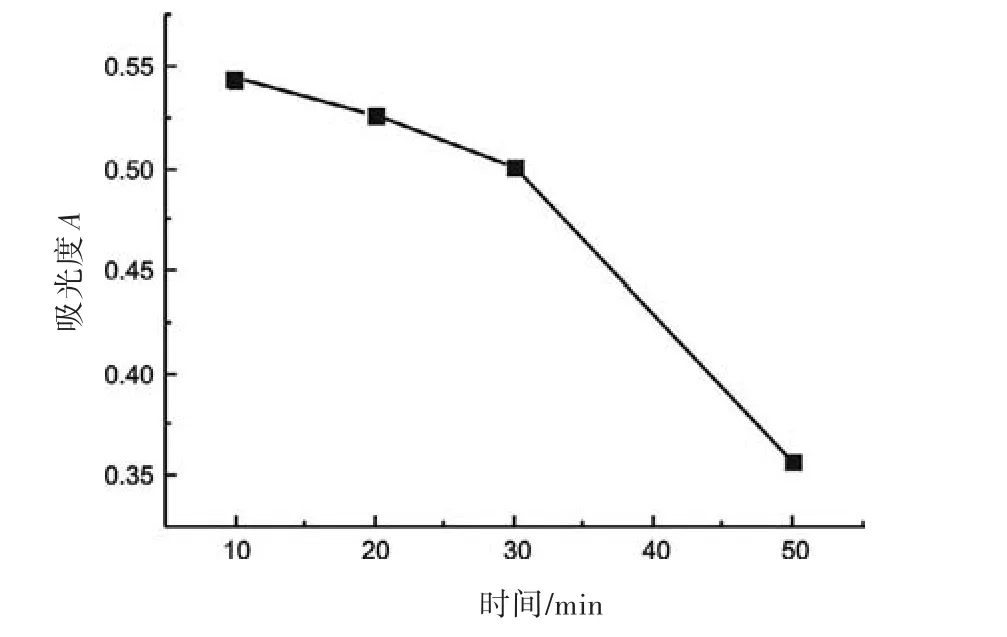
图2 时间对吸光度的影响
由图2可见,随着反应时间的延长,测得的吸光度减小,反应时间为10 min有最大的吸光度,故加入DES后反应时间定为10 min。
同样方法,改变加入K[3Fe(CN)6]溶液后的反应时间,结果表明,反应时间为40 min有最大吸光度,故反应时间定为40 min。
2.2.3 反应温度的影响 依据1.2.2的实验步骤,考察了温度对体系吸光度的影响。FeCl3溶液中加入一定量DES后,控制反应温度分别为30℃(室温)、40℃、50℃、60℃,反应10 min,然后加入K[3Fe(CN)6]溶液,反应40 min,后用试剂空白做参比,测吸光度(图3)。

图3 体系反应温度对吸光度的影响
由图3可知,随温度的升高测得的A值减小,温度为30℃时有最大的吸光度,故实验时加入DES后反应时的温度定为30℃。
同样方法,改变加入K3[Fe(CN)6]溶液后的反应的温度,结果表明,温度为40℃时有最大的吸光度,故反应温度定为40℃。
2.2.4 FeCl3、K3[Fe(CN)6]溶液用量的影响依据1.2.2的实验步骤,考察了FeCl3用量对体系吸光度的影响。固定 DES、CTMAB、K3[Fe(CN)6]溶液用量,改变FeCl3用量,设定FeCl3溶液的加入量为0.8、1.2、1.6、2.0、2.4、3.0 mL,试剂空白做参比,在选定波长下测吸光度,其结果如图4。
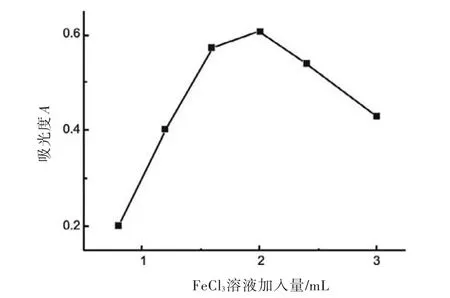
图4 FeCl3溶液用量对吸光度的影响
如图4所示,当FeCl3加入量小于2 mL时,随着FeCl3加入量增加,吸光度逐渐增大,超过2 mL后吸光度随FeCl3加入量增大而减小,因此实验中将FeCl3溶液用量定为2.0 mL。
同样方法只改变K[3Fe(CN)6]用量,固定其他各试剂加入量不变,K[3Fe(CN)6]溶液加入量为2.0 mL时有最大的吸光度,因此实验中K[3Fe(CN)6]溶液用量定为2.0 mL。
2.2.5 CTMAB用量和加入顺序的影响 按照1.2.2实验方法,考察了CTMAB加入量对体系吸光度的影响。固定DES、FeCl3、K[3Fe(CN)6]溶液用量,改变CTMAB用量,设定CTMAB溶液的加入量为0、100、200、400、600 μL,试剂空白做参比,在选定波长下测吸光度(图5)。
如图5所示,体系加入CTMAB后吸光度增大,且最大吸收波长发生红移。当CTMAB溶液加入量大于100 μL后,体系的吸光度没有明显的增大,加入量在200~400 μL之间体系的吸光度和红移值几乎相同没有明显变化,当加入量到600 μL时,吸光度明显降低,因此实验中TMAB溶液用量定为200 μL。
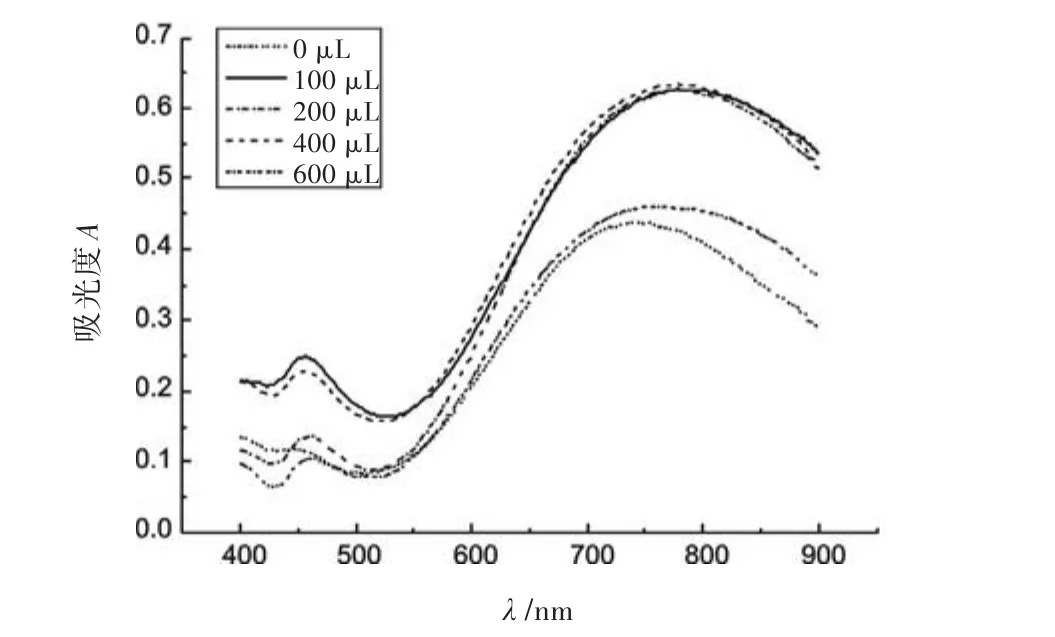
图5 CTMAB用量对吸光度的影响
CTMAB在本体系中起着增溶增敏作用,其机理是:①表面活性剂的阳离子和显色剂的络阴离子形成离子对,会形成长链铵胶束,增加其离解度,使溶液最大吸收红移。②季铵盐胶束的形成可起分散剂的作用,使这些离子对发生胶束增溶作用,使较多的显色络合物质点保持在水相,同时使光的吸收增大。③季铵盐的存在,使金属和有机配位体形成高配位数的络合物,灵敏度增加。
依据1.2.2实验方法,固定DES、CTMAB、FeCl3、K3[Fe(CN)6]溶液用量不变,改变各溶液加入的先后顺序,测体系摩尔吸光系数ε值。分别以如下的各试剂加入先后顺序做实验:
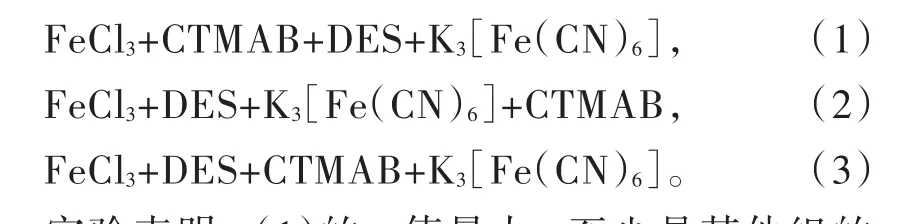
实验表明,(1)的ε值最大,至少是其他组的1.2倍,故各试剂加入先后顺序应按(1)的顺序加。CTMAB在(1)中能使FeCl3与DES之间的相互接触更充分,反应更完全,具有相转移催化作用。
2.3 标准曲线和检出限
依据1.2.2实验方法,准确加入不同体积的DES,绘制标准曲线(见图6)。

图6 标准曲线
DES的质量浓度在0.03256~0.6521 μg/mL范围内符合比尔定律,线性回归方程为A=0.0027+0.3990 ρ(μg/mL),相关系数R2=0.9991。
根据线性回归方程计算出DES摩尔吸光系数ε=5.43×105L/(mol·cm)。根据实验步骤,平行测定11份空白溶液,按照空白测得值的标准偏差的3倍除以工作曲线拟合方程斜率,求出其检出限为1.35 mg/L,相对标准偏差0.89%。
2.4 样品分析
准确称取2.0 g奶粉试样于10 mL具塞刻度离心管中,加4.0 mL乙腈混匀,超声提取20 min,后以4000 r/min离心10 min,取上清液静置,重复3次,合并上清液,40℃下用N2吹干,残余物用乙腈溶解并定容至2 mL,用于实验检测。
用空白奶粉试样进行添加回收实验,精密称取样品2.0 g,添加浓度为1.5 μg/mL DES标准液。按1.2.2实验方法测定空白和加标样品在736 nm处的吸光度,计算其回收率。测3次取平均值,回收率在89.3%~101.6%。
3 结论
利用DES具有将Fe(Ⅲ)还原成Fe(Ⅱ)的特性,探索了由CTMAB、Fe(Ⅱ)、K3[Fe(CN)6]等组成的多元络合体系为探针的可见分光光度法测试DES的新方法。实验表明DES的质量浓度在0.03256~0.6521 μg/mL范围内与吸光度呈良好线性关系,线性回归方程 A=0.0027+0.3990ρ(μg/mL),相关系数R2=0.9991,摩尔吸光系数ε=5.43×105L/(mol·cm)。CTMAB在该分析方法中具有催化和增敏作用。在对奶粉样品的加标实验中,回收率为89.3%~101.6%。
[1]罗板鑫,陈昌云.一种简单快速的己烯雌酚定性检测方法研究[J].中国教育技术装备,2012(6):126-127.
[2]杜志峰,黄金凤.动物肌肉组织中己烯雌酚残留量的液相色谱-串联质谱法测定[J].分析测试学报,2007,26(6):823-826.
[3]祝伟霞,刘亚风,袁萍,等.液相色谱-串联质谱法快速测定婴幼儿配方奶粉中39种激素残留量[J].色谱,2010,28(11):1031-1037.
[4]潘自红,马丹丹,李子贺,等.FeCl3-铁氰化钾体系分光光度法测定酚磺乙胺[J].分析试验室,2013,32(1):111-113.
[5]王瑶,周建华.食品中己烯雌酚的检测方法[J].食品工业科技,2012,2(33):373-375.
[6]张建华,张水凤.吸收光谱线型分析用于十六烷基溴化铵临界胶束浓度的测量[J].应用化学,2007,24(3):306-309.

