硫酸铵法硝酸磷肥生产高品质硫酸钙工艺研究
向 伟,王 勃,应建康
(四川大学化学工程学院,四川成都 610065)
硝酸磷肥是硝酸分解磷矿制得的含氮磷复合肥料,生产中可以不用硫酸,在硫资源缺乏地区有技术和经济优势[1]。在硝酸-硫酸(盐)法硝酸磷肥中,硫酸钙多作为磷石膏废物,或转化为硫酸铵予以利用,但流程长,投资大[2]。若分离硝酸分解磷矿液中酸不溶物后,再用硫酸铵结晶,能得到杂质少、纯度高的硫酸钙,则可满足磷石膏作为建筑材料、化工原料及水热合成高附加值硫酸钙晶须[3]的要求,实现工业资源化利用。硫酸钙晶体的质量和分解液除钙操作密切相关。粗大、规整的石膏晶体易过滤和洗涤,可减少杂质夹带,提高硫酸钙纯度、硬度等物理性质。控制条件,减少结晶过程沉积到硫酸钙晶格中的HPO42-(共晶磷)也是提高磷石膏品质的重要途径[4]。郑晓霞等[5]发现硫酸钙在高硝酸含量的硝酸-磷酸介质中的结晶细小化。为消除过量硝酸存在对硫酸钙结晶的影响,笔者用理论用量95%的硝酸分解磷矿(P2O5收率为98%),滤去酸不溶物后的滤液与硫酸铵反应,研究工艺条件对硫酸钙晶体大小、石膏过滤强度及共晶磷含量的影响,为实际生产提供数据参考。
1 实验
1.1 实验原料和仪器
昆阳磷矿硝酸分解液(组成见表1),硫酸铵(分析纯),乙二醇二乙醚二胺四乙酸(EGTA,分析纯),无水乙醇。

表1 昆阳磷矿硝酸分解液化学分析 %
电子天平,恒温水浴锅,电动搅拌器,250 mL玻砂漏斗,250 mL三角烧瓶,红外转速仪,真空抽滤泵,Nikon YS100型显微镜,72E型可见分光光度计。
1.2 实验步骤及表征
将加有50 mL酸解液的250 mL三角烧瓶在恒温水浴锅中加热至设定温度,在恒定搅拌速率下(100 r/min)将预热的硫酸铵溶液滴加到烧瓶中反应至指定时间。取少量硫酸钙晶体于载玻片上用无水乙醇置换水并分散,在显微镜(400倍数)下观测晶体形貌。将反应液全部转移至250 mL玻砂漏斗中于-0.03 MPa下真空恒压抽滤,记录抽滤时间。用蒸馏水洗涤滤饼至滤液 pH=6.5~6.8[6],烘干,用偏钒酸铵分光光度法测定共晶磷含量[7]。进行反应结晶条件实验,确定适宜的反应结晶条件。将适宜条件下得到的硫酸钙结晶置于50℃的烘箱中烘干,研磨后取样进行XRD分析,确定硫酸钙结晶晶型的存在状态,并测定杂质含量。
2 实验结果及讨论
2.1 硫酸铵用量对硫酸钙结晶的影响
在温度为90℃,硫酸铵质量分数为30%,进料时间为20 min,反应时间为2 h的条件下,考察了硫酸铵用量对硫酸钙结晶的影响。显微镜观测发现,随着硫酸铵用量的增加,晶体由短小的棒状变为稍粗大的棒状,再到产生双晶体或者形成由若干个斜方六面晶形的柱形晶体按任意方向缔合在一起的多晶体,最后得到针状外形的晶体。硫酸铵用量为理论用量的110%时(下同),晶体尺寸大、形貌较为规整。硫酸铵用量对过滤时间和共晶磷含量的影响见图1。从图1中过滤时间的变化可以看出,在硫酸铵用量为110%时有较好的过滤强度。SO42-浓度不足或过量太多时,硫酸钙结晶过滤强度都下降。从图1还可知,随着硫酸铵用量的增加共晶磷取代降低。硫酸铵低于理论用量时,因HPO42-的几何形状非常接近SO42-,溶液中HPO42-易取代SO42-进入硫酸钙的结晶中,并形成磷酸氢钙与石膏的复盐(CaSO4·CaHPO4·4H2O)[4],阻碍了石膏结晶的成长,恶化结晶条件。随着硫酸铵用量的增加,溶液中剩余SO42-与Ca2+的盐析作用使CaSO4=Ca2++SO42-的反应平衡向左移动,减小了硫酸钙溶解度和极限过饱和度。另一方面,增加硫酸铵用量,又增大了溶液中硫酸钙的浓度。这两方面都加剧了溶液的过饱和度,使溶液易于超过极限过饱和度,核晶过程的频率增大,从而使晶体细小化。溶液的过饱和度增大,晶体成长速率增大,促进了硫酸钙晶体沿C轴方向成长的速率[4],从而得到针状外形的晶体。

图1 硫酸铵用量对过滤时间和共晶磷含量的影响
2.2 温度对硫酸钙结晶的影响
在硫酸铵用量为110%,硫酸铵质量分数为30%,进料时间为20 min,反应时间为2 h的条件下,考察了反应温度对结晶的影响。显微镜观察不同反应温度的硫酸钙晶体形貌发现,随反应温度升高,晶体由细小的针尖状变为棒状,再到斜方六面晶形的柱形晶体缔合的多晶体,最后形成粗大棒状及多个晶体聚集形成聚晶的硫酸钙结晶。不同温度的过滤时间和共晶磷含量变化如图2所示。由图2可知,随温度升高,过滤时间迅速减少。随温度升高,硫酸钙中共晶磷的含量显著降低。硫酸钙的饱和溶解度及极限过饱和度均随温度的升高而增大。随着温度升高,溶液中硫酸钙的浓度与饱和溶解度差值减小,硫酸钙晶体成长速率减慢。同时随着温度的升高,体系中硫酸钙的饱和溶解度与极限过饱和度的差值增大,故高温下溶液结晶进入饱和溶解度与极限过饱和度之间的频率增大,而超过极限过饱和度生成晶核的频率减小,核晶作用减弱,晶核生成频率下降。另一方面,温度升高,溶液的黏度减小,溶质由溶液主体扩散到晶体表面的阻力减小。因此较高的反应温度更有利于SO42-和Ca2+扩散到晶体表面,使晶体易于长大。
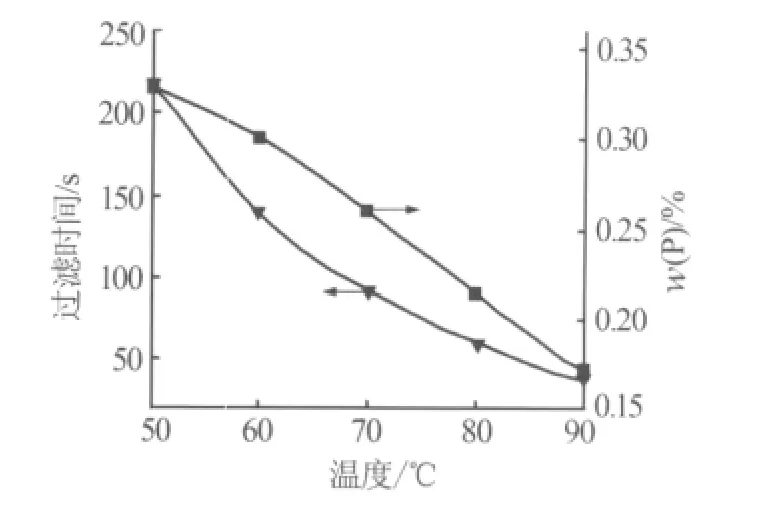
图2 温度对过滤时间和共晶磷含量的影响
2.3 硫酸铵浓度对硫酸钙结晶的影响
在硫酸铵用量为110%,反应温度为90℃,进料时间为20 min,反应时间为2 h的条件下,考察了硫酸铵质量分数对硫酸钙结晶的影响。显微镜观测不同硫酸铵质量分数时硫酸钙晶体的形貌发现:随硫酸铵溶液浓度增大,硫酸钙由粗大棒状晶体缔合的聚集变为夹杂有大量小棒状晶体的结晶。不同硫酸铵浓度下过滤时间和共晶磷含量变化见图3。由图3可知,低浓度硫酸铵将减少过滤时间。硫酸铵质量分数为30%时共晶磷取代作用较高浓度时小。随着硫酸铵浓度的增大,溶液的过饱和度升高,核晶频率增大,结晶细小化。同时,增大硫酸铵浓度使溶液黏度增大,传质扩散阻力增大,结晶条件恶化。

图3 硫酸铵浓度对过滤时间和共晶磷含量的影响
2.4 加料时间对硫酸钙结晶的影响
在硫酸铵用量为110%,反应温度为90℃,硫酸铵质量分数为30%,反应时间为2 h的条件下,考察了进料时间对硫酸钙结晶的影响。显微镜观测发现随着加料时间的延长,硫酸钙晶体由针尖状变为短小的棒状再到粗大棒状的缔合晶体。当加料时间增大到20 min后,晶体大小改变不大。不同加料时间下过滤时间和共晶磷含量变化见图4。由图4可知,增大加料时间将使过滤时间显著减少。硫酸钙中共晶磷含量随加料时间增加而显著降低。增大加料时间,单位时间进入反应体系的硫酸铵量减少,从而降低了溶液的过饱和度。
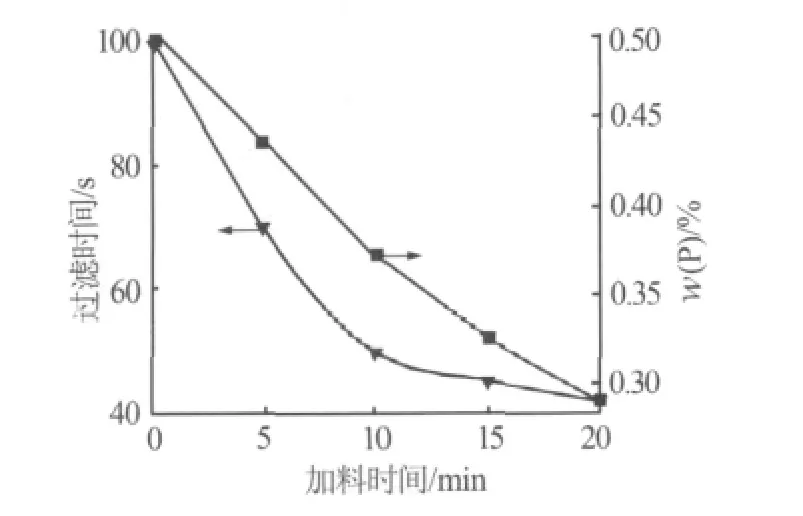
图4 加料时间对过滤时间和共晶磷含量的影响
2.5 反应时间对硫酸钙结晶的影响
在硫酸铵用量为110%,反应温度为90℃,硫酸铵质量分数为30%,进料时间为20 min的条件下,考察了反应时间对硫酸钙结晶的影响。不同反应时间下硫酸钙晶体显微镜观测结果表明:随着反应时间增加,硫酸钙晶体变化不大,但反应2 h时晶体稍大。不同反应时间下过滤时间和共晶磷含量变化见图5。由图5可知,反应2 h物料的过滤时间较短,石膏过滤强度较高。反应时间对共晶磷含量的影响与过滤时间变化同步。反应时间对硫酸钙晶体产生的影响,可能是由于溶液在90℃和此P2O5浓度下,由半水硫酸钙转化为无水硫酸钙的转化潜期和实际转化时间已足够长,使半水硫酸钙在反应时间内稳定存在,半水硫酸钙不能转化为细小无水物硫酸钙晶体,再延长反应时间则搅拌碰碎晶体的频率增大,过滤强度反而降低。
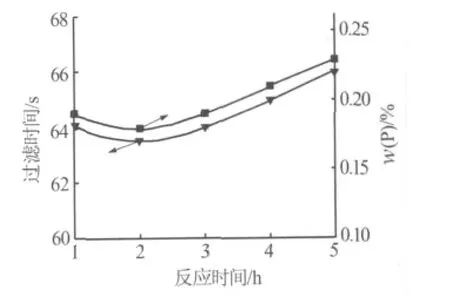
图5 反应时间对过滤时间和共晶磷含量的影响
2.6 试样XRD谱图分析与化学分析
用X射线衍射仪测定实验所得硫酸钙样品,并与标准衍射卡对照,根据特定衍射角出现的特征衍射峰,分析样品的物相组成和晶体结构。
硫酸钙试样X射线衍射结果如图6所示,其中A,B分别表示二水硫酸钙和半水硫酸钙的特征衍射峰。由图6可见,谱图上出现了较强的半水和二水硫酸钙特征衍射峰,硫酸钙的晶体并没有以单一的晶相存在,而是半水物和二水物的混合体。
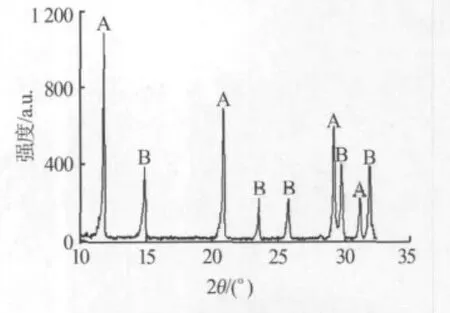
图6 硫酸钙试样XRD谱图
分析测定了试样硫酸钙化学成分,如表2所示。试样硫酸钙中主要杂质磷和氟的含量满足GB/T 23456—2009《磷石膏》中规定的磷石膏主要限量杂质 w(P)≤0.8%,w(F)≤0.5%的要求。

表2 试样硫酸钙化学分析 %
3 结论
昆阳磷矿硝酸酸解液和硫酸铵反应制备硫酸钙的适宜工艺条件为:硫酸铵用量为110%、硫酸铵质量分数为30%、反应温度为 90℃、加料时间为20 min、反应时间为2 h。在此条件下可得到粗大整齐、过滤强度高的以半水硫酸钙和二水硫酸钙混合晶型存在的硫酸钙结晶。化学分析表明硫酸钙中磷质量分数为0.179%、氟质量分数为0.06%,满足磷石膏杂质限量标准,纯度指标达到建筑石膏和纸面板石膏要求。实验表明在硝酸-磷酸介质中硫酸钙结晶主要受溶液的过饱和度影响。低过饱和度下,硫酸钙晶体粗大整齐,共晶磷含量少。共晶磷的取代程度和结晶条件相关联,结晶条件恶化,共晶磷含量增大。在实际生产中应降低溶液的过饱和度,以提供较好的结晶条件。
[1]丁德承.硝酸磷肥[M].北京:化学工业出版社,1980.
[2]Livingston O W.Recycling ammonium sulfate in nitric phosphate processing:US, 3515534 [P].1970-06-02.
[3]杨林,柏光山.磷石膏水热合成硫酸钙晶须的研究[J].化工矿物与加工,2010(3):16-19.
[4]吴佩芝.湿法磷酸[M].北京:化学工业出版社,1987.
[5]Zheng Xiaoxia,Jing Hongjian,Feng Junqiang,et al.Study on the solubility and morphology of calcium sulfate dihydrate in nitric acid and phosphoric acid aqueous medium[C]//International Conference on Mechanic Automation and Control Engineering,2010:3931-3934.
[6]许立信.高品质磷石膏生产工艺研究[J].化工矿物与加工,2004(5):28-30.
[7]徐静安,潘振玉.分析测试方法[M].北京:化学工业出版社,2000.

