硅基季铵化分离材料对Tc(Ⅶ)及U、Np、Pu的吸附行为研究
孔彦荣,贾永芬,李辉波,王孝荣,王 辉,娄海林
(中国原子能科学研究院,北京 102413)
锝主要是由反应堆中铀的热中子诱发裂变产生的放射性核素,其中99Tc是裂变产额较大的长寿命β放射性核素,半衰期为2.13×105a[1]。由于99Tc的半衰期长,且地球化学活性和生物转移活性大,是影响放射性废液进一步处理处置的重要核素之一。锝的化学行为复杂,在乏燃料后处理工艺流程中主要进入铀、钚等元素被分离后留下的废液中。含锝废液放射性活度大、溶液体积大,组分复杂且微量。另外,金属锝及其与钼的合金在低温下是超导体[2],99Tc也可以用于制备β放射源[3]。国内外对如何从放射性废液中分离锝有较多研究。
目前,国内乏燃料后处理流程产生的放射性废液都呈酸性(酸度为2~3mol/L),因此研究以阴离子交换法从酸性废液中提取Tc(Ⅶ)有重要意义。根据相关文献,采用离子交换法能实现从硝酸溶液体系中吸附分离 Tc(Ⅶ)[4-5],但后处理废液中微量铀、镎、钚等离子对硅基季铵化分离材料SiR4N从硝酸体系吸附Tc(Ⅶ)的影响未见有报道。SiR4N从硝酸溶液中静态吸附Tc(Ⅶ)的行为研究已证实,在0.50mol/L HNO3介质中,SiR4N对Tc(Ⅶ)的吸附分配系数为508,吸附平衡时间为35min,相比其他吸附材料有较好的吸附效果。在静态试验基础上,试验考察了溶液流速、穿透曲线参数等对SiR4N吸附Tc(Ⅶ)的影响,并通过考察SiR4N对铀、镎、钚的吸附情况,反推铀、镎、钚对SiR4N吸附Tc(Ⅶ)的影响。
1 试验部分
1.1 主要设备及试剂
玻璃离子交换柱:ø3mm×120mm,ø3.5 mm×210mm 等;KSY-12-12箱式高温炉,天津;LS-6000低本底液体闪烁仪,美国Bechman公司;分光光度计,PerlinElmer公司。
硅基阴离子交换剂[6](简称SiR4N),粒度15~25mm,自制;高锝酸铵,分析纯,美国橡树岭国家试验室;铀、镎、钚,中国原子能科学研究院。
1.2 溶液配制及试验方法
1.2.1 主要溶液的配制
TcO-4溶液的配制:用一定量高锝酸铵加水溶解而成。
Np(Ⅳ)溶液的制备:取纯的镎储备液,加入硝酸调节酸度至1mol/L,加入一定量1mol/L氨基磺酸亚铁将镎还原成Np(Ⅳ)。用等体积的TTA-二甲苯溶液萃取Np(Ⅳ),负载有机相中的Np(Ⅳ)用等体积的8mol/L HNO3反萃取至水相,转移水相待用。
Np(Ⅴ)溶液的制备:取Np(Ⅳ)储备液,加入1mL TTA,除去其中的Pa;然后转移水相至小烧杯中,加热至近干时加入浓硝酸溶解,再蒸发至近干,重复6次。用一定量0.05mol/L NaNO2-0.1 mol/L HNO3溶解并转移至萃取管中备用。
Np(Ⅵ)溶液的制备:取Np(Ⅳ)储备液,加入1mL TTA,除去其中的Pa;然后转移水相至小烧杯中,加热至近干时加入浓硝酸溶解,再蒸发至近干,重复6次。用1mol/L硝酸溶解,转移至萃取管中备用。
1.2.2 试验方法
静态试验:称取0.02g SiR4N,用0.5mol/L硝酸溶液浸泡24h,调整酸度,加入配制的铀、镎、钚溶液,恒温(25±1)℃下静态吸附。分析溶液中铀、镎、钚浓度,计算分配系数Kd和吸附率E。
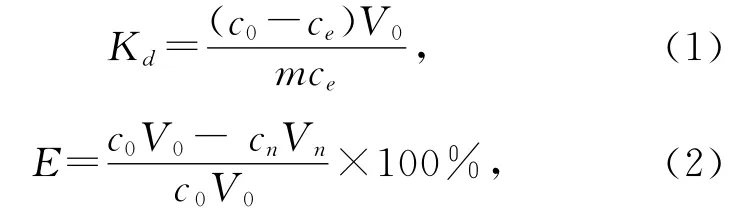
式中:c0—起始溶液中被吸附离子浓度,mmol/L;V0—起始溶液体积,mL;cn—吸附后溶液中被吸附离子浓度,mmol/L;Vn—吸附后溶液体积,mL;ce—吸附平衡时溶液中被吸附离子浓度,mmol/L;m—树脂质量,g。
动态吸附试验在玻璃离子交换柱中进行。称取一定质量SiR4N,用0.50mol/L硝酸浸泡24 h,然后湿法装柱。将配制好的料液以一定流速通过离子交换柱,每隔一定时间收集流出液,分析其中待测元素浓度,计算吸附率。
1.3 分析方法
溶液中只存在单一元素时,用LS-6000低本底液体闪烁谱仪测其计数,并换算浓度;铀、镎、钚、锝同时存在时,具体分析方法如下。
1)总镎的分析:取一定量溶液,调节酸度至1.0mol/L HNO3,加氨基磺酸亚铁将钚、镎、铀分别转化成Pu(Ⅲ)、Np(Ⅳ)、U(Ⅵ),用 TTA-二甲苯溶液萃取;然后取一定体积有机相制源,以α能谱法测定其中镎的浓度。
2)钚的分析:取一定量溶液,调酸度至1.0 mol/L HNO3,加入1.0mol/L亚硝酸钠,放置,然后加入TTA-二甲苯溶液定量萃取钚。取一定量有机相制源,以α能谱法测定其中钚的浓度。
3)锝的分析:取一定量溶液,加入碳酸钾至浓度为2.0mol/L,然后用1.0mL三甲基吡啶萃取振荡2.0min,离心分相后,取一定量有机相加入闪烁液,用LS-6000低本底液体闪烁谱仪测其计数,根据标准曲线计算锝浓度。
4)U(Ⅵ)的分析:取0.5mL溶液加入5.0mL容量瓶中,依次加入掩蔽剂、缓冲溶液、显色剂、去离子水,用无水乙醇稀释至刻度,摇匀,放置30min后,取3.0mL加入到比色皿中,用分光光度计在575nm处测量吸光度,计算U(Ⅵ)的浓度。
2 试验结果与讨论
2.1 溶液流速对SiR4N吸附Tc(Ⅶ)的影响
称取0.02g SiR4N(干)湿法装柱,将0.5 mol/L HNO3-10.1mg/L TcO-4溶液以3.58 cm/min的速度流经离子交换柱(ø4.0mm×210 mm),直至Tc(Ⅶ)穿透。再称取0.02g SiR4N重新湿法装柱,降低流速至3.18cm/min进行吸附。两次吸附流出曲线如图1所示。

图1 不同流速下,SiR4N对TcO-4的吸附曲线
从图1看出:流出液中锝质量浓度随流出液体积增大而增大;流速越快,流出液中锝质量浓度增加的越快,表明同样体积树脂所能处理的含锝废液的体积随流速增大而减小。这是因为,随溶液流速增大,液体流经树脂床层的时间减少,有可能导致离子交换尚未达到平衡。试验中,后续料液进柱流速均小于3.18cm/min。
2.2 料液酸度对SiR4N吸附Tc(Ⅶ)的影响
静态吸附试验结果表明:料液中硝酸浓度≥2 mol/L时,SiR4N对Tc(Ⅶ)的吸附分配系数≤48;硝酸浓度≤1mol/L时,SiR4N对 Tc(Ⅶ)的吸附分配系数≥160。国内大部分放射性废液的酸度为2~3mol/L,如果用离子交换法去除Tc(Ⅶ),则废液酸度要调至≤1mol/L。为了考察料液酸度的影响,试验分别配制0.50mol/L HNO3-124.0mg/L TcO-4和1.0mol/L HNO3-122.0TcO-4mg/L料液,均以2.0cm/min的速度流经离子交换柱(ø3.5mm×210mm)。流出液中Tc(Ⅶ)质量浓度与流出液体积的关系如图2所示。可以看出,料液酸度越高,吸附效果越差。
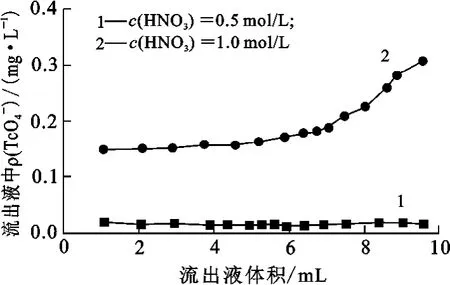
图2 料液酸度对SiR4N吸附Tc(Ⅶ)的影响
2.3 解吸剂硝酸浓度对TcO-4解吸的影响
将0.50mol/L HNO3-7.86mg/L TcO-4料液5.0mL以2.07cm/min的流速通过离子交换柱,然后用0.50mol/L硝酸洗涤,用不同浓度硝酸淋洗。每隔一定时间收集流出液,分析其中TcO-4质量浓度。不同浓度硝酸溶液的淋洗曲线如图3所示。
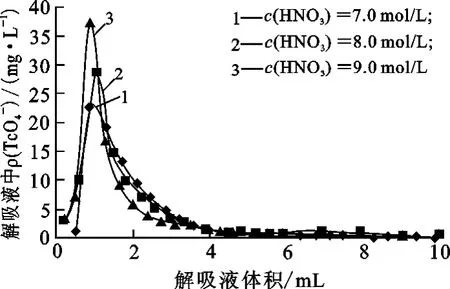
图3 不同酸度下,吸附在SiR4N上的Tc(Ⅶ)的解吸曲线
由图3看出:酸度越高,解吸液流出半高峰宽度越小,解吸效果越好,产生的废液量也越少;硝酸浓度为8.0mol/L和7.0mol/L的解吸曲线相差不大,解吸率均大于97%。但解吸液酸度高会给后续脱硝带来负担,因此,以下试验中硝酸浓度均选择7.0mol/L。
2.4 SiR4N对Tc(Ⅶ)的吸附穿透曲线
穿透曲线能反映吸附料液组分、浓度、操作方式及一定温度下吸附材料的交换区高度、吸附容量等参数。交换区高度计算公式[7]为:
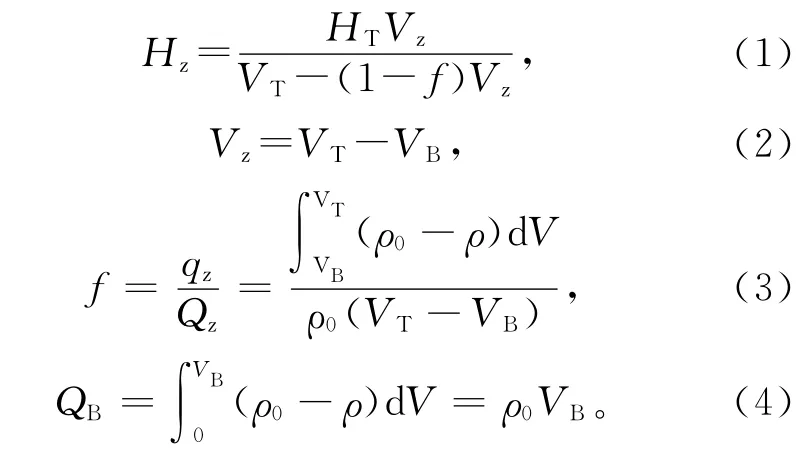
其中:Hz—交换区高度,cm;VT—饱和点流出液体积,mL;VB—穿透点流出液体积,mL;ρ0—初始质量浓度,mg/L;ρ—流出液中质量浓度,mg/L;HT—吸附材料床层高度,cm;QB—吸附材料操作交换容量,mg/g(干)。
将0.53mol/L HNO3-162.0mg/L TcO4-料液以2.07cm/min的流速通过离子交换柱(φ3.5 mm×120mm),吸附曲线如图4所示。
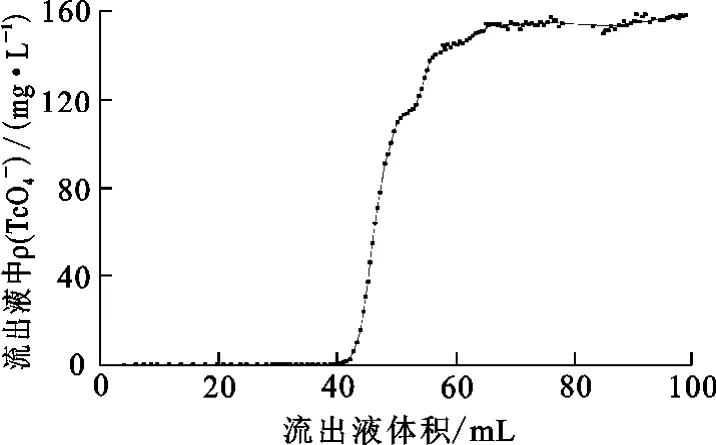
图4 SiR4N吸附Tc(Ⅶ)的穿透曲线
离子交换前后,吸附材料平均高度为40 mm,穿透点按照0.04ρ0、饱和点按0.95ρ0计,交换区高度及操作容量计算结果见表1。

表1 SiR4N对Tc(Ⅶ)的吸附交换参数
2.5 U、Np、Pu对SiR4N吸附Tc(Ⅶ)的影响
考虑到后处理废液中可能含有微量的铀、镎、钚,因此在上述工作基础上,考察了铀、镎、钚对SiR4N吸附Tc(Ⅶ)的影响。鉴于条件限制,试验只考察了单体系条件下SiR4N对铀、镎和钚的吸附情况,根据试验结果,反推铀、镎和钚对SiR4N吸附Tc(Ⅶ)的影响。
2.5.1 SiR4N对U(Ⅵ)的吸附行为
2.5.1.1 吸附时间对SiR4N吸附U(Ⅵ)的影响
吸附液体积为3mL、U(Ⅵ)质量浓度为50.0 mg/L,硝酸浓度为 0.5mol/L,SiR4N 质量为0.02g(干)(以下静态试验SiR4N质量均相同),恒温(25±1)℃下静态吸附。试验结果见表2。
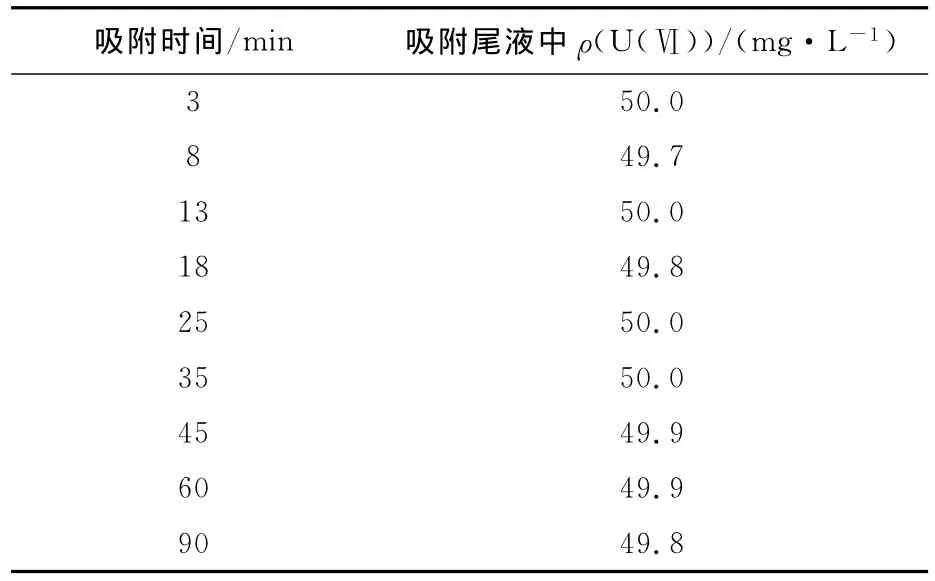
表2 吸附时间对SiR4N吸附U(Ⅵ)的影响
由表2看出:随吸附时间延长,溶液中U(Ⅵ)的质量浓度变化不大,表明硝酸浓度为0.50 mol/L时,SiR4N几乎不吸附U(Ⅵ)。这主要是因为U(Ⅵ)在酸性溶液中主要以UO2+2形式存在,其不与吸附剂发生离子交换反应。
2.5.1.2 硝酸浓度对SiR4N吸附U(Ⅵ)的影响
吸附体系酸度不同,体积为3mL,ρ(U(Ⅵ))=15.0mg/L,恒温静态吸附至平衡(90min)。试验结果见表3。
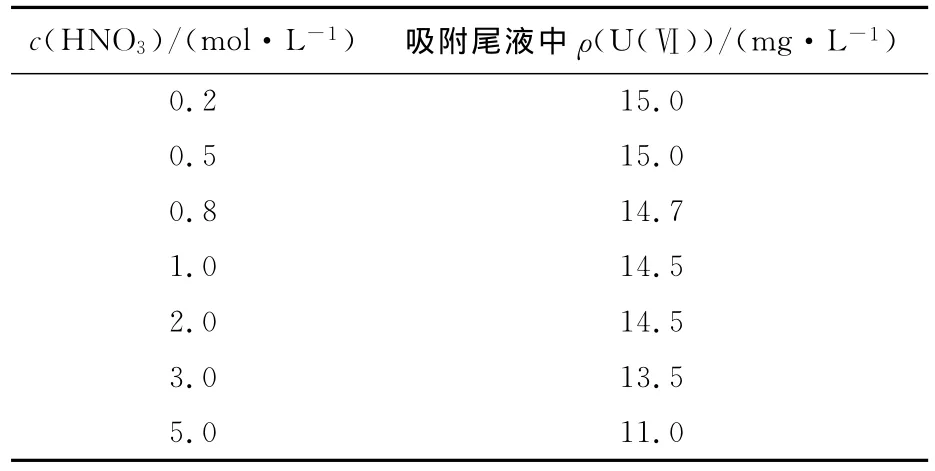
表3 硝酸浓度对SiR4N吸附U(Ⅵ)的影响
由表3可以看出:随硝酸质量浓度增大,吸附尾液中U(Ⅵ)质量浓度逐渐减小,但变化平缓;低酸度时,硝酸浓度对SiR4N吸附U(Ⅵ)的影响很小。
2.5.2 SiR4N对Pu(Ⅳ)的吸附行为
2.5.2.1 吸附时间对SiR4N吸附Pu(Ⅳ)的影响
吸附液体积为3mL,Pu(Ⅳ)质量浓度为1.08mg/L,硝酸酸度为0.5mol/L。吸附时间对SiR4N吸附Pu(Ⅳ)的影响如图5所示。可以看出,吸附90min后,SiR4N对微量Pu(Ⅳ)的吸附率趋于不变,说明吸附达到平衡。相比而言,SiR4N对微量Pu(Ⅳ)的吸附平衡时间远大于对Tc(Ⅶ)的吸附平衡时间,即对微量Pu(Ⅳ)的吸附速度远小于对Tc(Ⅶ)的吸附速度。
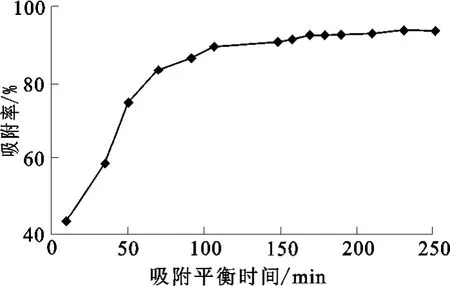
图5 SiR4N对Pu(Ⅳ)的吸附平衡曲线
2.5.2.2 硝酸浓度对SiR4N吸附Pu(Ⅳ)的影响
溶液体积为3mL,ρ(Pu(Ⅳ))=1.08mg/L,恒温静态吸附至平衡(90min)。硝酸浓度对SiR4N吸附Pu(Ⅳ)的影响试验结果如图6所示。
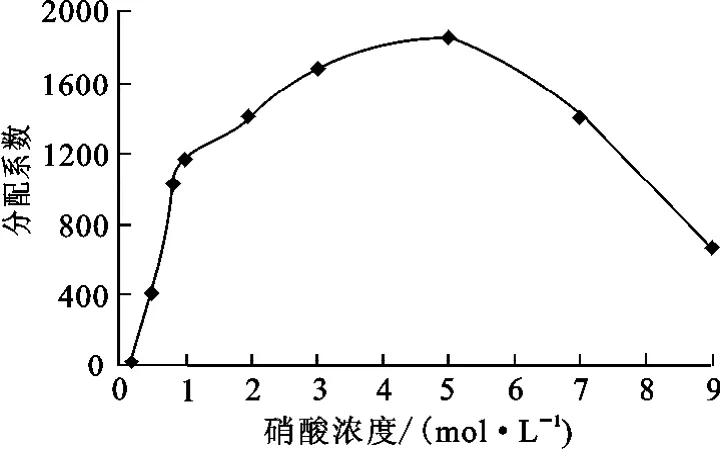
图6 HNO3浓度对SiR4N吸附Pu(Ⅳ)的影响
由图6可知:硝酸浓度小于5mo/L时,随硝酸浓度增大,SiR4N对Pu(Ⅳ)的吸附分配系数增大;硝酸浓度大于5mol/L时,随硝酸浓度增大,分配系数反而下降。这是因为随溶液中[H+]增大,H+与[Pu(NO3)6]2-形成[HPu(NO3)6]-或H2Pu(NO3)6的趋势增大,能够与SiR4N发生阴离子交换的钚络合阴离子的量减少,从而降低了SiR4N 对Pu(Ⅳ)的吸附分配系数[6]。
2.5.3 SiR4N对不同价态镎的吸附行为
2.5.3.1 吸附时间对SiR4N吸附Np(Ⅳ)、Np(Ⅴ)、Np(Ⅵ)的影响
Np(Ⅳ)、Np(Ⅴ)、Np(Ⅵ)的质量浓度均为20mg/L,溶液体积3mL,硝酸浓度均为0.5 mol/L。吸附时间对SiR4N 吸附 Np(Ⅳ)、Np(Ⅴ)、Np(Ⅵ)的影响如图7所示。
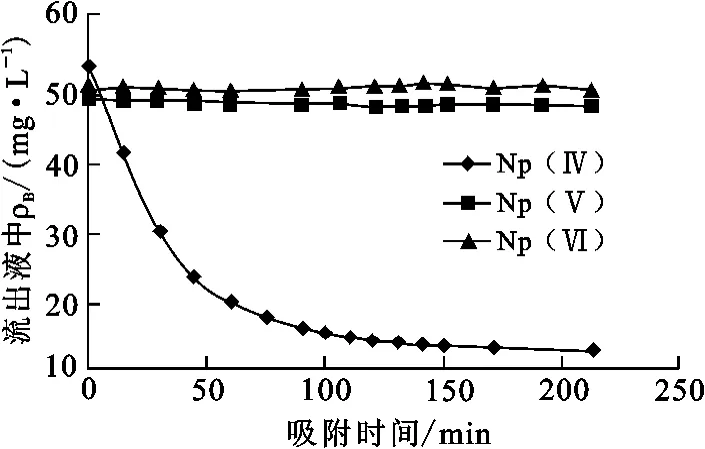
图7 SiR4N对Np(Ⅳ)、Np(Ⅴ)、Np(Ⅵ)的吸附平衡曲线
由图7看出:随吸附时间延长,Np(Ⅳ)的残余质量浓度逐渐减小,即SiR4N对Np(Ⅳ)的吸附率逐渐增大,吸附2h后基本达到平衡;SiR4N基本不吸附Np(Ⅴ)和Np(Ⅵ)。
2.5.3.2 硝酸浓度对SiR4N吸附Np(Ⅳ)、Np(Ⅴ)、Np(Ⅵ)的影响
Np(Ⅳ)、Np(Ⅴ)、Np(Ⅵ)的质量浓度分别为54.1、47.7、52.1mg/L,溶液体积均为3mL,恒温静态吸附至平衡(90min)。硝酸浓度对SiR4N吸附Np(Ⅳ)、Np(Ⅴ)、Np(Ⅵ)的影响如图8所示。
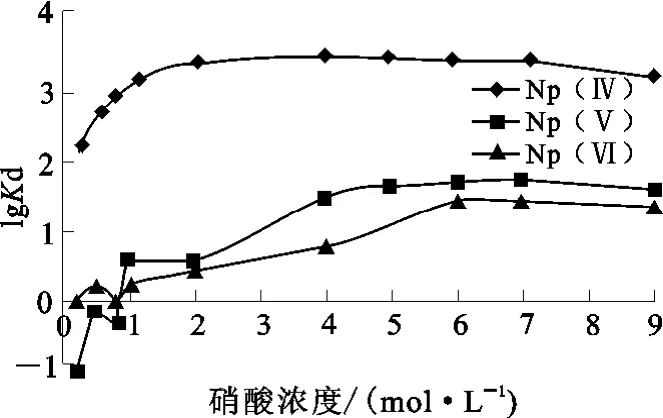
图8 HNO3浓度对SiR4N吸附Np(Ⅳ)、Np(Ⅴ)、Np(Ⅵ)的影响
由图8看出,硝酸浓度在0.2~9.0mol/L范围内,SiR4N对Np(Ⅴ)、Np(Ⅵ)的吸附分配系数均小于60,而SiR4N对Np(Ⅳ)的吸附分配系数最大达2 903。与硝酸浓度对SiR4N吸附微量Pu(Ⅳ)的影响相似:当硝酸浓度小于5mo/L时,随硝酸浓度增大,SiR4N对Np(Ⅳ)的吸附分配系数增大;当硝酸浓度大于5mol/L时,随硝酸浓度增大,分配系数反而下降。
2.6 模拟料液吸附试验
配制含铀、钚、锝3种离子的模拟料液,其中铀、钚、锝的质量浓度分别为5.48、4.11和14.08 mg/L,溶液中硝酸浓度为0.55mol/L。将40mL模拟料液连续通过装有SiR4N的离子交换柱(φ3 mm×120mm),层高为26mm,流速为2.0cm/min。吸附后,依次用0.5mol/L硝酸溶液洗涤,用7mol/L硝酸溶液解吸试验结果如图9所示。
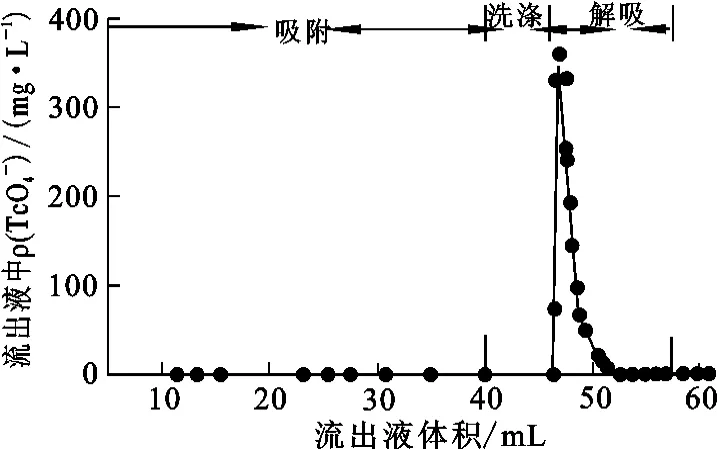
图9 SiR4N对模拟料液的吸附、解吸行为曲线
从图9看出:模拟料液中约99.8%的Tc(Ⅶ)被吸附在SiR4N上;约7.0mL硝酸溶液(7.0 mol/L)就可以解吸99.99%的 Tc(Ⅶ)。SiR4N在吸附Tc(Ⅶ)的同时,料液中95%的Pu(Ⅳ)也被吸附,但在洗涤流出液和解吸流出液中没有检测到Pu(Ⅳ);微量铀不被SiR4N吸附。由此说明,SiR4N能够很好地吸附废液中的锝,实现锝与锕系元素的分离。
3 结论
1)试验结果表明:SiR4N对Tc(Ⅶ)的交换容量为21.8mg/g(干);用7.0mol/L HNO3可以解吸吸附在SiR4N上的Tc(Ⅶ),解吸率大于99.9%。
2)在0.50mol/L HNO3溶液体系中,SiR4N不吸附 U(Ⅵ)、Np(Ⅴ)和Np(Ⅵ),而对Np(Ⅳ)、Pu(Ⅳ)的吸附率较高。Np(Ⅳ)、Pu(Ⅳ)和Tc(Ⅶ)同时在0.5mol/L HNO3介质中被SiR4N吸附后,用7.0mol/L HNO3溶液解吸Tc(Ⅶ)时,Np(Ⅳ)和Pu(Ⅳ)不被解吸,Tc(Ⅶ)可以与Np(Ⅳ)、Pu(Ⅳ)很好分离。
3)对于成分复杂的后处理放射性废液,利用离子交换法提取Tc(Ⅶ)后,再通过蒸馏、脱硝等工艺可以提纯锝。
[1]Firestone Richard B,Shirley Virginia S,Baglin Coral M,et al.Table of Isotopes[M].8th ed.New York:John Wiley and Sons,1996:695.
[2]谢高阳,俞练民,刘本耀,等.锰分族 铁系 铂系[M]//张青莲.无机化学丛书:第九卷.北京:科学出版社,1996:80.
[3]Schwochau Klaus.Technetium Chemistry and Radiopharmaceutical Applications[M].Weinheim:Wiley-VCH,2000:87.
[4]Suh Moo Yul,Lee Chang Heon,Han Sun Ho,et al.Separation and Determination of Technetium-99in Spent PWR Nuclear Fuels[J].Bull Korean Chem Soc,2003,24(11):1686-1688.
[5]Zilberman B Ya,Pokhitonov Yu A,Kirshin M Yu,et al.Prospects for Development of A Process for Recovering Technetium From Spent Fuel of Nuclear Power Plants[J].Radiochemistry,2007,49(2):156-161.
[6]李辉波,叶国安,王孝荣,等.硅基季铵化分离材料对Pu(IV)的吸附性能及机理研究[J].核化学与放射化学,2010,32(2):65-69.
[7]姜志新,宋正孝,竟清.离子交换分离工程[M].天津:天津大学出版社,1992:157-170.

