还原半反应的相关热力学计算湖北省教育厅重点科技
余高奇 陈阳 李凤莲
(武汉科技大学化学工程与技术学院 湖北武汉 430081)
还原半反应的相关热力学计算湖北省教育厅重点科技
余高奇 陈阳 李凤莲
(武汉科技大学化学工程与技术学院 湖北武汉 430081)
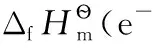
关键词还原半反应 热力学 电子的标准摩尔熵 热力学“0”标准
研究项目(No.2002A01018);湖北省优秀青年人才科研计划项目(No.2002B011004);武汉科技大学校教改项目(No.2007050X)
尽管还原半反应目前已经在氧化剂和还原剂相对强弱的比较、氧化还原反应进行方向的判断和氧化还原反应进行程度的衡量等领域得到了应用[1-3],但它的热力学研究仍略显欠缺,主要表现在:(1) H+(298.15K,aq,∞)的标准摩尔生成焓、标准摩尔生成吉布斯自由能及标准摩尔熵均规定为0的理由探讨不充分[4-6];(2) 离子的热力学数据与单质或化合物的热力学数据能否互相借用不明确[7-8];(3) 在还原半反应中,电子的角色及其对应的标准热力学数据研究不深入[9-10]。本文针对上述问题,拟从不同角度探讨还原半反应的热力学规律。
1 水溶液中,热力学“0”标准的选取




表1 质子及电子的标准热力学数据(298.15K,100kPa)[11-12]
2 离子的热力学数据与单质或化合物的热力学数据互相借用
离子的热力学数据与单质或化合物的热力学数据可以互相借用。这一点可由298.15K、100kPa时,水合氯离子的标准摩尔生成焓、标准摩尔吉布斯自由能及标准摩尔熵数据的获取说明。
设计原电池:
Pt∣Cl2(100kPa,g)∣Cl-(1.0mol·dm-3,aq)‖H+(1.0mol·dm-3,aq)∣H2(100kPa,g)∣Pt
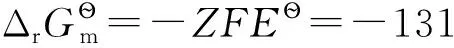
(2-1)
H2、Cl2是稳定单质,在298.15K时,它们的标准摩尔生成焓及标准摩尔吉布斯自由能均为0;同时298.15K时质子的标准摩尔生成焓和标准摩尔吉布斯自由能均为0,质子的标准摩尔熵也为0;另查热力学数据表可得298.15K时H2、Cl2的标准摩尔熵数据。
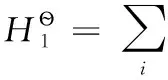
(2-2)
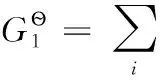
(2-3)
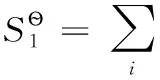
(2-4)
可以看出,离子的标准摩尔生成焓和标准摩尔生成吉布斯自由能数据是在承认稳定单质及质子的标准摩尔生成焓和标准摩尔生成吉布斯自由能均为0的前提下得到的;同时离子的标准摩尔熵是在认同稳定单质H2、Cl2的标准摩尔熵数据及质子的标准摩尔熵为0前提下所得。这些表明两套热力学数据可以互相借用。
3 还原半反应热力学计算公式
还原半反应:aOx+ne-=bRed;热力学计算时,电子可看成是一独立反应物,地位与氧化型物质Ox和还原型物质Red完全相同,相应计算公式为:

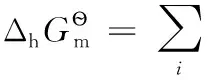
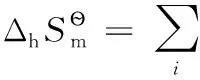

式中i代表氧化性物质Ox、电子及还原性物质Red中的任意一种。
4 不同类型电极的还原半反应计算实例
4.1 氧化还原电极之一
例:Fe3++e-=Fe2+,标准电极电势为EӨ=0.769V,相关热力学数据参见表2。


另:
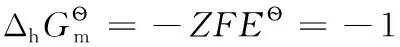

又因为

将有关数据代入得:

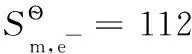

表2 一些物质的标准热力学数据(298.15K,100kPa)[16-17]
4.2 氧化还原电极之二

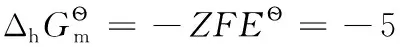
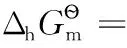






4.3 金属电极
例:Li++e-=Li,标准电极电势为EӨ=-3.040V,相关热力学数据参见表2。
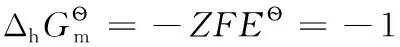





4.4 气体电极
例:2H++2e-=H2,标准电极电势为EӨ=0.000V,相关热力学数据参见表2。



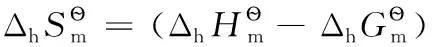


4.5 难溶氧化物电极
例:PbO2(s)+4H++2e-=Pb2++2H2O(l),标准电极电势为EӨ=1.458V,相关热力学数据参见表2。






4.6 难溶盐电极
例:AgCl(s)+e-=Ag(s)+Cl-,标准电极电势为EӨ=0.2222V,相关热力学数据参见表2。






由上述还原半反应热力学计算结果可得电子标准摩尔熵的平均值为:


以上热力学计算结果进一步证实:离子的热力学数据与单质或化合物的热力学数据可以互相借用;在298.15K及标态下,还原半反应中电子的标准摩尔生成焓、标准摩尔生成吉布斯函数变均为0,电子的标准摩尔熵近似为65.32J·mol-1·K-1,同时计算也表明了相关热力学计算公式的正确性。
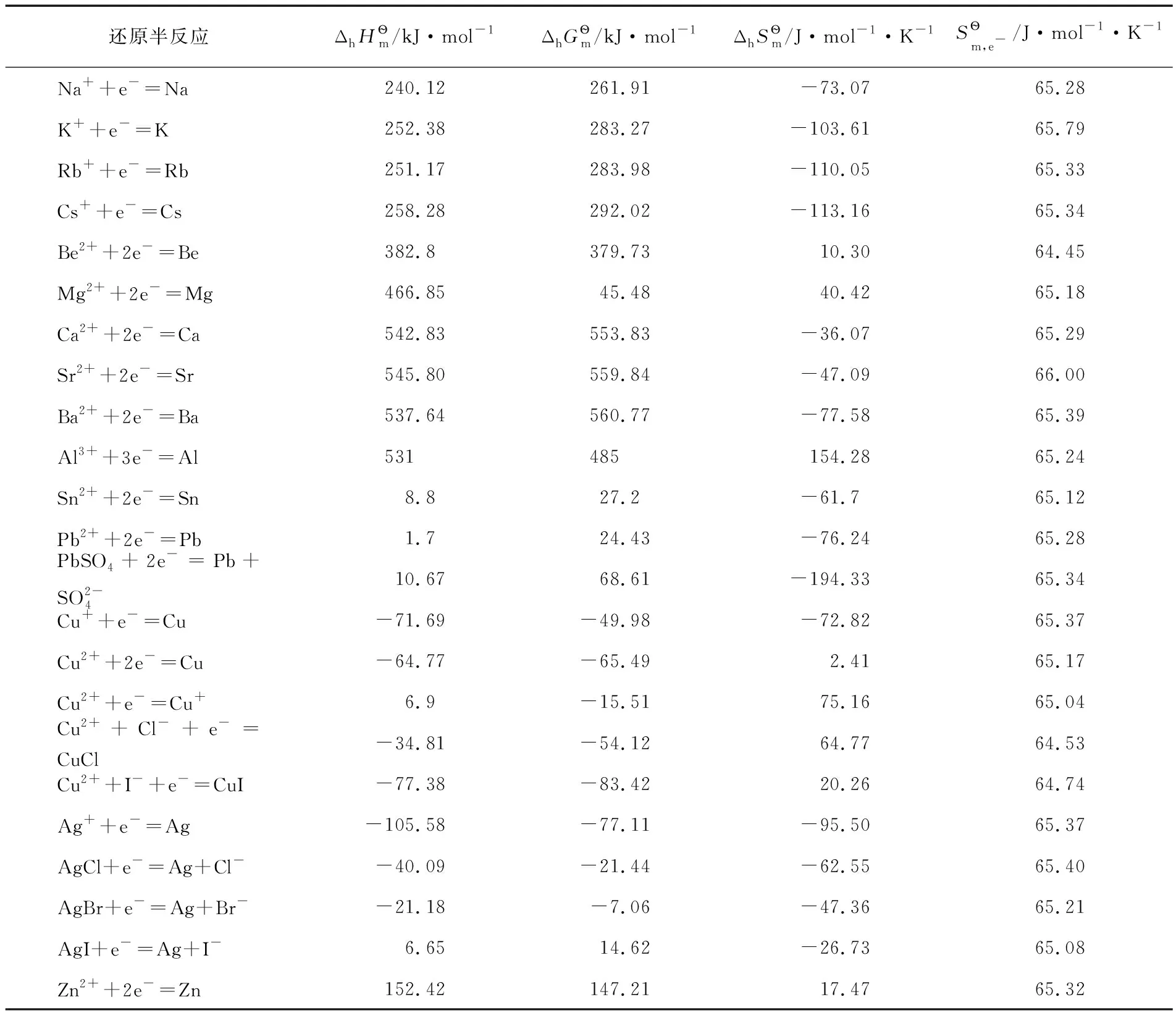
表3 还原半反应的标准摩尔焓变、标准摩尔吉布斯函数变、标准摩尔熵变及电子的标准摩尔熵

续表
5 结论
(2) 离子的热力学数据与单质或化合物的热力学数据可以互相借用。
(3) 还原半反应:aOx+ne-=bRed,相关热力学计算公式为:

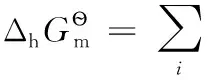
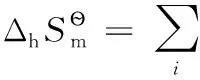
式中i代表氧化性物质Ox、电子及还原性物质Red中的任意一种。
参 考 文 献
[1] Jamroziak K,Jargulinski W.ArchMaterSciEng,2010,41(1):21
[2] Carleton A C,George K S.JGeol,1947,55(1):43
[3] 惠永基.高等学校化学学报,1989,10(7):775
[4] Branko R,Reinhardt E P,Melita L M,etal.JPhysChemA,2004,108(45):9979
[5] Vanderzee C E,Wauch D H,Hass N C,etal.JChemThermodyn,1980,12(1):27
[6] 李建宇.大学化学,2001,16(3):55
[7] Marky L A,Breslauer K J.Biopolymers,1987,26(9):1601
[8] Zwolinski B J,Danti A.AnnuRevPhysChem,1961,12:325
[9] Robaszkiewicz S,Micnas R,Chao K A.PhysRevB,1981,23:1447
[10] Galam S,Hansen J P.PhysRevA,1976,14:816
[11] Némethy O,Scheraga H A.JChemPhy,1962,36(12):3401
[12] Redlich O,Kister A T.IndEngChe,1948,40(2):345
[13] 天津大学物理化学教研室.物理化学.第5版.北京:高等教育出版社,2009
[14] Bassett R L.GeochimCosmochimActa,1980,44(8):1151
[15] Noyes R M.JAmChemSoc,1962,84(4):513
[16] 梁英教,车荫昌.无机物热力学数据手册.沈阳:东北大学出版社.1993
[17] 大连理工大学无机教研室.无机化学.第5版.北京:高等教育出版社,2006

