紫杉醇脂质体联合奥沙利铂和替吉奥方案治疗晚期胃癌临床观察
金时代,何靓,李俊,何湘,卢凯华*,刘平,束永前
(1.南京医科大学第一附属医院肿瘤科,南京 210029;2.南京医科大学第一附属医院消化科,南京 210029)
胃癌在我国发病率与病死率均居国内消化系统恶性肿瘤的首位。大多数患者早期症状不典型,就诊时往往疾病已进展至晚期,丧失了根治性手术的机会[1]。胃癌为化疗中度敏感的恶性肿瘤,Meta分析表明化疗可以延长晚期胃癌患者的整体生存时间,其中联合化疗较单药化疗的效果更加显著[2]。目前对于晚期胃癌的一线化疗,国内一般采用以5-氟尿嘧啶(5-Fu)和铂类(顺铂或奥沙利铂)及紫杉类药物联合的两药或三药方案。目前研究的热点在于如何合理地联合应用化疗药物,使其疗效提高的同时尽可能减轻毒性反应。
既往的临床研究已经证实紫杉醇在晚期胃癌中的疗效,但是因为采用聚氧乙基代蓖麻油和无水乙醇作为溶媒,易产生过敏等严重不良反应;而紫杉醇脂质体以磷脂和胆固醇为膜材,可以避免上述缺点[3]。本研究观察紫杉醇脂质体联合奥沙利铂和替吉奥方案一线治疗晚期胃癌患者,探讨其疗效及安全性,现报告如下。
1 资料与方法
1.1 临床资料
2011年2月~2013年1月本科收治的22例入组患者,均经病理学证实为胃腺癌,临床分期为局部晚期或转移的Ⅲb~Ⅳ期患者,或术后出现淋巴结或远处脏器转移,所有病例均有可测量病灶。其中男16例,女6例;年龄29~78岁,中位年龄59岁;原发部位:贲门5例,胃体8例,胃窦9例;转移部位中包括肝转移10例,肺转移3例,腹、盆腔淋巴结转移17例,锁骨上淋巴结转移4例,骨转移3例;其中1处转移10例,2处转移10例,3处及以上转移2例。一般状况(ECOG)评分为0~2分,预计生存期>3个月,化疗前血常规、肝肾功能及心电图检查基本正常,无外周神经疾病。
1.2 治疗方法
紫杉醇脂质体(商品名:力朴素,南京绿叶思科药业有限公司)175mg/m2,静脉滴注3h,第1天;奥沙利铂130mg/m2,静脉滴注2h,第2天;替吉奥胶囊(S-1)根据体表面积来确定初始剂量,体表面积<1.25m2给予40mg,bid,体表面积1.25~1.5m2给予50mg,bid,体表面积>1.5m2给予60mg,bid,早、晚饭后口服,连续服用14d,21d为1周期。在使用紫杉醇脂质体前30min给予地塞米松(5 mg,静滴)、苯海拉明(25mg,口服)、西咪替丁(400 mg,静滴)进行预处理。所有患者化疗前常规给予5-HT3受体拮抗剂预防呕吐,并予质子泵抑制剂保护胃黏膜,用药期间避免接触冰冷物质。在取得疾病控制者最多治疗6个周期,至少完成2个周期后进行疗效和毒副反应评价。如在化疗中出现Ⅲ级以上骨髓抑制,则在下一周期预防性应用粒细胞集落刺激因子;如出现Ⅳ度粒细胞减少性发热,Ⅲ度以上神经毒性和Ⅳ度口腔黏膜溃疡,则后续化疗药物剂量降低25%。
1.3 疗效及不良反应评价
近期疗效评价按RECIST实体瘤客观疗效评价标准进行[4],分为完全缓解 (CR)、部分缓解(PR)、稳定(SD)和进展(PD),客观缓解率(ORR)=CR+PR,疾病控制率(DCR)=CR+ PR +SD。毒副反应评价:毒副反应分级参照美国国立癌症研究所的药物毒性判定标准3.0版(NCI-CTC 3.0)[5]。肿瘤进展时间(TTP):开始用药至确定疾病进展的时间;总生存时间(OS):开始用药至死亡或末次随访时间。采用电话随访截至2013年7月20日,22例患者中无失访病例,中位随访时间为12.5个月。
1.4 统计学方法
采用SPSS 17.0统计软件进行数据处理,生存分析采用 Kaplan-Maier法,用Log-rank检验比较两组生存率,采用Fisher’s精确检验比较两组有效率,P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效
全部22例共完成82个周期化疗,平均3.7个周期,均可评价疗效,其中CR 0例,PR 10例,SD 9例,PD 3例,ORR为45.5%,DCR为86.4%。中位随访12.5个月(5.5~24个月),中位疾病进展时间(TTP)为5.1个月,中位生存时间(OS)为11.7个月(见图1、图2)。朱蔚友等[6]曾报道PFC(紫杉醇联合氟尿嘧啶和顺铂)方案治疗晚期胃癌25例,ORR为52%,中位TTP为6.5个月。本研究结果与其相比,疗效的差异无统计学意义(ORR:45.5%Vs 52%,P=0.772;TTP:5.1个月 Vs 6.5个月,P=0.880)(见表1)。
2.2 毒副反应
22例患者均可评价毒副反应。化疗的毒副反应以血液学毒性为主,白细胞下降发生率50%,Ⅲ~Ⅳ度白细胞降低发生率13.6%。非血液学毒性包括恶心呕吐、肌肉关节酸痛、外周神经毒性、脱发、肝功能损害、腹泻、手足综合症等,多为Ⅰ~Ⅱ度,无化疗相关性死亡病例(见表2)。

表1 两种方案治疗晚期胃癌疗效比较
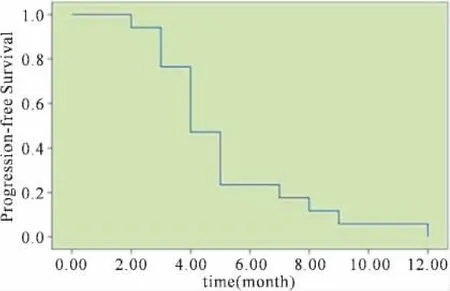
图1 所有患者无进展Kaplan-Meier生存曲线
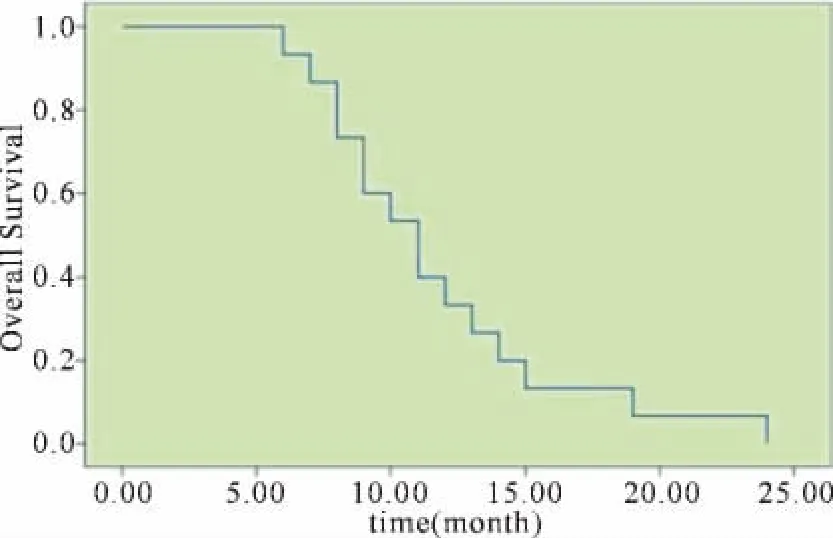
图2 所有患者总体Kaplan-Meier生存曲线
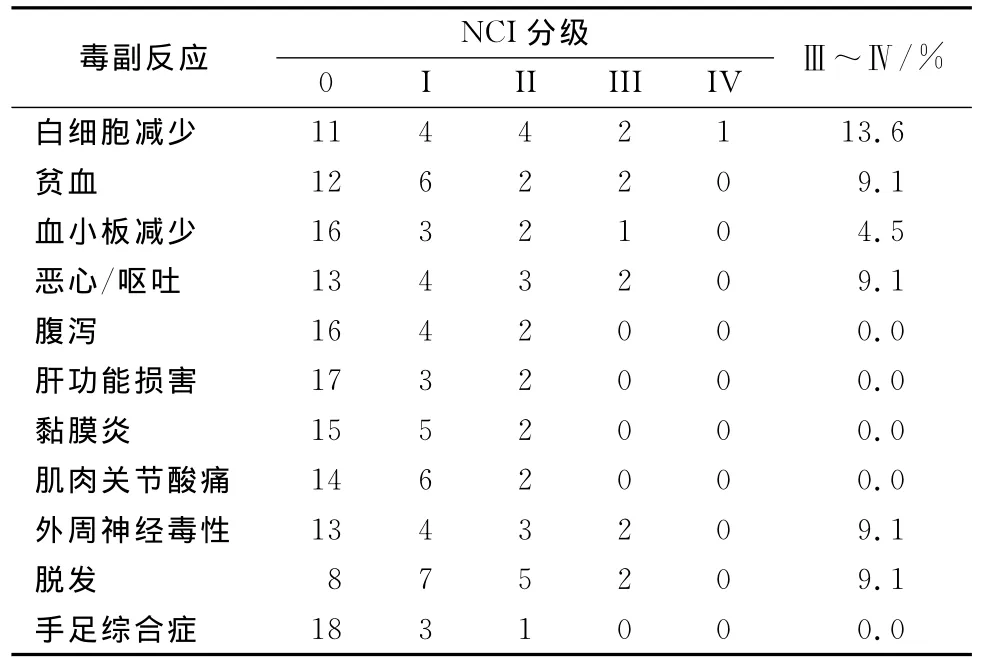
表2 紫杉醇脂质体联合奥沙利铂和替吉奥方案治疗晚期胃癌毒副反应(n)
3 讨论
胃癌仍是我国发病率和病死率居于前列的恶性肿瘤,且新发患者有年轻化的趋向[7]。胃癌发病时多无典型的临床表现,且大多数以低分化腺癌为主,易出现早期转移及术后复发。对于晚期胃癌,化疗是其主要的治疗手段。晚期胃癌的化疗目前尚无标准方案,以5-Fu及铂类为主的化疗方案仍是主要选择,且研究表明三药联合优于单药及二药联合,而其中以多西紫杉醇联合5-Fu及顺铂方案对进展期胃癌有显著疗效[8]。来自美国的多中心Ⅲ期临床研究(V325)结果表明[9],多西紫杉醇联合顺铂及5-Fu(DCF)方案与顺铂联合5-Fu(CF)方案比较,疾病进展期和总生存期均有显著延长。
紫杉醇与多西紫杉醇同属紫杉类化疗药,而紫杉醇脂质体将难溶于水的紫杉醇包封在新型药物载体-脂质体磷脂双分子层中,用卵磷脂等将紫杉醇进行包裹,在提高药物水溶性的同时明显降低变态反应的发生率[10]。另外,脂质体在肿瘤治疗中本身有很好的被动靶向作用[11],在提高疗效的同时还可降低毒性,减轻化疗药物对正常组织的损伤[12]。奥沙利铂是第三代铂类化疗药,在体内与DNA结合的速度较顺铂快10倍以上,具有更强的细胞毒作用,比顺铂有更广谱的抗癌活性,且与5-Fu有协同作用。奥沙利铂在胃癌中疗效确切,其剂量限制性毒副反应主要是外周神经毒性,多为可逆性,同时骨髓抑制和胃肠道反应轻,无肾毒性,不需要水化。在胃癌V325研究方案的基础上,我们尝试以紫杉醇脂质体代替多西紫杉醇、以奥沙利铂代替顺铂,目的在改善疗效的同时减轻化疗毒性反应,提高治疗的顺应性。
替吉奥是新型的氟尿嘧啶类口服制剂,由替加氟(FT)、吉美嘧啶(CDHP)和奥替拉西钾(OXO)以1∶0.4∶1摩尔比组成的复方制剂。FT是5-Fu的前体药物,在肝脏经细胞色素P450系统作用生成5-Fu,而发挥其抗肿瘤作用。CDHP是5-Fu分解代谢的关键酶-二氢嘧啶脱氢酶(DPD)的特异性抑制剂,能够阻止5-Fu降解,使5-Fu在血浆和肿瘤组织中能够更长时间地保持较高的稳定血药浓度,进而增强抗肿瘤活性。OXO主要对消化道内分布的乳清酸磷酸核糖转移酶有选择性拮抗作用,能阻断5-Fu磷酸化,减轻5-Fu引起的胃肠道毒副作用。与传统抗癌药物5-Fu相比,S-1不仅延长血液和肿瘤组织中5-Fu的药效时间以增加抗癌作用,还降低胃肠道等毒副作用,是新一代完全有效的抗癌药物。现有研究表明替吉奥单药治疗晚期胃癌的RR为21.2%,中位OS为15.7个月[13]。联合方案中报道较多的是替吉奥联合铂类(顺铂或奥沙利铂)或紫杉类药物(紫杉醇或多西他赛),联合化疗的近期有效率为37.8%~61.0%,中位PFS为5.0~6.8个月,中位OS为11.8~13.0个月,同时安全性较好[9,14-18,21]。
长期以来,肿瘤学界对于晚期胃癌化疗采用“两药”还是“三药”联合方案更优一直存有争论。以DCF方案和ECF(表柔比星+顺铂+5-Fu)方案为代表的“三药”方案理论上可以提高疗效,但同时必须面对毒性反应发生率高和患者耐受性差等问题。比如在V325研究[9]中,DCF方案Ⅲ~Ⅳ度粒细胞减少的发生率高达82.3%,粒细胞减少性发热的发生率为29%,从而导致患者难以耐受;另外5-Fu需要长时间持续静脉滴注,增加了静脉炎、静脉置管并发症等不良反应和住院治疗费用,患者依从性差。因此,上述“三药”改良方案的设计和研究应受到重视[19]。国际多中心的 REAL-2研究[20]目的就是对ECF方案的改良和优化,结果显示以奥沙利铂和卡培他滨分别取代顺铂和5-Fu疗效相当,且EOX(表柔比星+奥沙利铂+卡培他滨)方案安全性更好。
本研究采用“三药”联合方案,是基于对DCF方案改良和优化的考虑。采用紫杉醇脂质体较常规的紫杉醇或者多西紫杉醇毒性降低,奥沙利铂的胃肠道反应和肾毒性也显著低于顺铂;替吉奥可以门诊口服给药,避免了5-Fu持续静脉泵输注带来的不便和可能的并发症(如静脉血栓形成等),耐受性更好。研究结果显示,紫杉醇脂质体联合奥沙利铂和替吉奥治疗晚期胃癌总有效率为45.5%,疾病控制率为86.4%,中位TTP为5.1个月,中位OS为11.7个月。该方案治疗晚期胃癌疗效与我科既往报道的PFC(紫杉醇联合氟尿嘧啶和顺铂)方案[6]相比,差异无统计学意义,同时毒副反应可以耐受、安全性更好。研究结果提示紫杉醇脂质体联合奥沙利铂和替吉奥方案治疗晚期胃癌疗效较高,毒副反应较轻,多数患者耐受良好,值得今后扩大样本继续观察并进一步开展多中心、随机对照研究。
[1]Siegel R,Naishadham D,Jemal A.Cancer statistics,2013[J].CA:A Cancer Journal for Clinicians,2013,63(1):11-30.
[2]Wagner AD,Grothe W,Haerting J,etal.Chemotherapy in advanced gastric cancer:a systematic review and metaanalysis based on aggregate data[J].Journal of Clinical Oncology,2006,24(18):2903-2909.
[3]Xu X,Wang L,Xu HQ,etal.Clinical Comparison between Paclitaxel Liposome(Lipusu)and Paclitaxel for Treatment of Patients with Metastatic Gastric Cancer[J].Asian Pacific Journal of Cancer Prevention,2013,14(4):2591-2594.
[4]杨学宁,吴一龙.实体瘤治疗疗效评价标准-RECIST[J].循证医学,2004,4(2):85-90.
[5]Trotti A,Colevas AD,Setser A,etal.CTCAE v3.0:development of a comprehensive grading system for the adverse effects of Cancer treatment[J].Semin Radiat Oncol,2003,13(3):176-181.
[6]朱蔚友,金时代,束永前,等.紫杉醇联合氟尿嘧啶和顺铂方案治疗晚 期 胃 癌 [J].临 床 肿 瘤 学 杂 志,2005,10(5):489-491.
[7]吴春晓,郑莹,鲍萍萍,等.上海市胃癌发病流行现况与时间趋势分析[J].外科理论与实践,2008,13(1):24-29.
[8]Park SC,Chun HJ.Chemotherapy for Advanced Gastric Cancer:Review and Update of Current Practices[J].Gut and Liver,2013,7(4):385-393.
[9]Van Cutsem E,Moiseyenko VM,Tjulandin S,etal.Phase III study of docetaxel and cisplatin plus fluorouracil compared with cisplatin and fluorouracil as first-line therapy for advanced gastric cancer:a report of the V325Study Group[J].Journal of Clinical Oncology,2006,24(31):4991-4997.
[10]Straubinger RM,Arnold RD,Zhou R,etal.Antivascular and antitumor activities of liposome-associated drugs [J].Anticancer Res,2004,24(2a):397-404.
[11]Harrington KJ,Mohammadtaghi S,Uster PS,etal.Effective targeting of solid tumors in patients with locally advanced cancers by radiolabeled pegylated liposomes[J].Clinical Cancer Research,2001,7(2):243-254.
[12]Al-Batran SE,Hartmann JT,Probst S,etal.Phase III trial in metastatic gastroesophageal adenocarcinoma with fluorouracil,leucovorin plus either oxaliplatin or cisplatin:a study of the Arbeitsgemeinschaft Internistische Onkologie[J].Journal of Clinical Oncology,2008,26(9):1435-1442.
[13]Koizumi W,Akiya T,Sato A,etal.Phase II study of S-1as first-line treatment for elderly patients over 75years of age with advanced gastric cancer:the Tokyo Cooperative Oncology Group study [J].Cancer Chemotherapy and Pharmacology,2010,65(6):1093-1099.
[14]Koizumi W,Takiuchi H,Yamada Y,etal.Phase II study of oxaliplatin plus S-1as first-line treatment for advanced gastric cancer(G-SOX study)[J].Annals of Oncology,2010,21(5):1001-1005.
[15]Liu B,Ying J,Luo C,etal.S-1combined with oxaliplatin as first line chemotherapy for chinese advanced gastric cancer patients[J].Hepato-Gastroenterology,2012,59 (114):649-653.
[16]Luo H,Yu Z,Gao H,etal.Efficacy and tolerability of docetaxel and cisplatin plus S-1for advanced gastric cancer[J].J BUON,2013,18(1):154-161.
[17]Huang D,Ba Y,Xiong J,etal.A multicentre randomised trial comparing weekly paclitaxel+ S-1with weekly paclitaxel+5-fluorouracil for patients with advanced gastric cancer[J].Eur J Cancer,2013,49(14):2995-3002.
[18]Shigeyasu K,Kagawa S,Uno F,etal.Multicenter phase II study of S-1and docetaxel combination chemotherapy for advanced or recurrent gastric cancer patients with peritoneal dissemination[J].Cancer Chemother Pharmacol,2013,71(4):937-943.
[19]Keskin S,Yildiz I,Sen F,etal.Modified DCF(mDCF)regimen seems to be as effective as original DCF in advanced gastric cancer(AGC)[J].Clin Transl Oncol,2013,15(5):403-408.
[20]Cunningham D,Okines AF,Ashley S.Capecitabine and oxaliplatin for advanced esophagogastric Cancer[J].N Engl J Med,2010,362(9):858-859.
[21]温爱萍.奥沙利铂联合5-氟尿嘧啶及亚叶酸钙治疗晚期胃癌的疗效研究[J].中国医药导报,2013,10(10):87-89.

