有机硼化合物的分类和名称
聂永 苗金玲
(济南大学化学化工学院 山东济南250022)
有机硼(organoboron)化合物是指一类含有硼碳键的有机化合物。近年来,研究有机硼化合物的化学——有机硼化学发展很快。有机硼化合物的成键和结构类型多样,具有独特的物理和化学性质,在有机合成、药物化学、新型材料、生命科学等领域有广泛的应用。
在许多教科书和参考资料中,对有机硼化合物的分类方法不尽相同,一般有广义和狭义的两种[1]。按照广义的分类方法[1-3],除了含有硼碳键的化合物之外,还包括有机硼化合物的母体——硼氢化合物(即硼烷(borane))、含有硼氮(磷)键、硼氧(硫)键的化合物等;而按照狭义的分类方法[4],则只讨论含有硼碳键的化合物,包括笼状的碳硼烷簇合物。
关于硼化合物的命名,国际纯粹与应用化学联合会(IUPAC)对硼氢化合物等提出过专门的命名规则,包含了一部分有机硼化合物[5]。中国化学会《无机化学命名原则》(1980年)也介绍了一部分含硼碳键的有机硼化合物,包括部分碳硼烷簇合物及其金属化合物。部分有机硼化合物特别是一些有机硼杂环化合物的中文译名散见于资料中[1-4,6],值得进一步归纳和探讨。
本文按照狭义的分类方法对有机硼化合物的分类进行探讨,对各类有机硼化合物的命名进行归纳,并给出一些代表性化合物的英汉对照名称。同时,也适当提及有机硼化学领域的一些相关的新进展。需要指出的是,有机硼化学是属于有机化学和无机化学交叉的领域(金属有机化学或元素有机化学),不同的分类方法只是视角不同。
根据硼原子的配位数不同,有机硼化合物可以分为一配位、二配位、三配位、四配位以及高配位5类[1]。一配位的 RB属于硼烯类(organoborylene或 organoborene),二配位的 R2B·属于硼自由基(organoboryl),这两类都是高活性的中间体;三配位和四配位的硼化合物是有机合成中应用较多的;而高配位(五配位和六配位)的硼一般存在于碳硼烷簇合物中。根据所带电荷的不同,有机硼化合物可以分为中性和离子型两大类。
根据结构类型,有机硼化合物可以分为以下几种:烃基硼烷、烃基硼酸(酯)、烃基硼烷路易斯碱加合物和离子型有机硼化合物、有机硼杂环及其金属配合物、碳硼烷簇合物及其金属化合物。非簇状有机硼化合物一般以其硼烷或硼酸母体或碳环母体进行命名,前面加上取代基团的名称;簇状的碳硼烷类化合物遵从硼烷簇合物的命名规则;对于含硼的金属化合物,则一般按照硼烷簇合物或配位化合物的规则命名。
1 烃基硼烷
从结构上看,此类有机硼化合物可以看成是甲硼烷(BH3)的衍生物,主要有BR3,R2BX,RBX2(X=H、F、Cl、Br、I;R=烷基、烯基、炔基、芳基)等,一般命名为某硼烷,含卤原子的硼烷也可以根据习惯命名为卤化硼。这些化合物均为中性化合物,其中硼为+3价。从配位数看,硼均为3配位,具有平面三角形的结构。此类化合物也包括含有硼碳键的有机硼聚合物。
例如:
BMe3:三甲基硼(烷)(trimethylborane);
BPh3:三苯基硼(烷)(triphenylborane);
Ph2BCl:二苯基氯硼烷(diphenylchloroborane)或二苯基氯化硼(diphenylboronchloride);
Me2B-BMe2(化合物1):四甲基联硼或四甲基乙硼烷(4)(tetramethyldiboron或tetramethyldiborane(4)),数字4表示其硼烷母体含有4个氢原子,即B2H4;
FcBBr2(化合物2,其中Fc为二茂铁基):二茂铁基二溴硼烷(ferrocenyldibromoborane)或二茂铁基二溴化硼(ferrocenylborondibromide)。
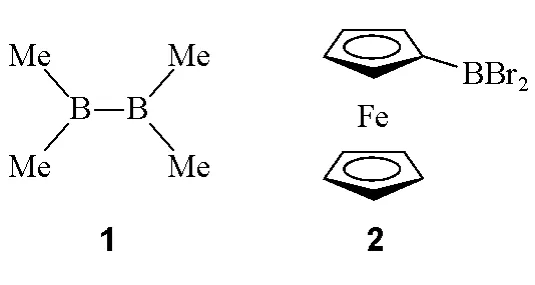
在有些化合物中,也可以把部分含硼基团称为(取代)硼基(boryl)。例如,上述二茂铁化合物(化合物2)也可以命名为二溴硼基二茂铁(dibromoborylferrocene)。
2 有机硼酸及有机硼酸酯
此类有机硼化合物本质上仍属于烃基硼烷的范围。和许多烃基硼烷相比,有机硼酸及其酯在有机合成等领域(例如钯催化的偶联反应如Suzuki反应)具有更多的实际应用,已成为一大特殊的“家族”。其命名一般也遵从上述烃基硼烷的规则,但因含有羟基OH或烷氧基团OR,一般命名为烃基有机硼酸(boronicacid或borinicacid;看作硼酸B(OH)3的有机衍生物)及有机硼酸酯(boronicester/boronate ester或 borinicester/borinateester)。
例如:
PhB(OH)2:苯基硼酸(phenylboronicacid);
Ph2B(OH):二苯基硼酸(diphenylborinicacid);
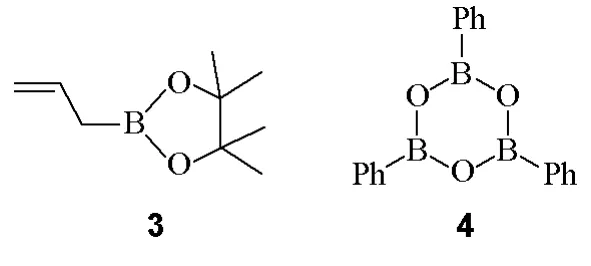
化合物3:烯丙基硼酸频哪酯(allylboronicacidpinacolester);
化合物4:苯硼酸酐(phenylboronicacidanhydride)或三苯基间硼氧六环(triphenylboroxin)。
最近,吴国庆建议将有机硼酸RB(OH)2和R2B(OH)分别命名为焩(音平)酸和亚焩酸(“焩”为“碳”和“硼”的切合字),有机硼酸酯则相应地分别命名为焩酸酯和亚焩酸酯[7]。
3 烃基硼烷路易斯碱加合物及离子型有机硼化合物
从配位数看,这些化合物中的硼原子一般为4配位,具有四面体构型,带有部分负电荷(如R4B-)。
例如:
Et2S·BH2Me:二乙基硫醚·甲基硼烷(diethylsulfide-methylborane);
LiBPh4:四苯基硼酸锂(lithiumtetraphenylborate)。
阳离子型的有机硼物种(硼鎓离子)比较少,活性很高,需要与路易斯碱结合才稳定。这类化合物主要有R2B+(borinium)、R2B+L(borenium)和R2B+L2(boronium)3种类型(其中L为路易斯碱),前两者中的硼分别为二配位和三配位,而boronium中的硼为四配位。
最近几年出现的分子内或分子间的有机硼烷与大位阻路易斯碱的组合——受阻路易斯酸碱对(frustratedLewispair,FLP;如B(C6F5)3/PtBu3)[8]很有发展潜力。不同于一般的路易斯酸碱直接结合形成的加合物,FLP体系由于位阻因素,有机硼烷等路易斯酸位点不能与路易斯碱位点直接结合,但却有独特的反应活性,能活化H2等小分子。
4 有机硼杂环及其金属配合物
有机硼杂环是一类在环上含有一个或多个硼原子的杂环化合物,包括饱和的和不饱和的有机硼杂环及其离子。环上除碳原子外,还可同时包括氧、硫、氮、磷、硅等杂原子。由于硼的缺电子性,一些不饱和的有机硼杂环除了具有供体性质,还具有部分受体性质,能与金属原子进行双面配位,形成(多层)夹心型配合物。在这些配合物中,不饱和的有机硼杂环充当了茂环(即环戊二烯基)的类似物,它们具有金属有机化合物的通性,如易溶于有机溶剂、熔点较低、易升华等。从簇合物多面体的观点来看,这些夹心型配合物也可以看成相应的闭式(closo)或巢式(nido)金属碳硼烷簇合物。有机硼杂环化合物往往还有一些专有名称,如硼杂环丙烯(boracyclopropene)为borirene,硼杂环戊烷(boracyclopentane)为borolane,硼杂环己烷(boracyclohexane)为borinane,硼杂环庚烷(boracycloheptane)为borepane。
例如:
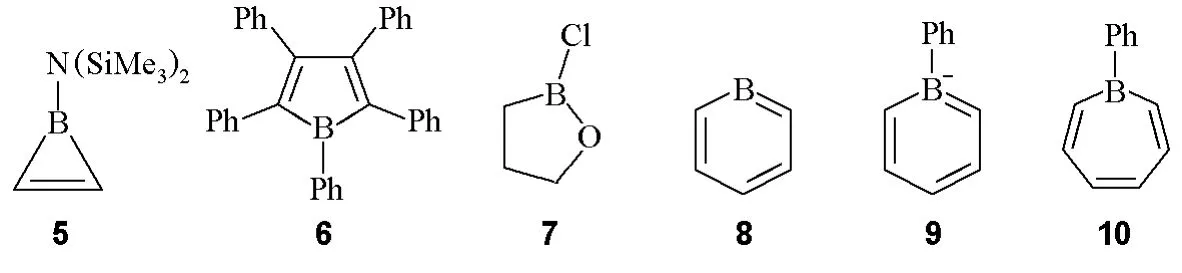
化合物5:1-双((三甲基硅基)氨基)硼杂环丙烯(1-bis(trimethylsilylamino)borirene);
化合物6:五苯基硼杂环戊二烯(pentaphenylborole);
化合物 7:2-氯-1,2-氧硼杂环戊烷(2-chloro-1,2-oxaborolane);
化合物8:硼杂苯(borabenzene,bora表示B取代了CH);
化合物9:1-苯基硼杂苯阴离子(1-phenylboratabenzene;borata表示BR-取代了CH);
化合物10:1-苯基硼杂环庚三烯(1-phenylborepine)。
一些不饱和有机硼杂环形成的夹心型配合物举例如下:
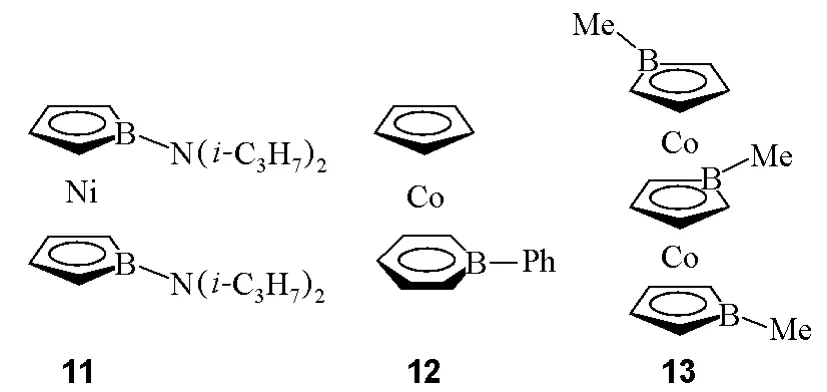
化合物11:双(η5-1-二异丙基氨基硼杂环戊二烯基)镍(bis(η5-1-diisopropylaminoborolyl)nickel);
化合物12:(η5-环戊二烯基)(η6-硼杂苯)钴((η5-cyclopentadienyl)(η6-1-phenyl-1-boranuidabenzene)或(η5-cyclopentadienyl)(η6-boratabenzene)cobalt,前者中boranuidabenzene为IUPAC的最新推荐命名);
化合物13:三(η5-1-甲基硼杂环戊二烯基)二钴(tris(η5-1-methylborolyl)dicobalt)。
5 碳硼烷簇合物及其金属化合物
硼烷簇合物中的部分硼原子被碳原子取代即形成碳硼烷(carbaborane,简称carborane)[9]。除了碳原子,同时含有硫、氮、磷等其他杂原子的称为杂碳硼烷(heterocarborane),杂原子为金属时则称为金属碳硼烷(metallacarborane)。在已知的非稠合型碳硼烷簇合物中,碳原子数目一般为1~4,簇合物顶点数为5~14,结构类型也与其硼烷母体类似,有闭式(closo)、巢式(nido)、网式(arachno)等类型。其中,研究最多的体系是具有二十面体构型的闭式二碳代十二硼烷closo-C2B10H12,根据其碳原子的相对位置不同,有3种异构体(图1,其中涂黑的顶点表示CH,其他为BH;数字表示各顶点的位次),分别命名为1,2-,1,7-,1,12-二碳代闭式十二硼烷(12)(1,2-,1,7-,1,12-dicarba-closo-dodecaborane(12),数字 12表示其母体中有 12 个氢原子),简称为邻-、间-、对-碳硼烷(ortho-,meta-,para-carborane或 o-,m-,p-carborane)[9]。近年来,人们已经合成了超越十二顶点界限的非稠合型的“超碳硼烷”——十三顶和十四顶的碳硼烷以及十四顶和十五顶的金属碳硼烷簇合物。
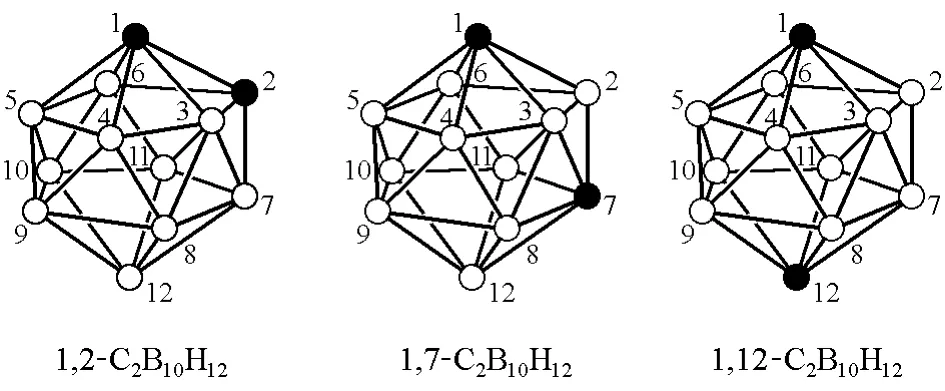
图1 closo-C2B10H12的3种异构体
由于碳和硼的电负性差异,邻-、间-、对-碳硼烷中CH基团的氢具有一定的酸性(其酸性与炔氢相当),可以与丁基锂等有机金属试剂发生金属化反应,生成相应的碳硼烷金属化合物。另外,碳硼烷经过转化(如脱去一个硼原子或还原开笼)可以形成相应的碳硼烷阴离子,为茂环的三维类似物,既能与金属化合物反应生成金属碳硼烷簇合物,也可以形成夹心型的化合物。为了方便,杂碳硼烷簇合物中顶点的位次一般仍按碳硼烷母体中的顺序编号,这一点与IUPAC的命名规则不同。例如,由邻碳硼烷衍生的C2B9H2-11阴离子(又称为“二碳硼壶”离子(dicarbollide或 dicarbollyl),壶口为五边形)形成的金属化合物分别为:
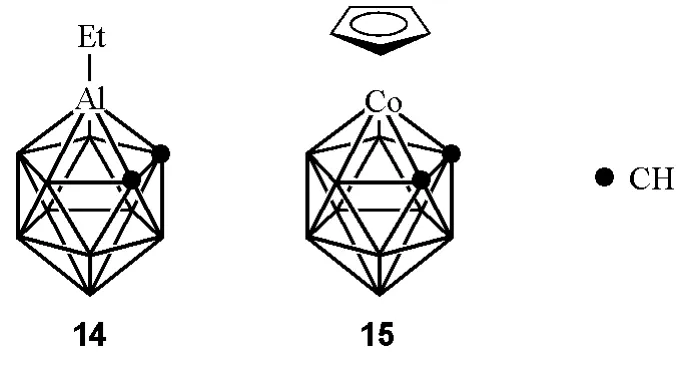
化合物14:1,2-二碳杂-3-乙基铝杂闭式十二硼烷(12)(1,2-dicarba-3-ethylalumina-closo-dodeca-borane(12))
化合物15:1,2-二碳杂-3-(η5-环戊二烯基)钴杂闭式十二硼烷(12);也可以按照配合物的命名规则命名为:(η5-环戊二烯基)(η5-7,8-二碳杂巢式十一氢十一硼酸根)钴
除了上述几种主要的类型以外,还有一些较为特殊的有机硼化合物。例如:有机硼自由基化合物(如[Ph3B·]-Na+,可以命名为三苯硼化钠(sodiumtriphenylboron));最近报道的首个含有硼硼双键的中性化合物和首个含有硼硼三键的化合物(其中NHC均为氮杂环卡宾),可分别称之为乙硼烯(diborene)和乙硼炔(diboryne)。
[1]周伟克.金属有机化合物在有机合成中的应用.上海:上海科学技术出版社,1990
[2]曾昭伦,董世华.有机硼化合物化学.“元素有机化学”第3分册.北京:科学出版社,1965
[3]赵玉芬,赵国辉.元素有机化学.北京:清华大学出版社,1998
[4]王积涛,宋礼成.金属有机化学.北京:高等教育出版社,1989
[5]InternationalUnionofPureandAppliedChemistry.PureApplChem,1972,30:683
[6]冯春祥,宋永才,谭自烈.元素有机化合物及其聚合物.长沙:国防科技大学出版社,1999
[7]吴国庆.中国科技术语,2010(6):50
[8]彭斌,聂永.中国科技术语,2010(6):44
[9]聂永.中国科技术语,2012(3):25

