锂离子电池负极材料钛酸锂的掺镁改性
肖志平,肖方明,王 英,唐仁衡
[广东省工业技术研究院(广州有色金属研究院) 稀有金属研究所,广州 510650]
尖晶石型钛酸锂(Li4Ti5O12)是动力型锂离子电池的理想负极材料之一,但Li4Ti5O12结构内部电子充满的O:2p6(价带)与未填充电子的Ti:t2g(导带)之间的能隙在3.0 eV以上,电子传导能力很差(约10-13S/cm),难以满足大电流条件下的实际应用需求[1]。目前,对此采取的主要措施是在材料颗粒表面引入第二导电相[2]、利用溶胶-凝胶等纳米技术制备小尺寸颗粒[3]。这些方法可在一定程度上改善材料的倍率性能,但对材料晶格内部的本征电子导电率作用不明显,且制备条件苛刻,过程复杂。也有研究者引入异价金属离子进行掺杂[3],改变能带结构以提高本征电子导电率,能获得较好结果,但掺杂源价格相对昂贵,增加了制作成本。
本文作者采用简易的二步固相法在空气气氛下,以价廉易得的Mg2+部分取代Li+,制备掺镁Li4Ti5O12,并综合分析掺杂对Li4Ti5O12物相结构、颗粒形貌及电化学性能的影响。
1 实验
1.1 材料的制备
按目标化合物物质的量比称取Mg(CH3COO)2·4H2O(天津产,AR)、TiO2(上海产,AR)和Li2CO3(天津产,AR),其中Li2CO3过量8.0%,弥补烧损,以无水乙醇(广东产,AR)为介质,将混合物在QM-3SP2 型行星式球磨机(南京产)中以450 r/min 的转速球磨(球料比3∶1)24 h,再将得到的前驱体置于箱式炉中,先以10℃/min 的速率升温到600℃、保温10 h,再以12℃/min 的速率升温到850℃、恒温2 h,反应完毕后,随炉冷却至室温,轻度研磨,过300 目筛,即得到样品Li4-xMgxTi5O12(x=0、0.12、0.20、0.30 和0.50)。
1.2 研究电极的制备和模拟电池的组装
将活性物质、聚偏氟乙烯(上海产,电池级)、导电炭黑(上海产,电池级)按质量比8∶1∶1混匀,以N-甲基-2-吡咯烷酮(天津产,电池级)为溶剂制成浆料,涂覆于直径为14 mm、25 μm 厚的Al 箔(深圳产,电池级)圆片上,再在60℃下烘至半干,以20 MPa 的压力压实,在120℃下真空(-0.1 MPa)干燥12 h,即制得约含4 mg 活性物质的工作电极。
以金属锂片(北京产,电池级)为对电极,Celgard 2400 膜(美国产)为隔膜,1 mol/L LiPF6/EC +DEC(体积比1∶1,广州产,电池级)为电解液,在充满氩气的手套箱内组装CR2032 型扣式电池。电池静置24 h 后,再进行电性能测试。
1.3 性能测试
用RINT-1100X 型射线衍射仪(日本产)对样品的物相及结构进行分析,CuKα、λ=0.154 06 nm,管压40 kV、管流40 mA,扫描速率为10 (°)/min,步长为0.02 °;用JSM-5910型扫描电子显微镜(日本产)观察样品的颗粒形貌。
用2000 型电池测试系统(武汉产)进行恒流充放电测试,电压为1.0~3.0 V;用Parstat2273 电化学工作站(美国产)进行交流阻抗测试,频率为10-2~105Hz,振幅为5 mV。
2 结果与讨论
2.1 结构和形貌
Li4-xMgxTi5O12(x=0、0.12、0.20、0.30 和0.50)的XRD图见图1。
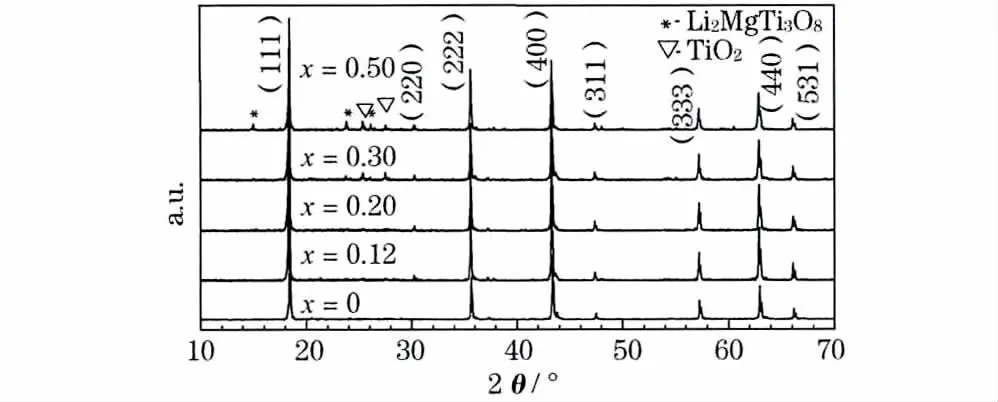
图1 Li4-xMgxTi5O12(x=0、0.12、0.20、0.30 和0.50)的XRD 图Fig.1 XRD patterns of Li4-xMgxTi5O12(x=0,0.12,0.20,0.30 and 0.50)
将图1 与标准卡片(PDF:49-0207)对比可知,当掺杂量x≥0.30 时,所得产物中除了Li4Ti5O12主相之外,还产生了Li2MgTi3O8和TiO2等杂相,尤其是x=0.50 时,杂质相峰谱甚为明显,过多杂质将降低电极中实际参与电化学反应的活性物质,同时阻碍Li+快速迁移,严重影响电池的充放电,因此后文不再研究该样品。当x≤0.20 时,仅有纯尖晶石相,且峰型尖锐,结晶度完整,表现在18.42 °、35.64 °、43.30 °、47.40 °、57.26 °、62.88 °和66.10 °出现的几个强特征峰,说明x 应控制在合理的范围。从图1 还可发现,与未掺杂样品相比,掺杂样品在30.2 °处均有较明显的尖晶石相(220)晶面特征峰。该峰取决于尖晶石结构中四面体8a 位置的阳离子,而位于四面体8a 位置的Li+本身的衍射强度很小,预示着其他相对密度更大的阳离子占据了部分8a 位置。Mg2+与Li+的半径相近且电负性更大,掺杂的Mg2+更倾向于占据Li4Ti5O12结构中的Li 位,因此推测:进入Li4Ti5O12晶格内部并占据四面体8a 位置的阳离子为Mg2+,实现了部分取代掺杂[4]。Mg2+在尖晶石结构中的具体占位情况,还有待进一步研究。利用XRD 测试的数据,运用三点抛物线法分别确定6 个强峰的峰位,再根据柯亨(M.U.Cohen)最小二乘法[5]计算各样品的晶胞参数a0和晶胞体积V0,结果见表1。
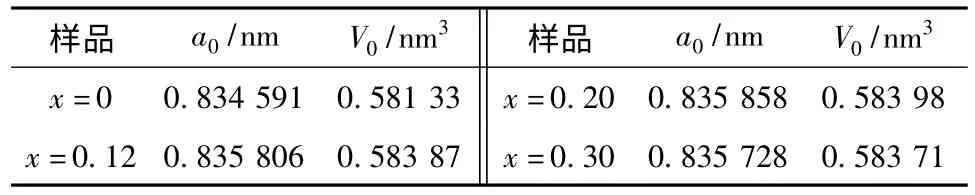
表1 Li4-xMgxTi5O12(x=0、0.12、0.20 和0.30)的晶胞参数及晶胞体积Table 1 Lattice constant and cell volume of Li4-xMgxTi5O12(x=0,0.12,0.20 and 0.30)
从表1 可知,相比于未掺杂样品,掺杂样品的a0增大,原因是高价态Mg2+取代Li+后,为了维持晶体内部电荷平衡,出现了半径较大的Ti3+。当x≤0.2 时,随着x 的增加,晶胞体积变大[6];当x=0.3 时,晶胞体积略有下降,可能是由于O—Mg 键的键强大于O—Li 键,导致晶胞发生收缩。
Li4-xMgxTi5O12(x=0、0.12、0.20 和0.30)的SEM 图见图2。

图2 Li4-xMgxTi5O12(x=0、0.12、0.20 和0.30)的SEM 图Fig.2 SEM photographs of Li4-xMgxTi5O12(x=0,0.12,0.20 and 0.30)
从图2 可知,掺杂样品的颗粒变得细小,平均粒径从未掺杂样品的1.0 μm 下降到x=0.20 样品的0.6 μm,颗粒间的结合更松散,孔隙率增加,且形状较规则,近似于球形。这说明掺杂Mg 不仅降低了颗粒度,对产物形貌也产生了积极影响,可能与醋酸盐在热分解过程中产生了气体有关。较小的颗粒度及减轻由颗粒内部与表面Li+浓度差引起的极化,可提高活性物质的嵌脱锂深度。粒度分布越均匀,电极各部位的电阻、电流密度及反应状态越稳定。此外,不同Mg 掺杂量的样品,颗粒形貌没有明显的差别。
2.2 电化学性能
Li4-xMgxTi5O12(x=0、0.12、0.20 和0.30)在0.2 C 倍率下的首次充放电曲线见图3。
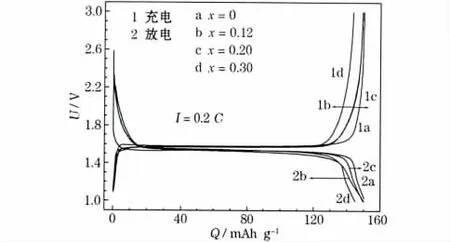
图3 Li4-xMgxTi5O12(x=0、0.12、0.20 和0.30)的首次充放电曲线Fig.3 Initial charge-discharge curves of Li4-xMgxTi5O12(x=0,0.12,0.20 and 0.30)
从图3 可知,各样品在充放电过程中均有宽而平坦的充放电电压平台,平台容量占总容量的90.0%以上,具有明显的两相共存特征。x=0、0.12、0.20 和0.30 的样品,首次放电比容量分别为151.2 mAh/g、149.0 mAh/g、150.1 mAh/g和145.0 mAh/g,掺杂样品的放电比容量略有降低,与文献[4]的结果一致。x=0.30 的样品放电比容量最低,主要与形成了非活性物质有关。掺杂样品的充放电平台电压差小于未掺杂样品,说明Mg 掺杂减轻了电极在充放电过程中的极化,细小颗粒有利于缩短Li+在嵌脱过程中的扩散路径,同时,高价态的Mg2+取代Li+,使材料内部出现了Ti4+/Ti3+混合价[4],有助于提高贫锂相和富锂相界面的电子导电性。
Li4-xMgxTi5O12(x=0、0.12、0.20 和0.30)样品在不同倍率下进行充放电测试,结果见图4。
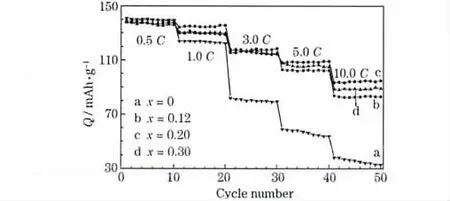
图4 Li4-xMgxTi5O12(x=0、0.12、0.20 和0.30)在不同倍率下的循环性能Fig.4 Cycle performance of Li4-xMgxTi5O12(x=0,0.12,0.20 and 0.30)at different rates
从图4 可知,x=0、0.12、0.20 和0.30 的样品在低倍率(0.5 C)时的放电比容量分别为141.0 mAh/g、139.2 mAh/g、138.2 mAh/g 和138.0 mAh/g,相差不大。随着倍率的增加,样品的循环性能发生变化。Mg 掺杂可改善Li4Ti5O12的倍率性能,x=0.20 的样品以10.0 C 倍率循环10 次,放电比容量基本上没有衰减,高倍率容量性能较理想。Mg 掺入过多,参与实际反应的活性物质会减少,产生的非活性物质还会阻碍Li+的传输;掺入不足,由正电荷缺陷的补偿产生的空穴密度及进入极化能力较强的Ti4+离子d 能带的电子数不够。这两种情况,均会影响Li+的扩散速率和电子导电[7]。
Li4-xMgxTi5O12(x=0、0.12、0.20 和0.30)样品以5.0 C倍率循环200 次,结果见图5。
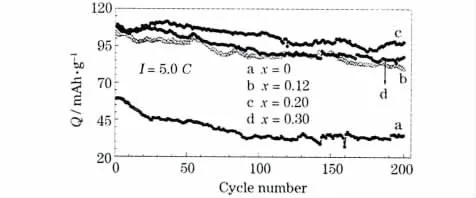
图5 Li4-xMgxTi5O12(x=0、0.12、0.20 和0.30)的5.0 C 循环性能Fig.5 Cycle performance of Li4-xMgxTi5O12(x=0,0.12,0.20 and 0.30)at 5.0 C
从图5 可知,与未掺杂样品相比,掺杂样品的循环性能得到改善,其中x=0.20 的样品在第200 次循环时,容量保持率仍有90.5%,x=0.12 和0.30 的样品分别为77.5%、81.5%,而未掺杂样品仅为41.0%。在充放电过程中,Li+和电子不断通过形成新的两相界面维持有效电流。在大电流条件下,如果Li+扩散速率或电子传导能力有限,随着两相界面不断缩小,Li+的扩散量或电子传导不足以维持有效电流,充放电将提前停止,颗粒内核部分的活性物质不能被充分利用,造成容量损失。颗粒度和晶体结构是影响Li+扩散的两个重要因素,掺Mg 样品的颗粒度下降,缩短了Li+的有效扩散路径,且晶胞参数的增大有利于扩充Li+扩散通道;另外,充放电过程是离子和电子相互协同的过程,大电流条件下,电极材料不仅应具有较高的离子导电性,还应是电子的良好导体或半导体。掺Mg 样品的高倍率循环稳定性较好,可能是由于Li 位掺杂Mg,产生了更多的Ti4+/Ti3+混合价,在导带和价带之间产生新的能带,带隙减小,提高了电子传递能力。Mg 掺杂量存在上限,本实验以x=0.20 为上限,否则会产生杂质相。分散在活性物质颗粒中间的杂质相,不仅阻碍Li+的扩散,还减弱颗粒之间的电接触。
为了进一步研究Li4-xMgxTi5O12(x=0、0.12、0.20 和0.30)样品电性能的差别,进行了交流阻抗分析,结果见图6,对相关动力学参数进行计算比较,关系式见式(1)、(2)。
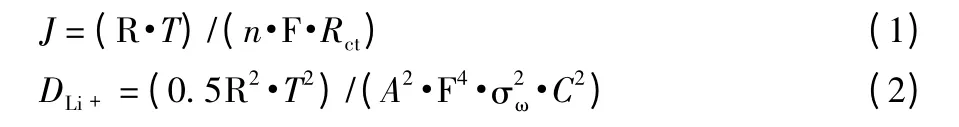
式(1)、(2)中:J 为交换电流密度(A/cm2),R 为气体常数,T 为绝对温度(K),n=1,A 为电极材料与电解液的接触面积(cm2),F 为法拉第常数,C 为Li+的物质的量浓度(mol/cm3),σω为韦伯阻抗系数(Ω·cm2/s0.5),DLi+为Li+扩散系数(cm2/s),Rct为界面电荷转移阻抗。
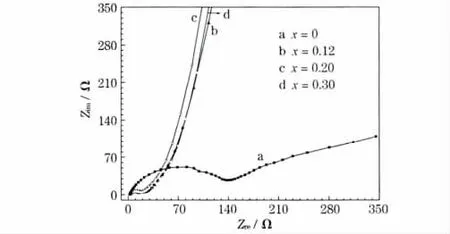
图6 Li4-xMgxTi5O12(x=0、0.12、0.20 和0.30)的交流阻抗谱Fig.6 A.C.impedance spectra of Li4-xMgxTi5O12(x=0,0.12,0.20 and 0.30)
从图6 可知,各样品曲线的形状大体相同,由中高频区代表Rct的半圆和低频区代表Warburg 阻抗的斜线构成。用ZsimpWin3.10 软件拟合可得,x=0、0.12、0.20 和0.30 的样品,Rct分别为131.6 Ω、23.1 Ω、16.2 Ω 和20.5 Ω,掺杂样品的Rct降低,其中x=0.20 的样品最小,反映了掺杂后快速的脱嵌锂动力学机制。由式(1)可知,Rct越小,J 越大,意味着x=0.20 的样品,电极体系具有相对较高的可逆性[8],与该电极体系较好的电化学性能相符。Li+在晶格内部的扩散速度,是影响材料锂深度和电化学性能的重要因素[9]。
交流阻抗谱低频直线区实部Zre与角频率开平方倒数ω-0.5关系的拟合曲线见图7。
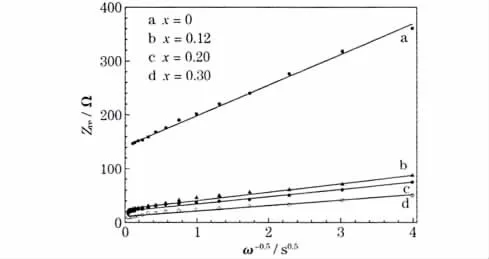
图7 Li4-xMgxTi5O12(x=0、0.12、0.20 和0.30)交流阻抗谱低频直线区(Zre)与ω-0.5的关系Fig.7 Relation between low frequency region of the straight line(Zre)of A.C.impedance spectra and ω-0.5 for Li4-xMgxTi5O12(x=0,0.12,0.20 and 0.30)
结合图7,通过式(2)可得到各样品的DLi+,结果见表3。

表3 Li4-xMgxTi5O12(x=0、0.12、0.20 和0.30)的交流阻抗参数Table 3 A.C.impedance parameters of Li4-xMgxTi5O12(x=0,0.12,0.20 and 0.30)
从表3 可知,掺杂Mg 后,Li+在材料中的扩散能力提高,其中x=0.20 的样品最好,DLi+较未掺杂样品提高了1 个数量级,达5.58 ×10-9cm2/s。掺杂Mg 增加了Ti4+/Ti3+混合价的数量和空穴密度,改善了导电性,加快了发生在电极表面的电荷转移动力学过程;同时,Li4Ti5O12的晶胞参数随着x的增加而增大,而晶胞参数的增大有可能扩张Li+的迁移通道,提高Li+的运动能力,改善大电流条件下的电化学性能。综合实验结果,本实验中,Mg 掺杂量x 以0.20 为最好。
3 结论
以醋酸镁为掺杂源,在空气气氛中采用二步固相法合成Li 位掺杂的含Mg 钛酸锂Li4-xMgxTi5O12。少量掺杂并未引起晶体结构和物相成分的改变,掺杂量控制在x≤0.20 为宜,否则有杂质相产生。掺杂Mg 有利于减小材料的粒径,平均粒径从未掺杂的1.0 μm 降至x=0.20 的0.6 μm。与未掺杂样品相比,掺杂样品的Rct下降,x=0.20 的样品Rct最小,仅16.2 Ω,DLi+也提高了1 个数量级,达5.58 ×10-9cm2/s。10.0 C 倍率时,x=0.20 的样品首次放电比容量为93.8 mAh/g,以5.0 C 倍率循环200 次,容量保持率为90.5%。
[1]Lippens P E,Womes M,Kubiak P,et al.Electronic structure of the spinel Li4Ti5O12studied by ab-initio calculations and X-ray absorption spectroscopy[J].Solid State Sciences,2004,6(2):161-166.
[2]Li H S,Shen L F,Zhang X G,et al.Nitrogen-doped carbon coated Li4Ti5O12nanocomposite:superior anode materials for rechargeable lithium ion batteries[J].J Power Sources,2013,221:122-127.
[3]Qiu C X,Yuan Z Z,Liu L,et al.Sol-gel preparation and electrochemical properties of La-doped Li4Ti5O12anode material for lithium-ion battery[J].J Solid State Electrochem,2012,17(3):841-847.
[4]Chen C H,Vaughey J T,Jansen A N,et al.Studies of Mg-substituted Li4-xMgxTi5O12spinel electrodes(0≤x≤1)for lithium batteries[J].J Electrochem Soc,2001,148(1):A102-A104.
[5]LI Shu-tang(李树棠).晶体X 射线衍射学基础[M].Beijing(北京):Metallurgical Press(冶金工业出版社),1990.
[6]Li X,Qu M Z,Yu Z L.Structural and electrochemical performance of Li4Ti5-xZrxO12as anode material for lithium-ion batteries[J].J Alloys Compd,2009,487(1/2):L12-L17.
[7]YANG Jian-wen(杨建文).Li4Ti5O12基混合超级电容器负极材料的开发及相关机理研究[D].Changsha(长沙):Central South University(中南大学),2005.
[8]Cui Y,Zhao X L,Guo R S.Improved electrochemical performance of La0.7Sr0.3MnO3and carbon co-coated LiFePO4synthesized by freeze-dry process[J].Electrochim Acta,2010,55(3):922-926.
[9]TANG Zhi-yuan(唐致远),YANG Xiao-xia(阳晓霞),CHEN Yuhong(陈玉红),et al.Mg2+、Zr4+离子掺杂对Li4Ti5O12电化学性能的影响[J].Fine Chemicals(精细化工),2007,24(3):273-277.

