不同生育期花生渗透调节物质含量和抗氧化酶活性对土壤水分的响应
张智猛,宋文武,丁 红,慈敦伟,康 涛,2,宁堂原,戴良香,*
(1.山东省花生研究所,青岛 266100;2.新疆农业大学农学院,乌鲁木齐 830052;3.山东农业大学农业部作物水分生理与抗旱种质改良重点实验室,泰安 271018)
水分条件是植物生长的重要环境因子之一,也是各种胁迫环境中最常见、最普遍的逆境因子之一,植物对土壤水分胁迫的响应包含着极其复杂的生理生化变化,形成了酶促和非酶促两大类保护系统以清除活性氧,减轻或避免活性氧对细胞造成的伤害,这些抗氧化酶系的表达量和渗透调节物质的积累量受遗传性制约[1-6],并与植物对逆境胁迫的抗性密切相关,最终体现为植物对水分胁迫的适应或产生抗性[6-7]。同时,渗透调节物质含量和膜脂过氧化代谢对水分胁迫的响应较为复杂,不仅与作物类型、基因型、胁迫程度及持续时间、不同生育期等密切相关,而且与酶的类型有关[8-12]。
我国花生的集中产区主要分布于干旱半干旱地区的古河道故道、丘陵坡地等地,属于典型的旱区雨养农业。花生虽是较耐旱耐瘠的经济和油料作物,也是发展旱作农业、充分开发利用旱薄地资源的理想作物,但生育期内降雨量偏少、雨水集中或季节性干旱,仍成为限制花生产量与质量提高的主要因子,因此,选育节水抗旱花生品种及其优化配套的栽培管理措施是实现花生高效用水、减少因水分环境剧变带来的损失经济而有效的途径,并已成为农业中重要的研究课题。传统农业认为丰水高产,相同栽培条件下,在花生需水量以上的灌溉条件下,经济产量和生物产量随着灌水量的增加而下降,随着灌水次数的增加而提高,多余灌溉反而减产,降低水分利用效率[13]。已有研究表明,适度水分亏缺使作物产生适应性调节反应,做出最优化选择,可提高作物根冠比、保护酶活性、渗透调节物质含量,水分利用效率明显提高,但不同作物类型、品种和生育时期忍受水分亏缺的程度不同[10,13-14]。只要采用适宜的栽培技术,适当减少灌溉次数和灌水量,并不影响产量,却能显著提高水分利用效率[15]。对作物在干旱逆境下适应能力及其反应的研究,应该充分重视干湿交替和旱后复水条件下,作物生长和生理功能的恢复能力[16]。关于水分胁迫对植物类型、品种、生育阶段等的保护酶系统、渗透调节及膜脂过氧化的影响的研究认为[8-9,11-12],水分胁迫前期或轻中度胁迫下,SOD、POD、CAT活性、MDA含量升高,抗氧化酶活性增加,活性氧造成的伤害得以缓解[17-18];抗旱性强的品种在逆境条件下保护酶活性能维持在一个较高的水平和较低的MDA含量及变幅,有利于清除自由基以降低膜脂过氧化水平,减轻膜伤害程度[12,19-20]。膜质过氧化是花生干旱伤害的重要原因,而较高的CAT活性则降低这一伤害的程度从而使叶片维持较高的光合速率[21-22]。但有关不同生育时期灌水对花生抗氧化酶系统、渗透调节及膜脂过氧化影响的研究鲜见报道。本试验以不同花生品种为材料在不同生育时期进行灌水,探讨不同生育期浇水对不同花生品种叶片抗氧化酶活性、渗透调节物质含量和膜脂过氧化作用的影响,为不同基因型花生抗旱适应性机理、选择优良耐旱种源以及建立节水高效的非充分灌溉与调亏灌溉综合技术模式提供理论依据。
1 材料方法
1.1 试验设计
试验在山东省花生研究所试验站进行,采用防雨棚池栽试验。以小粒型花生品种花育20号(百仁重67.9 g)和花育27号(百仁重68.9 g)为研究对象。土壤基础肥力为有机质8.70 g/kg、水解氮83.29 mg/kg、速效磷59.56 mg/kg和速效钾73.55 mg/kg,pH 值6.79,土壤田间持水量24.90%。
栽培池面积12 m2,每池种植8行,行距40 cm,穴距20 cm,每穴2粒,重复3次。设置全生育期干旱(W0,植株中午有50%出现萎蔫时进行灌水,灌水量控制在0—20cm土层土壤相对含水量40%—50%,使其全生育期均处于中度干旱胁迫条件)、全生育期浇水(W1,苗期、花针期和结荚期均灌水,每次灌水量控制在0—20cm土层土壤相对含水量75%—80%,使其全生育期土壤相对含水量均保持60%—70%)、苗期浇水(W2)、花针期浇水(W3)、结荚期浇水(W4)5个水分处理,W2、W3、W4各生育期浇水处理的灌水量控制以0—20cm土层土壤含水量为依据,各浇水处理的灌水量均控制在0—20cm土层土壤相对含水量75%—80%,其余生育期控制0—20cm土层土壤相对含水量为45%—55%。播前底墒水浇水量均为1200 m3/hm2,土壤含水量采用烘干法测定。
播种前基施氮磷钾三元复合肥(15-15-15)600 kg/hm2,管理措施同高产田。5月6日播种,9月24日收获。
自出苗开始,观察植株生长发育状况,分别于苗期(出苗后30d)、花针期(出苗后60d)、结荚期(出苗后90d)、饱果期(出苗后110d)和成熟期(出苗后125d)采集各处理植株样品,采集时间在浇水结束后24 h的9:00—11:00进行。每小区分别采取有代表性的植株3穴共6株,用蒸馏水洗净并吸干,迅速放入冰盒中带回室内;采取叶片样品部位为主茎和分枝上倒数第3—4片展开复叶;于-40℃低温冰箱内保存,备测定相关生理生化指标。
所有数据处理及统计分析采用Excel和SPSS统计软件进行分析整理。
1.2 测定项目及方法
酶液的提取:称取0.5 g左右鲜样剪碎,加0.05 mol/L、pH7.8的磷酸缓冲液(内含1%的PVP)5.0 mL及少量石英砂,于冰浴中研磨提取,15 000×g,4℃下离心15 min,上清液定容至10 mL,上清液为酶提取液,用于SOD、POD、CAT活性、MDA及可溶性蛋白质含量的测定。
SOD、CAT和POD活性测定:以反应抑制氮蓝四唑(NBT)光氧化还原50%的酶量为一个酶活力单位测定SOD,用unit/mg鲜重表示[23];采用高锰酸钾滴定法[23]测定CAT,以30℃下每克鲜重样品每分钟内分解H2O2的毫克数为酶活力单位(μmol H2O2g-1鲜重 min-1);采用愈创木酚法测定 POD,以 ΔOD470g-1鲜重 min-1表示酶活力单位[23]。
参考李合生的方法[24]测定丙二醛(MDA)含量;采用考马斯亮蓝染色法测定,并用牛血清白蛋白作标准曲线[24]测定可溶性蛋白质含量;采用茚三酮法[24]测定游离氨基酸和脯氨酸含量;采用蒽酮法[23]测定可溶性糖含量。
2 结果分析
2.1 叶片保护酶系统
图1看出,两品种生育前期叶片SOD活性变化因苗期灌水与否而不同,苗期不灌水(干旱)使叶片SOD活性显著高于苗期灌水处理,且灌水后其活性显著降低。苗期和花针期灌水使两品种SOD活性均显著降低,而结荚期灌水未出现降低。两品种W0处理与其他处理间差异均不显著,但均以W3处理活性较高。花育20号W1处理显著低于其他处理,对水分反应强烈,而花育27号各灌水处理间差异不显著,SOD活性对适应土壤水分逆境响应强烈。同一生育时期花育27号SOD活性高于花育20号。
不同灌水时期不影响叶片POD活性的变化趋势,随生育进程推进,两品种均呈“双峰曲线”型变化,峰谷均出现在结荚期,峰值时两品种各处理间差异显著。生育前期两品种W2、W3处理活性较高;后期则以W0和W4处理活性较高。两品种各处理POD活性均无明显变化,全生育期内,花育20号活性高于花育27号(图1)。
两品种全生育期叶片CAT活性变化趋势不受灌水时期的影响,均呈“抛物线型”,但峰值因灌水时期不同而异,花育20号W3和W4处理峰值滞后到饱果期,W1、W2分别出现在花针期和结荚期,而W0一直表现降低趋势,花育27号各处理均出现在结荚期;花育20号各处理间差异显著。苗期和花针期灌水使CAT活性降低,而结荚期灌水未出现降低。全生育期灌水处理的CAT活性显著低于其他处理,且生育后期两品种均以W3处理活性最高。花育20号的W0处理显著低于其他处理,对水分反应强烈,而花育27号各处理间差异不显著(图1)。
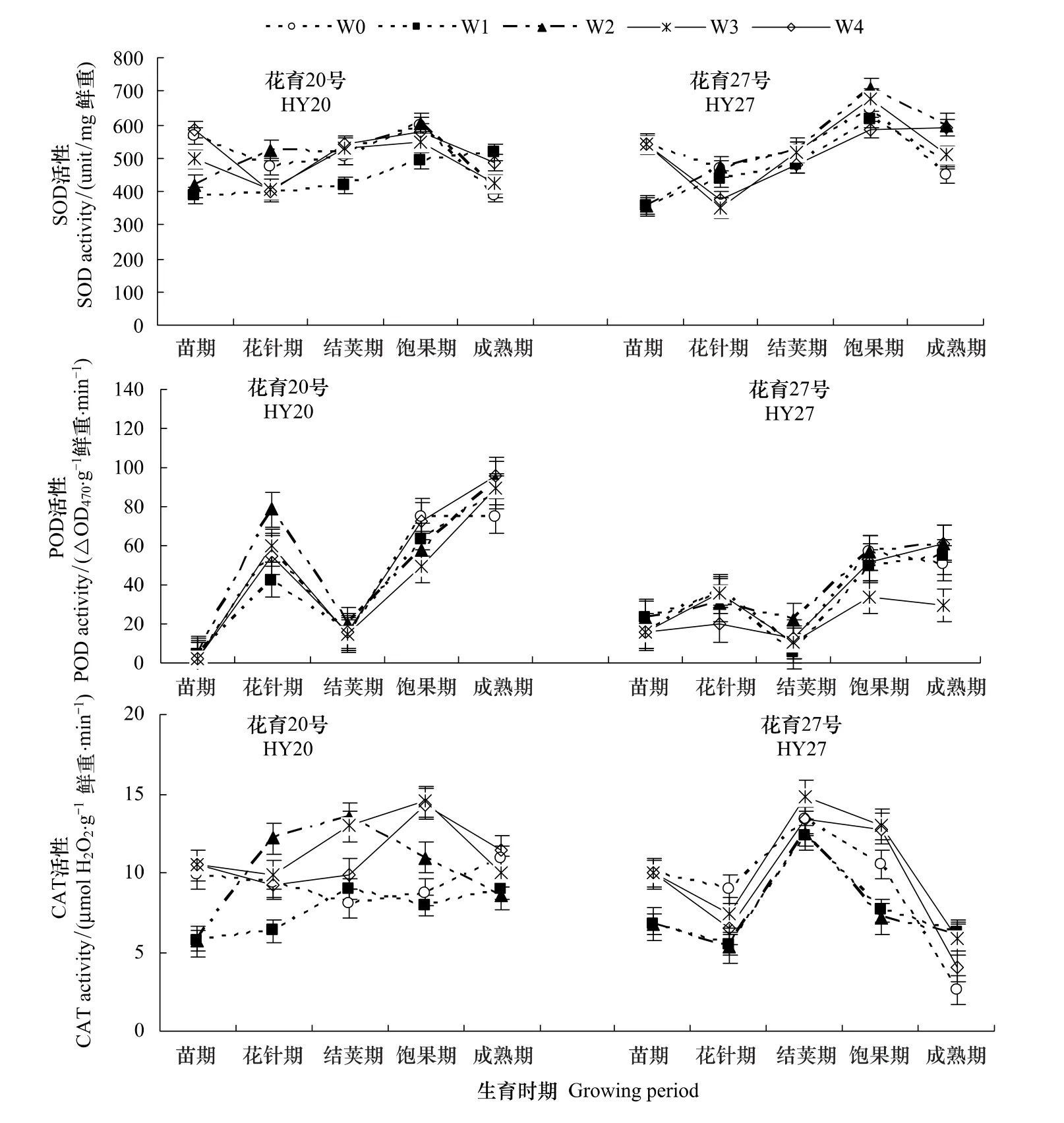
图1 不同水分处理对花生叶片抗氧化酶活性的影响Fig.1 Changes of protective enzyme activities in peanut leaves under non-sufficient irrigation in different growth stages
2.2 渗透调节物质含量
图2 表明,叶片中可溶性糖含量的变化趋势不受灌水时期的影响,均随生育时期推进呈渐升的变化态势,且处理间差异不显著。两品种W3处理叶片可溶性糖含量在生育前期较高,生育后期W0处理显著高于其他处理。两品种W1处理均较低,灌水后使叶片中可溶性糖含量降低,长期干旱胁迫使其含量陡增,生育后期可溶性糖含量对土壤水分的响应强于前期。
不同生育时期灌水对花生叶片可溶性蛋白质含量变化趋势无影响,均呈渐升趋势,因灌水时期不同升幅不同。全生育期内,花育20号升幅高于花育27号,其W0、W1、W3处理的升幅分别为10.57%、82.8%、59.66%和5.87%、54.74%、52.12%。两品种W1处理显著低于其他处理,W3处理高于其他处理。灌水后或随干旱加剧叶片可溶性蛋白质含量降低,但干旱初期其含量防御性升高(图2)。
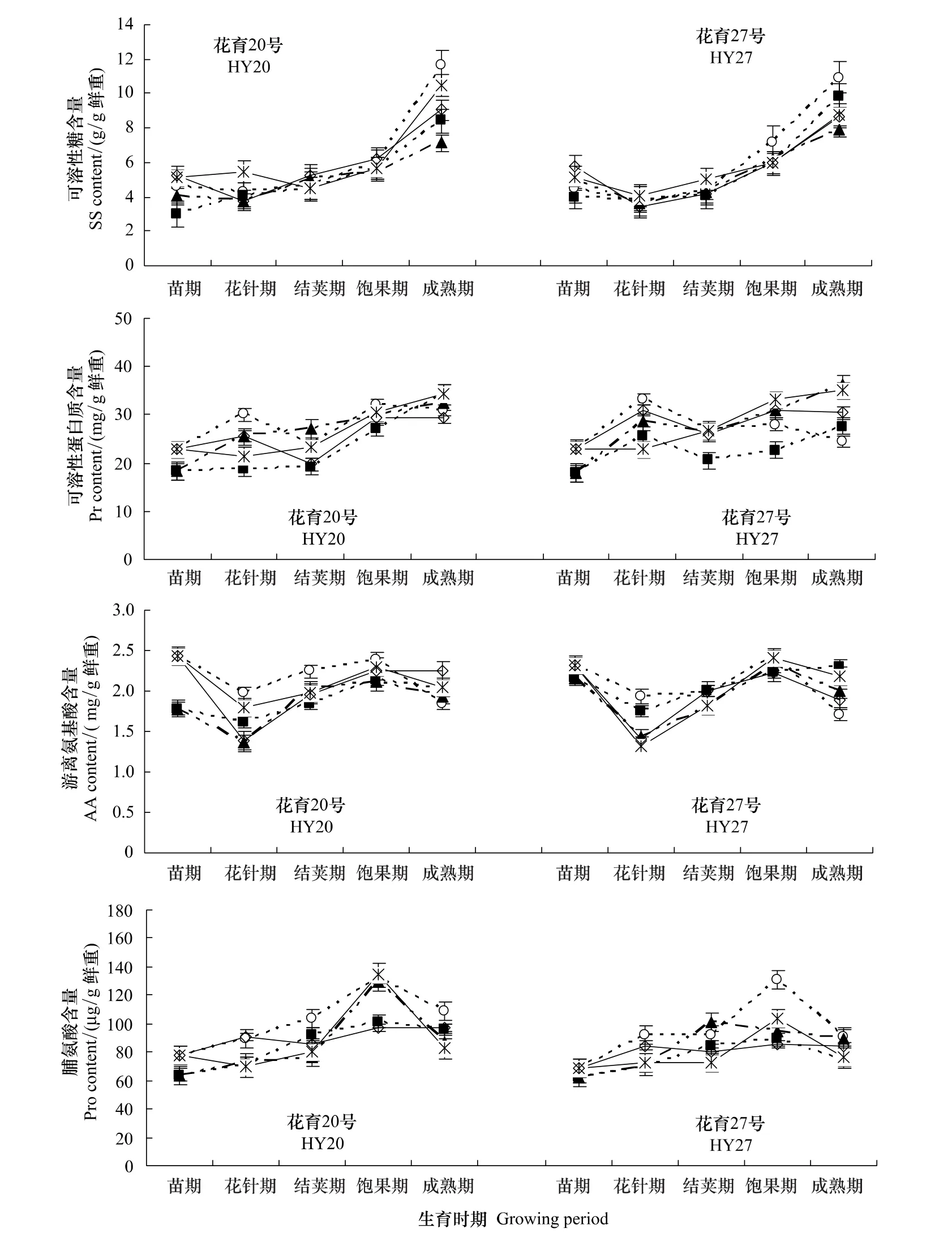
图2 不同水分处理对叶片渗透调节物质含量变化的影响Fig.2 Changes of the content of osmotic adjustment solutes in peanut leaves under non-sufficient irrigation in different growth stage
不同生育时期灌水对花生叶片游离氨基酸含量的变化趋势无影响,均呈“抛物线”型,其峰值均出现在饱果期。苗期灌水使两品种叶片游离氨基酸含量显著降低;W0处理下,两品种叶片游离氨基酸含量显著升高,开花下针期灌水使其含量先降后升,花育27号升幅较大,花育20号和花育27号的升幅分别为10.47%、37.68%。开花下针期灌水对叶片游离氨基酸含量的影响作用较大,尤以花育27号明显(图2)。
生育期灌水处理对叶片脯氨酸含量的变化趋势亦无影响。W1处理脯氨酸含量较低,W0、W2、W3处理较高。苗期和花针期浇水使其含量略有降低,但随后的土壤水分胁迫又使其升高;结荚期浇水脯氨酸含量变化不大。两品种W0处理的叶片脯氨酸含量显著高于其他处理,可见,两品种脯氨酸含量对土壤水分胁迫的响应能力较强(图2)。
花生渗透调节物质类型对水分胁迫的响应因品种的不同而不同,花育20号和花育27号可溶性蛋白质、游离氨基酸和脯氨酸含量变化对土壤水分含量的变化响应较强烈,但可溶性糖含量在生育前期作用较弱。可见渗透调节类型对水分胁迫调节作用的差异。两品种渗透调节物质对浇水处理表现出一致的调节能力,其调节能力表现为脯氨酸、可溶性蛋白质>可溶性糖>游离氨基酸。
2.3 膜脂过氧化作用
图3表明,灌水时期不影响花生叶片膜脂过氧化程度的变化趋势,但灌水时期影响脂质受伤害程度。W1处理下MDA含量显著低于其他处理,W0处理显著升高,灌水后叶片MDA含量降低。全生育期内花育20号MDA含量高于花育27号。

图3 不同水分处理对丙二醛含量变化Fig.3 Changes in MDA content of peanut leaves under non-sufficient irrigation in different growth stage
3 讨论
细胞中SOD、POD、CAT活性和MDA含量变化与作物的抗旱性强弱有关,且作物对逆境胁迫的敏感性因类型、品种、生育期不同而有很大差异。抗旱性强的品种在逆境条件下保护酶活性能维持在较高的水平,有利于清除自由基以降低膜脂过氧化水平,减轻膜伤害程度[25-28]。本试验结果表明,花生叶片保护酶活性的变化受土壤水分状况的影响,土壤水分适宜叶片保护酶活性明显低于轻度干旱胁迫处理且无剧烈升高或降低,干旱胁迫使叶片SOD、POD、CAT等保护酶活性明显升高,随胁迫历时延长,不同品种、不同酶类型的表现不同,两品种SOD和CAT活性的变化对水分胁迫的响应强于POD。
研究表明,渗透胁迫后各种渗透调节物质含量增加的幅度依次是脯氨酸>可溶性糖>游离氨基酸,小麦和水稻叶片渗透调节能力则是可溶性糖>游离氨基酸>脯氨酸[30-31]。抗旱性不同的玉米自交系幼苗渗透调节能力有差异,旱21和齐319以可溶性糖和脯氨酸为主要的渗透调节因子,黄早四则以脯氨酸为主要的渗透调节物质[32];花生抗旱性相关性次序为丙二醛>过氧化氢酶、可溶性蛋白质含量[21-22]。本试验结果表明,对水分最为敏感的开花下针期灌水渗透调节物质上升幅度最大,其渗透调节能力依次为脯氨酸、可溶性蛋白质>可溶性糖>游离氨基酸,花育27号渗透调节能力较大。反映了花生不同生育时期对水分胁迫渗透调节能力的差异和渗透调节物质相对贡献率的差异,表明花生通过渗透调节适应干旱的生理机制。
花生生长前期耐旱性很强,苗期干旱对产量影响不显著,而且苗期适当干旱对单株有效花数、结实数、饱果数有明显增加,苗期适当控制土壤水分有利于植株健壮生长和产量提高[16,22]。可见,花生生长前期虽有一定的耐旱性,但长期干旱会严重影响其地上部生长发育。开花下针期干旱,使花期延长,下针结果期延迟11—13d,荚果发育速率降低至 11.5—12.6 mg/d,苗期降低 25.9%—32.4%,最终导致产量降低[33],这与本试验结果一致。
土壤水分状况影响花生光合作用、保护酶系统和渗透调节能力。研究表明,苗期灌水量不能低于60—80mm,否则会导致叶片光合速率下降,MDA含量增加;若苗期适当干旱(灌水60—80mm),可增加叶片SOD、POD、CAT的活性,提高叶片可溶性蛋白质含量;充分灌水后,叶中SOD、POD、CAT活性和Pr、MDA含量显著降低,而光合速率显著升高[33]。早熟花生苗期0—10cm或0—30cm土层含水量分别不低于14.5%、23.5%时,其生长发育与水分利用率都较高[34-35]。本试验条件下,除脯氨酸和MDA外,苗期灌水仅影响生育前期花生抗氧化酶和渗透调节系统,对生育后期无影响,且苗期灌水与全生育期灌水处理间无显著差异。因此,花生生长前期耐旱性很强,苗期适当控制土壤水分有利于花生植株健壮生长和产量提高,是花生节水栽培技术的一项重要措施。
花针期是花生营养生长与生殖生长均进入旺盛阶段,对水分较为敏感,此期受到水分胁迫,复水后尽管根冠生长均有恢复,但很难超过正常生长状况。想通过轻微水分胁迫再复水以促进生长来提高水分利用率,也要避开花针期;否则造成的后果是日后难以弥补的[34-36]。本试验结果表明,花针期灌水可明显提高抗氧化酶活性和渗透调节能力物质含量的升幅,降低MDA含量。不同生育期渗透调节能力大小的顺序为:花针期>结荚期>苗期,可见花针期是花生对水分反应的敏感期,也是花生需水的临界期,此期土壤水分状况对花生叶片保护酶活性影响较大,进而影响花生叶片的光合作用以及物质合成与运输。水分亏缺时必须通过灌水来调节体内代谢的平衡,达到高产高效。
结荚期是花生生理发育的旺盛期,是籽仁充实饱满关键时期,也是需水和耗水量较大时期。试验结果表明,此期灌水并不造成叶片保护酶、渗透调节物质含量的降低和MDA含量的升高,反而略有上升或降低。但此期水分不足,光合产物积累降低,产量损失严重,一般能减产80%左右。此期不能耐受水分胁迫,如此期遇旱,应尽力进行灌溉,生产上不应忽视。
[1] Shan L.Development trend of dryland farming technologies.Scientia Agricultura Sinica,2002,35(7):848-855.
[2] Shan L,Zhang SQ.Water saving agriculture and its biological basis.Research of soil and Water Conservation,1999,(6):3-6.
[3] Li X,Yan X F,Yu T.Effects of water stress on protective enzyme activities and lipid peroxidation in Phellodendron amurense seedlings.Chinese Journal of Applied Ecology,2005,16(1):2353-2358.
[4] Wang J,Li D Q.The Accumulation of Plant Osmoticum and Activated Oxygen Metabolism under Stress.Chinese Bulletin of Botany,2001,18(4):459-465.
[5] Chaves M M,Oliveira M M.Mechanisms underlying plant resilience to water deficits:prospects for water-saving agriculture.Journal of Experimental Botany,2005,55,2365-2384.
[6] Chen SF,Shu Q Y.Biological Mechanism of and Genetic Engineering for Drought Stress Tolerance in Plants.Chinese Bulletin of Botany,1999,16(5):555-560.
[7] Tang Z C.Proline accumulation in plants under stress conditions and its possible significance.Plant physiology communications,1984,(1):15-21.
[8] Boyer I S.Plant productivity and environment.Science,1982,218:443-448.
[9] Guo W D,Shen X,Li J R,Zheng X Q.Molecular Mechanism of Plant Drought Tolerance.Acta Universitatis Agriculturalis Boreali-Occidentalis,1999,27(4):102-106.
[10] Jiang H F,Ren X P.The effect on SODactivity and protein content in groundnut leaves by drought stress.Acta Agronomica Sinica,2004,30(2):169-174.
[11] Liu Z Q,Zhang SC.Plant Physiology on Stress Resistance.Beijing:China Agriculture Press,1994.
[12] Zhang L X,Li SX.Effects of Nitrogen,Potassium and Glycinebetaineon the Lipid Peroxidation and Protective Enzyme Activities in Water-Stressed Summer Maize.Acta Agronomica Sinica,2007,33(3):482-490.
[13] Su P X,Chen H S.Changes in Yield under Different Irrigating Schemes and Photosynthetic Characte-ristics of Peanut in Oasis.Acta Agronomica Sinica,2005,31(12):1660-1664.
[14] Zhang Q D,Lui H Q,Zhang J H,Li J M.Effects of Limited Irrigation on Some Photosynthetic Functions of Flag Leaves in Winter Wheat.Acta Agronomica Sinica,2000,26(6):869-873.
[15] Shan L,Deng X P,Su P,Zhang SQ,Huang Z B,Zhang Z B.Exploitation of crop drought resistance and water-saving potentials—adaptability of the crops to the low and variablewater conditions.Review of China Agricultural Science and Technology,2000,2(2):66-70.
[16] Giayetto O,Cerioni GA,Amín M S.Water Use,Growth and Pod Yield of Two Peanut Cultiva under Different Interrow Spacings.Journal of Peanut Science,2005,34(2):5-13.
[17] Li GM,Tang L S,Shang ZQ,Chi SM.Effect of Osmotic Stress on Protective Enzyme Systems in Maize Seedlings and Their Relationship to Drought Resistance.Journal of Agricultural University of Hebei,1994,17(2):1-5.
[18] Zhu H S,Huang P S.Water Stress in Soil and Activated Oxygen Metabolism in Rice.Journal of Nanjing Agricultural University,1994,17(2):7-11.
[19] Deng SX,Zeng M,Xiong W,Luo GJ,Zhang GY,Lui P.Effects of Drought Stress on the Antioxidative Enzyme System in Citrus Leaves.Journal of Southwest University(Natural Science Edition),2011,31(2):61-64.
[20] Wu Q,Zhang X M.Effects of Moisture Conditions on the Gas Exchange of Haloxylon ammodendron.Arid Zone Research,2005,22(1):79-84.
[21] Xue H Q,Sun L Z.Effect of Water Stress om Physiological Character in Different Drought Resistant Peanut Varietie.Agricultural Research in the Arid Areas,1997,15(4):82-85.
[22] Xue H Q,Sun L Z,Gan X M.Study on Comprehensive Assessment and Mechanism of Drought Resistance in Peanut Cultivers.Agricultural Research in the Arid Areas,1999,17(1):83-87.
[23] Li H S.Experimental Principles and Techniques of Plant Physiology and Biological Chemistry.Beijing:Higher Education Press,2000:164-179.
[24] Zhang X Z,Chen F Y,Wang Y F.Plant Physiological Experimental Technology.Shengyang:Liaoning Scienceand Technology Press,1994.
[25] Chen SF,Shu Q Y.Biological Mechanism of and Genetic Engineering for Drought Stress Tolerance in Plants.Chinese Bulletin of Botany,1999,16(5):555-560.
[26] Chen SY.Membrane-lipid Peroxidation and Plant Stress.Chinese Bulletin of Botany,1989,6(4):211-217.
[27] Cabuslay G S,Ito O,Alejar A A.Physiological evaluation of responses of rice to water deficit.Plant Science,2002,163:815-827.
[28] Celikkol Akcay U,Ercan O,Kavas M,Yildiz L,Yilmaz C,Oktem H A,Yucel M.Drought-induced oxidative damage and antioxidant responses in peanut(Arachis hypogaea L.)seedlings.Plant Growth Regulation,2010,61(1):21-28.
[29] Wang W,Li D Q,Li C X,Zou Q.Effects of Water Stress on Osmotic Adjustment of Leaves and Roots of Maize with Different Drought Resistance.Acta Agriculturae Boreall sinica,2000,15(S1):8-15.
[30] Li C X,Wang W,Li D Q.Effects of long-term water stress on osmotic adjustment and osmolytes in wheat roots and leaves.Acta Botanica Borealioccidentalia Sinica,2001,21(5):924-930.
[31] Cai K Z,Wu X Z,Luo S M.Effects of water stress on osmolytes at different growth stages in rice leaves and roots.Journal of Ecology(Chinese Version),2008,32(2):491-500.
[32] Pei R Q,Shi Y S,Lui P Q,Song Y C,Wang T Y,Li Y.Effect of Drought Stress on Osmotic Adjustment in Different Maize Inbred Lines at Seedling Stage.Journal of Plant Genetic Resources,2010,11(1):40-45.
[33] Yan M L,Li X D,Lin Y J,Wang L L,Zhou L Y.Effects of drought during seedling stage on physiological traits,yield and quality of different peanut cultivars.Acta Agronomica Sinica,2007,33(1):113-119.
[34] Yao JP,Luo Y N,Yang X D.A primary study on the critical moisture of early and middle peanut varieties during different growth periods.Chinese Journal of Oil Crop Sciences,1984,(3):36-43.
[35] Yao J P,Yang X D.The studies on suitable water in summer peanut.Peanut Sci Technol,1986,15(2):31-32.
[36] Yao C M,Yang P L,Hao Z Y,Wang Q H.Dynamic analysis on root/shoot development of peanut under different water regimes.Journal of China agriculture university,1999,4(4):40-44.
参考文献:
[1] 山仑.旱地农业技术发展趋势.中国农业科学,2002,35(7):848-855.
[2] 山仑,张岁岐.节水农业及其生物学基础.水土保持研究,1999,(6):3-6.
[3] 李霞,阎秀峰,于涛.水分胁迫对黄檗幼苗保护酶活性及脂质过氧化作用的影响.应用生态学报,2005,16(12):2353-2358.
[4] 王娟,李德全.逆境条件下植物体内渗透调节物质的积累与活性氧代谢.植物学通报,2001,18(4):459-465.
[6] 陈善福,舒庆尧.植物耐干旱胁迫的生物学机理及其基因工程研究进展.植物学通报,1999,16(5):555-560.
[7] 汤章城.逆境条件下植物脯氨酸的积累及其可能的意义.植物生理学通讯,1984,(1):15-21.
[9] 郭卫东,沈向,李嘉瑞,郑学勤.植物抗旱分子生理.西北农业大学学报,1999,27(4):102-106.
[10] 姜慧芳,任小平.干旱胁迫对花生叶片SOD活性和蛋白质的影响.作物学报,2004,30(2):169-174.
[11] 刘祖琪,张石诚.植物生理抗性学.北京:中国农业出版社,1994.
[12] 张立新,李生秀.氮、钾、甜菜碱对水分胁迫下夏玉米叶片膜脂过氧化和保护酶活性的影响.作物学报,2007,33(3):482-490.
[13] 苏培玺,陈怀顺.荒漠绿洲区花生在不同灌溉条件下的产量变化及光合生理特性.作物学报,2005,31(12):1660-1664.
[14] 张其德,刘合芹,张建华,李建民.限水灌溉对冬小麦旗叶某些光合特性的影响.作物学报,2000,26(6):869-873.
[15] 山仑,邓西平,苏佩,张岁岐,黄占斌,张正斌.挖掘作物抗旱节水潜力——作物对多变低水环境的适应与调节.中国农业科技导报,2000,2(2):66-70.
[17] 李广敏,唐连顺,商振清,池书敏.渗透胁迫对玉米幼苗保护酶系统的影响及其与抗旱性的关系.河北农业大学学报,1994,17(2):1-5.
[18] 朱杭申,黄丕生.土壤水分胁迫与水稻活性氧代谢.南京农业大学学报,1994,17(2):7-11.
[19] 邓胜兴,曾明,熊伟,罗光杰,张广越,刘平.干旱胁迫对柑橘叶片保护酶系统的影响.西南大学学报(自然科学版),2009,31(2):61-64.
[20] 吴琦,张希明.水分条件对梭梭气体交换特性的影响.干旱区研究,2005,22(1):79-84.
[21] 薛慧勤,孙兰珍.水分胁迫对不同抗旱性花生品种生理特性的影响.干旱地区农业研究,1997,15(4):82-85.
[22] 薛慧勤,孙兰珍,甘信民.花生品种抗旱性综合评价及其抗旱机理的数量分析.干旱地区农业研究,1999,17(1):83-85.
[23] 李合生.植物生理生化实验原理和技术.北京:高等教育出版社,2000:164-179.
[24] 张宪政,陈凤玉,王荣富.植物生理分析技术.沈阳:辽宁科学技术出版社,1994.
[25] 陈善福,舒庆尧.植物耐干旱胁迫的生物学机理及其基因工程研究进展.植物学通报,1999,16(5):555-560.
[26] 陈少裕.植物膜脂过氧化与逆境.植物学通报,1989,6(4):211-217.
[29] 王玮,李德全,李春香,邹琦.水分胁迫对抗旱性不同的玉米品种根、叶渗透调节能力及渗透调节物 质的影响.华北农学报,2000,15(增刊):8-15.
[30] 李春香,王玮,李德全.长期水分胁迫对小麦生育中后期根叶渗透调节能力、渗透调节物质的影响.西北植物学报,2001,21(5):924-930.
[31] 蔡昆争,吴学祝,骆世明.不同生育期水分胁迫对水稻根叶渗透调节物质变化的影响.植物生态学报,2008,32(2):491-500.
[32] 裴二芹,石云素,刘丕庆,宋燕春,王天宇,黎裕.干旱胁迫对不同玉米自交系苗期渗透调节的影响.植物遗传资源学报,2010,11(1):40-45.
[33] 严美玲,李向东,林英杰,王丽丽,周录英.苗期干旱胁迫对不同抗旱花生品种生理特性、产量和品质的影响.作物学报,2007,33(1):113-119.
[34] 姚君平,罗瑶年,杨新道.早、中熟花生不同生育阶段临界水分研究初报.中国油料,1984,(3):36-43.
[35] 姚君平,杨新道.夏花生适宜水分研究.花生科技,1986,15(2):31-32.
[36] 姚春梅,杨培岭,郝仲勇,王泉海.不同水分条件下沙地花生的根冠发育动态分析.中国农业大学学报,1999,4(4):40-44.

