脱氢卡维丁的肠道转运特性研究
史月姣, 谢 辉*, 毛春芹, 张兴德, 郑雪平
(1.南京中医药大学,江苏南京 210046;2.南京市中医院,江苏南京 210001)
岩黄连为罂粟科植物石生黄堇Corydalis saxicolaBunting的全草及肥大的根茎部,是黔、桂高寒山区珍贵的中药材[1]。从岩黄连中分离得到生物碱类化合物具有降低血清转氨酶活性、降低肝组织羟脯氨酸水平,抑制肝纤维化,减轻肝组织的病变程度等作用。脱氢卡维丁是岩黄连总生物碱中主要活性成分,具有镇静、镇痛、解痉、抗菌和增加肝糖元生成的作用[2]。本研究采用大鼠外翻肠囊模型,考察岩黄连总生物碱中主要活性成分脱氢卡维丁在大鼠肠道的吸收特性,并采用人源结肠腺癌Caco-2细胞单层体外培养模型研究脱氢卡维丁的肠转运特点以及转运蛋白在其转运中的作用,为岩黄连生物碱口服制剂研究提供试验依据。
1 材料与仪器
1.1 药物与试剂
脱氢卡维丁对照品 (批号111667-200401)、盐酸维拉帕米对照品 (批号100223-200102),均购自中国药品生物制品检定所,供含量测定用;岩黄连总生物碱 (本实验室自制,含脱氢卡维丁10.16%);DMEM培养基 (南京凯基生物科技发展有限公司);胎牛血清 (Equitech-BioInc.公司);非必需氨基酸、HEPES粉末、谷氨酰胺、胰蛋白酶、Hank's平衡盐粉末 (sigma公司);乙腈、甲醇为色谱纯,水为超纯水,其余试剂为分析纯。
1.2 仪器
ALC-M离体组织器官试验系统 (上海奥尔科特生物科技有限公司);二氧化碳培养箱(Hearous,德国);320型pH计 (Metller-Toledo分析仪器有限公司);Millicell-ERS跨膜电阻仪 (Millipore,美国);Transwell培 养 板 (NUNC,丹麦);Waters 515型高效液相色谱仪,2487紫外检测器 (Waters,美国);Agilent 1200高效液相色谱仪,Agilent 6120单四极杆质谱检测器(Agilent,美国);涡旋混合仪 (上海沪西分析仪器厂);高速台式离心机 (上海安亭科学仪器厂)。
1.3 细胞
Caco-2 TC7细胞株,由法国 Moniqué Rousset博士馈赠。
1.4 动物
SD大鼠,雄性,体质量 (250±30)g,购自苏州工业园区爱尔麦特科技有限公司,合格证号SCXK(苏)2009-0001。
2 方法与结果
2.1 大鼠外翻肠囊模型试验
2.1.1 岩黄连总生物碱溶液的配制 称取岩黄连总生物碱适量,用新鲜配制的台氏液溶解并定容,配制成岩黄连总生物碱质量浓度分别为0.03、0.06、0.10 mg/mL的高、中、低3个质量浓度的含药台氏液,其中脱氢卡维丁的质量浓度分别为3.05、6.10、10.16 μg/mL。
2.1.2 外翻肠囊试验 参照文献方法[3],大鼠禁食 (不禁水)12 h,乙醚麻醉后沿腹中线开腹,小心地将大鼠肠管与肠系膜剥离,分别取十二指肠(幽门下1 cm为起始点)、空肠上段 (以幽门下15 cm为起始点)、回肠 (以盲肠上20 cm为起始点)各7 cm,放入37℃台氏液中,冲洗至无内容物流出,小心剥离肠段表面的脂肪和血管。将肠段小心翻转,使肠黏膜层在外,浆膜层在内,用手术线结扎一端,向囊内注入台氏液400 μL后结扎另一端使之呈囊状物,将其放入已有含药台氏液9 mL的麦氏浴槽中。试验过程中保持37℃恒温,并向浴槽中通入95%O2和5%CO2的混合气体。分别在15、30、45、60 min取出肠段,用滤纸吸干黏膜面水分,吸取囊内液,测定其中脱氢卡维丁的含量,测量肠管的长与宽。
2.1.3 HPLC样品分析 Agilent XDB C18色谱柱(150 mm×4.6 mm,5 μm);流动相为乙腈-0.01 mol/L磷酸二氢钾-水溶液 (18.5∶81.5);体积流量1.0 mL/min;检测波长347 nm;柱温30℃。色谱图见图1。

图1 台氏液中脱氢卡维丁测定HPLC图Fig.1 HPLC chromatogramsofdehydrocavidine in Tyrode
方法学验证:精密称取脱氢卡维丁对照品10.30 mg,加甲醇溶解并定容至10 mL,制成1.03 mg/mL的脱氢卡维丁贮备液。精密量取贮备液适量分别配制成不同质量浓度的脱氢卡维丁对照品溶液,进样分析,结果表明脱氢卡维丁在1.03~20.60 μg/mL范围内,峰面积(Y)与质量浓度(X)呈良好线性关系,回归方程为Y=35 578.096 1X-3 538.938 7,r=0.999 3。日内、日间精密度RSD均低于5%(n=6),24 h稳定性RSD为2.23%,回收率为97.57%±0.45%。
精密吸取肠囊内液200 μL,于离心机中离心10 min(12 000 r/min),取上清液进样测定,以外标两点法计算脱氢卡维丁的质量浓度。
2.1.4 数据分析 根据测定结果,计算脱氢卡维丁在各肠段的单位面积渗透量和表观渗透系数。表观渗透系数 (Papp)的计算公式如下[4]:
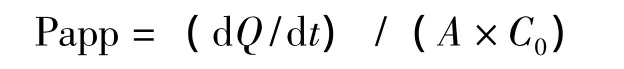
式中,dQ/dt为单位时间药物渗透量 (ng/s),A为肠囊表面积 (cm2),C0为脱氢卡维丁的初始质量浓度 (ng/mL)。
脱氢卡维丁在大鼠各肠段的经时渗透曲线见图2、图3、图4,各肠段表观渗透系数见表1。试验结果表明,随着药物质量浓度的增大,各肠段脱氢卡维丁的单位面积渗透量均有增加;相同的质量浓度下,各肠段脱氢卡维丁的单位面积渗透量随着时间的延长而逐渐增加;十二指肠和空肠的单位面积渗透量比较接近,回肠的单位面积渗透量明显较小。试验质量浓度下同一部位肠段脱氢卡维丁表观渗透系数无显著性差异,十二指肠与空肠的表观渗透系数无显著性差异,回肠的表观渗透系数较小。
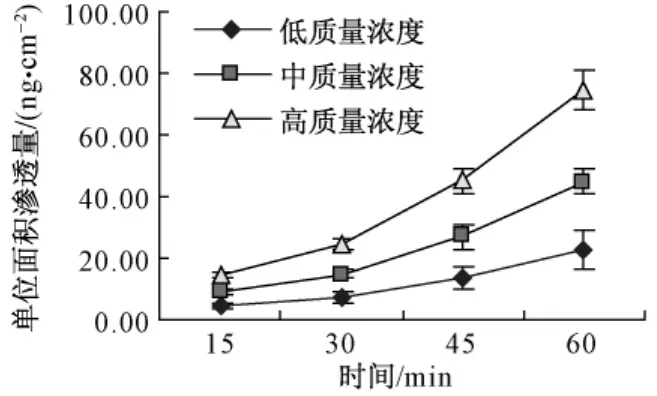
图2 脱氢卡维丁在大鼠十二指肠的渗透曲线Fig.2 Permeability curve of dehydrocavidine in rat's duodenum
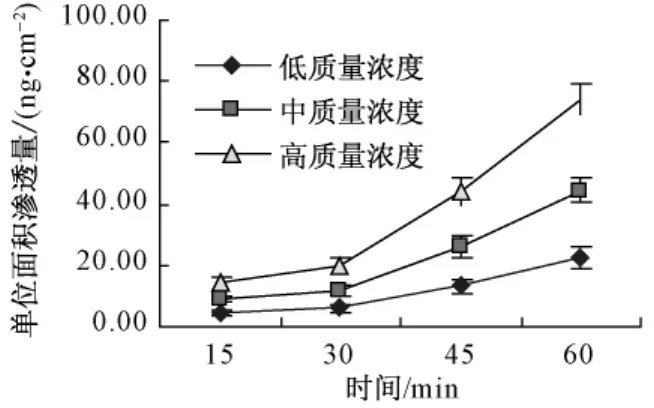
图3 脱氢卡维丁在大鼠空肠的渗透曲线Fig.3 Permeability curve of dehydrocavidine in rat's jejunum
2.2 Caco-2细胞单层模型试验
2.2.1 药物溶液的配制 精密称取脱氢卡维丁10.59 mg,加入DMSO 2 mL,用超纯水稀释定容至10 mL作为贮备液。将贮备液用 HBSS溶液(pH7.4)稀释至质量浓度为6.99 ng/mL(即20.0 μmol/L)的脱氢卡维丁溶液。
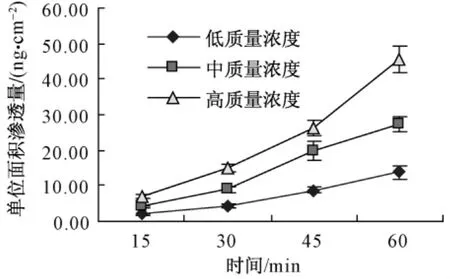
图4 脱氢卡维丁在大鼠回肠的渗透曲线Fig.4 Permeability curve of dehydrocavidine in rat's ileum

表1 脱氢卡维丁在大鼠各肠段的表观渗透系数Tab.1 Apparent permeability coefficient of dehydrocavidine in rat's intestine
精密称取盐酸维拉帕米对照品适量,与上述脱氢卡维丁对照品贮备液用HBSS(pH7.4)溶解并配制成含盐酸维拉帕米的脱氢卡维丁溶液,其中脱氢卡维丁的质量浓度为6.99 ng/mL,盐酸维拉帕米为9.80 ng/mL。
2.2.2 双向跨膜转运试验 参考文献 [5-7],建立Caco-2细胞单层模型。试验前首先用37℃预热的Hank's平衡盐溶液 (HBSS,pH7.4)溶液洗涤细胞单层3次,用跨膜电阻仪检测跨膜电阻,各孔跨膜电阻值均大于空白对照值100 hm/4.2 cm2以上,即符合实验要求可用于试验。加入预热的HBSS(pH7.4)溶液,于37℃摇床中孵育1 h,吸弃HBSS(pH7.4)溶液。
脱氢卡维丁从A侧到B侧的转运:将脱氢卡维丁溶液加至细胞绒毛面Apical(A)侧为供给液,同时将空白HBSS(pH7.4)溶液加至细胞基底面Basolateral(B)侧作为接收液,将Transwell培养板置于转速为50 r/min的37℃恒温摇床中,分别在0、1、2、3、4 h吸取供给池、接收池溶液各400 μL待测,同时补加等容积相应的溶液。
脱氢卡维丁从B侧到A侧的转运:将脱氢卡维丁溶液加至B侧作为供给液,空白的HBSS(pH7.4)溶液加至A侧作为接收液,其余操作与上述从A侧到B侧的转运相同。
盐酸维拉帕米对脱氢卡维丁双向跨膜转运的影响:对含盐酸维拉帕米的脱氢卡维丁溶液按上述操作进行双向跨膜转运试验。
2.2.3 HPLC/MS样品分析 Sapax BR-C18色谱柱(2.1 mm×50 mm,1.8 μm)(苏州赛分科技有限公司);Sapax BR-C18保护柱 (2.0 mm×10 mm,1.8 μm)(苏州赛分科技有限公司);流动相为0.1%甲酸-甲醇 (70∶30);体积流量0.2 mL/min;柱温30℃。
质谱条件:ESI;工作模式:SIM;m/z350;裂解电压150 V;毛细管电压3 000 V;喷雾器压力206.82 kPa;脱溶剂温350℃;脱溶剂气体体积流量480 L/h。色谱图见图5。
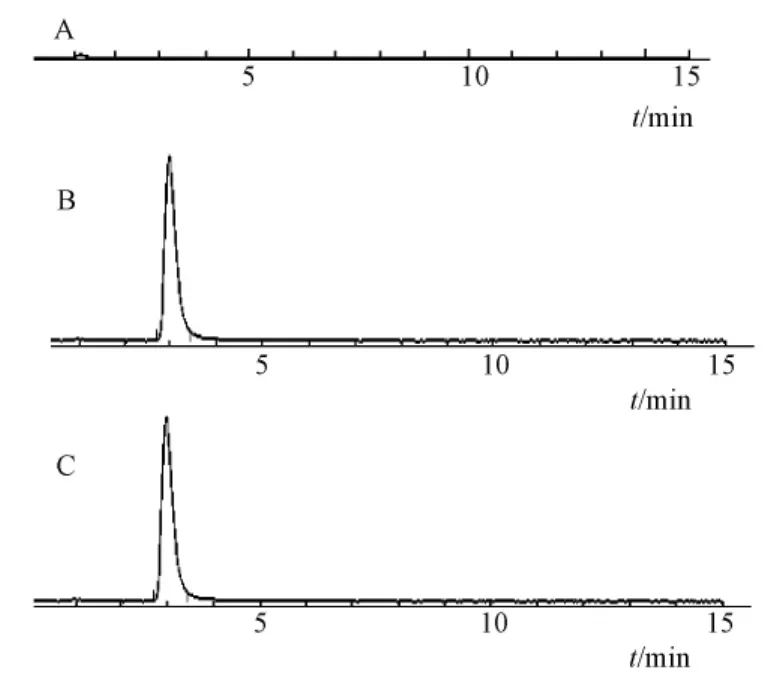
图5 HBSS中脱氢卡维丁测定HPLC/MS图Fig.5 HPLC/MS chromatograms of dehydrocavidine in HBSS
方法学验证:精密量取脱氢卡维丁贮备液适量分别稀释配制成不同质量浓度的脱氢卡维丁对照品溶液,进样分析。结果表明,脱氢卡维丁在0.10~105.90 ng/mL范围内,峰面积值 (Y)与质量浓度 (X)呈良好的线性关系,回归方程为Y=420.423 3X+7.387 1,r=0.999 9。日内、日间精密度RSD均低于2%(n=6),24 h稳定性RSD为1.10%,回收率为98.33%±0.71%。
在上述转运试验取样溶液中,精密加入甲醇400 μL,涡旋混匀,于离心机中12 000 r/min离心15 min,取上清液进样测定,以外标两点法计算脱氢卡维丁的质量浓度。
2.2.4 数据分析 计算各时间点的累计转运量,并按2.1.4项下公式计算表观渗透系数,公式中A为转运膜的面积4.2 cm2。
脱氢卡维丁双向累计转运量随时间的变化见图6,表观渗透系数测定结果见表2。
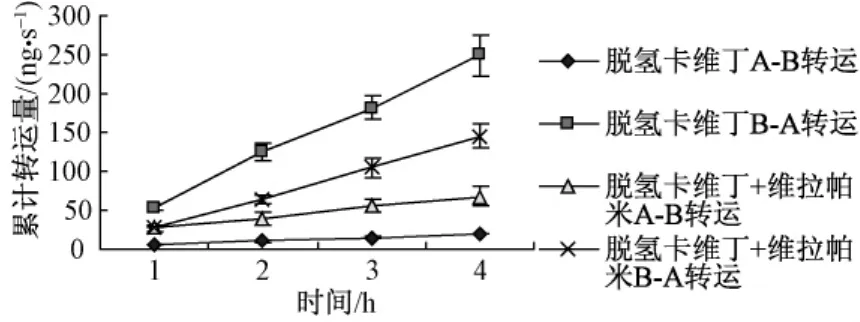
图6 脱氢卡维丁1-4 h跨膜转运量Fig.6 Cumulative transport amount of dehydrocavidine in 1-4 hours

表2 脱氢卡维丁的双向转运行为及盐酸维拉帕米对其转运的影响Tab.2 Bi-directional transport characteristics of dehydrocavidine and the influence of transport by verapamil hydrochloride
试验结果表明,随着时间延长,脱氢卡维丁的累计转运量逐渐增加,两者间呈较好的正相关性。脱氢卡维丁从B侧到A侧的渗透系数即分泌渗透系数 (PBA)比其吸收渗透系数PAB大 (P<0.05),两者均值的比值即外排比率PBA/PAB>4,提示脱氢卡维丁在小肠吸收转运的过程中存在载体的外排作用。
Caco-2细胞单层顶侧膜上有丰富的P-gp的表达,盐酸维拉帕米为P-gp抑制剂,盐酸维拉帕米能显著促进脱氢卡维丁通过Caco-2单层细胞模型的A到B侧的转运量。加入盐酸维拉帕米后,脱氢卡维丁的吸收渗透系数增加了2.68倍,脱氢卡维丁在Caco-2细胞模型中的外排比率比未加盐酸维拉帕米的对照组下降了75.56%,提示脱氢卡维丁在Caco-2细胞单层中的转运存在P-gp的外排作用。
3 讨论
口服给药系统设计中,活性成分在肠道的转运是影响生物利用度的重要因素。本研究首先采用外翻肠囊模型考察不同质量浓度岩黄连生物碱中脱氢卡维丁在大鼠不同肠段的转运特性。预试验发现岩黄连总生物碱在台氏液中质量浓度超过0.1 mg/mL时不能完全溶解,为避免对试验结果产生影响,最高质量浓度选择0.1 mg/mL,结合药效试验剂量,最低质量浓度选择0.03 mg/mL。通过试验发现岩黄连总生物碱中脱氢卡维丁在不同部位的离体肠囊内均有吸收,但表观渗透系数均较小。脱氢卡维丁在回肠的渗透性小于十二指肠与空肠。试验质量浓度下,同一部位肠段脱氢卡维丁表观渗透系数无显著性差异,表现出被动转运的特征。
肠壁细胞膜内侧存在的药物外排泵如P-gp和MRP等,能将药物从肠浆膜转到肠黏膜而排入肠腔,从而导致药物吸收量减少。本项目前期研究制得的岩黄连提取物中生物碱类成分占56.89%,通过紫外光谱、高分辨质谱及二级质谱分析,结果表明其中含多种原小檗碱类化合物,主要包括脱氢卡维丁、盐酸巴马汀、盐酸小檗碱等。文献研究显示,盐酸巴马汀与盐酸小檗碱在肠道的转运均受P-gp外排作用影响[8-10],这两种成分的量在制备的提取物中仅次于脱氢卡维丁。为了考察P-gp是否影响同为原小檗碱型生物碱的脱氢卡维丁的肠道转运,本实验采用Caco-2细胞单层模型进一步研究脱氢卡维丁双向跨膜转运行为。转运蛋白多具有饱和性,本研究在设定浓度时,选用了较低的药物浓度 (20 μmol/L),避免了可能存在的外排蛋白被饱和现象对结果的影响。脱氢卡维丁在试验浓度下转运4 h试验结束后未见细胞跨膜电阻下降,说明在该浓度条件下不会出现细胞毒性。通过研究P-gp抑制剂盐酸维拉帕米添加前后脱氢卡维丁双向转运行为的变化,发现脱氢卡维丁在Caco-2细胞单层中的转运存在P-gp的外排作用。
根据试验结果,分析认为脱氢卡维丁的肠黏膜转运存在转运蛋白的外排机制,但在提取物中多种生物碱组分共存条件下,因转运蛋白外排的饱和而呈现一定的被动转运特征。其他膜转运蛋白在脱氢卡维丁跨膜转运过程中的影响有待进一步研究。
[1]中国科学院广西植物所.广西植物志[M].南宁:广西科学技术出版社,1993:410.
[2]陈重阳,赵 一.中药岩黄连主要成分脱氢卡维丁的药理研究[J].中药通报,1982,2:31-34.
[3]魏 伟,吴希美,李元建,主编.药理实验方法学 (第4版)[M].北京:人民卫生出版社,2010,526.
[4]Artursson P,Karlsson J.Correlation between oral drug absorptionin in humans and apparent drug permeability coefficients in human intestinal epithelial(Caco-2)cells[J].Biochem Biophys Res Commun,1991,175(3):880-885.
[5]Hu M,Chen J,Tran D,et al.The Caco-2 cell monolayers as an intestinal metabolism model:metabolism of dipeptide PhePro[J].Drug Target,1994,2:79-89.
[6]Hu M,Chen J,Zhu Y,et al.Mechanism and kinetics of transcellular transport of a new β-actam antibiotic loracarbef across a human intestinal epithelial model system(Caco-2)[J].Phrm Res,1994,11:1405-1413.
[7]陈 彦,贾晓斌,胡 明,等.淫羊藿苷在Caco-2细胞单层模型中的吸收机制[J].中国中药杂志,2008,33(10):1164-1167.
[8]张新峰,裘福荣,蒋 健,等.LC-MS/MS测定药根碱、巴马汀和小檗碱在Caco-2细胞的摄取特性[J].中国药学杂志,2010,45(19):1504-1508.
[9]Maeng H J,Yoo H J,Kim I W,et al.P-glycoprotein-mediated transport of berberine across Caco-2 cell monolayers[J].J Pharm Sci,2002,91:2614-2621.
[10]PanG Y,Wang G J,LiuX D,et al.The involvement of P-glycoprotein in berberine absorption[J].Pharmacol Toxicol,2002,91:193-197.

