HPLC法测定地奥司明原料药及片剂的含量和有关物质
赵 喆,唐素芳(天津市药品检验所,天津 300070)
地奥司明临床上用于治疗与静脉、淋巴功能不全相关的各种疾病(如静脉性水肿、软组织肿胀、四肢沉重等)及急性痔发作,其制剂主要有地奥司明片。目前,地奥司明原料药及制剂尚未载入2010年版《中国药典》,而执行的标准是国家食品药品监督管理局暂行标准(国标)[1]。现版的国外药典中如《欧洲药典》(EP7.0)[2]和《英国药典》(BP)2012年版[3]仅收载地奥司明的原料药,均未收载制剂。根据国家药典委员会2011年基本药物标准提高的任务分工,我所对该品种质量标准进行了修订,对质量标准中性状、鉴别、检查和含量测定等项目均进行了试验研究,并结合样品的检验情况,拟订了质量标准。其中有关物质的研究工作参考了EP7.0有关物质的检查方法并结合国内产品的生产工艺等实际情况,对本品的杂质情况进行了研究和考察,建立了有效可控的有关物质检查方法,并采用同一色谱系统对含量进行了测定,完善了质量标准,有效控制了本品的质量,本文对此报道如下。
1 材料
1200系列高效液相色谱(HPLC)仪,包括泵、脱气机、二极管阵列检测器、自动进样设备、柱温箱等(美国Agilent公司);AE 240型分析天平(瑞士Mettler Toledo仪器公司)。
地奥司明对照品(某药厂提供,批号:120501,纯度:98.1%);橙皮苷对照品(中国食品药品检定研究院,批号:110721-201115,纯度:95.3%);地奥司明系统性试验对照品(购自欧洲药品质量管理局,为包含地奥司明和6种杂质的混合对照品);地奥司明原料药(四川某公司,批号:C006G110301、C006G110601、C006G110602;江苏某公司,批号:100908、100909、100910;纯度:均>90%);地奥司明片(江苏某公司,批号:120606、120607、120608;武汉某公司,批号:110207、110302、110303,规格:均为每片0.45g);乙腈、甲醇均为色谱纯,水为纯化水。
2 有关物质测定
2.1 色谱条件
色谱柱:Phenomenex C18(100mm×4.6mm,3μm);流动相:水-甲醇-冰醋酸-乙腈(66∶28∶6∶2,V/V/V/V),流速:0.7ml/min;检测波长:275nm;柱温:40℃;进样量:10μl。
2.2 溶液的制备
系统适用性溶液:称取系统适用性对照品5mg,加二甲基亚砜(DMSO)5ml溶解,即得。
橙皮苷对照品贮备液:精密称取橙皮苷对照品10mg,置于10ml量瓶中,加DMSO溶解并稀释至刻度,摇匀,即得。
供试品溶液a(有关物质):精密称取原料药(或片粉)适量,加DMSO溶解并制成1mg/ml的溶液,摇匀(片剂溶液过滤,取续滤液),即得。
对照溶液(有关物质):精密量取橙皮苷对照品贮备液1ml和供试品溶液a 3ml,置于100ml量瓶中,加DMSO稀释至刻度,摇匀,即得。
供试品溶液b(含量测定):精密称取原料(或片粉)适量,加DMSO溶解并制成0.2mg/ml的溶液,摇匀(片剂溶液过滤,取续滤液),即得。
辅料溶液:按照江苏某公司提供的处方比例,按供试品溶液b配制方法配制不含主成分的辅料溶液。
2.3 系统适用性试验
量取系统适用性溶液10μl注入色谱仪,考察分离效果。结果显示,系统适用性溶液中的6个杂质(A、B、C、D、E、F)全部检出并达到基线分离,橙皮苷峰与主峰的分离度为8.0,理论板数按主峰计为3700,详见图1。
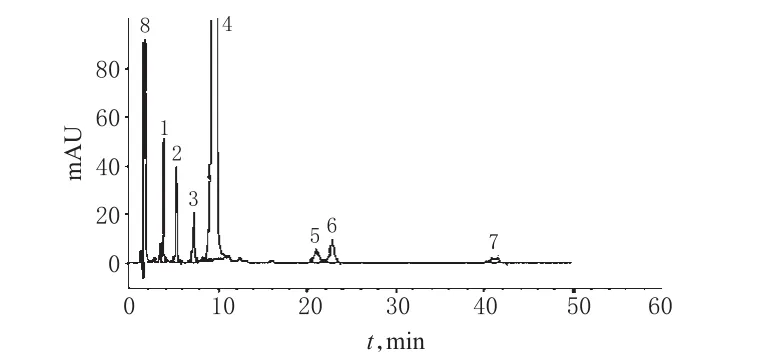
图1 系统适用性溶液色谱图1.杂质A;2.杂质B(橙皮苷);3.杂质C;4.地奥司明;5.杂质D;6.杂质E;7.杂质F;8.溶剂Fig 1 HPLC chromatogram of system suitability test1.impurity A;2.impurity B(hesperidin);3.impurity C;4.diosmin;5.impurity D;6.impurity E;7.impurity F;8.solvent
系统适用性对照品目前国内无法提供,只能购自欧洲药品质量管理局,且价格昂贵,而中国食品药品检定研究院仅能够提供橙皮苷对照品。为适应国内的检验条件,本次试验选择了3根不同品牌的色谱柱Phenomenex、Inertsil ODS-3、Waters Atlantis T3[分别编号①、②、③,规格均为(100mm×4.6mm,3μm)],分别取系统适用性溶液进样考察,拟通过限定橙皮苷峰与主峰的分离度作为系统适用性试验的条件,确保所有杂质的分离和检出,结果分离度分别为8.0、5.3、4.6,理论板数分别为3700、7000、6500。表明系统适用性溶液中的6个杂质如能全部检出并达到基线分离,橙皮苷峰与主峰的分离度应至少>4.6。不同色谱柱的理论板数差异较大,结合试验数据将理论板数定为不低于3000。根据试验结果,拟定色谱条件与系统适用性试验为“2.1”项下色谱条件,量取对照溶液注入色谱仪,记录色谱图,橙皮苷峰与主峰的分离度应不低于4.6,理论板数按主峰计算应不低于3000。
2.4 有关物质的测定方法及限度的确定
量取对照溶液适量,用DMSO稀释20倍作为灵敏度测试溶液,注入色谱仪,调节检测灵敏度,使主峰的信噪比不小于10;再精密量取供试品溶液a与对照溶液分别注入色谱仪,记录色谱图至主峰保留时间的5倍。杂质的限度和计算方法经参考EP7.0中地奥司明的杂质限度,并结合收集到的样品有关物质的测定结果,修订为:已知杂质橙皮苷按外标法计算,限度不得过5.0%;其他单个杂质按主成分自身对照法计算,含量在1.0%~3.0%的杂质不得多于3个,剩余的其他单个杂质不得过1.0%。总杂质(含橙皮苷)按主成分自身对照法计算,原料药限度不得过10.0%;片剂考虑其生产及贮存过程中杂质可能增加的情况,并结合收集到的样品的有关物质的测定结果,修订为“不得过13.0%”。
2.5 专属性试验
分别取地奥司明原料药(批号:C006G110301)25mg、片粉(批号:120606)40mg和辅料10mg各4份,分别加DMSO 15ml进行如下处理。(1)酸破坏:加1mol/L的盐酸溶液4ml,80℃水浴加热10min,放冷,用氢氧化钠试液调至pH为7,加DMSO稀释至25ml(片粉和辅料溶液需过滤,以下同)。(2)碱破坏:加氢氧化钠试液1ml,放置2h,用1mol/L盐酸溶液调至pH为7,加DMSO稀释至25ml。(3)氧化破坏:加30%过氧化氢溶液1ml,80℃水浴加热30min,放冷,加DMSO稀释至25ml。(4)高温破坏:80℃水浴加热30min,放冷,加DMSO稀释至刻度,摇匀。(5)光照破坏:加DMSO稀释至刻度,摇匀,直接光照5d。分别取上述5种溶液,进样测定,结果表明在上述条件下,除高温和光照条件下溶液比较稳定,色谱图基本无变化外,其余条件下主峰均有降解,但降解的杂质均可与主峰达到基线分离。说明拟定的色谱条件专属性较好,辅料溶液基本无变化,对测定无干扰,详见图2。
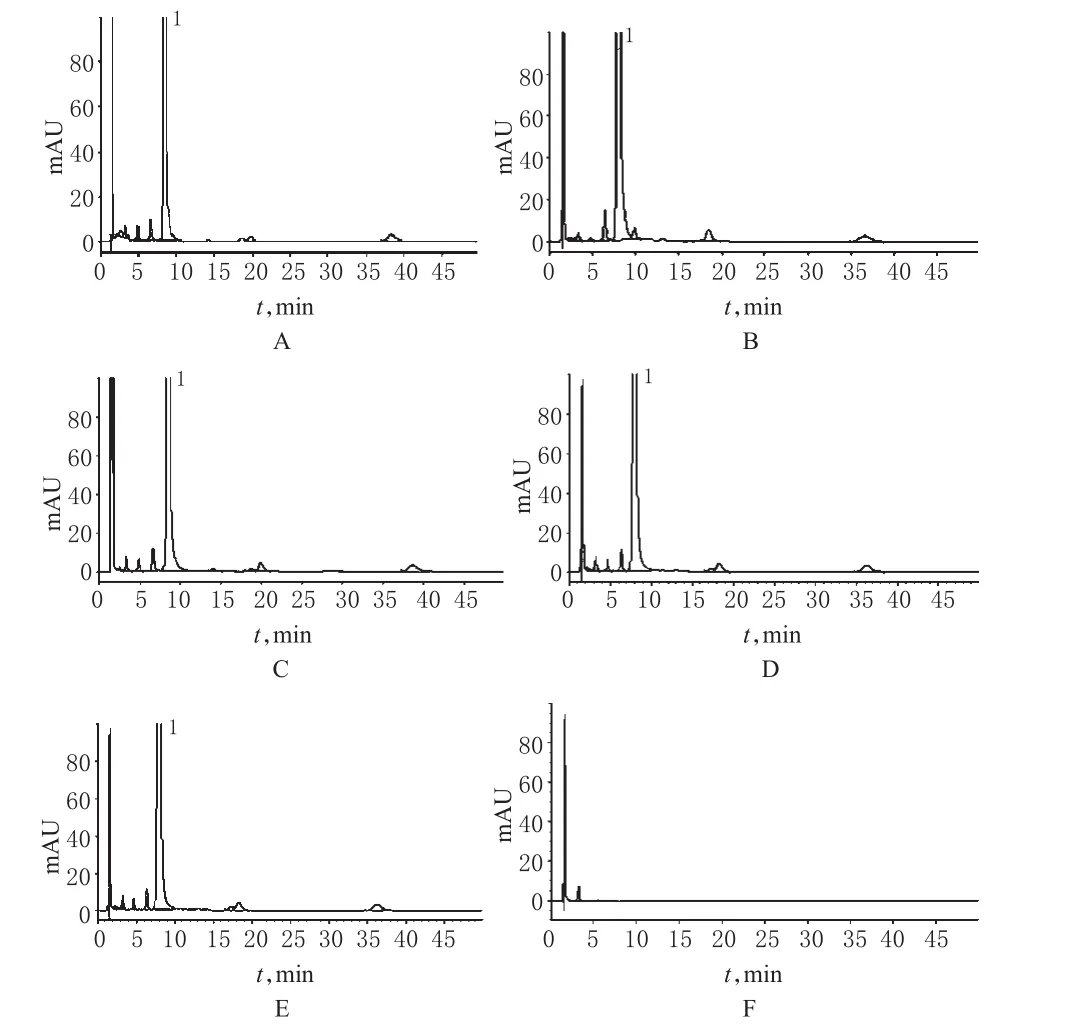
图2 专属性试验高效液相色谱图A.酸破坏样品;B.碱破坏样品;C.氧化破坏样品;D.高温破坏样品;E.光照破坏样品;F.辅料;1.地奥司明Fig 2 HPLC chromatograms of specificity testA.samples destroyed by acid;B.samples destroyed by alkali;C.samples destroyed by oxidant;D.samples destroyed by high temperature;E.samples destroyed by strong light;F.excipients;1.diosmin
2.6 线性关系试验
精密称取橙皮苷和地奥司明对照品适量,用DMSO稀释制成二者质量浓度均为0.5、1.0、2.0、5.0、10.0、30.0、50.0、100.0μg/ml的系列溶液,分别注入色谱仪,记录色谱图;分别以橙皮苷和地奥司明的质量浓度(c)为横坐标,以相应的峰面积(A)为纵坐标,进行线性回归。结果,橙皮苷线性方程为A=1.99×10c-1.404(r=0.9999,n=7)(相应的杂质限度范围为0.1%~10.0%),检测质量浓度线性范围为0.996~99.7μg/ml;地奥司明线性方程为A=1.64×10c-12.449(r=0.9999,n=6)(相应的杂质限度范围为0.25%~10.0%),线性范围为2.47~98.9μg/ml。
2.7 检测限确定
取“2.6”项下溶液适量,采用逐步稀释法稀释,进样测定,结果信噪比为3时,地奥司明、橙皮苷的检测限分别为15、5ng。
2.8 系统精密度试验
取对照溶液和供试品a溶液(批号:C006G110301)适量,分别重复进样6次,对照溶液中橙皮苷、地奥司明峰面积RSD分别为0.4%、0.5%,供试品溶液a中地奥司明峰面积RSD为0.2%,表明本系统精密度良好。
2.9 方法精密度试验
按照“2.2”项下方法配制6份供试品(批号:C006G110301)溶液进样测定,计算,结果基本一致,详见表1。
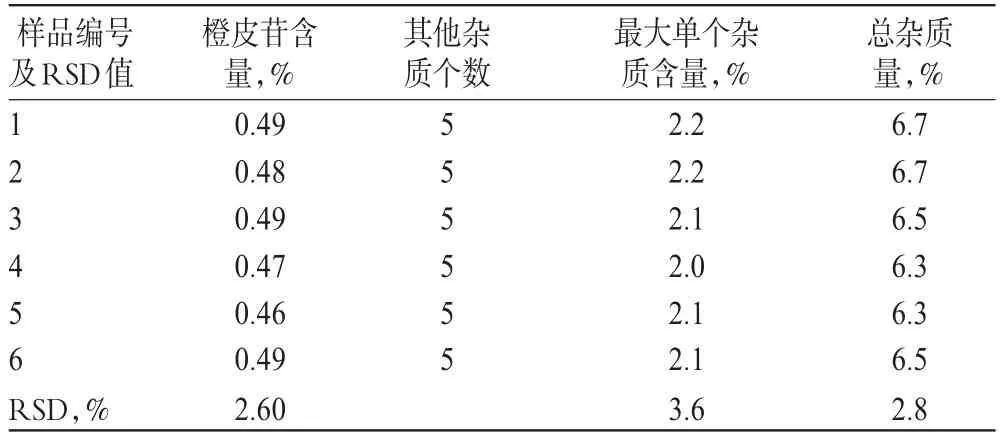
表1 有关物质精密度试验结果Tab 1 Results of precision test of related substances
2.10 稳定性试验
取对照溶液及供试品溶液a适量在室温下分别放置0、4、8、12、24h,测定。结果对照溶液中橙皮苷峰面积的RSD为0.5%,供试品溶液中地奥司明、橙皮苷峰面积的RSD分别为0.5%、2.6%。表明溶液在24h内基本稳定。
2.11 橙皮苷加样回收率试验
分别精密称取地奥司明原料药(批号:C006G110301)7份(其中1份作为空白),每份100mg,置于100ml量瓶中,加DMSO适量,使溶解,精密加入橙皮苷对照品贮备液1ml,加DMSO稀释至刻度,摇匀,注入色谱仪,记录色谱图;空白溶液同法测定橙皮苷,扣除峰面积后计算回收率。结果平均回收率为98.8%,RSD为1.1%(n=6)。
2.12 耐用性试验
本次试验采用3种不同型号的色谱柱,对不同厂家的同一批样品进行耐用性考察,按“2.3”项下色谱柱编号进行试验,结果基本一致,详见表2。
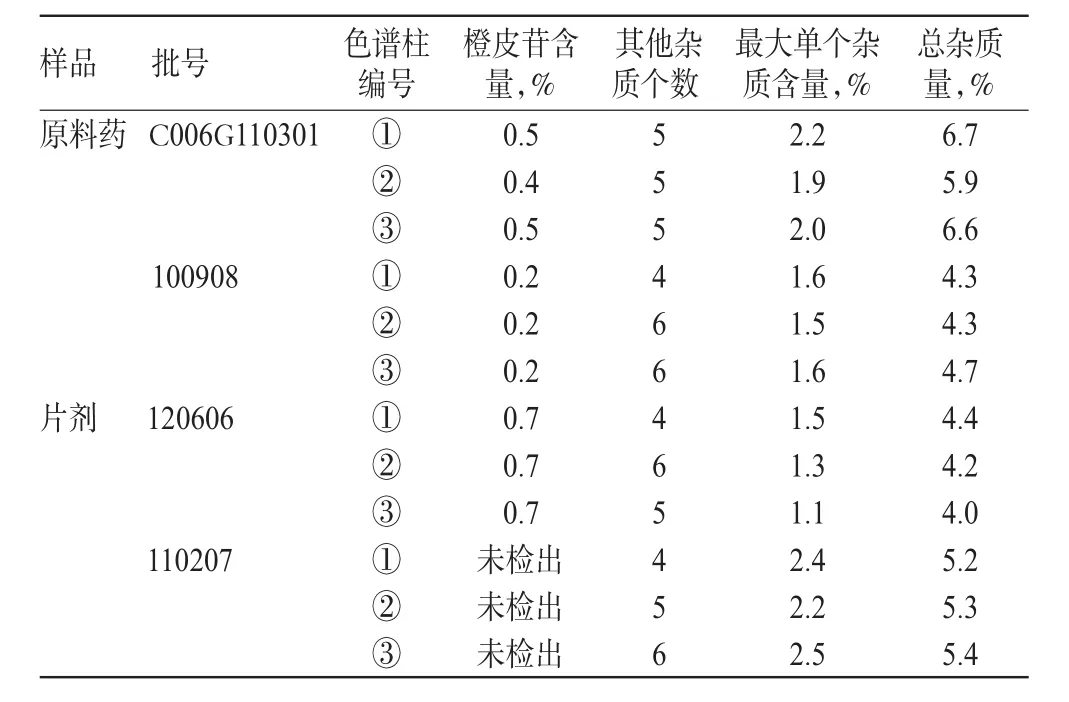
表2 耐用性试验结果(n=3)Tab 2Results of durability test(n=3)
上述结果显示,采用不同的色谱柱测定,检出杂质个数基本相同,最大单一杂质和总杂质量的测定结果基本一致,橙皮苷的测定结果也基本一致。表明本方法的耐用性较好,不同型号的C18色谱柱均适用。
2.13 有关物质测定结果
精密量取对照溶液与供试品溶液a,按照“2.4”项下方法,对6批原料药和6批片剂进行有关物质测定,结果见表3、图3。
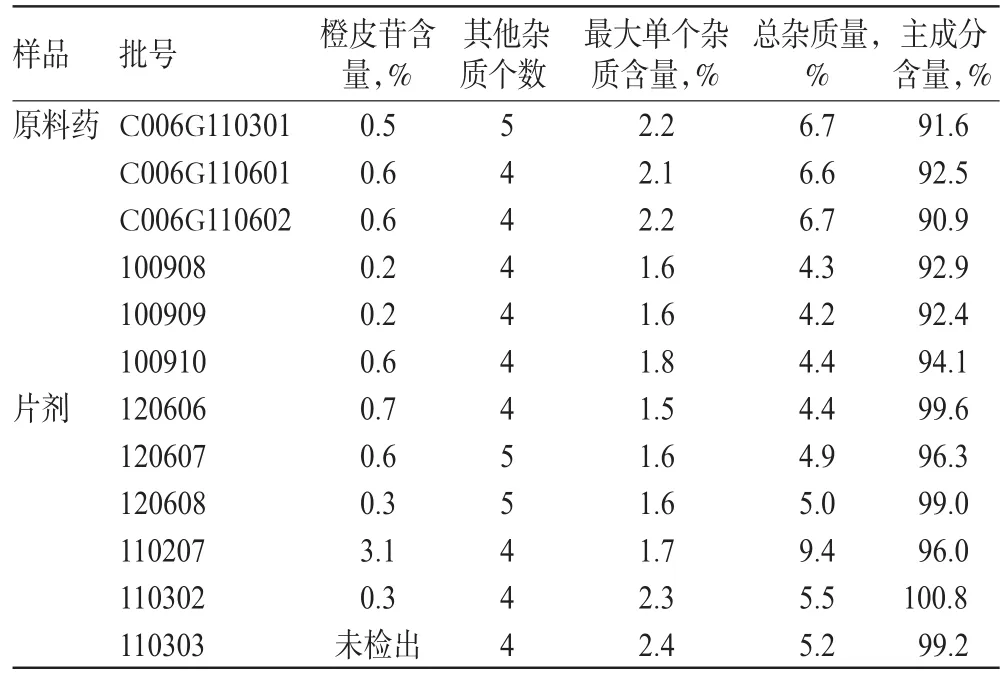
表3 样品测定结果(n=2)Tab 3Results of content determination of samples(n=2)
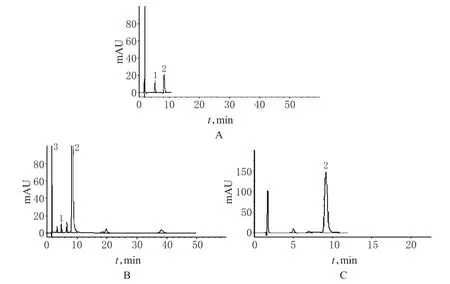
图3 样品测定高效液相色谱图A.对照溶液;B.供试品溶液a;C.供试品溶液b;1.橙皮苷;2.地奥司明;3.溶剂Fig 3 HPLC chromatograms of samplesA.control solution;B.test solution a;C.test solution b;1.hesperidin;2.diosmin;3.solvent
3 主成分含量测定
采用有关物质项下的色谱系统,供试品溶液的质量浓度修订为0.2mg/ml。经试验,地奥司明线性方程为A=1.62×10c-1.05×10(r=0.9999,n=5),检测质量浓度线性范围为99.63~298.9μg/ml,平均回收率为 99.2%(RSD=0.5%,n=6)。按照拟定方法测定6批原料药和6批片剂中主成分的含量,结果见表3、图3。
4 讨论
4.1 色谱系统的选择
前期试验中采用国家标准中色谱系统对系统适用性溶液进行试验,结果其中的6个杂质(A、B、C、D、E、F)在该色谱系统中未能全部检出,而在EP7.0的色谱系统中能全部被检出,表明EP7.0的流动相系统优于现有国家标准。
4.2 色谱柱的选择(5μm和3μm色谱柱的选择)
本文建立的方法采用色谱柱为C18(100mm×4.6mm,3μm),规格较特殊,在日常检验工作中不常使用。因此,对可否用常规的色谱柱替代,笔者做了如下比对试验:选用了3根不同品牌的常规C18(250mm×4.6mm,5μm),用系统适用性溶液分别进样,考察分离效果。结果显示,5μm色谱柱中,只有1根(Phenomenex)色谱柱能全部检出6个杂质,但杂质B与杂质C未达到基线分离,且杂质的相对保留时间与EP7.0中标注的完全不同,其他2根色谱柱均不能完全分出6个杂质;而不同品牌的3μm内径的色谱柱能将6个杂质全部分离出来,且杂质的相对保留时间与EP7.0基本相同。表明内径3μm色谱柱的分离效果明显优于5μm的色谱柱,更有利于杂质的全部检出。故拟定标准中规定选用特殊规格的色谱柱。
综上所述,本文的色谱系统能完全有效地检出并分离地奥司明原料药及片剂的有关物质,可有效地控制本品的质量,优于国家现行质量标准。
[1] 国家食品药品监督管理局.YBH01832009地奥司明[S].2009-02-10.
[2] Directorate for the Quality of Medicines&Healthcare of the Council of Europe(EDQM).European Pharmacopoeia[S].7.0.Strasbourg :Council of Europe,2010:1864-1865.
[3] British Pharmacopoeia Commission.British Pharmacopoeia[S].2012edition.London:Stationary Office,2011:729-730.

