金鱼藻对重金属Cr6+的吸附特征研究
盛周君,陈 玉
(1.安徽绿华环境科技发展有限公司,安徽 合肥 230061;2.安徽省环境科学研究院,安徽 合肥 230061)
1 引言
铬(Cr)遍布于自然界,在水体和大气中均含有微量的铬。铬有多种价态,其中仅Cr3+与Cr6+具有生物意义[1]。铬是人体必需的微量元素,但存在大量的铬污染环境,则会危害人体健康。随着铬的价态不同,人体吸收铬的效率也不一样,大量摄入铬可以在体内造成明显的蓄积。Cr3+和Cr6+对水生生物都有致死作用[2]。其中,Cr6+和毒性比Cr3+高100倍左右。
铬及其化合物是冶金工业、金属加工电镀、制革、油漆、颜料、印染、制药、照相制版等行业必不可少的原料,因此广泛应用于工业生产的各个领域。目前,处理铬污染的方法主要有还原沉淀法、电解法沉淀过滤、膜分离法、吸附法、光催化法等。其中,生物吸附法是一种新兴的重金属废水处理技术[3,4],它利用廉价的生物材料对重金属进行吸附,尤其适宜低浓度重金属废水的处理,并且具有吸附量高,吸附速度快等优点。
近年来,植物材料作为一种有竞争力的、潜在的生物吸附剂开始受到广泛关注[5]。但以往的这些研究多以叶幅较宽的轮叶黑藻等为对象,较少涉及具针状叶的金鱼藻;另外,所研究的重金属多为 Cu2+和 Cd2+[6~8],涉及Cr6+的研究不多;此类研究多针对非活性的植物材料[9~12],而对活体沉水植物则研究较少。
金鱼藻为安徽安庆地区常见的沉水植物,2006年安庆沿江湖泊通江以来,通江渠已成为工农业废水入江的主要通道。相关调查表明[13],金鱼藻在通江渠内繁殖较快,具有明显的竞争优势。金鱼藻对Cr6+的吸附,能直接影响电镀废水入江的污染物浓度。研究金鱼藻对Cr6+的吸附特征,对电镀废水中重金属的去除以及重金属污染水体水质功能恢复具有十分重大的意义。
2 材料和方法
2.1 仪器
JH722可见分光光度计(上海菁华科技仪器有限公司);比色皿(1cm);50mL具塞比色管;移液管;容量瓶;锥形瓶(250mL);FA2104N电子天平(上海精密科学仪器有限公司);SHA-C水浴恒温振荡器(JinTan Heng-Feng Instrument Factory)。
2.2 试剂
丙酮;(1+1)硫酸;(1+1)磷酸;铬标准贮备液:称取于120℃干燥2h的重铬酸钾(分析纯)0.2829g,用水溶解,移入1000mL容量瓶中,用水稀释至标线,摇匀。每毫升贮备液含0.100mgCr6+;5)二苯碳酰二肼溶液:称取二苯碳酰二肼0.2g溶于50mL丙酮中,加水稀释至100mL,摇匀,贮于棕色瓶内,置于冰箱中保存。
2.3 材料准备
沉水植物金鱼藻取自长江,实验前室内驯化2周后,截取新鲜健康形态较一致的顶枝,用3%的盐酸溶液浸洗后再用蒸馏水冲洗,用滤纸吸干植物表面水分后备用。将分析纯铬标准贮备液配制成浓度为1mg/L的Cr6+使用液于1000mL容量瓶(25℃)中备用。
2.4 实验办法
2.4.1 金鱼藻处理
取100mL初始Cr6+浓度分别为0、0.1、0.2、0.4、0.6、0.8、1.0mg/L的溶液于一系列的250mL锥形瓶中,用0.1mol/L的 H2SO4溶液调pH值至5~6,最后加入1g金鱼藻(鲜重),在实验过程中不再调节pH值。将反应器(250mL锥形瓶)放在摇床中振荡(200r/min,25℃±1℃)。由于沉水植物对重金属离子的吸附速度较快,一般在20min内即可达到吸附平衡[14],因此本实验为使吸附完全选定吸附时间为90min。停止振荡后,过滤锥形瓶中的溶液,使植物与溶液分离。用分光光度法测定滤液中Cr6+浓度。实验设置2个平行组,同时进行一系列未加植物材料的实验对照组,以避免玻璃容器的器壁对Cr6+的吸附和水解沉淀。对照实验表明,实验容器(锥形瓶)的器壁没有吸附Cr6+也没有产生水解沉淀现象。
2.4.2 实验标定
(1)标准曲线的绘制。取9支50mL比色管,依次加入 0、0.20、0.50、1.00、2.00、4.00、6.00、8.00、和10.00mL铬标准使用液,用水稀释至标线,分别加入(1+1)硫酸0.5mL和(1+1)磷酸0.5mL,摇匀。加入2mL显色剂溶液(二苯碳酰二肼溶液),摇匀。5~10min后,于540nm波长处,用1cm比色皿,以去离子水做参比,测定吸光度。以吸光度为纵坐标,相应Cr6+含量为横坐标绘出标准曲线。
(2)样品的测定。取10mL滤液于50mL比色皿中,用水稀释至标线,以下步骤同标准溶液测定。进行空白校正后根据标准曲线查得Cr6+含量。
2.4.3 计算
Cr6+(mg/L)=m/V。式中,m 为从标准曲线上查得得Cr6+量,ug;V 为水样的体积,mL。
2.4.4 数据处理
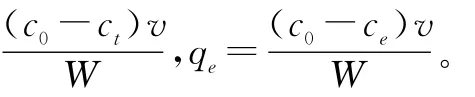
3 结果与讨论
3.1 吸附模型
将整个吸附过程用吸附等温线来描述[15]常用来评价吸附剂的吸附能力。为了研究沉水金鱼藻对Cr6+的最大吸附量和吸附模型,采用2种最常用的吸附等温式Langmuir和Freundlich模型来拟合吸附过程。
3.1.1 Langmuir模型
Langmuir模型是根据气固二相间的单分子层吸附的假设而推导得出的,适用于短时间的单组分重金属的生物吸附,其方程表达式如(1)式:

(1)式可写成以下线性表达式如式(2):

式中,qm最大吸附量;ka是吸附平衡常数。以ce/qe对ce做图,运用最小乘法进行线性拟合。根据斜率和截距可求出吸附参数qm和ka。
3.1.2 Freundlich模型
Freundlich方程是一个半经验方程,可用于各种非理想条件下的表面吸附以及多分子层吸附。Freundlich方程表达式如(3)式:

等式两边分别求对数可得其线性表达式如(4)式:

式中,kF和n是常数。同样可以根据斜率和截距求出吸附参数n和kF。
3.2 拟合结果分析
分别采用式(2)、(4)对金鱼藻吸附Cr6+的等温曲线进行线性拟合。结果见表1。

表1 沉水植物金鱼藻吸附Cr6+的Langmuir和Freundlich模型的线性拟合参数
根据表1分析结果,金鱼藻对Cr6+的吸附既符合Langmuir模型(R2=0.9947),也符合Freundlich模型(R2=0.9568)。为了比较不同模型拟合的效果,本实验利用实验测得的数据与2种拟合模型重新计算获得的数据进行了比较,结果见图1。

图1 线性拟合的Langmuir、Freundlich吸附等温线与实测数据的比较
由图1可见:在平衡质量浓度较低(ce<0.2mg/L)时,Freundlich模型拟合的效果更符合客观实际;在平衡质量浓度较高(ce>0.2mg/L)时,两种模型的拟合效果基本重合,均和实测数据较为吻合。根据R2比较,Langmuir模型拟合效果较好,但图1所示,Freundlich模型拟合效果相对更好。造成这一差异的原因是:R2仅仅是拟合效果的一个参数,它能反映拟合效果,但不能仅仅根据R2的大小来判断何种模型拟合效果更适合。因此为了获得更为真实的拟合结果,在实践中可以利用实验测得的数据与拟合模型重新计算获得的数据进行了比较,并根据吸附反应本身的特点进行综合判断,然后选择合适的吸附模型。
3.3 金鱼藻对Cr6+的等温吸附特征
沉水植物金鱼藻对Cr6+的吸附等温曲线见图2。
如图2所示,吸附等温曲线在开始阶段有较大的斜率,表明沉水植物金鱼藻对Cr6+有较强的吸附亲合力,在后一阶段吸附曲线较为平缓。Wang等[16]的研究结果表明,死亡后的水生植物吸附能力依然存在,这表明水生植物的这种吸附作用与细胞的生理活动无关,本实验在较短的时间内达到吸附平衡,说明本实验中沉水植物对重金属离子的去除主要是通过吸附过程来实现的,与生理代谢活动无关。本实验可初步反映沉水植物金鱼藻对Cr6+的吸附容量大小,然而,有关沉水植物生物吸附机理的解释仍需更进一步的详细研究。

图2 沉水植物金鱼藻对Cr6+的吸附等温曲线
4 结语
(1)采用不同等温吸附模型评价植物对重金属的吸附时,根据拟合参数R2进行适用性判断并不准确,在实践中应利用实测数据与拟合模型重新计算获得的数据进行比较,并根据吸附反应本身的特点进行综合判断选择合适的吸附模型。
(2)在本实验中,沉水植物金鱼藻吸附Cr6+的行为在平衡质量浓度较低(ce<0.2mg/L)时,Freundlich模型拟合的效果更符合客观实际;在平衡质量浓度较高(ce>0.2mg/L)时,两种模型的拟合效果基本重合,均和实测数据较为吻合;且在Cr6+的浓度小于0.2mg/L时,金鱼藻对Cr6+有较强的吸附亲合力。
(3)根据Langmuir模型线性拟合参数,沉水植物金鱼藻对Cr6+的最大吸附量为1.5142×10-2mg/g。
[1]栾广忠,李宏军,张宗岩.铬─人体重要的保健微量元素[J].中国乳品工业,1999(6).
[2]陆祖宏.基因芯片的研究和应用[J].中国病理生理杂志,2000(10).
[3]王文华,冯咏梅,常秀莲,等.玉米芯对废水中铅的吸附研究[J].水处理技术,2004,30(2):95~98.
[2]刘 刚,李清彪.重金属生物吸附的基础和过程研究[J].水处理技术,2002,28(1):17~22.
[3]Wang X S,Qin Y.Equilibrium sorption isotherms for Cu2+ on rice bran[J].Process Biochem,2005,40(2):677~680.
[4]Schneider I A H,Rubio J,Smith R W.Effect of some mining chemicals on biosorption of Cu(Ⅱ)by the non-living biomass of the freshwater macrophyte Potamogeton lucens[J].Mineral Engineering,1999,12:255~260.
[5]Ho Y S,Huang C T,Huang H W.Equilibrium sorption isotherm for metal ions on tree fern[J].Process Biochem,2002,37:1421~1430.
[6]曾阿妍.沉水植物对重金属Cu2+的吸附特征及其逆境生理研究[D].长春:吉林大学,2006.
[7]曾阿妍,昌 宙,相 灿,等.金鱼藻对Cu2+的生物吸附特征[J].中国环境科学,2005,25(6).
[8]李国新,李庆召,薛培英,等.黑藻吸附Cd2+和Cu2+的拓展Langmuir模型研究,农业环境科学学报,2010,29(1).
[9]王圣瑞,赵海超,金相灿,等.沉水植物黑藻对不同磷化合物的转化与吸收[J].中国环境科学,2005(6).
[10]郑逢中,洪丽玉,郑文教.红树杆物落叶碎屑对水中重金属吸附的初步研究[J].厦门大学学报:自然科学版,1998(1).
[11]张亚楠.绿色巴夫藻的重金属胁迫效应及吸附能力的研究[D].暨南大学,2003
[12]王圣瑞,赵海超,金相灿,等.沉水植物黑藻对不同磷化合物的转化与吸收[J].中国环境科学,2005(6).
[13]陈书琴,路 杨,储昭升,等.破罡湖通江前后湖滨带夏季水生植物对比研究[J].生物学杂志,2009(3).
[14]施 红.生物吸附法处理废水中重金属离子的研究[D].南京:河海大学,2006.
[15]颜昌宙,曾阿妍,金相灿,等.沉水植物轮叶黑藻和穗花狐尾藻对Cu2+的等温吸附特征[J].环境科学,2006,27(6).
[16]Wang T C,Weissman J C,Ramesh G,et al.Parameters for removal of toxic heavy metals by water milfoil(My riophyllumspicat um)[J].Bull Environ Contam Toxicol,1996(57):779~786.
——以武汉东湖为例
——以武汉紫阳湖为例
- 绿色科技的其它文章
- 遂昌县林地资源现状及开发利用的保障措施研究

