单唾液酸四己糖神经节苷脂钠注射液的制备工艺
罗 宏 邹意琼
(西南药业股份有限公司 药物研究所,中国 重庆400038)
单唾液酸四己糖神经节苷脂(monosialoganglioside,简称GM1)在哺乳动物中枢神经系统中神经节苷脂含量丰富,其中以神经系统灰质含量最高。 GM1 是神经细胞膜的重要组分,是唯一能透过血脑屏障的外源性神经节苷脂制剂[1]。 GM1 能促进各种原因所致中枢神经系统损伤的功能恢复,对损伤后继发性神经退化有预防作用[2]。动物实验已证明[3-4],在脑损伤早期给予单唾液酸四己糖神经节苷脂治疗,可提高平均动脉压,保护脑组织内Ca2+-ATP 酶活性,起到稳定细胞膜的作用,防止细胞内钙超载,改善脑组织缺血缺氧,加强能量代谢,从而减轻脑水肿,阻断继发性脑损伤的发展。另外,单唾液酸四己糖神经节苷脂钠是一种神经修复药物,它可以清除自由基、保护多巴胺能神经元,从而减轻帕金森病(Parkinsin's Disease,PD)患者的症状[5]。 因此,临床上GM1 主要用于治疗急性中枢神经系统损伤以及帕金森病。
GM1 由一个唾液酸,一个葡萄糖,二个半乳糖,一个氨基半乳糖及一个神经酰胺残基组成,具有水溶性和脂溶性,GM1 钠盐具有较好的水溶性。 且对热稳定性较好。 因此,将GM1 做成注射剂。 按照注射剂的质量标准,性状、可见异物、不溶性微粒、细菌内毒素、无菌、有关物质和含量必须符合质量标准。目前,应用临床上的GM1 制剂主要是从猪脑中提取出来的,原料中除GM1 外,还有杂蛋白、GM2、GD3和其它杂质等。 这些杂质都会对GM1 注射剂质量有影响。 因此,需要摸索GM1 注射剂的生产工艺, 使之尽量除去杂蛋白对注射剂澄清度的影响,同时减少有关物质的量。
1 试验材料
1.1 药品与试剂
单唾液酸四己糖神经节苷脂杂质对照品(由中国药品生物制品检定所提供);单唾液酸四己糖神经节苷脂钠注射液(以下简称GM1 注射液,自制);单唾液酸四己糖神经节苷脂钠(湖南赛隆药业有限公司);氯化钠(自贡鸿鹤药业有限公司);针用活性炭(上海活性炭厂);磷酸(重庆川东化工有限公司);乙晴(成都金山化学试剂有限公司)和四氢呋喃(天津市光复精细化工研究所)等。
1.2 仪器
高效液相色谱仪(安揭伦科技公司)、pH 计(上海雷磁仪器厂)、紫外分光光度计(安揭伦科技公司)、不溶性微粒检测仪(北京东方森联自动化技术有限公司)和澄明度检测仪(天津大学精密仪器厂)等。
2 方法与结果
2.1 GM1 注射液的制备
先加入配置总量80%的注射用水, 注射用水温度控制在75-85℃,将氯化钠等辅料溶解后,再加入单唾液酸四己糖神经节苷脂钠原料,,搅拌溶解。 最后加入活性炭,并保温20 分钟,待药液冷却后,用氢氧化钠溶液调pH,通过115℃灭菌30min 后,得到单唾液酸四己糖神经节苷脂钠注射液。
2.2 GM1 含量测定
照高效液相色谱法(中国药典2010 年版二部附录VD)测定。
色谱条件及系统适用性试验: 用十八烷基硅烷键合硅胶为填充剂;以0.05mol/L 磷酸溶液(用三乙胺调节pH 至3.5)-乙腈(15:85)为流动相;检测波长为205nm;理论塔板数按单唾液酸四己糖神经节苷脂钠峰计算应不低于500。
测定法: 精密移取单唾液酸四己糖神经节苷脂钠注射液1mL 置于25mL 容量瓶中加水稀释至刻度,摇匀,作为供试品溶液(浓度为0.4mg/mL);另取工作对照品适量,精密称定,用水定量稀释成每1mL中约含0.4mg 的溶液,作为对照品溶液,分别取供试品溶液和对照品各溶液20μl,注入液相色谱仪,记录色谱图,量取峰面积,用外标法计算,单唾液酸四己糖神经节苷脂钠的含量应为标示量的90.0-110.0%。
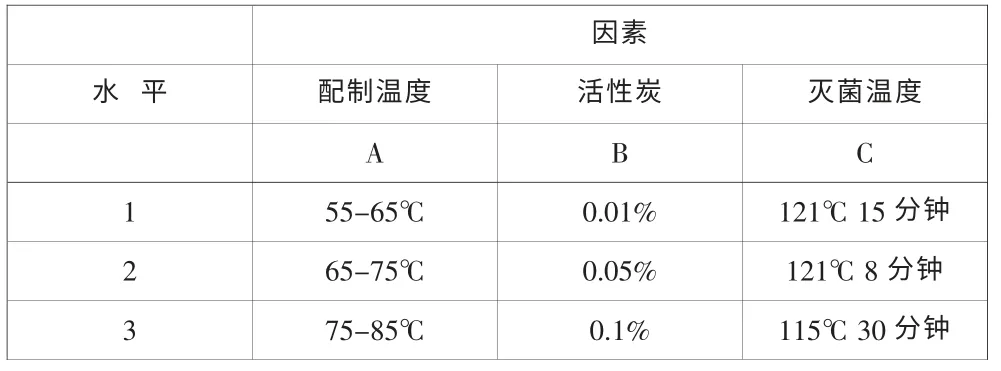
表1 因素水平表

表2 正交试验结果分析表
2.3 单唾液酸四己糖神经节苷脂钠注射液制备工艺的考察
2.3.1 有关指标
①药液灭菌后pH 测定: 参照 《中国药典》2010 版二部附录ⅥH pH 测定法。 ②药液可见异物检查:按照《可见异物检查细则和判断标准》的规定检查,应符合规定。 ③有关物质的测定:有关物质用高效液相法测定,单杂应不超过1.0%,总杂应不超过5%。 ④GM1 含量测定:用高效液相法测定GM1 的含量,含量应在90%~110%范围内。
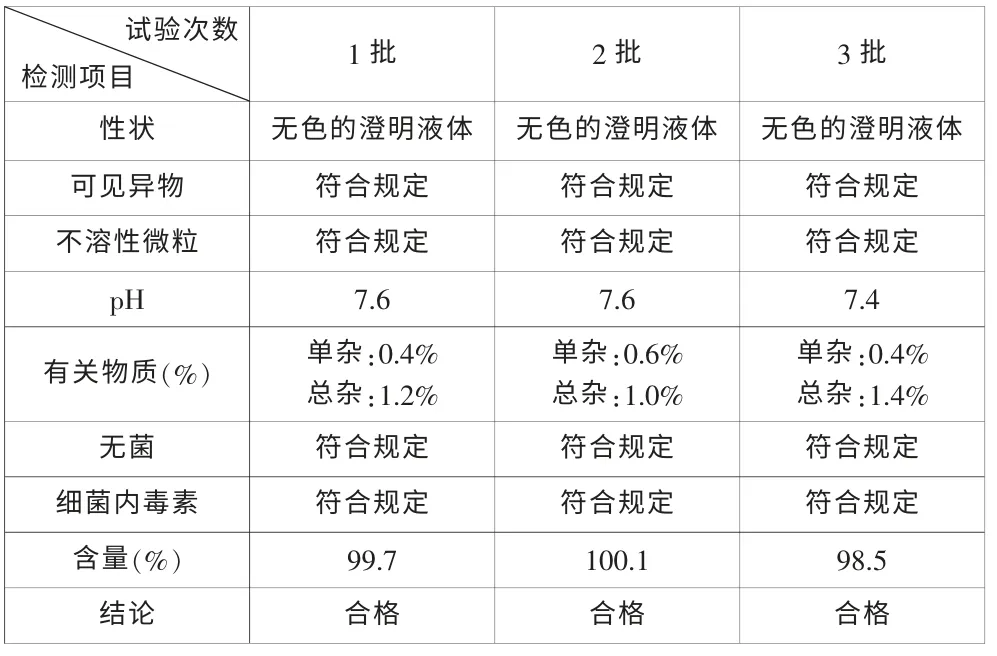
表3 实验结果表

表4 高温、光照试验结果
2.3.2 正交试验结果:根据以上实验设计方案,对单唾液酸四己糖神经节苷脂钠注射液工艺影响较大的几个方面如药液配制温度、活性炭、灭菌温度进行正交设计试验,以筛选最佳处方,如表1。 结果见表2。
由表2 可知,对单唾液酸四己糖神经节苷脂钠注射液含量的影响因素B〉C〉A,并得知最佳方案为A3B1C3。
2.3.3 单唾液酸四己糖神经节苷脂钠注射液质量检测:按照A3B1C3方案在公司小容量注射剂车间中试放大三批, 药液经过0.45μm 和0.22μm 两级过滤,灌封后通过115℃灭菌30min,样品经过质量检测,结果见表3。 并且检验合格的第三批样品放置在高温(60±2)℃,相对湿度(75±5)% ;光照(4500±500)Lx 条件下10d,于第5、第10 天取样检测,结果见表4。 可见,用A3B1C3方案制备的注射液结果较好。
3 讨论
3.1 GM1 是从猪脑中提取出的物质,原料中除GM1 外,还有杂蛋白、GM2、GD3和其它杂质等。 这些杂质都会对注射剂质量有影响。 因此必须在配制过程中保持一定温度,使原料中的杂质通过高温变性,并且加适量活性炭将杂质和变性后的杂蛋白除去, 同时要保证注射剂无菌,需要灭菌。
3.2 在配制过程中将药液温度控制在75-85℃,以除去杂蛋白。 GM1原料中有杂蛋白,杂蛋白如果控制不好,影响药液的可见异物,根据蛋白质的性质,选择加热使蛋白质变性。 再通过加入活性炭吸附和过滤方式除去蛋白质。
3.3 活性炭有吸附杂质、 除去热原等作用。 GM1 注射液中加入活性炭,将变性后的蛋白质和其它杂质除去,保证药液可见异物符合规定,同时降低有关物质的量。 注射剂中活性炭常用量为0.01-0.5%。 但活性炭同时对GM1 有吸附作用。为保证主药含量的准确性,进行了不同浓度活性炭对主药的吸附的考察,从试验结果表明,活性炭的用量为0.01%,既保证主药含量,又能使药液可见异物符合标准规定。
3.4 灭菌温度的确定:根据注射剂的要求,对热稳定的产品,其F0值必须大于8,最好采用过度杀灭法,按此要求,选择不同的灭菌温度试验,结果是采用过度杀灭法有关物质中单杂明显升高,且不符合标准规定,而采用残存概率法灭菌,其质量均符合标准规定,因此,灭菌温度确定为115℃灭菌30 分钟。
[1]姜静岩,范雪亮,等.单唾液酸四己糖神经节苷脂治疗颅脑损伤的临床观察[J].西南国防医药,2012,22(2):144-146.
[2]姜静岩,刘顺良,李慧,等.单唾液酸四己糖神经节苷脂治疗急性颅脑损伤201 例[J].临床医药,2011,20(7):54-55.
[3]陈志刚,卢亦成,朱诚,等.神经节苷脂GM1 在颅脑损伤早期的脑保护作用[J].第二军医大学学报,2002,23(4):420-422.
[4]Ledeen RW,Wu G.Nuclear lipids: key signaling effectors on the nervoussystem and other tissues [J].J Lipid Res,2004(45):1-8.

