注射用盐酸吉西他滨细菌内毒素检查方法的研究
周 梅,武 谷(安徽省食品药品检验所,合肥 230051)
盐酸吉西他滨全称为2′-脱氧-2′,2-二氟胞嘧啶盐酸盐(β异构体),其结构与阿糖胞苷类似,是新一代抗代谢药。盐酸吉西他滨作为一种前药在细胞内是脱氧胸苷激酶磷酸化的良好底物。注射用盐酸吉西他滨(β异构体)为注射用无菌冻干粉末,用于治疗局部晚期或已转移的非小细胞肺癌[1]。现有国家标准采用热原方法进行其生物安全性质量检查。笔者按照《中国药典》2010年版(二部)“细菌内毒素检查法”[2],对注射用盐酸吉西他滨进行了细菌内毒素检查方法的研究,以探讨其代替热原检查法的可行性。
1 材料
1.1 仪器
S648恒温水浴锅(上海医疗器械七厂);HS-1300净化工作台(苏净集团安泰公司);MS3digital旋涡混旋器(德国IKA公司);试验所用容器和用具均经250℃干烤2 h。
1.2 药品与试剂
注射用盐酸吉西他滨(浙江海正药业股份有限公司,批号:20100924、20100925、20100926,规格:每支0.2 g);细菌内毒素工作标准品(中国食品药品检定研究院,批号:150601-200966,规格:每支120 EU);鲎试剂(湛江博康海洋生物有限公司,批号:10103012;福州新北生化工业有限公司,批号:1106010;灵敏度:均为0.25 EU/ml);细菌内毒素检查用水(BET,福州新北生化工业有限公司,批号:10060321,规格:每支100 ml)。
2 方法与结果
2.1 鲎试剂灵敏度复核
用BET将细菌内毒素工作标准品溶解,置于混旋器混合15 min,然后制成0.5、0.25、0.125、0.062 6 EU/ml的稀释液,依据《中国药典》[2]2010年版二部附录方法[2]进行复核试验。结果,鲎试剂灵敏度的测定值(λc)均在0.5λ~2λ之间,表明所用鲎试剂均可用于细菌内毒素检查,结果详见表1(表中“+”表示凝胶形成,“-”表示凝胶未形成)。

表1 鲎试剂灵敏度复核结果Tab1 TALsensitivity check results
2.2 细菌内毒素理论限值的确定[3]
参考注射用盐酸吉西他滨的说明书,其临床使用最大剂量为1 250 mg/m2(人的体表面积按1.62 m2计),因此M(M为人用每千克体质量每小时的最大供试品剂量)定为1 250×1.62/60(kg·h);内毒素限值(L)按公式L=K/M(K为人每千克体质量每小时最大可接受的内毒素剂量)计算:L=5 EU/(kg·h)×60 kg×1 h/1 250/1.62 mg=0.148 EU/mg。根据《中国药典》2010年版(二部)“化学药品注射剂安全性检查法应用指导原则”要求[2],细菌内毒素检查限值按规定要求计算,由于药物和适应证(如抗感染、抗肿瘤、心血管药等急重病症用药,儿童老人用药,复合用药,大输液等)的不同,限值可适当严格,即至计算值的1/3~1/2,以保证安全用药。因此将注射用盐酸吉西他滨细菌内毒素理论限值确定为每1 mg吉西他滨中含细菌内毒素的量不得过0.10 EU。
2.3干扰试验最小有效稀释质量浓度c(mg/ml)的计算
根据公式:最大有效稀释倍数(MVD)=cL/λ,并考虑到目前市售鲎试剂有0.5、0.25、0.125、0.062 5、0.03 EU/ml 5种灵敏度,对于规格为0.2 g的样品MVD0.5-0.03=0.14 EU/mg×200 mg/ml/(0.5~0.03)EU/ml=56倍~933倍,则该品种最小有效稀释质量浓度c为3.57~0.214 mg/ml。
2.4 内毒素标准品的稀释
用BET将细菌内毒素工作标准品稀释成0.5、0.25、0.125、0.062 5 EU/ml系列内毒素溶液备用,作为Es系列。
2.5 供试品的干扰预试验[4]
为确定注射用盐酸吉西他滨对方法的影响,首先采用直接稀释法进行供试品干扰预试验。用BET将样品溶解,制备成不同质量浓度的溶液:0.25、0.5、1.0、2.0、3.5、7.0 mg/ml溶液,记为SW系列;另再分别制备1份同样质量浓度的供试品溶液,在制备中加入内毒素工作标准品,使每一水平的样品溶液中含2λc的内毒素,记为SE系列。选用灵敏度λc为0.25 EU/ml的鲎试剂分别与SW和SE反应,相应得供试品阴性对照(NPC)系列和供试品阳性对照(PPC)系列,每一稀释质量浓度平行做2个反应管,同时做BET阴性对照(NC)和阳性对照(PC)。结果发现,如果采用直接稀释法,即使将供试品稀释至0.25 mg/ml时对细菌内毒素和鲎试剂的反应也有干扰。
取注射用盐酸吉西他滨1支,加BET 10 ml,摇匀,测其pH值为3.07。由于细菌内毒素检查试验pH值最佳范围为6.0~8.0,因此将上述溶液调节pH值在6.0~8.0之间,再进行干扰预试验。称取碳酸钠适量置于无菌容器中,加BET制备成1 mol/L的溶液;取注射用盐酸吉西他滨1支,加BET 10 ml,摇匀,取碳酸钠溶液适量加入此溶液中,调节pH值至7.0,再进行干扰预试验,结果见表2。
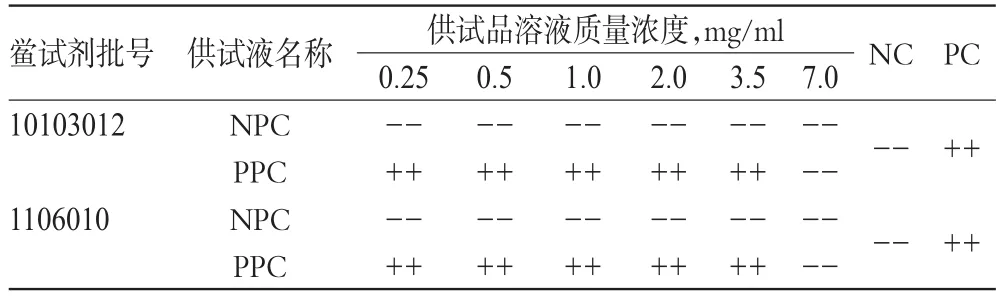
表2 供试品干扰预试验结果Tab2 Results of interference pretest of samples
表2结果表明,供试品质量浓度在0.25~3.5 mg/ml时对细菌内毒素和鲎试剂的反应未见干扰,故取供试品质量浓度为3.5 mg/ml进行干扰试验以进一步验证。
2.6 供试品干扰试验
取注射用盐酸吉西他滨1支,加BET 10 ml,摇匀,取1 mol/L的碳酸钠溶液适量加入此溶液中,调节pH值至7.0,再用BET稀释至3.5 mg/ml。采用2个不同厂家的鲎试剂,按2010年版《中国药典》(二部)附录[2]方法进行试验,结果见表3。
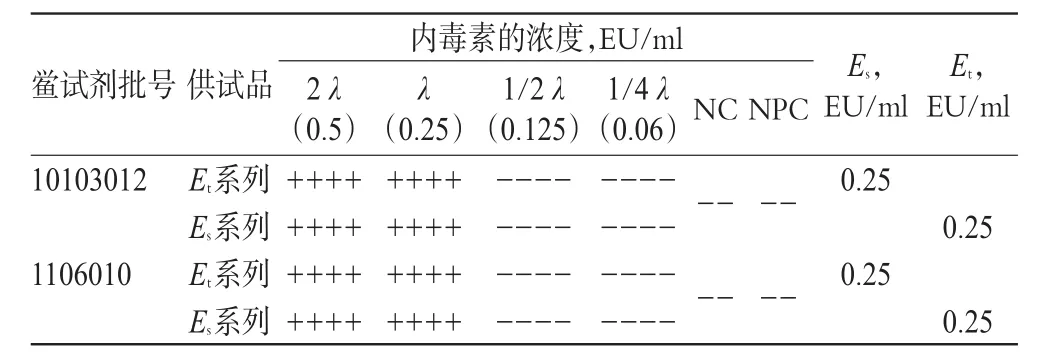
表3 供试品干扰试验结果Tab3 Results of interference test of samples
从表3结果可知,上述供试品的Et均在0.5Es~2.0Es之间,即供试品质量浓度在3.5 mg/ml时与2个厂家的鲎试剂试验均不产生干扰。根据公式MVD=cL/λ,当供试品为注射用无菌粉末时MVD取1,计算此时L值为0.07 EU/mg,低于确定的理论值。因此可采用L值为0.10 EU/mg对注射用盐酸吉西他滨进行细菌内毒素检查。
2.7 样品细菌内毒素检查
取注射用盐酸吉西他滨1瓶,加BET 10 ml溶解,再加碳酸钠溶液适量(调pH至7.0),用BET将样品稀释成2.5 mg/ml(L值为0.10 EU/mg)的溶液,用灵敏度为0.25 EU/ml的鲎试剂检查,结果见表4。
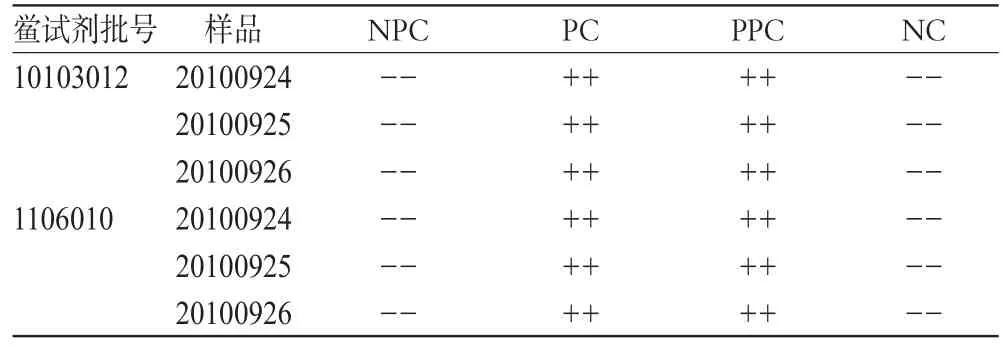
表4 样品中细菌内毒素检查结果Tab4 Results of endotoxin detection of samples
表4检测结果显示,样品中细菌内毒素含量均低于0.10 EU/mg。
3 讨论
细菌内毒素检查法是通过鲎试剂与细菌内毒素间产生凝聚反应以判断供试品中细菌内毒素是否符合规定的一种方法,其具有操作简单、检测周期短、灵敏度高、结果准确等优点,可替代家兔热原检查法用于注射液的质量控制。由于不同厂家生产的鲎试剂的抗干扰能力存在差别,为保证试验结果的可靠性,该试验一般选择2个厂家生产的鲎试剂对样品进行干扰试验。通过预试验发现,本品对鲎试剂凝集反应具有较强的抑制作用,仅通过稀释的方法不能排除干扰。为此,笔者分析了该药的组成及溶液的pH值。由于本品的主要成分为盐酸吉西他滨,辅料为甘露醇、醋酸钠和氢氧化钠,测其pH值为3.07,而适合鲎试剂反应水平的pH值范围为6.0~8.0,药物pH值偏酸或偏碱,超出了鲎试剂缓冲能力就会抑制或促进凝聚的形成。因此,本试验采用1 mol/L的碳酸钠溶液调pH值至7.0。结果表明调pH值后再稀释至3.5 mg/ml时就可以排除本品对鲎试剂凝集反应的干扰作用。因此将L值定为0.10 EU/mg,并认为注射用盐酸吉西他滨采用细菌内毒素检查法代替家兔热原检查法进行生物安全性质量检查是可行的。
[1]金薇,杨永健.高效毛细管电泳分离和测定注射用盐酸吉西他滨中有关物质[J].药物分析杂志,2004,24(5):476.
[2]国家药典委员会.中华人民共和国药典:二部[S].2010年版.北京:中国医药科技出版社,2010年:附录99-102.
[3]国家药典委员会.临床用药须知:二部[S].2000年版.北京:化学工业出版社,2000:573.
[4]叶青,王伟,迪丽努尔·沙比托夫.盐酸多巴胺注射液细菌内毒素检查方法的研究[J].中国药房,2010,21(41):3 918.

