星点设计-效应面法优化α-细辛脑脂质体喷鼻剂的制备工艺Δ
陈颖,黄海潮,朱庆玲,祝红,伍善广(.广东食品药品职业学院,广州50520;2.柳州医学高等专科学校,广西柳州 545006)
α-细辛脑(α-Asarone,ARE)是天南星科植物石菖蒲的主要活性成分之一,又名α-细辛醚、细辛醚和细辛脑(Asarone)[1]。可用于止咳、化痰、平喘,对肺炎、慢性气管炎、支气管哮喘均有较好的疗效[2-3]。细辛脑为脂溶性极强的化合物,制成生物利用度高的口服固体制剂有一定困难。文献报道细辛脑胶囊剂绝对生物利用度仅为2.7%,片剂绝对生物利用度也很低,仅9.7%[4]。效应面法(Response surface methodology,RSM)是统计与设计试验技术相结合的方法[5-6],与正交设计和均匀设计相比,效应面法可用非线性数学模型拟合,预测试验结果[7]。
笔者采用星点设计(Central composite design,CCD)-效应面法优化ARE脂质体喷鼻剂的制备工艺,用乙醇注入法[8]将细辛脑包入脂质体,制备成喷鼻剂,达到肺部直接给药,对于提高细辛脑治疗肺部疾病的效果与细辛脑的生物利用度有重要意义。
1 材料
DF-101S集热式磁力搅拌器(金坛市晶玻实验仪器厂);FJ-200高速分散匀质机(上海标本模型厂制造);岛津高效液相色谱仪,包括LC-10AT泵、SPD-10A紫外检测器(日本岛津公司);Nano-ZS 90粒径测定仪(英国马尔文公司);JEM.100CX型透射电镜(日本日立公司)。
ARE对照品及原料药(广西亿康药业股份有限公司,批号:080626,纯度:98.6%);卵磷脂(德国利保益有限公司,批号:1032917);胆固醇(上海蓝季科技发展有限公司,批号:100918);维生素E(武汉银河化工有限公司,批号:20091015);Sephadex-G50(上海源聚生物科技有限公司,进口分装);甲醇为色谱纯,其余试剂均为分析纯。
2 方法与结果
2.1 单因素试验
精密称取卵磷脂、胆固醇、维生素E,置于小烧杯中,加入适量的恒温无水乙醇,搅拌使溶解,再加入ARE,搅拌混匀。慢慢匀速注入水浴恒温的磷酸盐缓冲液(PBS)中,搅拌30 min,水浴保温50 min,放置1 h使其充分水合,用高速分散匀质机以5 000 r/min匀质3次,每次10 min,分装至喷雾器中,冷处保存,即得ARE脂质体喷鼻剂。单因素试验以制剂在显微镜下观察的形态、放置是否分层以及包封率为主要指标进行考察。
2.1.1 磷脂含量的影响。磷脂是脂质体成膜的主要成分,本试验考察了1%~8%的磷脂含量。结果当磷脂含量达6%时,脂质体就会出现不同程度的析出;而磷脂含量过低,则会不利于包封率的提高;当磷脂含量在3%~5%时,稳定性和包封率都较高;磷脂含量为4%时,包封率最高。磷脂含量对包封率的影响结果见图1。
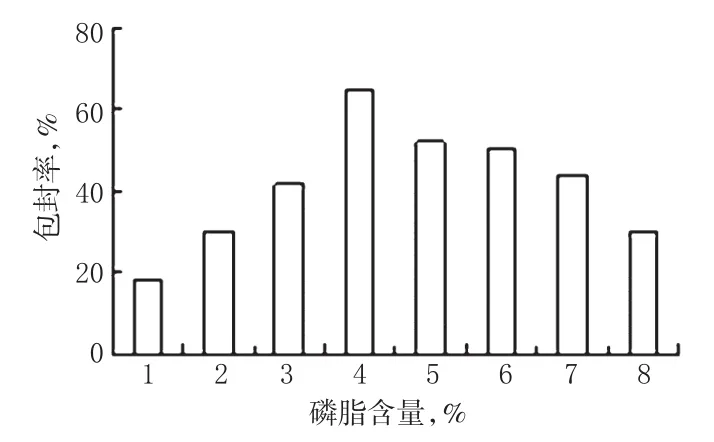
图1 磷脂含量对包封率的影响结果Fig1 Effects of phospholipid content on entrapment efficiency
2.1.2 胆固醇含量的影响。胆固醇是膜固化的重要成分,本试验以磷脂-胆固醇之比固定胆固醇的含量,考察了磷脂-胆固醇为1∶1~10∶1的比例。结果当胆固醇含量过低,会影响脂质体的成膜性;当磷脂-胆固醇之比达10∶1时,脂质体容易出现絮凝或沉淀现象;磷脂-胆固醇之比在4∶1~8∶1时,稳定性和成膜性较佳。胆固醇含量对包封率的影响结果见图2。
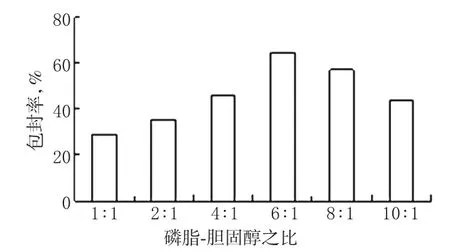
图2 胆固醇含量对包封率的影响结果Fig2 Effects of cholesterol content on entrapment efficiency
2.1.3 PBS pH值的影响。本试验考察了pH值为6.3、6.5、6.8、7.0、7.2的PBS。试验结果表明,pH值对脂质体的包封率影响不大,但是对脂质体的稳定性影响比较大,pH 6.8、7.0的PBS制备的脂质体稳定性较好。考虑到pH 6.8更接近鼻腔pH值[9],故选择PBS的pH值为6.8。
2.1.4 投药量的影响。本试验以磷脂-药物之比固定投药量。结果,随着ARE的投药量的增加,包封率呈上升趋势;但当磷脂-ARE之比小于30∶1时,显微镜下观察可见不同程度的晶体,且包封率呈降低趋势。投药量对包封率的影响结果见图3。
2.1.5 维生素E用量的影响。维生素E有抗氧化的作用,有利于脂质体的稳定性,但如果用量太大,反而会加速脂质体的絮凝与析出。当维生素E含量为0.1%(W/W)时,显微镜观察无油滴析出,且脂质体稳定性最好。
2.1.6 水浴温度的影响。制备温度对制剂影响较小,考虑到高温可加速磷脂和药物的氧化,通过试验且参考有关文献[10],将制备温度控制在55℃左右。
2.2 中心组合优化设计
综合单因素试验结果,选取磷脂含量(X1),磷脂-胆固醇之比(X2)和磷脂-药物之比(X3)3个因素,采用3因素5水平效应面分析方法,星点设计因素水平见表1。
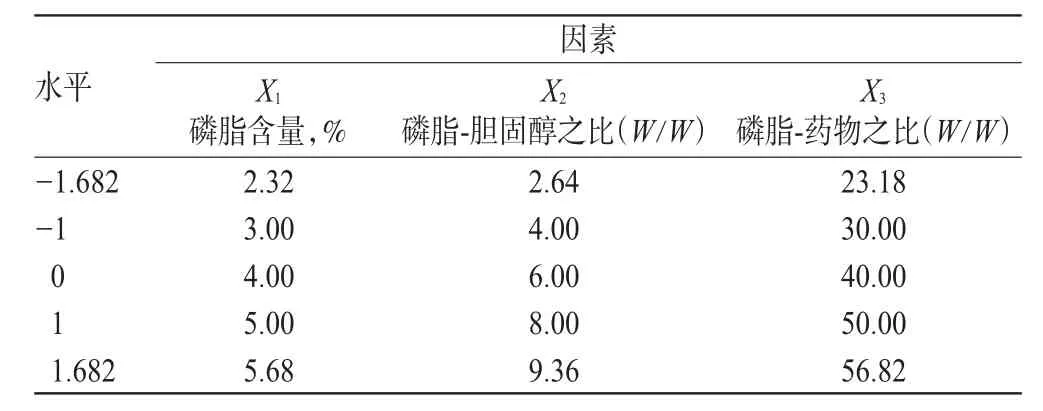
表1 星点设计因素水平Tab1 Levels and factors of central composite design
2.3 包封率的测定[11]
2.3.1 色谱条件。采用高效液相色谱法测定ARE含量。色谱柱:Agilent Hypersil ODS(250 mm×4.6 mm,5 μm);流动相:甲醇-水(65∶35,V/V);流速:1.0 ml/min;紫外检测波长:313 nm;进样量:20 μl。
2.3.2 标准曲线的绘制。精密称取ARE对照品10 mg,置于50 ml量瓶中,加甲醇-水(65∶35,V/V)溶解并稀释至刻度,摇匀,得ARE对照品贮备液。精密量取该贮备液0.4、1.6、3.2、4.0、5.0、6.0 ml分别置10 ml量瓶中,加甲醇-水(65∶35,V/V)稀释至刻度,摇匀。分别取上述溶液各20 μl,进样,记录色谱图。以峰面积(A)对质量浓度(c)进行回归分析,得方程A=40 040c+50 817(r=0.999 5,n=5)。结果表明,ARE在8~120 μg/ml检测质量浓度范围内与峰面积积分值线性关系良好。
2.3.3 精密度和重复性试验。取“2.3.2”项下64 μg/ml的溶液,重复进样6次,测定峰面积,计算得出RSD=0.32%(n=6),表明进样精密度良好。取同一批ARE脂质体5份,按“2.3.5”项下方法,测定ARE的含量,结果RSD=1.11%(n=5),表明该含量测定方法重复性良好。
2.3.4 稳定性试验。取同一供试品溶液,室温放置0、1、2、4、6、8 h后分别测定ARE的含量,结果RSD=0.92%(n=6),表明供试品溶液在8 h内基本稳定。
2.3.5 加样回收率试验。将一定量的ARE对照品贮备液与空白脂质体按一定比例混合成50%、60%、70%的ARE浓度,加入一定量的甲醇破乳,用甲醇-水(65∶35,V/V)稀释的样品各3份,按“2.3.1”条件进行测定,计算回收率。结果平均回收率为98.21%,RSD=1.16%(n=9)。
2.3.6 凝胶柱分离测定脂质体中游离药物。吸取1 ml的脂质体,上样于已用pH 6.8 PBS平衡好的Sephadex-G50柱(1.6 cm×50 cm)上,用pH 6.8 PBS洗脱,流速为1.0 ml/min。分次收集洗脱液,每次5.0 ml,通过观察流动吸光度的变化监测脂质体与药物的分离情况。收集游离药物,按“2.3.1”条件测定药物质量浓度。
2.3.7 柱回收率考察。吸取“2.3.5”的高、中、低浓度的ARE对照品与空白脂质体的混合液各1 ml,按“2.3.6”项下的条件进行试验,测得柱加样回收率平均值为98.5%。配制高、中、低浓度的ARE对照品溶液,吸取1 ml,同法测定。结果ARE柱回收率平均值为99.2%。
2.3.8 包封率的计算。精密量取ARE脂质体0.2 ml,置于25 ml容量瓶中,加入一定量的甲醇破乳,摇匀,待溶液完全澄清透明后用甲醇-水(65∶35,V/V)稀释至刻度,摇匀,按“2.3.1”条件进行测定,求出脂质体中ARE的含量。精密量取ARE脂质体混悬液1 ml,按“2.3.6”项下的条件进行试验,测定游离药物的量。按下式计算包封率[12]:
包封率(%)=(W总-W游)/W总×100%(W总:总药物量,W游:未包入脂质体的游离药物量)
2.4 星点设计-效应面法优化处方[13-14]
以包封率(Y)为评价指标进行试验,设计及结果见表2,回归模型各项方差分析表3。
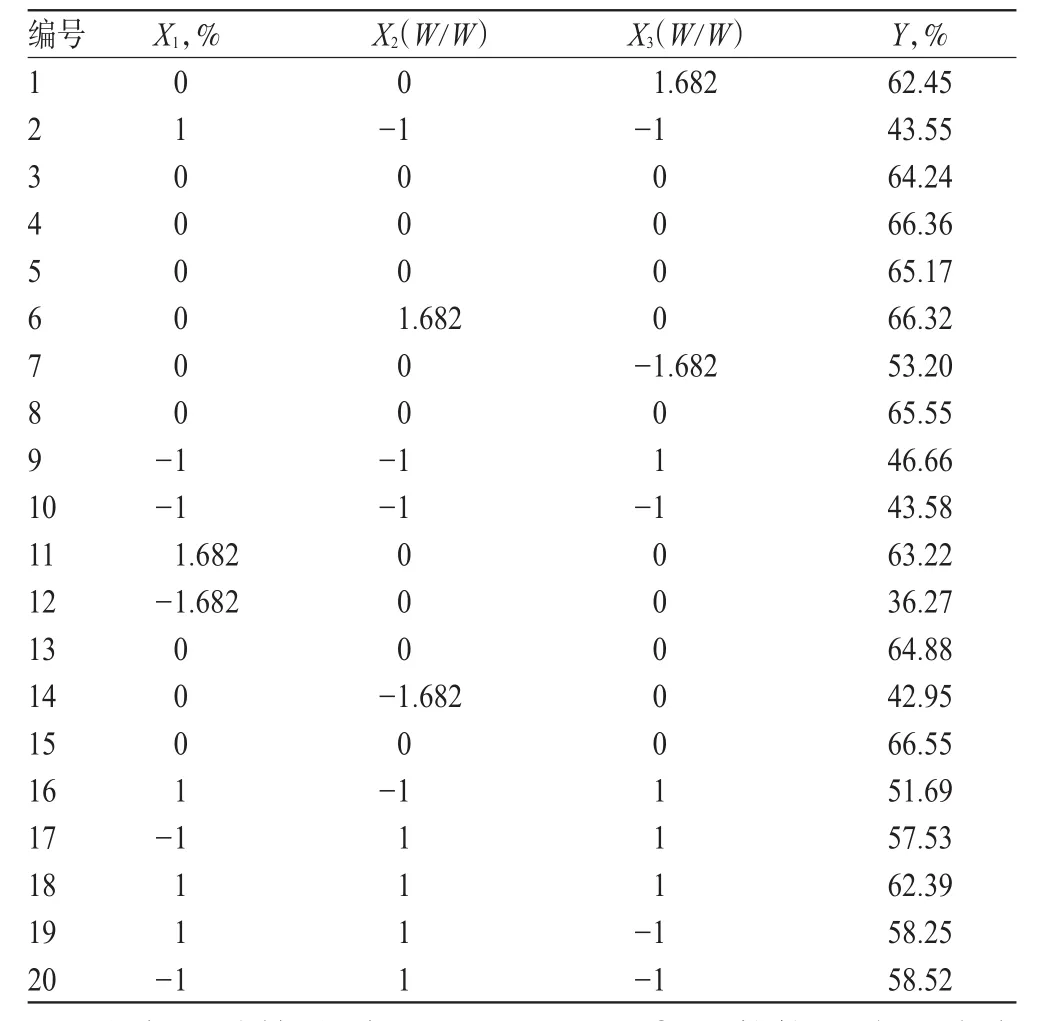
表2 星点设计及结果Tab2 Central composite design and its results
根据试验结果,应用Design-Expert®8.0软件,进行二次多项式逐步回归拟合,得到模型为:Y=65.48+4.02X1+6.63X2+2.19X3-0.051X1X2+1.27X1X3-1.01X2X3-5.68X12-3.95X22-
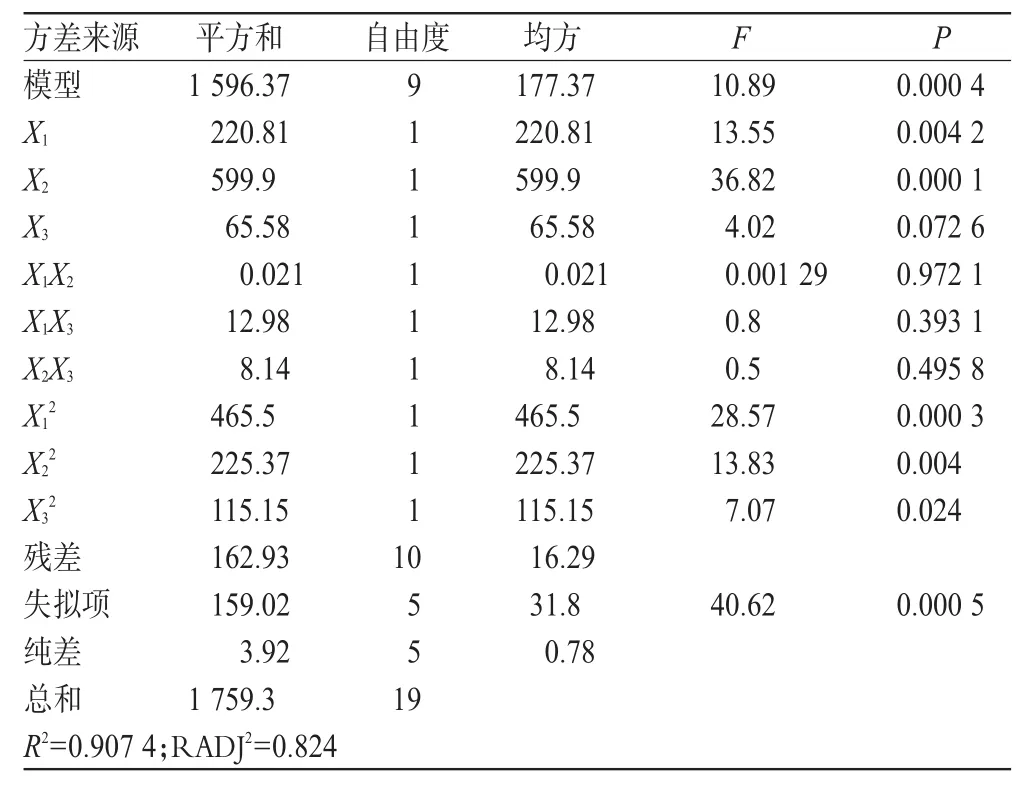
表3 回归模型各项方差分析Tab3 Analysis of variance for fitted regression model
从表3方差分析结果可见,试验模型具有高度的显著性(P<0.01)。X1、X2对包封率影响显著(P<0.05);交互项X1X2、X1X3、X2X3的P值均大于0.05,说明这3个因素之间的交互作用不大。R2=0.907 4,说明模型能够很好地反映响应值的变化,拟合度好。可以用此模型来分析和预测ARE脂质体的工艺结果。
各因素的交互结果见图4。
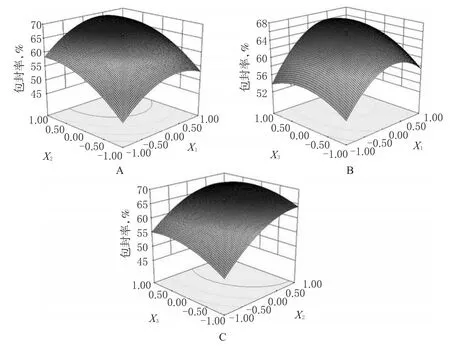
图4 不同因素组合对包封率影响的曲面图A.Y=f(X1,X2)的效应面图;B.Y=f(X1,X3)的效应面图;C.Y=f(X2,X3)的效应面图Fig4 Response surfaces of the effects of different factors on entrapment efficiencyA.response surface of Y to X1and X2;B.response surface of Y to X1and X3;C.response surface of Y to X2and X3
由图4可见,磷脂-胆固醇之比对脂质体包封率影响较为显著,表现为曲线较陡,最佳值为7.59;磷脂-药物之比影响较小,曲线较为平滑,最佳值为43.32。
2.5 最优处方工艺验证
通过Design-Expert®8.0软件,结合表3方差分析的结果,在得到最大包封率的同时综合考虑工业可行性和投入产出比,选取ARE脂质体最佳制备工艺:磷脂含量4.5%、磷脂-胆固醇之比7.5、磷脂-药物之比45。按照选取的最佳工艺条件重复3次试验,将预测值与实测值进行比较并计算偏差[偏差=(预测值-实测值)/预测值×100%],结果见表4。
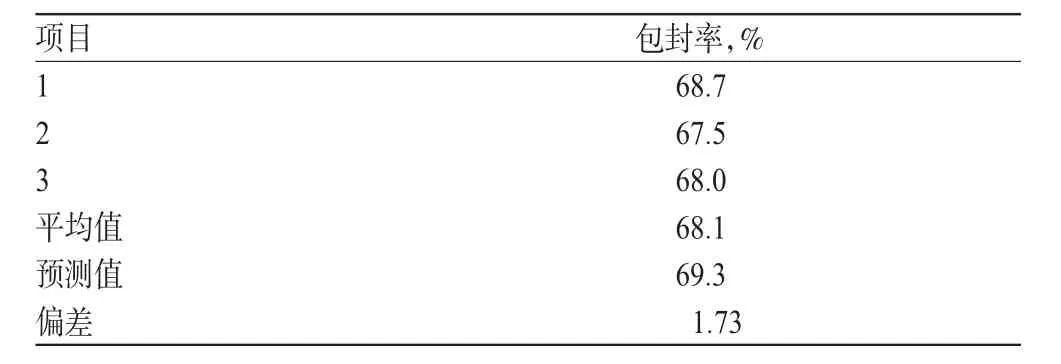
表4 验证试验结果(n=3)Tab 4Results of validation test(n=3)
由表4可见,预测值与实测值的偏差为1.73%,说明采用效应面分析法得到的工艺准确可靠。
2.6 脂质体形态观察
对最优工艺制备的脂质体进行粒径、Zeta电位测定,电镜扫描表面形态。经激光粒度分析仪测定,ARE脂质体粒径主要集中在200 nm波长处,ARE脂质体的的粒径分布见图5;Zeta电位为-24.9 mV;用透射电子显微镜观察并拍摄照片,ARE脂质体的扫描电镜图见图6。
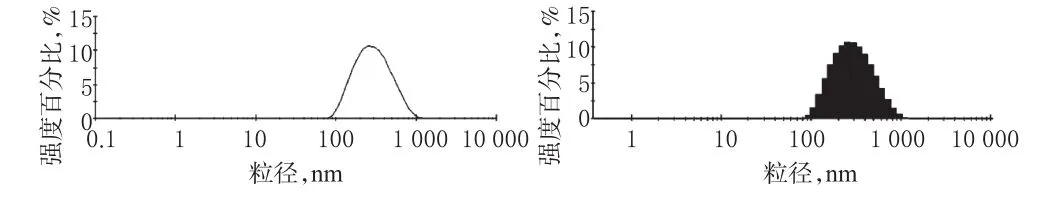
图5 ARE脂质体的的粒径分布Fig5 Distribution of particle size ofARE liposome

图6 ARE脂质体的扫描电镜图(×27 000)Fig6Scanning electron micrograph ofAREliposome(×27000)
由图6可见,不同粒径的脂质体形态完整,双分子膜结构清晰,均属于单室脂质体,脂质体内部包裹有细辛脑使脂质体在透射电镜下颜色变亮,脂质体的相互分界明显。
3 讨论
脂质体肺部给药具有吸收迅速、刺激性小、耐受性好、安全性高,可实现持续缓慢释药、生物利用度高等优点。脂溶性药物在水中的溶解性差,肺部溶解量有限;制成脂质体后,可改善溶解性,从而提高有效药物浓度。乙醇注入法制备脂质体是最简单的制备方法之一,该方法操作简便、设备简单、重现性好,适合于大规模工业生产的需要。将ARE制成脂质体,经喷雾器雾化实现鼻腔给药,吸入肺部,在治疗肺局部疾病(如哮喘、肺气肿及囊性纤维化等)时,使药物直接浓集于病灶区,起效快、剂量低、作用时间长、进入体循环的药量小、不良反应少。
星点设计-效应面法是比较适宜进行非线性拟合的优化法。结果表明该组数据代入最佳模型方程获得的理论预测值与实测值比较吻合,证实所建立的数学模型具有较好的预测性。此外,通过最优处方工艺验证试验证明,所得处方工艺包封率高、重现性较好,达到了优选处方工艺的目标。
[1]杨云,冯卫生.中药化学成分提取分离手册[M].北京:中国中医药出版社,2001:119.
[2]周晖,王东凯.α-细辛脑巴布剂的制备和体外经皮渗透性的研究[J].华西药学杂志,2006,21(5):452.
[3]杨玉.α-细辛脑片治疗148例慢性阻塞性肺疾病[J].新药与临床,1986,5(4):210.
[4]吴闯.细辛脑片剂的生物利用度[J].中国医院药学杂志,2003,23(10):597.
[5]Attivi D,Wehrle P,Ubrich N,et al.Formulation of insulin-loaded polymeric nanoparticles using response surface methodology[J].Drug Dev Ind Pharm,2005,31(2):179.
[6]Wu W,Cui GH.Central composite design and response surface method and its application in pharmacy[J].Foreign Med Sci:Sect Pharm,2000,27(5):292.
[7]张栋,孙晓燕,顾纪锋,等.星点设计-效应面法优化富马酸美托洛尔脉冲控释片最佳处方[J].中国生化药物杂志,2011,32(1):14.
[8]Pons M.Liposomes obtained by the ethanol injection method[J].Int J Pharm,1993,95(1):51.
[9]文卫平,庄惠文,许庚,等.局部糖皮质激素对慢性鼻炎患者鼻腔菌群及pH值的影响[J].中华耳鼻咽喉头颈外科杂志,2005,40(12):917.
[10]耿传信,杨海,刘雪丽.灰树花多糖脂质体的制备方法研究[J].中国药房,2010,21(39):3 687.
[11]蔡周权,梁臻,金辉,等.α-细辛脑静脉乳剂的制备与质量评价[J].华西药学杂志,2007,22(6):611.
[12]国家药典委员会.中华人民共和国药典:二部[S].2010年版.北京:中国医药科技出版社,2010:204.
[13]杨涛,盛欢欢,李岩,等.星点设计-效应面法优化穿心莲提取工艺[J].中国药学杂志,2011,46(3):208.
[14]韩帅,李淑燕,陈芹芹,等.响应面分析法优化闪式提取胡柚皮中黄酮类化合物工艺[J].食品科学,2011,32(10):52.

