11 例先天性心脏病封堵术后残余漏的介入治疗
申俊君 张智伟 王树水 石继军 潘微 钱明阳 李渝芬
介入治疗已成为目前治疗常见先天性心脏病(动脉导管未闭,patent ductus arteriosus,PDA;房间隔缺损,atrial septum defects,ASD)的常规方法,但手术后有部分患者的封堵器可出现再通,通常的处理方法为开胸手术修补[1-3]。我中心自开展先天性心脏病介入治疗以来,收治PDA 手术后再通患者9例,ASD 手术后再通患者2 例,均应用介入治疗再次封堵,现介绍如下。
对象与方法
1. 研究对象:2002 年8 月至2012 年3 月,在广东省人民医院心儿科收治经心脏彩超诊断为PDA、ASD 封堵术后再通的患者11 例(男性5 例,女性6例),其中PDA 9 例,ASD 2 例,再次介入时年龄6 ~34 岁。11 例患者曾于1994—2002 年在我院或外院行封堵手术,7 例患者因“活动后气促、胸痛2 周~1年”,4 例患者于随诊过程中发现大量残余分流再次入院。10 例患者在第一次介入手术后均进行定期随访,术后即刻复查心脏彩超和胸片提示介入装置位置正常,大小适中,可探及少量的残余分流,在术后长期随访复查的过程中,发现残余分流逐渐增多,封堵器内呈低回声,对穿隔血流无任何阻挡,心脏腔室也逐渐增大,伴有瓣膜反流及肺动脉压力增高。另1 例PDA 患者第一次介入术后未进行随访,无不适症状,于手术后第七年复查心脏超声时发现大量残余分流。11 例患者在体检中均在胸前区闻及病理性心脏杂音。最终诊断依赖超声心动图,彩色多普勒探及穿过介入装置(蘑菇伞封堵器、弹簧圈、补片等)的大量残余分流,并伴随有心脏腔室的扩大及瓣膜反流(图1)。具体的临床资料见表1。
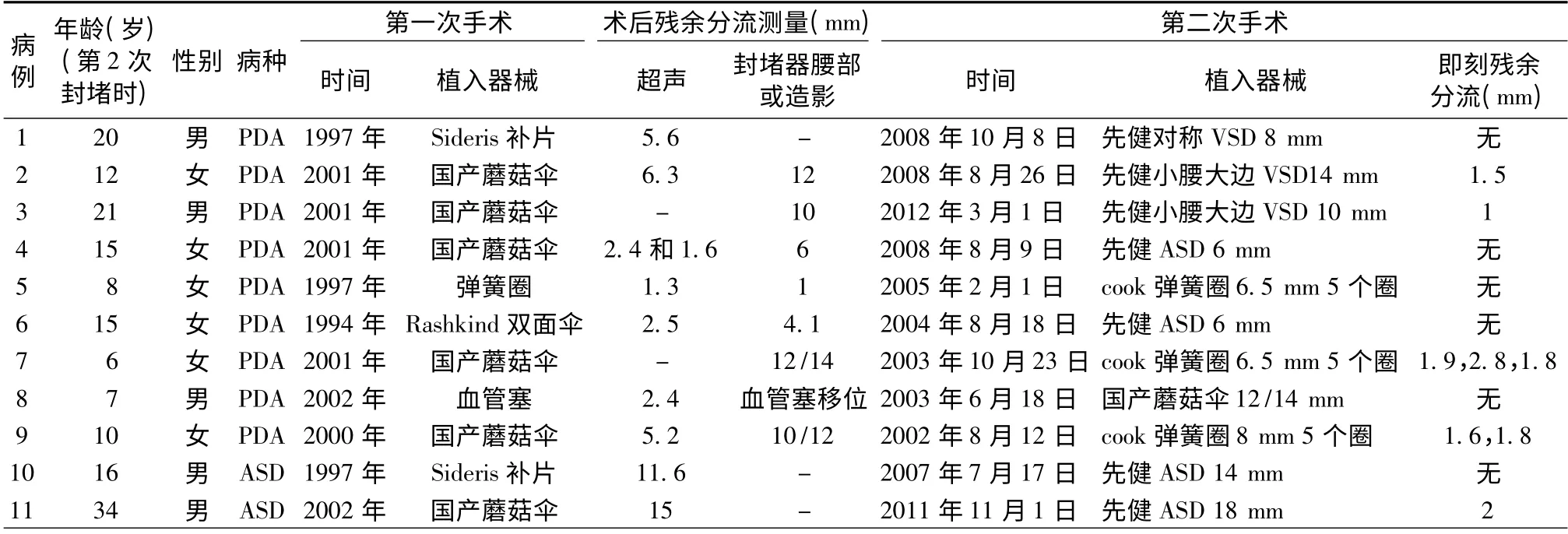
表1 11 例先天性心脏病封堵术后再通患者临床资料
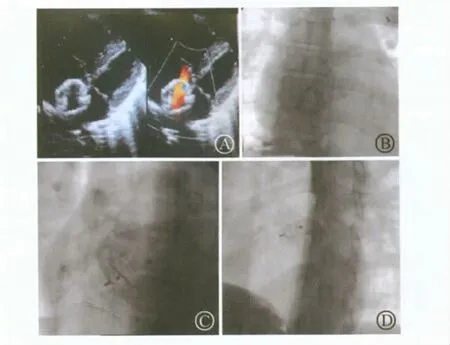
图1 超声心动图显示再通房间隔缺损封堵器及使用封堵器再次封堵
2. 动脉导管未闭再通的介入治疗:使用cook 弹簧圈封堵残余分流的患者有3 例,有1 例患者原封堵装置为弹簧圈,2 例为国产蘑菇单盘伞。封堵方法与常规使用弹簧圈封堵PDA 的过程相似,使用右冠管经股动脉-降主动脉-PDA 原封堵器处-主肺动脉-右室送交换导丝,选择cook 可控弹簧圈在PDA之肺动脉端释放2 个圈,原封堵器/弹簧圈内释放1个圈,PDA 之主动脉端释放余下的2 个圈,再次造影验证有无残余分流。
使用蘑菇伞再次封堵的患者有6 例,其中3 例原封堵器为国产蘑菇单盘伞封堵器。先行常规左右心导管检查进行血流动力学分析,然后于封堵器的切线位(左侧位90°或右侧位40°)行主动脉弓降部造影,可以显示出大量对比剂通过伞面到达肺动脉(图2A),并且可以测量原封堵器腰部的直径为再次选择封堵器的依据。选择6 F 右冠导管置于降主动脉原封堵器处,导入直头导丝(加硬导丝、泥鳅导丝、普通导丝)穿过原封堵器伞面中央处至肺动脉,自股静脉导入圈套器(图2B),建立轨道,再由静脉系统送入内芯逐步扩张(6 F 鞘管内芯开始至大于目标鞘管大小的内芯)原封堵器网孔,最终选择鞘管,沿导丝送至降主动脉(图2C),送入封堵器,于原封堵器之降主动脉端释放前盘,于原封堵器之肺动脉端释放后端,使目标封堵器完全覆盖在原封堵器的前后盘上,造影及超声心动图判断无残余分流、降主动脉及左肺动脉血流无梗阻后释放封堵器(图2D)。1 例患者使用的原封堵装置为血管塞,封堵后1 年经造影及超声证实血管塞移位至左肺动脉,对血流无任何影响,但PDA 呈开放状态,使用国产蘑菇单盘伞封堵器再次封堵并成功。第一次封堵使用Rashkind 和Sideris 纽扣式补片的患者各有1 例,由于原封堵装置腰部纤细,使用导丝在肺动脉端通过残余分流较容易,故其封堵过程与常规使用蘑菇伞封堵器封堵PDA 的过程相似(图2E)。
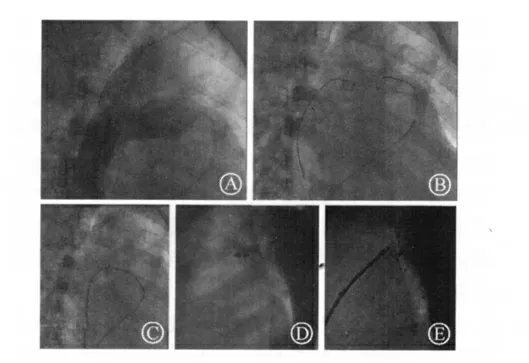
图2 使用封堵器封堵再通的动脉导管未闭
3. 房间隔缺损再通的介入治疗:2 例ASD 再通患者,1 例原封堵器为Sideris 纽扣式补片,1 例为国产早期封堵器。导丝较容易通过再通的Sideris 纽扣式补片,封堵过程同ASD 的封堵过程大致相似(图1D)。另一例患者2002 年于外院行ASD 封堵术,采用国产早期蘑菇双盘伞封堵,超声显示封堵器位置正常,房间隔中央对血流几乎无阻挡左右(图1A),先行常规右心导管检查,选择房间隔穿刺针及穿刺鞘,经原封堵器中部穿刺入右房后造影证实鞘管的位置,沿鞘管送导丝至左上肺静脉(图1B)。选择7 F 长鞘管,选择先健ASD 18 mm 双盘封堵器,于原封堵器之左房面释放前盘,在原封堵器内部释放部分后盘,于原封堵器右房面内释放部分后盘,使目标封堵器的左房盘面覆盖在原封堵器的左房盘外,右房盘面及腰部则固定在原封堵器的腰部及右房盘面内(图1C)。
结 果
11 例患者均再次使用介入方法选择封堵器/弹簧圈封堵残余分流(表1)。2 例ASD 患者术后即刻复查心脏超声,有1 例患者的封堵器边缘出现残余分流,大小2 mm,术后1 月复查时残余分流消失。术后服用阿司匹林(3 ~5 mg/kg)抗凝半年,定期复查心脏彩色超声心动图超声、心电图、胸片、血常规、凝血指标等均未见异常,患者症状较术前明显缓解。
9 例PDA 患者中再次封堵时有3 例选择了cook可控弹簧圈,1 例选择国产蘑菇伞封堵器,5 例选择了先健ASD/VSD 封堵器,术后即刻复查心脏超声心动图有4 例患者出现边缘极少量残余分流,在术后1 个月复查超声心动图提示残余分流消失;有2例患者(再次封堵时均使用cook 弹簧圈)术后出现溶血,1 例临床表现为出现茶色和淡红色尿,使用碱化尿液等内科对症治疗后于术后第4 天尿色转清;另1 例患者术后4 小时开始排酱油色尿,并出现面色苍白,胃纳减小,进食后呕吐,查尿常规提示血红蛋白尿,予碱化尿液及补液治疗效果欠佳,于术后第二天行急诊外科PDA 缝闭术,术中拔出弹簧圈,并使用心包片包埋蘑菇伞并扩大主肺动脉分叉处,术后症状消失。其余5 例患者无残余分流。9 例患者随访1 个月~10 年,术后定期复查心脏彩超、心电图、胸片、血常规、尿常规、凝血指标等均未见异常。
讨 论
20 世纪80 年代早期以来,临床使用过的封堵ASD 的装置包括[4-6]:Cardioseal 间隔缺损闭合器;Sideris 纽扣式补片装置;Angel Wings 装置;Amplatzer 间隔闭合器等。封堵PDA 的装置包括:Rashkind 双面堵塞装置;Sideris 纽扣式补片装置;弹簧圈;Amplatzer 导管堵塞装置等。补片装置因失败率较高,残余分流多已经被取代。本研究中3 例患者曾于1997 年行补片装置封堵ASD、PDA,10 年后发现残余分流量大,再次使用介入治疗封堵。4 例PDA/ASD 封堵后再通的患者使用的均为早期的国产蘑菇伞封堵器,早期PDA 封堵器内阻流体的主要成分为聚氨酯海绵,在随诊过程中发现这部分患者在早期存在少量残余分流,随着封堵器内聚氨酯海绵的逐步吸收,残余分流逐渐增多。心脏超声提示封堵器位置正常,但封堵器内部显示为低回声或无回声,对血流无任何阻挡作用。早期外科手术发现封堵器仅剩外部镍钛合金组织,其内无填充物。1例ASD 封堵后再通患者使用的是无纺聚酯纤维为填充物的房间隔缺损封堵器,超声心动图提示封堵器较大,基本占据全部房间隔组织,推测残余分流的原因可能为封堵器偏大,内皮组织不易移行,内皮覆盖不良。同时也不排除个体差异。
手术后再通的先天性心脏病患者往往不愿再次手术,介入封堵是比较理想的选择。针对封堵器大小及类型的不同,分别选择了VSD、ASD 封堵器及弹簧圈,超声心动图随访无封堵器的破损及移位,最长者随访已长达10 年。
在操作方法上,使用封堵器再次封堵Sideris 纽扣式补片与常规的封堵过程大致相同,因其残余分流的量较大,且补片腰部纤细,容易建立轨道。在超声或造影的指引下选择合适的封堵器封堵即可。第一次使用蘑菇伞封堵器封堵后再通,由于国产PDA蘑菇伞封堵器金属网眼小,再封堵时输送长鞘不易通过原封堵器,再次介入难度较大。本中心使用弹簧圈和封堵器两种封堵装置再次封堵。由于手术后动脉导管附近瘢痕的影响,动脉导管的走向可能发生变化,常规90°左侧位的角度不一定适用于所有再通的患者。可以以原封堵器为中心,在其切线位上操作,在降主动脉端使用直头导丝通过原封堵器中央部位,用圈套器从股静脉将交换导丝拉出建立轨道。使用右冠导管和输送长鞘通过封堵器的网眼有一定的难度,需要仔细操作,避免撕拉损伤血管及心脏。3 例PDA 再通患者均使用5 F 右冠导管先从动脉端通过封堵器,再使用6 F 输送长鞘的内芯导管自静脉端开始扩张,依次使用7 F、8 F 长鞘的内芯扩张原网眼,直至使用7 F 输送长鞘释放封堵器。我中心的4 例PDA 患者使用了VSD、ASD 封堵器。使用VSD 封堵器封堵再通PDA 的优势在于其腰部细小,且左室盘面较大,可以完全覆盖原封堵器的主动脉端,VSD/ASD 封堵器的腰部和右室/右房盘面固定在原封堵器的内部和肺动脉端,起到固定封堵器的作用,这样新的封堵器可以完全封堵再通的封堵器,明显减少残余分流。
早期我中心3 例再通PDA 患者选择使用弹簧圈再次介入封堵残余分流,其中1 例使用的原介入装置为弹簧圈,再次介入后残余分流即刻消失,效果较好;另2 例为国产早期蘑菇伞封堵器,术后均出现溶血,1 例自愈,1 例于外科取出弹簧圈再次缝闭后症状消失。由于蘑菇伞封堵器残余分流较多,使用弹簧圈完全封堵残余分流有一定难度,且放置弹簧圈的数量有限,只能使较大股的残余分流被分割成多股小股残余分流,容易出现溶血。故使用弹簧圈介入治疗再通的PDA 适用于残余分流较少的患者,如封堵后有少量残余分流,需严密监测患者有无溶血等意外情况。
使用ASD 封堵器封堵再通的ASD 过程大致同PDA 再通相似,但无法建立静脉-动脉的轨道。使用直头导丝通过原封堵器的中央(导丝尽量与封堵器的两个盘面均垂直)后,沿轨道导丝扩张原封堵器的网眼,导管与原封堵器之间会产生较大的阻力,应循序渐进,避免暴力损伤血管和心脏。释放封堵器时使其左房盘面完全覆盖原封堵器的左房面,其腰部和右房盘面留在原封堵器的内部和右房面,起到固定封堵器的作用。释放封堵器是应保证两个封堵器的左房面同轴,使新的封堵器能起到阻挡分流的作用。
在封堵器大小的选择方面,我中心主要依赖于超声测量残余分流的大小,以及放射影像上测量原封堵器的腰部直径、造影测量残余分流的大小。因为手术后再通的治疗是在原封堵器内部释放新的封堵器,原封堵器无弹性,选择比原封堵器腰部相当或大1 ~2 mm 即可。
手术后再通的先天性心脏病是封堵治疗的适应证,国内已有几个中心再通后的介入治疗进行介绍[7-9]。本组病例显示,国产蘑菇伞封堵器封堵再通的PDA/ASD 是安全有效的方法,再封堵后随访1个月~10 年,再无残余分流,结果满意。但使用这种方法仍有一定的局限性,在原封堵器内再放置封堵器治疗有一定的限制,不能应用于原有封堵器过大的病例,且两个封堵器均在体内其金属含量高,重量大,对心脏功能及人体有无影响尚需密切的长期随访,远期疗效仍需进一步确定。
[1] 章斌,张宝仁,王志农. 动脉导管未闭封堵术后残余漏的急诊手术治疗. 中华胸心血管外科杂志,2000,16:314-314.
[2] 齐静,朱鲜阳,王辉山,等. 国产室间隔缺损封堵器的动物实验研究. 心脏杂志,2005,17:169-171.
[3] 章斌,张宝仁,朱家麟,等. 动脉导管未闭封堵术后残余漏二例. 中国胸心血管外科临床杂志,2001,8:88.
[4] Sharafuddin MJ,Gu X,Titus JL,et al. Transvenous closure of secundum atrial septal defects:preliminary results with a new selfe-xpanding nitinol prosthesis in a swine model. Circulation,1997,95:2162-2168.
[5] Latson LA.Per-catheter ASD closure. Pediatr Cardiol,1998,19:86-93.
[6] Thanopoulos BD,Laskari CV,Tsaousis GS,et al. Closure of atrial septal defects with the Amplatzer occulusion device:preliminary results. J Am Coll Cardiol,1998,31:1110-1116.
[7] 张庆桥,蒋世良,张岩,等. Amplatzer 法治疗Rashkind 伞封堵动脉导管未闭术后残余分流一例. 中华心血管病杂志,2001,29:682-682.
[8] 刘亚平,许国锋,孙建辉. 动脉导管未闭手术后再通的介入封堵.临床心血管病杂志,2006,22:753-754.
[9] 陈晓彬,蒲晓群,郑昭芬,等. 先天性心脏病封堵术后残余漏再封堵的治疗. 临床心血管病杂志,2007,23:384-385.
