基于个体CT影像的胸主动脉-血管内支架数值仿真初探
董智慧 李永生 符伟国 侯凯 许世雄 王盛章 郭大乔 徐欣 陈斌 王玉琦
(1.复旦大学附属中山医院血管外科,上海 200032;2.复旦大学力学与工程科学系,上海 200433)
十余年来,胸主动脉腔内治疗因其微创、有效的突出优点,已成为胸主动脉疾病(主要包括Stanford B型夹层和主动脉瘤)的首选治疗方法。血管内支架(以下简称支架)是胸主动脉腔内治疗的主要器械。大多数支架具有自膨特性,释放后顺应主动脉的弯曲而发生相应的变形,胸主动脉与支架之间由此产生力的相互作用。深入研究其相互作用对于了解胸主动脉腔内治疗术后重要并发症的发生机制、制定相应的防治方法以及指导支架设计等具有重要价值。数值模拟具有仿真度高、运算快、参数调整便捷等优点,近年来被逐步应用于主动脉病理数字模型、血管血流动力学、裸支架与外周动脉相互作用等方面的研究,而目前关于胸主动脉-支架数值仿真的研究报道尚且较少[1-5]。
1 资料与方法
1.1 资料来源 正常主动脉薄层增强CT断层图像来自1例胸痛待查患者,女性,41岁,CT图像未见异常。本研究取得患者知情同意。源图像为医学数字影像通信标准(digital image and communication on medicine,DICOM)格式,层厚0.8mm,分辨率0.6mm,扫描范围自颈部至腹股沟,涵盖主动脉弓及其3根主要分支髂外动脉远端,共751幅图像。
1.2 主动脉三维数值模型的构建 将CTA图像导入MIMICS软件,确认方位正确后剪切图像,获得主动脉弓至近端30cm的降主动脉的图像。在二维断层上沿主动脉画一条轮廓线,确定主动脉血液图像灰度值。新建蒙板,设定灰度值,采用阈值分割方法分离主动脉及与其图像灰度值保持一致的其他部分。去除与感兴趣区域不相连的部分和游离像素。采用蒙板剪切、3D蒙板编辑和蒙板光顺编辑修改主动脉蒙板,去除不需要的解剖结构。通过蒙板计算3D模型获得主动脉的三维数字化模型。对主动脉模型进行包裹、光顺操作,去除模型结构细节。采用表面网格优化功能,生成可用于有限元分析的面网格,并可进行局部网格加密。然后采用ABAQUS软件进行后续的分析和处理。
1.3 有限元建模 有限元建模采用ABAQUS软件完成,本研究的有限元模型主要包括血管、支架和压握工具三个部分。血管的模型来自MIMICS软件根据真实血管扫描而建立的三维数值模型。根据分析的需要,对血管模型进行几何重构并划分网格,见图1a~c。采用S4单元,单元数量为8552,节点数量为8654。血管采用等厚做简化,血管的厚度为1mm。支架模型为编制型金属支架,环形支架的直径为26.5mm,编制支架的金属条为圆柱截面,其截面直径为0.35mm,支架材料为镍钛合金,见图2a。压握工具为理想的圆柱面,见图2b,采用surface单元,压握工具的外径为29.3mm。在压握过程中,整个圆周面沿着径向方向位移8mm,将金属支架压入血管内部,见图2c。
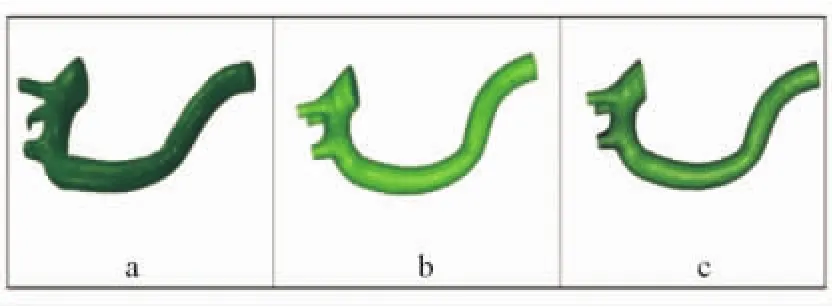
图1 a MIMICS软件提供的原始模型;b几何模型;c网络模型
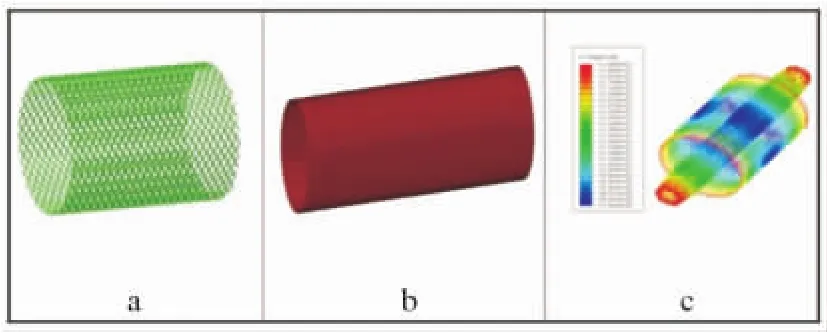
图2 a编制型血管支架;b压握工具的有限元网格模型;c血管支架的压握变形
1.4 有限元分析过程 整个过程采用通用接触,接触属性的切向接触摩擦系数为0.02。过程分两步:(1)通过定义压握工具的径向位移,对金属支架进行压握,直到目标位置,血管不参与接触分析;(2)撤出压握工具,释放金属支架,使金属支架与血管内壁发生接触,压握工具不参与接触分析。
为了显示结构的动态振动过程,同时解决结构的复杂接触的收敛问题,本研究采用显式分析,第一步的分析时间为1s,第二步的分析时间为10s,并根据需要加载适当的阻尼使结构稳定。
1.5 力学作用的计算与分析 本研究采用ABAQUS软件对模型进行分析计算。支架在压握过程中变形,绘制压握过程中的应力分布、最后应力分布以及支架在血管中稳定后的变形分布。着眼于血管角度,描绘血管的最终位移分布、应力分布、应变分布。
为了观察血管被支撑区域的局部变形,在血管上的血管支架的装配位置依次取3条周向的标记线,见图3a。标记线的长度变化代表血管的截面周长变化,红色为原血管的标记线,绿色为加血管支架后的标记线,见图3b。血管截面面积变化是由原截面和变形后调整到同一平面位置的截面面积比较获得,(严格意义上,血管的切面变形后为一曲面,可以认为近似平面),红色为原截面,绿色为变形后截面,见图3c~d。测试在上述3个截面上的12、3、18和9点钟的应力数值分布,见图4。
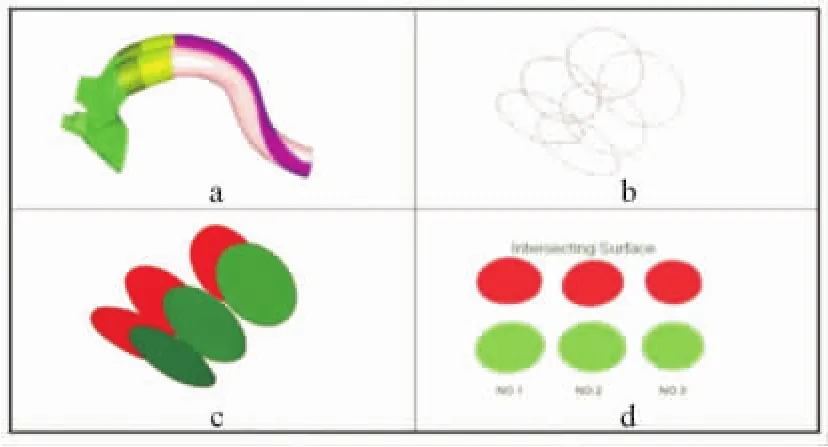
图3 a血管上的3条标记线变形;b血管标记线变形(空间位置);c血管标记线截面不变形(原始空间位置);d血管标记线截面不变形(同一位置)

图4 血管截面标记线应力分布
2 结 果
2.1 3条标记线的长度变化代表了血管周长的变化,长度的增长率分别为:6.99%、9.14%、8.61%,每个部位的增长率不同,但整体反映了血管结构的显著移动。见表1。
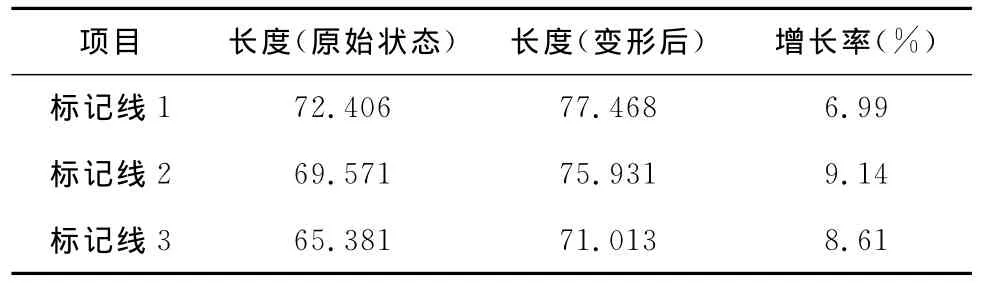
表1 血管标记线长度变化(mm)
2.2 血管截面的变化从另一角度反映了支架释放前后的血管结构面的移动范围,面积的增长率分别为:14.37%、19.47%、18.20%,面积变化存在显著性。见表2。
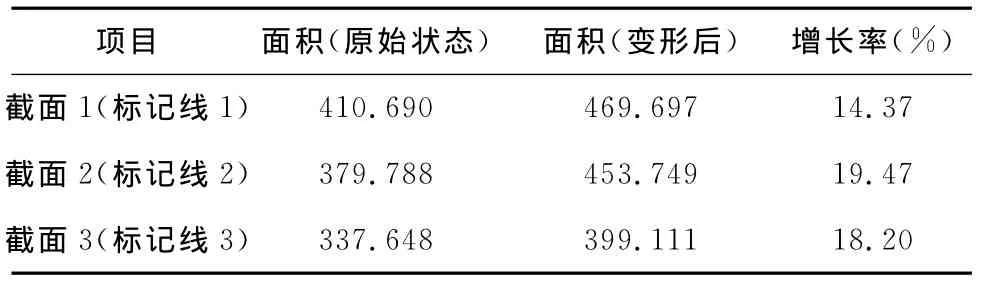
表2 血管标记截面面积变化(mm2)
2.3 血管标记线上的应力分布仿真结果显示,血管支架的两端附近应力相对较大而且分布不均匀。支架与主动脉接触的3个截面上分别在12、3、18和9点钟位置取点,检测支架对主动脉壁形成的应力,近端截面的12点钟位置的应力显著高于其他各点。见表3。

表3 血管标记线上标记点的应力(Mpa)
3 讨 论
从支架的构造特点及其在胸主动脉腔内治疗术中经常所固定的部位推测,支架对于主动脉的作用力主要来自于径向支撑力和弹性回直力两个方面。径向支撑力的大小主要取决于所用支架金属材质的特性以及选择支架时放大的程度,不管支架固定于主动脉的直形部位还是弯曲的部位,径向支撑力均存在。弹性回直力被认为产生于支架固定于主动脉弯曲部位时,例如在Stanford B型主动脉夹层腔内修复中,绝大多数支架均会跨主动脉弓降部释放,此时的支架犹如被动弯曲的弹簧,存在回复至其自然直形状态的倾向,由此产生弹性回直力,作用于主动脉弓降部的大弯侧。这些作用力被认为是主动脉夹层腔内修复术后发生主动脉新发撕裂的重要因素[6-7],在术后致死性因素中居首位[8]。然而,对于以上两种作用力的分析,目前仍然停留在推断、假说阶段。这些力是否确实存在?作用力的强度?在不同条件下的变化如何?在主动脉不同部位有何区别?对此均尚缺乏量化的研究。数值模拟仿真技术的发展为之提供了可能。
鉴于目前胸主动脉-支架数值仿真的研究仍缺乏成熟的技术路线,本研究初步探索了其技术可行性,所以:(1)选用了正常胸主动脉建立模型,暂不考虑病理状态下主动脉材料属性、主动脉形态学和血流变学等因素的影响;(2)选用了现有的编织型支架模型,其结构与节段型设计支架的结构有区别,但是对主动脉壁的作用力相同,能够作为今后进一步研究的技术参考依据;(3)实现模拟支架完全跨主动脉弓降部释放目前仍然有一定难度,故选择释放在接近弓降部的胸降主动脉,因支架近段略呈弯曲。将支架模型置入胸主动脉模型中的关键技术是我们采用的压握的技术,即应用有限元压握模型,将支架压缩,类似于将支架装载入释放系统中,经压缩后的支架模型导入胸主动脉模型,撤除压缩,使支架模型弹开,与胸主动脉接触,整个过程尽可能地接近临床胸主动脉腔内治疗术中支架释放的原理和操作。
我们在胸降主动脉近段,由近而远截取3个横截面,见图3a,观察了各自周长和截面积的变化。结果显示,原先的周长分别为72.406mm、69.571 mm和65.381mm,支架置配后分别增加至77.468 mm、75.931mm 和 71.013mm,增 长 率 分 别6.99%、9.14%和8.61%,见表1;原先的截面积分别为410.690mm2、379.788mm2和337.648mm2,支架置配后分别增加至469.697mm2、453.749 mm2和399.111mm2,增长率分别为 14.37%、19.47%和18.20%,见表2。以上结果提示,自膨式支架释放后促使主动脉扩张,释放即时所能达到的最大直径与主动脉原始直径有关,而并非均能扩大到等粗,这从一个侧面验证了支架对主动脉壁产生作用力的同时,主动脉也对支架产生着限制作用;在临床上我们发现,自膨式支架会不断扩大,尤其是夹层的真腔部分,这种力的平衡打破可能成为主动脉新发撕裂的潜在危险因素,主动脉发生变形的力主要来自支架的径向支撑力。本研究的分析结果显示,支架远端部分扩张幅度更加明显,变形更大。这一分析结果与临床现象及推测相符:主动脉夹层腔内修复术后支架远端的新发破口绝大多数发生在原假腔的内膜片上,据此推测其主要与支架的径向支撑力有关[6]。支架与主动脉接触的3个截面上,分别在12、3、18和9点钟位置取点,检测支架对主动脉壁形成的应力,见图4、表3。结果显示,近端截面的12点钟位置的应力显著高于其他各点,支架两端的应力总体大于支架中段所形成的应力。这与我们在临床上所观察到的支架源性新破口发生的位置基本相符:均位于支架的两端,其中近端破口均出现在弓降部大弯侧(相当于近端截面的12点钟位置)[6]。
本研究结果初步提示基于个体CT影像实现胸主动脉-支架数值仿真具有可行性,为分析主动脉与支架之间的相互作用以及支架源性力学损伤提供了可能。
[1] 付文宇,乔爱科.基于CT图像的胸主动脉瘤模型数值模拟[J].科技导报,2009,27(20):27-31.
[2] Frauenfelder T,Lotfey M,Boehm T,et al.Computational fluid dynamics:Hemodynamic changes in abdominal aortic aneurysm after stent-graft implantation[J].Cardiovasc Intervent Radiol,2006,29(4):613-623.
[3] 梁栋科,杨大智,齐民.一种血管内支架的有限元模型及计算流体动力学分析[J].生物医学工程学杂志,2007,24(3):549-553.
[4] Wang X,Li X.Fluid-structure interaction based study on the physiological factors affecting the behaviors of stented and nonstented thoracic aortic aneurysms[J].J Biomech,2011,44(12):2177-2184.
[5] Kleinstreuer C,Li Z,Basciano CA,et al.Computational mechanics of Nitinol stent grafts[J].J Biomech,2008,41(11):2370-2378.
[6] Dong ZH,Fu WG,Wang YQ,et al.Stent Graft-Induced New Entry After Endovascular Repair for Stanford Type B Aortic Dissection[J].J Vasc Surg,2010,52(6):1450-1457.
[7] Dong ZH,Fu WG,Wang YQ,et al.Retrograde Type A Aortic Dissection After Endovascular Stent Graft Placement for Treatment of Type B Dissection[J].Circulation,2009,119(5):735-741.
[8] 董智慧,符伟国,王玉琦,等.Stanford B型主动脉夹层腔内修复术后发生夹层及手术相关性死亡12例分析[J].上海医学,2009,32(12):1070-1073.

