盐卤浓浆豆腐凝胶形成作用力的研究
周淑红,陈野,张敏,刘君,王君予,郭爽
(天津科技大学食品工程与生物技术学院,天津 300457)
大豆是蛋白质含量最高的植物之一,含有人体必需的8 种氨基酸。中国传统的豆制品以豆腐及豆腐制品为主,在豆腐加工过程中,产生大量营养丰富的黄浆水,然而,目前我国大多数企业将黄浆水直接排放,不仅没有充分利用其营养价值,而且对环境造成污染,不利于增加大豆加工附加值和清洁生产[1]。
蛋白质凝胶是变性蛋白质分子间排斥和吸引相互作用力相平衡的结果,形成和维持蛋白质凝胶的主要作用力是静电相互作用、二硫键、疏水相互作用、氢键等物理作用力[2]。氢键、疏水相互作用、盐键、范德华力都是非共价键,键能虽然小,但由于数量大,并且具有加和性,因此是蛋白质之间不可忽视的作用力。使用不同的凝固剂形成的凝胶分子间作用力不同,目前对葡萄糖酸内酯(GDL)和硫酸钙豆腐凝胶研究较多,Hashizume 等[3-4]认为,对GDL 和硫酸钙豆腐凝胶的形成起重要作用的是二硫键、氢键和疏水相互作用。但Kohyama 等[5]认为,豆浆凝固时,由于pH 偏酸性,不利于疏基与二硫键的交换反应,因此在豆浆凝固过程中很难形成新的二硫键。此外,由于生豆浆只能形成沉淀,不能形成豆腐凝胶,所以氢键不可能是豆浆凝固的主要作用力:大豆蛋白之所以能够形成豆腐凝胶,主要是由于大豆蛋白变性后,暴露出疏水基团,于是在疏水相互作用下大豆蛋白分子相互结合,形成了豆腐凝胶。然而,对盐卤豆腐凝胶的分子间作用力研究较少,其凝胶形成机制与GDL 或硫酸钙豆腐凝胶是否相同仍未知。
目前主要用间接手段研究蛋白质凝胶过程中分子间的作用力,通过添加可以增强或削弱蛋白质分子间作用力的试剂观察凝胶特性的变化,如添加强的表面活性剂十二烷基磺酸钠(SDS)可以破坏疏水作用[6],而氯化钠等高溶解度的盐类可以破坏蛋白质分子间的静电引力[7]。
本研究采用浓缩方法,进而省去在豆腐的制备工艺中排出黄浆水这一工序制备浓浆豆腐,并且试图通过添加可影响特定化学作用力的氯化钠,DTT,SDS,脲等试剂考察其对豆腐凝胶质构特性的影响,分析各种化学作用力对稳定豆腐凝胶结构的重要性,这对掌握豆腐凝固机理,确定豆腐加工条件,无疑具有重要的意义。
1 材料与方法
1.1 试验材料
大豆:市售;盐卤(食品级):天津长芦海晶集团有限公司;氯化钠、盐酸、甘氨酸,EDTA,尿素、DTT、、SDS、脲等试剂均为分析纯。
1.2 试验设备
RE-3000A 真空旋转薄膜蒸发器:上海亚荣生化仪器厂;磨浆机:北京京美华研科技有限公司;TA-XT plus 型质构仪:北京微讯超技仪器技术有限公司;HH数显恒温水浴锅:金坛市金城国胜实验仪器厂;756PC UV 系列紫外可见分光光度计:天津市普锐斯仪器有限公司;RF-5301 荧光分光光度计:岛津公司;PHS-25 pH 计:上海今迈仪器仪表有限公司。
1.3 方法
1.3.1 浓浆豆腐的工艺流程
挑选颗粒饱满的优质大豆,按大豆干重∶水=1 ∶3的比例浸泡12 h 左右(20 ℃),使浸泡好的豆重约为干豆重2.2 倍~2.3 倍。按干豆重∶水=1 ∶8 的比例进行两次磨浆,过滤,浓缩至豆浆的蛋白质浓度约为10%。蒸汽加热至95 ℃保持5 min,冷水快速冷却,加入0.6%(w/v)的盐卤,快速搅拌均匀,90℃下水浴加热30 min,凝固成型,冷却30 min 后得到浓浆豆腐。
1.3.2 凝胶强度的测定方法
将上述制备的豆腐凝胶在冷藏箱(4 ℃)中静置10 h 后,取出于室温下放置1 h,用质构仪的TPA 模式测定其凝胶特性。采用P0.5 的探头,测前速度5 mm/s,检测速度1 mm/s,测后速度1 mm/s,时间5 s,力5.0 g,距离5 mm。每个样品平行试验3 次。
1.3.3 盐卤豆腐凝胶形成过程中巯基含量的测定
1.3.3.1 样品制备
将浓缩好的生豆浆加热至95 ℃保持5 min,冷水快速冷却,加入盐卤并搅拌均匀,90 ℃水浴,分别加热0、10、20、30、40、60 min 时取样。
1.3.3.2 巯基含量的测定
分别取上述制备的豆腐凝胶样品1 g,加入缓冲液(每升溶液含Tris 10.4 g,甘氨酸6.99 g,EDTA1.2 g,尿素480 g,pH=8.0)15 mL,均质1 min,在4 000 r/min下离心15 min,取上清液,滤渣中继续加缓冲液5 mL,4 000 r/min 下离心15 min,取上清液,合并前后两次的上清液。取合并后的上清液1 mL+缓冲液2.0 mL+Ellman 试剂0.02 mL,25 ℃保温5 min,在412 nm 下,用分光光度计测定溶液吸光值。实验以不加样品,而加Ellman 试剂为空白,以不加Ellman 试剂,而加样品的溶液确定其混浊度。
1.3.4 盐卤豆腐凝胶形成过程中表面疏水性的测定
1.3.4.1 制备样品
制备方法与上述测定巯基含量样品的制备方法相同。
1.3.4.2 表面疏水性的测定
采用ANS 荧光探针法。取3g 豆腐凝胶溶于150mL的0.01 mol/L 磷酸缓冲液中,然后在均质机上均质4 min,然后在5 000 r/min 下离心15 min,取上清液,用考马斯亮兰法测定溶液中蛋白质的浓度。然后再使用磷酸缓冲液将上清液稀释至0.02 mg/mL~0.10 mg/mL之间。然后,取不同浓度的样品溶液10 mL,采用荧光分光光度计在330.0 nm 的激发波长(狭缝宽度10.0 nm)和467.0 nm 的发射波长(狭缝宽度3.0 nm)下测定样品的荧光强度(FI0),以及样品中加入50 μL 浓度为8 mmol/L 的ANS 溶液后的荧光强度,振荡,静置10 min后测其荧光强度(FI1)。FI1和FI0的差值记为FI。以荧光强度对蛋白质浓度作图,初始段的斜率即为蛋白质分子的表面疏水性指数。
2 结果与分析
2.1 分子间静电作用对盐卤豆腐凝胶质构特性的影响
2.1.1 氯化钠对盐卤豆腐凝胶质构特性的影响
氯化钠对凝胶硬度和弹性的影响分别如图1 和图2所示。可知,随着氯化钠浓度的增加,盐卤豆腐的硬度呈现先增加后降低的趋势,在氯化钠浓度达到5 mmol/L 时,硬度达到最大值。而弹性趋势与之相反,即先降低后增加,在氯化钠浓度达到5 mmol/L 时,弹性为最小值。

图1 氯化钠浓度对凝胶硬度的影响Fig.1 Effect of NaCl concentration on on the hardness of gel

图2 氯化钠浓度对凝胶弹性的影响Fig.2 Effect of NaCl concentration the the springiness of gel
这是因为氯化钠在较低浓度(≤5 mmol/L)时,具有电荷中和的作用,其加入有利于中和豆腐凝胶表面的负电荷,降低肽链间的静电斥力,有利于凝胶的形成,因而凝胶硬度增加。氯化钠还可以使蛋白质的水化作用增强,破坏蛋白质间的次级键[6],因此,当氯化钠超过一定浓度,蛋白质的水化作用逐渐加强,阻碍蛋白质分子间的凝聚,不利于凝胶的形成,使得凝胶强度降低。
2.1.2 pH 对盐卤豆腐凝胶质构特性的影响
pH 对凝胶硬度和弹性的影响分别如图3 和图4所示。

图3 pH 对凝胶硬度的影响Fig.3 Effect of pH on the hardness of gel

图4 pH 对凝胶弹性的影响Fig.4 Effect of pH on the springiness of gel
由图可知,pH 由6.0 增加到9.0 的过程中,凝胶硬度呈现先增加后降低的趋势,在pH=7.0 时,凝胶硬度达到最大值。而弹性则随着pH 增加而降低。当pH 远离等电点时,蛋白质分子带有同种电荷,相互排斥力占主导,当静电排斥力与蛋白分子变性后暴露的疏水基团之间的吸引力达到平衡时,凝胶形成。因此pH 越高,游离水量越少,形成的豆腐凝胶情况越好,但pH过大会导致蛋白质分子变性[8]。
2.2 二硫键对盐卤豆腐凝胶质构特性的影响
2.2.1 二硫苏糖醇(DTT)对盐卤豆腐凝胶质构特性的影响
DTT 对凝胶硬度和弹性的影响分别如图5 和图6所示。
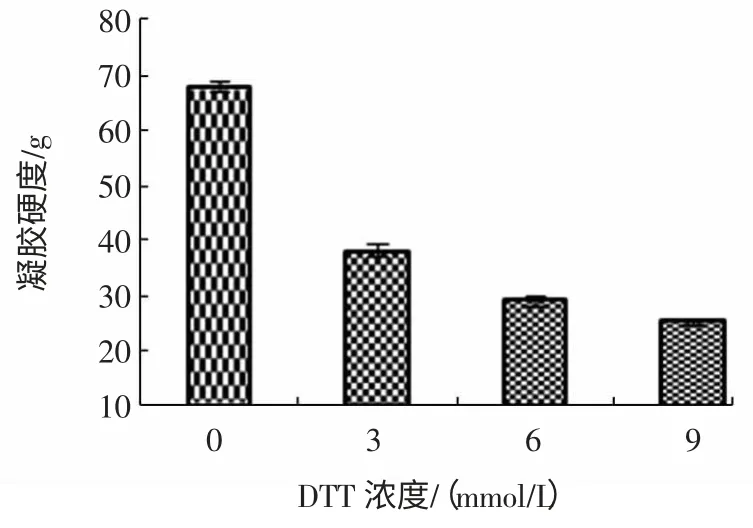
图5 DTT 浓度对凝胶硬度的影响Fig.5 Effect of DTT concentration on hardness of gel

图6 DTT 浓度对凝胶弹性的影响Fig.6 Effect of DTT concentration on the the the springiness of gel
由图可知,随着DTT 浓度的增加,盐卤豆腐凝胶的硬度呈现下降趋势,且低浓度范围内下降趋势较大,随着DTT 浓度的增加,下降趋缓。DTT 是常用还原剂,有抗氧化作用,可以稳定蛋白质的活性,同时又是蛋白质变性剂,可破坏二硫键,抑制二硫键的生成。有报道称,蛋白质中的二硫键经还原反应形成巯基后,蛋白质构象将变得松散[9]。由如图5 可以看出,在DTT存在下,盐卤豆腐凝胶的硬度降低。这说明凝集时发生了巯基的氧化,二硫键的生成对凝胶强度有一定的影响。
2.2.2 盐卤豆腐凝胶形成过程中巯基含量的变化
盐卤豆腐凝胶形成过程中巯基含量的变化如图7所示。

图7 盐卤豆腐凝胶形成过程中巯基含量的变化Fig.7 Changes of the sulfhydryl content during bittern tofu gel formation process
由图7 看出,随着凝固时间的延长,巯基含量基本呈下降趋势。巯基含量在凝胶凝固过程中降低,说明在水解过程中一些游离的巯基发生氧化,生成了二硫键。二硫键是共价键,键能大于疏水作用和氢键。二硫键,尤其是链间二硫键的生成对稳定和增强凝胶结构具有重要的作用[10]。
2.3 疏水相互作用对盐卤豆腐凝胶质构特性的影响
2.3.1 十二烷基硫酸钠(SDS)对盐卤豆腐凝胶质构特性的影响
SDS 对凝胶硬度和弹性的影响分别如图8 和图9所示。
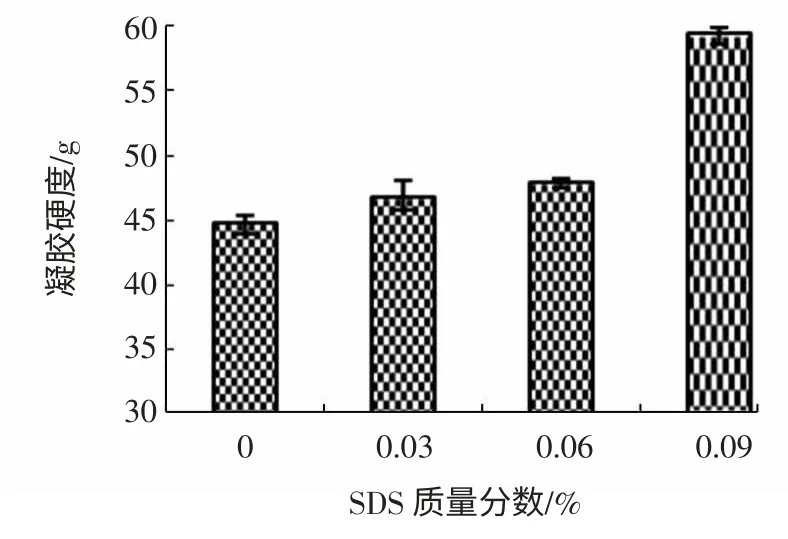
图8 SDS 对凝胶硬度的影响Fig.8 Effect of SDS concentration on the hardness of gel

图9 SDS 对凝胶弹性的影响Fig.9 Effect of SDS concentration on the springiness of gel
由图可知,随着SDS 质量分数的增加,盐卤豆腐凝胶的硬度呈缓慢增长趋势,当SDS 的质量分数达到0.09%时,凝胶的硬度达到了最大值。同样,弹性也随SDS 质量分数增加而增大。SDS 是一种强的亲水表面活性剂,加入后可以破坏蛋白质分子的疏水结合[6],有助于肽链的充分展开和疏水基团的暴露,使蛋白溶液的疏水性增大,有利于凝胶网络的形成。另外溶液的疏水性的增大,有利于链间二硫键的形成,从而有助于凝胶结构的稳定。
2.3.2 盐卤豆腐凝胶形成过程中表面疏水性的变化
盐卤豆腐凝胶形成过程中表面疏水性的变化如图10 所示。

图10 盐卤豆腐凝胶形成过程中表面疏水性的变化Fig.10 Changes of the surface hydrophobicity during bittern tofu gel formation process
随着盐卤豆腐凝胶形成时间的延长,凝胶的表面疏水性指数S0呈先增加后下降的趋势,当凝胶时间为30 min 时,表面疏水性指数达到最大值。这可能是因为随着凝固时间的延长,蛋白质的变性程度增大,疏水区域暴露在外,促进蛋白质通过疏水相互作用形成凝聚体。但是当凝固时间过长时,蛋白质通过疏水相互作用交联的机会增多,表现为表面疏水性指数降低,参与豆腐凝胶形成的疏水性基团减少,导致豆腐的凝胶强度降低[11]。
2.4 氢键对盐卤豆腐凝胶质构特性的影响
脲对凝胶硬度和弹性的影响分别如图11 和图12所示。
由图可知,随着脲浓度的增加,盐卤豆腐凝胶的硬度呈现显著下降趋势,弹性也呈现下降趋势。当脲的浓度为0.05 mol/L 时,凝胶硬度显著下降,继续增加脲的浓度,则凝胶无法形成。
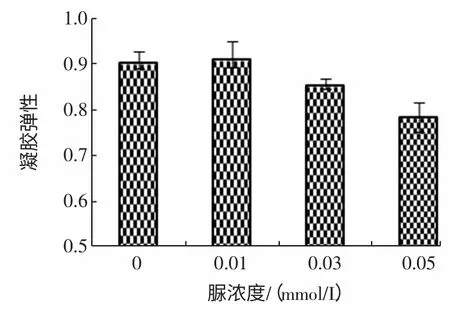
图12 脲的浓度对盐卤豆腐凝胶弹性的影响Fig.12 Effect of urea concentration on the springiness of gel
煮沸后蛋白质变性,肽链展开随机排列,破坏了原来的氢键,原来形成氢键的基团暴露,暴露的氢键基团促进展开的肽链相互聚集,氢键的结合使得肽链形成稳定结构。当加入一定浓度的脲后,脲与肽链间的氢键基团结合,肽链上的氢键基团被屏蔽,影响肽链间氢键的形成。因此,凝胶的硬度及弹性显现下降趋势,甚至不能形成凝胶。
实验数据表明随着脲浓度的增大,脲对肽链间氢键形成的影响加大,由此可以看出氢键是豆腐凝胶形成的分子间作用力之一,并且对豆腐凝胶的形成有重要的影响[8]。
3 结论
通过对不同pH 以及NaCl 浓度对盐卤凝固豆腐凝胶过程的影响的研究,结果表明:在腐凝胶形成过程中离子键的作用较大,凝胶的形成需要克服蛋白质分子间的静电斥力。通过DTT 对盐卤凝固豆腐凝胶过程中的影响以及巯基含量变化的研究可知,二硫键在凝胶形成过程中的起着重要作用,能够较大的促进凝胶的形成。结合SDS 对盐卤豆腐凝胶的影响以及疏水性的测定,可见疏水相互作用对豆腐凝胶有显著的作用。脲的添加也证实了氢键对形成凝胶的重要影响。因此,在盐卤浓浆豆腐凝胶形成中,静电相互作用,二硫键,疏水相互作用以及氢键对凝胶的形成都具有重要作用。
[1]唐鑫,陈卓然,黄薪安,等.豆制品生产中黄浆水的综合应用[J].农产品加工,2010(6):67
[2]董秋颖,杨玉玲,许婷.从质构学角度研究肌原纤维蛋白凝胶形成的作用力[J].食品与发酵工业,2009,35(5):45
[3]Hashizume K,Maeda M,Watanabe T.Relationships of heating and cooling condition to hardness of tofu[J].Nippon Shokuhin Kogyo Gakkaishi,1978,25:387-391
[4]Hashizume K,Ka G.Difference between tofus coagulated with glueono-delta-lacton and calcium salts[J].Nippon Shokuhin Kogyo Gakkaishi,1978,25(7):383-386
[5]Kohyama K,Sano Y,Doi E.Reological characteristics and gelation mechanism of tofu (soybean curd)[J].J Aghe Food Chem,1995,43:1808-1812
[6]沈同,王镜岩.生物化学[M].2 版.北京:高等教育出版社,1990:34-37
[7]RENKMA J M S,LAKEMOND C M M,JONGH H H J,et al.The effect of pH on heat denaturation and gel forming properties of soy proteins[J].Biotechnology,2000,79:223-230
[8]CHEFTEL C,CUQ J L,LORIENT D.Amino acids,peptides and pmteins[M].FEUNENM O R.Food Chemisty,1993:275-414
[9]田悦,社军保.二硫键和巯基在蛋白质结构功能中的作用及分析方法[J].实用儿科临床杂志,2007,22(19):1499-1501
[10]Cherry J P.Protein Functionality in Foods (ACS Symposium Series 147)[M].Washington:American Chemistry Society,1981:136-137
[11]李里特,汪立君,李再贵,等.大豆蛋白热变性程度对豆腐品质的影响[J].中国粮油学报,2002,17(1):3

