不同剂量rmhTNF 对大鼠移植性肝癌的治疗作用
夏 风,石小红
(1.湖北省妇幼保健院,湖北 武汉 430070;2.嘉鱼县人民医院)
本实验观察肌注重组改构人肿瘤坏死因子(rmhTNF)对大鼠移植性肝肿瘤(Walker-256)生长的抑制作用,旨在为rmhTNF 临床肝癌的治疗提供实验依据。
1 材料和方法
1.1 材料
实验中所用Wistar 大鼠共24 只,由华中科技大学同济医学院医学动物实验中心提供,注射用rmhTNF 由上海赛达生物药业有限公司提供,Walker-256 瘤株自上海医药研究所传代。
1.2 方法
Walker-256 瘤株先传代,约10d 后长出直径约1.5cm 的肿瘤结节,再将肿瘤种植于肝左外叶,10d 后经MRI 证实移植成功后,随机分成3组,每组8 只。对照组肌注生理盐水0.1ml,肌注1组(IM1组)肌注rmhTNF 16.7 万u,肌注2组(IM2组)肌注rmhTNF 33.3 万u,均为1次/d,连续10d后停止注射。
1.3 影像学检查
分别于肌肉注射前及注射后14d 行MRI 检查,测量肿瘤最大径(d1)及最小径(d2),通过公式V=0.5×d1×d22计算肿瘤治疗前后体积,分别用V1、V2 表示,对3组间肿瘤生长率(V2/V1)进行比较。
1.4 病理学检查
于移植术后14d,先行磁共振检查,然后处死荷瘤大鼠,肝脏肿瘤标本经10%甲醛溶液固定,石蜡包埋,分别切片染色。
2 结 果
所有动物均存活,MRI 检查均发现肝脏左叶肿瘤。同对照组相比,肌肉注射rmhTNF 能明显抑制大鼠Walker-256 移植瘤的生长(P<0.05),两组不同剂量治疗组间的抑瘤作用无显著性差异,见表1。观察肿瘤大体标本及HE 染色切片,发现肌注组肿瘤中央组织坏死范围较对照组广泛,且坏死较彻底,肿瘤向周边组织侵犯、扩散也明显少于对照组。
方差齐性检验方差齐同(P>0.05)单因素方差分析F=5.045,P<0.05,组间比较Student-Newman-Keuls 法肌注组与对照组有显著性差异(P<0.05),肌注组间无显著性差异(P>0.05)。
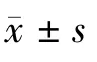
表1 肌肉注射rmhTNF 的抑瘤作用[,mm3]
3 讨论
天然TNF 是由激活的单核巨噬细胞、NK 细胞、T 细胞产生的多功能蛋白,包括TNF-α、TNF-β和TNF-γ,能够相对特异性地杀伤多种肿瘤细胞,具有抗肿瘤、调节免疫效应细胞、诱导细胞分化、调节机体代谢、参与免疫及炎症反应、抗菌、抗病毒、刺激细胞生长等多种生物学活性,通过多种因素的综合作用导致瘤细胞坏死[1]。研究表明,TNF 在小剂量时难以发挥抑瘤效果[2],必须在体内必须达到一定的血药浓度,才能够发挥抑制或者杀伤肿瘤细胞的作用,但由于全身大剂量应用TNF 可产生严重毒副作用[3],如发热、寒战、恶心、呕吐、食欲下降、头痛、乏力、白细胞减少、肝功能异常、血压下降、休克等,另外TNF 还有可能参与恶液质的形成[4]以及免疫病理损伤过程,因此限制了其临床应用。通过第四军医大学与上海赛达生物药业有限公司的合作,利用生物工程技术改造了天然TNF 构型,进而研制成rmhTNF,对比天然TNF,rmhTNF 的毒副作用明显降低,并且可肌肉注射,其作用时间延长,临床使用起来更加方便和安全。
rmhTNF 是将天然人TNF-α 基因的5’端1 至7个氨基酸编码序列删除,用Arg-Lys-Arg 编码序列取代8、9、10 位Pro、Ser、Asp 的编码序列,同时Phe 密码子取代Leu157 的密码子,产生新的突变基因,插入原核高表达载体从而构建出高表达菌株[5]。研究表明其对多种实体瘤均有效[6]。TNF对肿瘤作用的实验及临床研究主要集中于与其他治疗手段的结合使用上。本实验结果显示单用rmhTNF 对大鼠的移植性肝癌有显著抑制作用,实验中所使用的rmhTNF 剂量参考说明书推荐剂量。剂量加倍后疗效亦无明显增加,甚至对肿瘤生长的抑制作用稍有减弱,可能与TNF 受体饱和等因素有关。TNF-α 抗肿瘤作用的分子机理是由受体引发的信号传导。当TNF 与受体结合趋于饱和后,再增加剂量其效应增强也会十分有限。临床应用中的关键也就是选择一个合适的剂量,既能发挥最佳治疗效果,又能减轻其不良反应的发生。
Oldham 于1984年提出了生物反应调节(biological response modifiers,BRM)的理论,同时提出了肿瘤生物治疗(biotherapy)的概念。BRM 是指通过某种物质或措施,直接或间接改变宿主对肿瘤细胞的生物学反应,从而产生有利于宿主并不利于肿瘤治疗效应。由于生物治疗既能直接作用于肿瘤,抑制或直接杀灭肿瘤细胞,又可通过调节机体生物反应,通过其他多种生物因子的作用,抑制肿瘤生长或使肿瘤组织溶解,因此生物治疗已成为继手术、放疗、化疗等治疗手段之后临床上治疗肿瘤的又一重要方法。
[1]Van Ostade X,Vandenabeele P,Everaerbt B,et al.Human TNF mutants with selective activity on the p55 receptor[J].Nature,1993,361:266
[2]Blick M,Sherwin SA,Rosenblum M,et al.A phase study of recombinant tumor necrosis factor in cancer patients[J].Cancer Res,1987,47:2986
[3]Schilling PJ,Murray JL,Markowitz AB.Novel tumor necrosis factor toxic effects[J].Cancer,1992,69:256
[4]Guttridge DC,Mayo MW,Madrid LV,et al.NF-kB-induced loss of MyoD messenger RNA:Possible role in muscle decay and cachexia[J].Science,2000,289:2363
[5]张英起,赵宁,李波,等.应用基因工程方法制备新型重组人肿瘤坏死因子-?[J].细胞与分子免疫学杂志,2002,18:402
[6]秦凤展,郑荣生,陈余清,等.注射用重组改构人肿瘤坏死因子治疗恶性肿瘤Ⅲ期临床观察[J].中国新药杂志,2003,12:646

