正交试验法优选芪珠升白口服液最佳提取工艺*
范少敏 郭 琳 张 旋 刘 超 王 珊 杨新杰 宋小妹 陕西中医学院(咸阳712046)
芪珠升白口服液是多年临床应用经验方,由珠子参、黄芪两味中药组成,具有提高机体免疫力、升高白细胞数的作用,用于放化疗所致的白细胞减少症的治疗。现代研究表明,芪珠升白口服液富含多糖和皂苷,而且是其主要有效成分。因此,该实验采用L9(34)正交实验设计方案,分别以葡萄糖、竹节参皂苷IVa为对照品,以制剂中总多糖和总皂苷的含量及得率为评价标准[1,2],对该制剂的提取纯化条件进行优化,为该制剂的工业化生产提供科学依据。
1 仪器、试剂及药材
1.1 仪器 RE-52旋转蒸发仪(上海亚荣生化仪器厂),UV1102紫外分光光度计(上海天美科学仪器有限公司),GB-204电子天平(瑞士梅特勒拖利多),SHD-3循环水多用真空泵郑州杜甫仪器厂。
1.2 试剂 蒽酮、硫酸、香草醛、冰醋酸、无水乙醇、高氯酸、正丁醇。
1.3 药材及对照品 珠子参药材、黄芪药材,购自陕西省西安市万寿路药材市场。竹节参皂苷IVa对照品(自制,经1HNMR、13CNMR、HMBC、HMQC及HR-MS确定结构,面积归一法计算含量均大于98%);葡萄糖对照品(批号:110833-200503)。
2 方法及结果
2.1 总皂苷含量测定方法建立
2.1.1对照品溶液制备:精密称取竹节参皂苷IVa对照品10mg,用甲醇溶解并定容至10mL,摇匀,即得浓度为1mg/mL的竹节参皂苷IVa对照品溶液。
2.1.2 测定波长的选择:准确吸取上述对照品溶液0.1mL于10mL具塞试管中,精密加入新配制的50g/L 的香草醛-冰醋酸溶液0.2mL和高氯酸0.8mL,摇匀,置60 ℃水浴加热15 min,冰水冷却2min,精密加入冰醋酸5mL,摇匀,随行试剂做空白,用紫外分光光度计在700nm~400nm 波长范围内进行全程扫描,最大吸收波长在560nm 左右,故选择560nm 为测定波长。
2.1.3 标准曲线的绘制:精密吸取竹节参皂苷IVa对照品溶液0.1mL、0.2mL、0.3mL、0.4mL、0.5mL、0.6mL,分别置于具塞试管中,挥尽溶剂。参照上述2.1.2项下方法,于560nm测定吸光度(Abs),以竹节参皂苷IVa含量为横坐标(X),吸光度Abs)为纵坐标(Y)绘制标准曲线。竹节参皂苷IVa对照品在100μg~600μg 范围内线性关系良好,回归方程为Y=0.0563X+0.0001,r=0.9991。
2.2 总多糖含量测定方法建立
2.2.1葡萄糖对照品溶液制备:将葡萄糖对照品于60℃烘1h,再逐渐升温至105℃干燥至恒重。精密称取葡萄糖对照品33mg,置于100mL量瓶中,加水溶解并稀释至刻度,摇匀,即得每1mL含无水葡萄糖0.33mg的溶液,作为对照品溶液。
2.2.2 测定波长的选择:准确移取对照品溶液0.1mL 于10mL具塞试管中,用蒸馏水定容,取2mL 于10mL的具塞试管中,摇匀,在冰水浴中缓缓滴加0.2%蒽酮-硫酸溶液至刻度,混匀,放冷后置水浴中保温10min,取出,冰水浴冷却10min,取出,以相应试剂为空白,紫外分光光度计在800nm~400nm 范围全程扫描,结果显示在620nm 左右有最大吸收,故确定620nm 为测定波长。
2.2.3 标准曲线的绘制[3,4]:精密吸取标准溶液0.1mL,0.2mL,0.3mL,0.4mL,0.5mL,0.6mL分别置于10mL量瓶中,用蒸馏水定容,分别取2mL 于10mL 的具塞试管中,参照2.2.2项下方法,于620nm 波长处测定吸光度。以吸光度(Abs)为纵坐标,浓度为横坐标,绘制标准曲线。葡萄糖在33μg~198μg范围内呈良好线性关系,回归方程为Y=0.0265X-0.0011,r=0.9995。
2.3 提取工艺条件优化研究
2.3.1正交试验因素水平设计:多糖和皂苷为该复方制剂的主要有效成分。根据文献报道[1,2],影响皂苷、多糖提取的主要因素有提取时间、提取次数、溶剂体积,因此,在预实验的基础上,以总多糖和总皂苷的含量为评价指标,采用L9(34)正交试验方案对其提取工艺进行优选,因素水平见表1。

表1 因素水平表正交试验方案结果见表2 。
2.3.2供试品溶液制备:取处方量药材粉末12g,共9份。按上述正交表方案组合进行提取,浓缩,使各组药液至50mL,即为各样品溶液。
2.3.2.1多糖供试品溶液的制备:精密量取上述各样品溶液30mL,加无水乙醇80mL,摇匀,离心,分离沉淀,沉淀用热水溶解,冷却,定容至100mL,摇匀,即得。
2.3.2.2 皂苷供试液的制备:精密上述各样品溶液量取制剂20mL,以水饱和的正丁醇50mL 萃取两次(25,25mL),萃取液合并,蒸干,精密加甲醇10mL溶解残渣,摇匀,即得。
2.3.3 样品含量测定[3]
2.3.3.1 多糖含量测定:精密吸取多糖供试品1mL 于10mL具塞试管中,加水2mL,摇匀,缓滴加0.2%蒽酮-硫酸溶液至刻度,混匀,放冷后置60℃水浴中保温10min,取出,立即置冰水浴中冷却10min,取出,以相应试剂为空白,在620nm 处测定吸光度。从多糖标准曲线计算多糖量,结果见表2。
2.3.3.2 总皂苷含量测定:取样品溶液0.2mL 至10mL 的量瓶中,用甲醇定容至刻度,取0.5mL 至具塞试管中,在水浴中挥尽溶剂,立即取出,放冷,参照上述2.1.2 项下方法,在560nm 处测定吸光度。据皂苷标准曲线计算皂苷量,见表2。
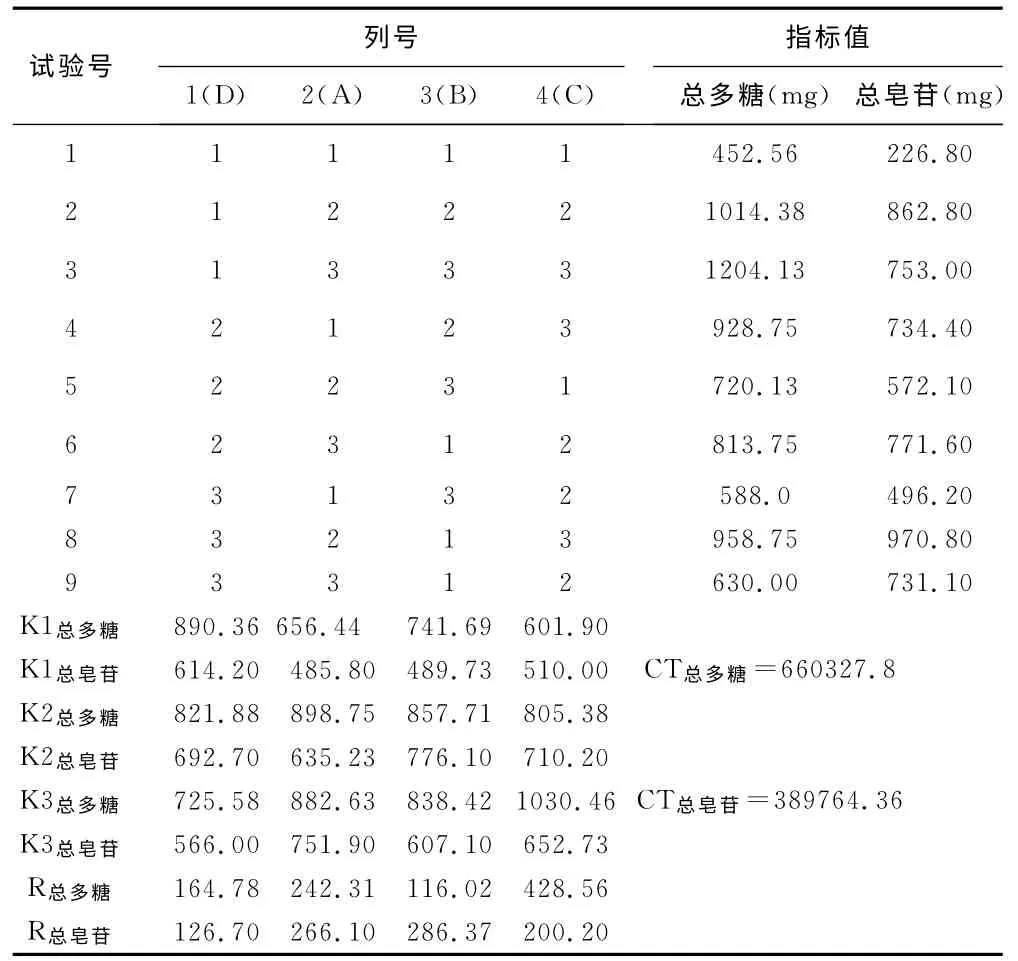
表2 正交试验方案及结果统计表
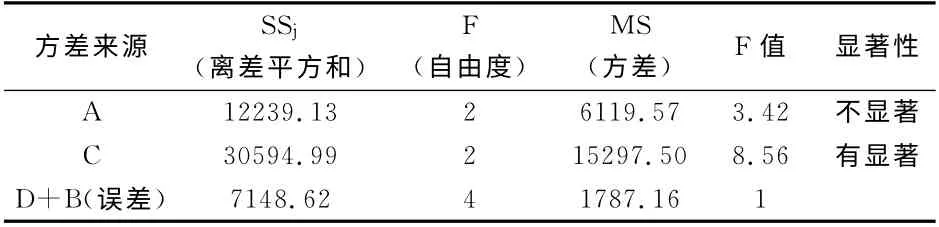
表3 多糖含量方差分析

表4 总皂苷含量方差分析
2.3.4 提取工艺的确定
2.3.4.1综合表2、表3的分析结果,影响多糖指标的因素大小顺序为C>A>D>B,且C 因素有显著性差异,A 因素K值大小顺序为K2>K3>K1,B 因素K 值大小顺序为K2>K3>K1,C因素K 值大小顺序为K3>K2>K1,综合考虑,为达到指标合理且除去杂质,从多糖指标得到的最优工艺组合为A2B2C3。
2.3.4.2 根据表2的正交实验结果及表4的皂苷指标方差分析数据,影响皂苷指标的因素大小顺序为B>A>C>D,但均无显著性差异,A 因素K 值大小顺序为K3>K2>K1,B 因素大小顺序为K2>K3>K1,C 因素大小顺序为K2>K3>K1,从皂苷指标得到的最佳工艺组合为A3B2C2。
1.3.4.3 综合对多糖和皂苷指标值及方差的分析,以及考虑到实际生产,得该口服液的最佳生产提取工艺为A2B2C3,即加8倍量水回流提取3次,每次1.5h。
2.4 验证性实验 按处方量分别取黄芪,珠子参各三份,按照优选的最佳工艺即8倍量水,回流提取3次,每次1.5h进行提取,使各组药液浓缩到50mL,按以上方法分别测定三组样品的总多糖和总皂苷含量,结果见表5。

表5 验证性实验结果
由表5可知,此方法稳定可靠,可以作为芪珠升白口服液的提取工艺。
3 讨 论 中药的提取效果直接关系到制剂的质量和疗效,选择合理的提取工艺是工业化大生产的前提和保障,合理的提取工艺评价指标是提取的有效成分质量的代表,也是提取物临床作用和疗效的体现。目前,用提取物中成分含量评价提取效果应用较多,此法量化程度高、易于操作,且具有耗资少的优点。本文分别以葡萄糖、竹节参皂苷IVa为对照品,以制剂总皂苷和总多糖的含量及得率为评价指标,将二者综合考虑作为工艺优化的指标。
[1] 王淑萍,李晓静,张桂珍.黄芪多糖提取分离纯化工艺的优化研究[J].分子科学学报,2008,24(1):60-64.
[2] 高培红,曹军毅,宋小妹.正交实验法优选珠子参总皂苷的提取工艺[J].陕西中医学院学报,2006,29(2):66-68.
[3] 王小平,王 进,陈建章.建昌帮与樟树帮、中国药典法炮制的熟地黄中多糖含量比较[J].陕西中医,2009,30(8):1066-1067.
[4] 王春燕,潘卫三,杨建春,等.正交实验法优选复方参芪软胶囊的提取工艺[J].中国药师,2009,12(9):1320-1321.

