Dawson型锌钨酸配合物催化苯乙烯氧化制苯甲醛正交试验研究
孙晶吴传德陈丽华唐晶刘立红代立梅张沐
(1.黑河学院 黑龙江黑河 164300;2.浙江大学化学系 浙江杭州 310000)
化合物的合成条件往往是受多因素制约,若进行全面试验,不但实验次数多,工作量大,而且实验数据不十分可靠,实验结果分析也存在一定的困难。如果采用正交试验法则可以用较少的试验次数,得到可靠的数据,而且实验结果也容易分析和比较。本文以Dawson型锌钨酸配合物催化苯乙烯氧化制苯甲醛为例,采用正交试验法进行研究,得出最佳的合成方案,为清洁苯甲醛生产工艺的开发提供基础研究依据。
一、实验部分
(一)试剂和仪器
所用试剂均为分析纯,催化剂合成后经元素分析、综合热分析、单晶结构测定等手段进行表征确定所合成产物的结构与文献描述相符,在此不再详细讨论。
(二)催化性能研究
在装有温度计、分水器、磁力搅拌器和回流装置的三口烧瓶中,按一定比例加入计量的苯乙烯、丙酮、30%H2O2和催化剂(目标配合物),回流反应一定时间后,冷却、过滤。滤液采用GC-MS分析其中苯甲醛和苯乙烯的含量,计算产品的收率,用以表示催化剂的活性,反应方程见图1。
图1 苯乙烯与过氧化氢的反应
(三)正交试验设计
正交试验设计参照文献[7]进行。
二、结果与讨论
(一)正交试验结果分析
在多个影响苯乙烯氧化制苯甲醛的因素中,选择反应时间(A)、反应温度(B)、催化剂用量(C)和过氧化氢用量(D)作为考察因素,用L16(45)安排正交试验。正交试验设计如表1所示。
正交试验结果与分析见表2。
从表2的极差分析可看出,R2>R4>R1>R3,即4因素对该反应的影响大小顺序依次为:反应温度、过氧化氢用量、反应时间、催化剂用量。由表2结果可看出,最佳的因素水平为A4B3C2D4,即优化的工艺条件是:反应时间达到20min,反应温度达到50℃,催化剂用量达到1.5g,过氧化氢用量达到4.0ml条件下,反应的酯化率可达89.5%。
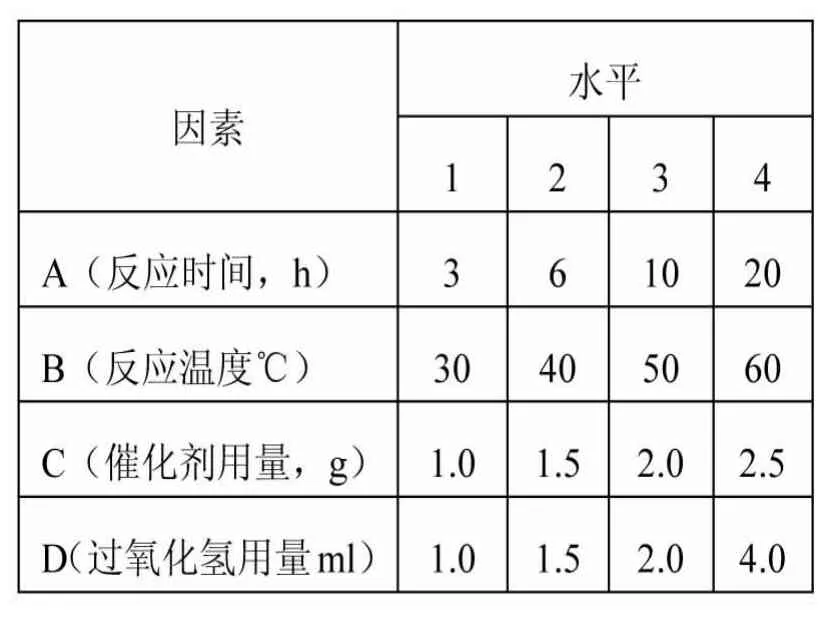
表1 L16(45)正交试验因素与水平
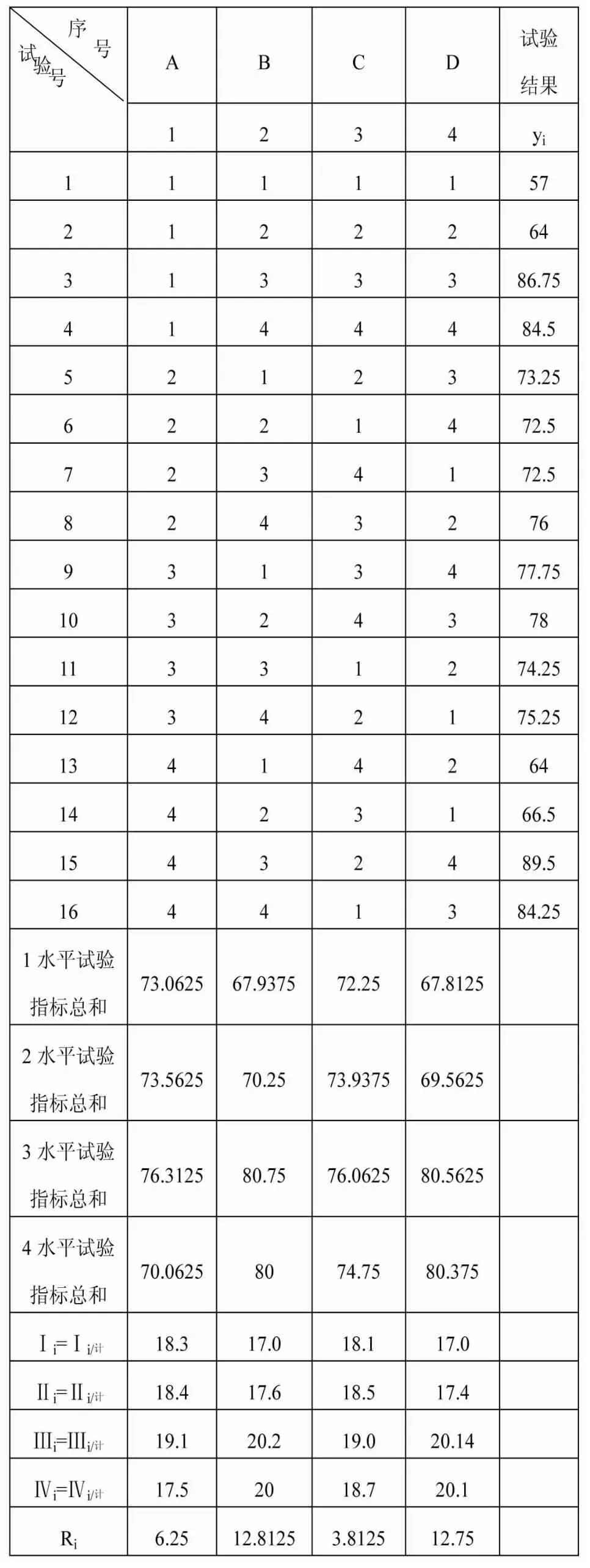
表2 正交试验结果与分析
在优化条件下进行多次验证试验,验证结果见表3。从表3可知,试验的重现性很好。

表3 优化工艺条件的验证试验结果
(二)催化剂种类对反应的影响
对相关化合物的催化活性比较结果(见表4):在同等条件下不加催化剂以CH3CN和DMF为溶剂试验,虽然苯甲醛的选择性为89%,但苯乙烯的转化率分别只有40%和15%。比较几种不同的催化剂,从表4中实验数据可以看出催化活性均较差。且[Na12Mn2Zn3W19]对反应无催化活性。实验证实,新型配合物中镍(Ⅱ)离子的存在具有良好的氧化还原活性。
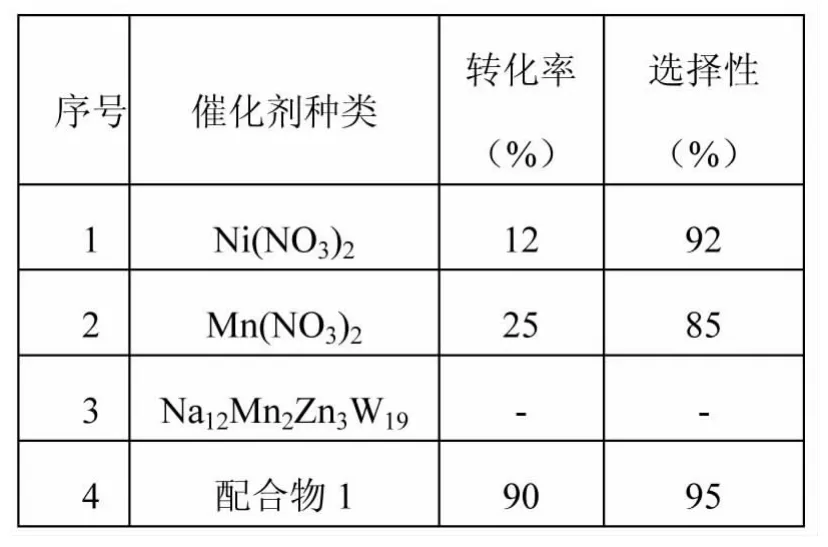
表4 催化剂种类对催化性能的影响
此外我们在优化的反应条件下对催化剂重复使用时的活性进行了考察。催化剂在6次循环后转化率下降到40%,但仍有活性。连续使用3次仍可得到较高的转化率。洗涤和重结晶提纯处理恢复了催化剂的结构,从而恢复其催化活性,表明该催化剂可再生,循环使用活性较好[8]。
三、结论
通过正交实验筛选出了Dawson型锌钨酸配合物催化苯乙烯氧化制苯甲醛的的最佳反应条件为:反应时间达到20min,反应温度达到50℃,催化剂用量达到1.5g,过氧化氢用量达到4.0ml条件下,反应的酯化率可达89.5%,反应选择性也很好。Dawson型锌钨酸配合物催化苯乙烯氧化制苯甲醛具有良好的催化活性,反应时间短,收率较高,无废酸排放,工艺流程简单,可降低生产成本。因此,采用新型镍取代Dawson型锌钨酸配合物做为催化剂氧化苯乙烯制苯乙醛,反应操作简单、反应条件温和、利用环境友好的氧化剂无污染,在苯甲醛合成工业方面具有良好应用前景。
[1]张复兴.正交试验设计法评价ZnO2/SO42-催化合成水杨酸甲酯的最佳反应条件[J].衡阳师专学报,1995(1):50-54.
[2]吕宝兰,施少敏,杨水金等.活性炭负载磷钨酸催化合成丁醛1,2-丙二醇缩醛的正交试验分析[J].稀有金属,2005(2):191-193.
[3]李家其,尹笃林,徐琼等.Dawson型磷钨杂多盐催化氧化苯乙烯制苯甲醛[J].化工进展,2008(7):1096-1099.
[4]朱宪,王彬,张彰等.苯甲醛清洁生产工艺技术研究进展[J].化工进展,2005(2):109-116.
[5]TOURNE C M,TOURNE G F,ZONNEVIJLLE F,ZONNEVIJLLE F.[J].Dalton Trans,1991,143-155.
[6]唐晶,秦华.一种新型镍取代Dawson型锌钨酸配合物的合成及对苯乙烯氧化制苯甲醛的催化性能研究[J].分子科学学报,2012(6):483-489.
[7]胡传荣,李云艳编.试验设计与数据处理[M].北京:化学工业出版社,2002:62-100.
[8]陈媛,尹笃林,钟文周等.五氧化二钒催化环己烯烯丙位氧化[J].绥化学院学报,2006(11):983-986.

