基于空壳钯和纳米金修饰的过氧化氢无酶传感器的研究
甘思文,齐骏飞,徐清浩,黄杉生
(上海师范大学生命与环境科学学院,上海 200234)
基于空壳钯和纳米金修饰的过氧化氢无酶传感器的研究
甘思文,齐骏飞,徐清浩,黄杉生*
(上海师范大学生命与环境科学学院,上海 200234)
制备并表征了空壳钯纳米粒子,将空壳钯纳米粒子和金纳米粒子修饰在玻碳电极(GC)表面,构建了新型的过氧化氢无酶传感器.通过循环伏安等电化学方法研究了修饰电极的电化学特性,结果表明:Pd/AuNPs/GC对过氧化氢(H2O2)的电极反应具有催化作用,空壳钯和纳米金在催化过氧化氢还原过程中表现出了良好的协同作用.过氧化氢的浓度在2~216 μmol/L(R=0.9993)范围内,与修饰电极的电流之间呈现出良好的线性关系,检测限为0.2 μmol/L(S/N=3).该传感器具有较好的稳定性、重现性、抗干扰性.
空壳钯;协同作用;修饰电极;过氧化氢
过氧化氢作为许多酶反应的中间产物[1],在许多领域中起着非常重要的作用,如:化学、生物、临床控制、环境保护等.因此,能够快速而又准确地检测过氧化氢的方法引起人们的广泛关注.目前,用于检测过氧化氢的分析方法很多,主要包括:滴定分析法、光谱分析法[2]、荧光分析法[3]以及电化学传感器[4]等方法.其中,电化学检测因为其操作简单、高灵敏度和选择性好等优点被广泛应用于检测过氧化氢.Dong[5]通过金纳米粒子自组装在三维的网状基底上制备了辣根过氧化物酶传感器;Wang等[6]制备了一种基于辣根过氧化物酶固定在金胶上修饰的ITO电极用于过氧化氢的检测.然而,酶电极存在一些缺点,例如:酶只能在一定适宜的条件下才能够有效的催化底物,当温度、酸碱性等条件发生变化时,酶很有可能失去催化活性.研究制备简单的无酶电化学传感器用于检测过氧化氢无疑具有重要意义.
金属纳米粒子,特别是新型的金属纳米粒子因为比表面积大[7]、电子的快速传递[8]和良好的催化性能[9]被广泛用于传感器的制备.迄今,已有文献报道以金纳米线[10]、多孔纳米金粒子[11]、金纳米椎体[12]、金纳米管[13]和金纳米粒子[14]等作为制备过氧化氢无酶传感器的底物.本文作者研究了一种基于空壳钯和纳米金修饰的过氧化氢无酶传感器,合成了空壳钯纳米粒子并且通过TEM进行了表征,采用循环伏安法和计时电流法对修饰电极的性能进行了考察和表征.空壳钯和金纳米粒子在催化过氧化氢的过程中表现出了良好的协同作用.该传感器制备简单且表现出了良好稳定性、重现性和选择性.
1 实验部分
1.1 仪器和试剂
电化学工作站(CHI760C,上海辰华仪器公司),透射电子显微镜(JEM- 2010,日本).实验中采用三电极体系,工作电极为修饰后的玻碳电极,参比电极为饱和甘汞电极(SCE),对电极为铂电极.
氯化钯(PdCl2)和季磷盐(Bu4PBr)购于百灵威公司,壳聚糖(Chit)、氯金酸(HAuCl4·4H2O)和硼氢化钠(NaBH4)购于上海试剂有限公司,其余试剂购于国药集团.磷酸缓冲溶液(PBS)的浓度为0.1 mol/L、pH为7.2.所有的化学试剂均为分析纯,实验用水均为超纯水.
1.2 修饰电极的制备
空壳钯按文献[15]所述方法制备.直径为3 mm的玻碳电极依次用1.0、0.3和0.05μm的氧化铝粉末抛光,然后依次用1∶1的硝酸溶液和超纯水超声洗净,在1 mmol/L的铁氰化钾溶液中进行循环伏安扫描,至氧化还原峰峰间距约小于100 mV.电极经水淋洗后用氮气吹干备用.在室温条件下将干净的裸玻碳电极置于镀金液(1 mmol/L HAuCl4·4H2O和0.2 mol/L Na2SO4)中,控制电压恒定为-0.2 V,电沉积时间为300 s.电沉积结束后,用超纯水清洗电极表面并置于干燥器中室温晾干备用,此电极标记为AuNPs/GC.取1 mg空壳钯纳米粒子分散于1 mL 0.5%的壳聚糖溶液中,混合液经超声1 h处理,取6μL此混合液滴涂到修饰电极(AuNPs/GC)表面,放入干燥器中室温晾干,得到修饰电极(Pd/AuNPs/GC).
2 结果与讨论
2.1 空壳钯的形貌表征通过透射电镜(TEM)表征了空壳钯纳米粒子的形貌(图1).由图1中可以观察到,实验所制备的纳米粒子是空壳结构,空壳钯纳米粒子的直径在50~100 nm之间且分散程度良好.
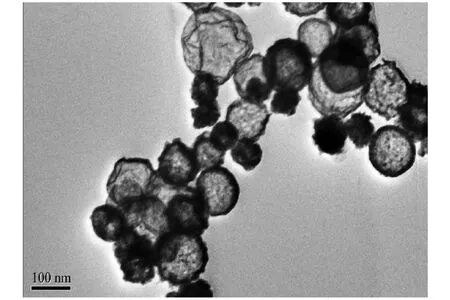
图1 空壳钯纳米粒子的TEM图
2.2 修饰电极的电化学特性图2为不同修饰层的电极在10 mmol/L K3[Fe(CN)6]/K4[Fe(CN)6](1∶ 1,含0.1 mol/L的KCl)中的循环伏安曲线.由图2可以观察到,裸GC的峰电流约为104μA;当电极修饰了金纳米粒子后,峰电流增加到187μA,说明作为一个微电子传递中心的纳米金可以有效的增强电极传递电子的能力.当空壳钯修饰到电极(AuNPs/GC)上后,峰电流增大至220μA,说明空壳钯也有利于电子的传递.峰电流的变化证明了金纳米粒子和空壳钯成功的修饰了电极上.电极的有效表面积可根据如下公式计算:其中,Ip是峰电流的数值,A是工作电极的有效表面积(cm2),n是在反应过程中传递电子数,D是扩散系数{(6.70±0.02)×10-6cm2·s-1},c是活性探针的浓度,v是扫速.由图2结果显示Pd/AuNPs/GC的有效表面积约为裸GC的1.6倍.通常,电极的有效表面积越大,表示有越多的活性物质覆盖在电极表面,传感器的灵敏度更高.

图2 不同修饰层电极在中的循环伏安图

2.3 修饰电极对过氧化氢的还原表征
实验考察了裸GC(a),AuNPs/GC(b),Pd/GC(c)和Pd/AuNPs/GC(d)在0.1 mol/L PBS(pH=7.2)中是否含有H2O2时的循环伏安特性(图3).当底液中不含H2O2时,在裸GC和AuNPs/GC上只能观察到背景电流,而在Pd/GC和Pd/AuNPs/GC上观察到1对氧化还原峰,峰电位分别是-0.018 V和-0.319 V.因为在底液中不存在其他具有氧化还原特性的物质,所以这一对氧化还原峰归因于空壳钯在电极上发生的氧化还原反应.当H2O2加入到底液中后,可以看到在AuNPs/GC,Pd/GC和Pd/AuNPs/GC上出现了明显的响应电流(图3曲线b和c),即金纳米粒子和空壳钯均可以对H2O2产生明显的催化作用.相比AuNPs/GC和Pd/GC,Pd/AuNPs/GC对H2O2的催化电流明显的增大2~3倍,且能够在更正的电位下产生催化作用.这一现象是归功于空壳钯纳米粒子和金纳米粒子在催化H2O2的电极反应过程中能够产生良好的协同作用.且随着H2O2浓度的不断增大,产生的还原电流随之增大,峰电位约为-0.3 V,响应电流和浓度呈现良好的线性关系(图4).
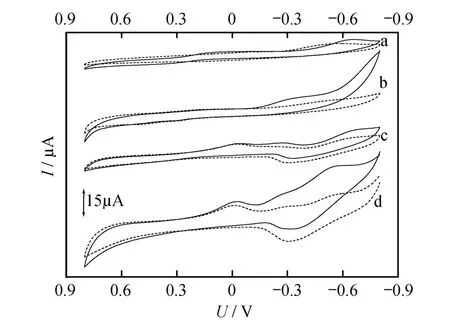
图3 H2O2在不同修饰电极上反应的循环伏安图
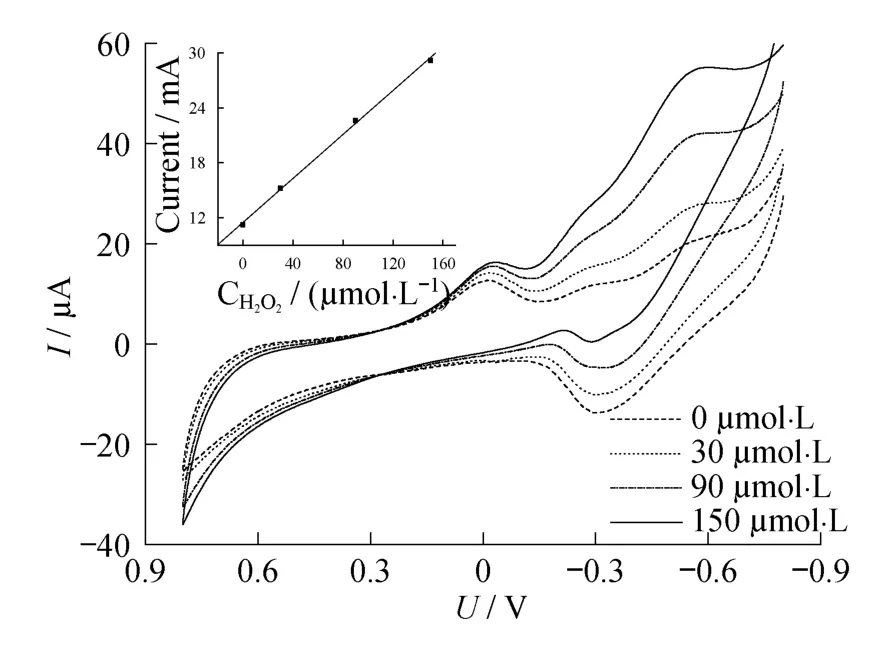
图4 H2O2在Pd/AuNPs/GC上的响应
2.4 实验条件的优化
实验探讨了金纳米粒子电沉积时间对响应电流的影响.电沉积时间在0 s~300 s之间时,响应电流随着电沉积时间的增加而增大,在电沉积时间为300 s时响应电流达到最大值,当电沉积时间超过300 s时,响应电流随着电沉积时间的增加反而减小.出现这一实验现象的原因可能是因为开始时随着电沉积时间的增加,电极表面的活性位点会不断增多,响应电流随之增大;但是,当电沉积时间过长时,则会形成较大形貌的金纳米粒子,从而导致活性位点的减小,所以响应电流也会随之减小,为此,实验选择300 s作为金纳米粒子的电沉积时间.工作电位也是影响传感器响应电流大小的一个重要因素,在-0.2~-0.6 V之间,修饰电极均可以对过氧化氢产生催化还原作用.在-0.3 V时,响应电流和过氧化氢的浓度之间呈现良好的线性相关性.当电位低于-0.3 V时,响应电流较小;当电位高于-0.3 V时,响应电流和过氧化氢的浓度之间的线性关系降低,且在较高的电位下会有较多的物质对测定产生干扰.综上所述,实验中选择-0.3 V作为最优的工作电位.
2.5 修饰电极Pd/AuNPs/GC对过氧化氢的计时电流响应
图5A为在0.1 mol·L-1PBS(pH=7.2)底液中连续加入H2O2时,Pd/AuNPs/GC的计时电流响应图,工作电位是-0.3 V.从图5可以看到,当H2O2加入到底液后,电极在不到2 s的时间内响应电流达到最大值.修饰电极的快速响应归功于空壳钯的空壳结构能够充分与过氧化氢接触.图5内插图为相应的线性校准曲线,在H2O2浓度在2~216μmol/L范围内,响应电流和H2O2浓度之间呈良好的线性关系.线性相关方程是:I=6.83+0.144c,线性相关系数为0. 9993,检测限是0.2μmol/L(3倍信噪比).结果显示,该传感器的性能良好,具备较低的检测限和较宽的线性范围.
2.6 修饰电极的抗干扰性,稳定性和重现性
实验考察了该修饰电极测定H2O2时对常见电活性的物质的抗干扰性.固定过氧化氢的浓度为2μmol/L,采用计时电流响应的方法,分别向底液(0.1 mol/L PBS,pH=7.2)中加入1 mmol/L的尿酸、抗坏血酸、葡萄糖和乙醇,测定其电流响应(图6).从图6可见,这些物质基本不产生干扰,说明传感器的选择性良好.
在含100μmol/L H2O2的10 mL 0.1 mol/L PBS(pH=7.2)的溶液中,连续测定7次,得到相对标准偏差(RSD)为6.4%;用3支不同的修饰电极分别检测相同浓度的H2O2,每支电极测3次,相对标准偏差(RSD)为4.4%,说明该传感器有较好的重现性.当该传感器不用时,置于4℃的PBS(pH=7.2)溶液中保存.1周后,该传感器响应电流为初始的94.9%,1个月后响应电流为原来的91.1%,说明此电极具有良好的稳定性.

图5 H2O2在Pd/AuNPs/GC上的计时电流响应图
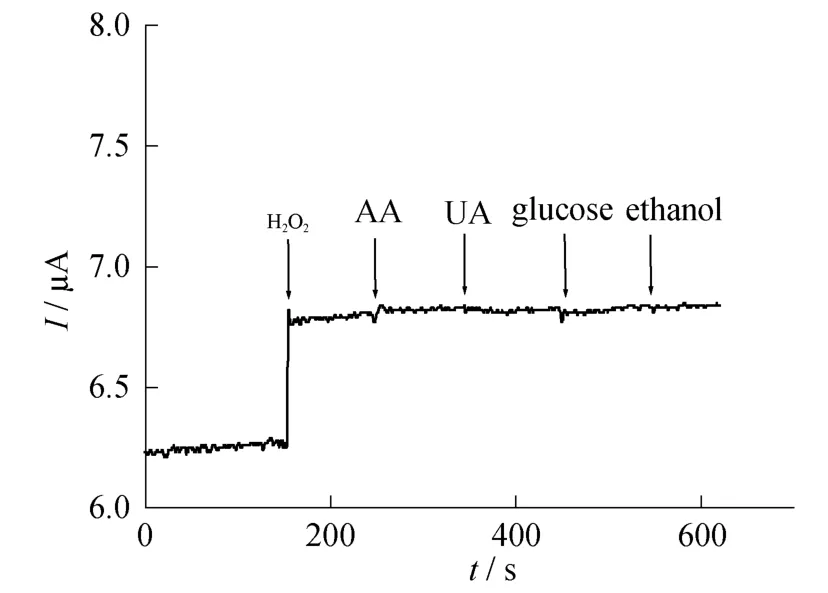
图6 修饰电极的抗干扰性
2.7 实际样品及回收率的测定
取市售的医用双氧水作为实际样品,首先对其进行稀释,测定其过氧化氢含量.然后取3份医用双氧水稀释液,分别向3份实际样品中加入100μmol/L过氧化氢标准溶液,进行回收率的测定.结果列于表 1,回收率为96%~102.6%.说明该过氧化氢无酶传感器有一定的实际应用价值.

表1 样品的检测(n=3)
3 结 论
基于空壳钯和纳米金修饰的过氧化氢无酶传感器,Pd/AuNPs/GC,修饰方法简单,响应速度快.该传感器对H2O2响应具备较宽的线性范围,较低的检测限和较好的选择性,具有实际应用价值.
[1] HOU M,ZHAIY M,DONG S J.Electrochemical sensing and biosensing platform based on chemically reduced graphene oxide[J].Anal Chem, 2009,81(14):5603-5613.
[2] MATSUBARA C,KAWAMOTO N,TAKAMURA K.Oxo[ 5, 10, 15,20-tetra(4-pyridyl)porphyrinato]titanium(IV):an ultra-high sensitivity spectrophotometric reagent for hydrogen peroxide[J].Analyst, 1992,117(11):1781-1784.
[3] HANAOKA S,LIN JM,YAMADA M.Chemiluminescent flow sensor for H2O2based on the decomposition of H2O2catalyzed by cobalt(II)-ethanolamine complex immobilized on resin[J].Anal Chim Acta, 2001,426(1):57-64.
[4] LI J,TAN SN,GE H L.Silica sol-gel immobilized amperometric biosensor for hydrogen peroxide[J].Anal Chim Acta, 1996,335(1):137-145.
[5] JIA JB,WANG B Q,WU A G,et al.A Method to Construct a Third-Generation Horseradish Peroxidase Biosensor:Self -Assembling Gold Nanoparticles to Three-Dimensional Sol-Gel Network[J].Anal Chem, 2002,74(9):2217-2223.
[6] WANG L,WANG E K.A novel hydrogen peroxide sensor based on horseradish peroxidase immobilized on colloidal Au modified ITO electrode[J].Electrochemistry Communications, 2004,6(2):225-229.
[7] DANIELM C,ASTRUC D.Gold nanoparticles:assembly,supramolecular chemistry,quantum-sized related properties,and applications toward biology,catalysis and nanotechnology[J].Chem Rev, 2004,104(1):293-346.
[8] NARAYANAN R,El-SAYEDM A.Raman studies on the interaction of the reactantswith the platinum nanoparticles surface during the nanocatalyzed electron transfer reaction[J].JPhys Chem B, 2006,109(39):18460-18464.
[9] MAHMOUND M A,El-SAYED M A.Reaction of platinum nanocatalyst with the ferricyanide reactant to produce Prussian blue analogue complexes[J].JPhys Chem C, 2007,111(46):17180-17183.
[10] GUO S,WEN D,DONG S,etal.Gold nanowire assembling architecture for H2O2electrochemical sensor[J].Talanta,2009(4),77:1510-1717.
[11] KAFIA K M,AHMADALINEZHAD A,WANG J,et al.Direct growth of nanoporous Au and its application in electrochemical biosensing[J].Biosensors and Bioelectronics, 2010,25(11):2458-2463.
[12] XIA P,LIU H,TIAN Y.Cathodic detection of H2O2based on nanopyramidal gold surface with enhanced electron transfer ofmyoglobin[J].Biosensors and Bioelectronics, 2009,24(8):2470-2474.
[13] DELVAUX M,WALCARIUSA,CHAMPAGNE SD.Electrocatalytic H2O2amperometric detection using gold nanotube electrode ensembles[J].Anal Chim Acta, 2004,525(2):221-230.
[14] MADURAIVEERAN G,RAMARAJR.Gold nanoparticles embedded in silica sol-gelmatrix as an amperometric sensor for hydrogen peroxide[J].JElectroanal Chem, 2007,608(1):52-58.
[15] LIH,LIU J,XIE SH,et al.Visicle-assisted assembly ofmesoporous Ce-doped Pd nanosphereswith a hollow chamber and enhanced catalytic efficiency[J].Adv Funct Mater, 2008,18(20):3235-3241.
Study of nonenzymatic H2O2sensor based on hollow palladium and Gold nanoparticlesmodified electrode
GAN Siwen,QIJunfei,XU Qinghao,HUANG shansheng*
(College of Life and Environment Sciences,Shanghai Normal University,Shanghai 200234,China)
A novel nonenzymatic amperometric sensor based on hollow palladium and gold nanoparticles for detection of hydrogen peroxide(H2O2)was developed.Themodified electrodewas prepared by electrodepositing gold nanoparticles(AuNPs)and then modifying the surface of the Au-glassy carbon electrode with hollow palladium.The electrochemical characteristics of the mochifed electrode(Pd/AuNPs/GC)were investigated by cyclic voltammetry.The results showed that Pd/AuNPs/GC displayed high electrocatalytic activity towards the reduction of H2O2due to the good synergetic effectof hollow Pd and AuNPs on the reaction of H2O2.The responding currents of the Pd/AuNPs/GC increased linearly with the concentration of H2O2in a wide range of 2-216μmol/L(R=0.9993)with a detection limit down to 0.2μmol/L(S/N=3).The sensor also exhibited good anti-interference ability to electroactivemolecules,including uric acid,ascorbic acid,glucose,and ethanol.
hollow palladium;synergetic effect;chemicallymodified electrode;hydrogen peroxide
O 657.1
A
1000-5137(2013)02-0161-05
(责任编辑:郁 慧)
2013-01-29
国家自然科学基金(21275100)
甘思文(1987-),女,上海师范大学生命与环境科学学院硕士研究生;黄杉生(1952-),男,上海师范大学生命与环境科学学院教授.
*通信作者

