SO催化剂在甲醇制烯烃的应用研究
赖华龙
(三明职业技术学院,福建三明365000)
赖华龙
(三明职业技术学院,福建三明365000)
采用溶胶-凝胶法制备SO催化剂的基体,用不同浓度的硫酸对催化剂基体进行浸渍,考察催化剂性能,选出制备催化剂的硫酸浓度。考察反应温度、甲醇流量对催化剂性能的影响;探讨了催化剂失活的原因。实验结果表明,催化剂S10活性最好;甲醇制烯烃的反应温度为410~430℃,具有98.8%的甲醇转化率和90.65%的乙烯选择性;反应时甲醇的流量为0.05mol·s-1。
甲醇制烯烃;催化剂;SO
甲醇制烯烃的工艺过程主要分为反应系统、分离净化系统和催化剂再生系统。这些工艺过程的原理和机理均较成熟,目前国际上的研究重点都在催化剂的筛选和制备技术方面[1],以及反应机理的研究,而国内主要研究重点除了催化剂的外,还主要研究了反应工艺和反应器的开发[2]。几十年来,许多不同种类的催化剂都被尝试应用于甲醇制烯烃的反应,甲醇制低碳烯烃催化剂包括菱沸石、毛沸石、SAPO-34、ZSM-5、丝光沸石等。其中ZSM-5分子筛是研究最多、最为成熟的催化剂之一[3-4]。虽用于甲醇制低碳烯烃仍然存在缺点,但是已经在甲醇制汽油获得了成功,实现了工业化。
固体超强酸作为新型催化材料,具有很高的酸强度,是理想的酸性催化剂,可作为有机物的分解、缩聚、异构化、烷基化和酯化等反应的催化剂,可使反应在较低温度下甚至室温下顺利进行,因而在石化和有机合成中受到重视,研究和应用进展迅速,成为催化领域的研究热点。在酯化反应中用固体酸催化剂取代传统硫酸催化剂的研究已很广泛,涉及的固体酸主要包括SO型固体超强酸、沸石分子筛、层柱粘土、离子交换树脂及杂多酸等。SO型固体超强酸具有很多优点,其制备方法通常为沉淀浸渍法[5]。为了提高其性能,改进方法有溶胶-凝胶法[6-8]等,该法得到的SO比表面积大(比表面积可达188 m2·g-1),活性比沉淀法制得的催化剂高50%以上。
本文采用溶胶-凝胶法制备SO42-/TiO2固体超强酸催化剂的基体,用不同浓度的硫酸对催化剂基体进行浸渍,考察催化剂性能,选出制备催化剂的硫酸浓度。以甲醇制烯烃反应为探针,考察反应温度、甲醇流量对优选催化剂性能的影响;探讨了催化剂失活的原因。
1 实验试剂
实验试剂见表1。

表1 实验试剂
2 SO42-/TiO2催化剂的制备
(1)采用溶胶-凝胶法[6-8]制备催化剂的TiO2基体以钛酸四正丁酯Ti(OC4H9)4为原料,无水乙醇C2H5OH为溶剂,加入一定量硝酸调节pH值为3.5。反应物的摩尔比为Ti(OC4H9)4∶C2H5OH∶H2O= 0.1∶3∶0.3。再用SC-CO2萃取法对醇凝胶进行干燥制备成粒子,充分研细,得催化剂的TiO2基体,记为S00。
(2)用浓硫酸(98%wt)分别配置0.5、1.0、1.5及2.0 mol·L-14种硫酸溶液250 mL,准备待用。称取3 g催化剂基体S00 4份,分别置于铂坩埚中,并分别加入浓度为0.5、1.0、1.5及2.0 mol·L-1的H2SO4溶液20 mL,并不断搅拌使催化剂基体充分溶解,待浸渍16 h后,放入55℃烘箱中干燥5 h,同时边搅拌,待绝大部分水分蒸发后,放入450℃马弗炉中焙烧4 h,烘干后,将固体粉碎,研细,分别得SO42-/TiO2固体超强酸催化剂[9-11]S05、S10、S15及S20。
3 SO42-/TiO2催化剂的活性评价
催化剂的活性评价在一套自制的连续固定床反应装置内进行,详见图1。
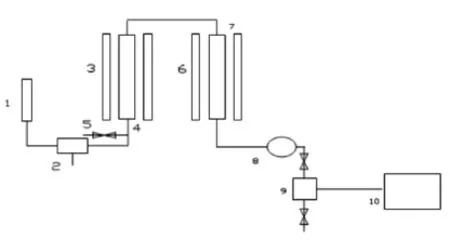
图1 催化剂活性评价实验装置图
甲醇溶液经微型泵打到气化室,进行甲醇气化,气化室由电炉加热,热电偶控温;甲醇气化后,进入固定床反应器,反应器为管式反应器,直径8 mm,长200 mm,反应器的两端装有填料,中间部分为催化剂,上部为拉西环填料,下部为石英沙填料,石英沙有过滤气体的作用,使结炭无法进入冷凝室,影响分析,反应器由电炉加热,热电偶控温;反应产物在160℃保温带保温下进入气相色谱在线分析。
催化剂活性评价实验所用的实验设备见表2。

表2 活性评价实验设备
通过比较催化剂S05、S10、S15及S20在温度400、410及420℃下所得的乙烯产率,选出性能最好的催化剂,结果如图2所示。硫酸浸渍后的4种催化剂都具有良好的催化活性,在反应温度为400℃时,甲醇转化率均能达到90%以上,且乙烯收率均能达到70%以上。这几种催化剂中,用1.0 mol·L-1硫酸浸渍液制备的催化剂(S10)催化性能最好,此时乙烯收率可达到85%以上。
从图2可知,催化剂的催化性能随硫酸浸渍浓度的变化而变化。催化剂在硫酸浓度低于1.0 mol·L-1时,乙烯产率随浓度的升高而升高,硫酸浓度大于1.0 mol·L-1时,乙烯产率随浓度的升高而降低。这主要因为硫是催化剂活性结构的组分之一,浸渍液浓度偏低时,氧化物表面结合的SO太少,酸性弱,酸活性中心数目少,催化活性低;H2SO4浸渍浓度过高时,易导致生成硫酸盐,得不到超强酸,影响催化剂的活性和催化剂的产率。因此,选择H2SO4浸渍浓度为1.0 mol·L-1作为SO型催化剂的制备条件,所得的优选催化剂记为S10。
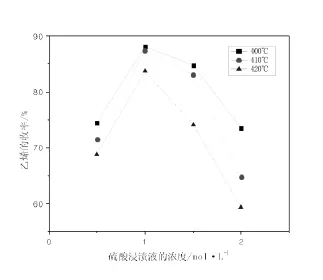
图2 硫酸浸渍液浓度与乙烯收率的关系
4 工艺条件对反应产率的影响
4.1 反应温度影响
4.1.1 甲醇转化率
以甲醇制烯烃反应考察不同反应温度对S10性能的影响。实验中可发现,催化剂在不同的反应温度下,甲醇转化率相差甚大,结果可见图3。
从图3可知,温度低于180℃,甲醇几乎不转化;温度为180℃时,甲醇开始转化,而后转化速率随温度升高而急剧增大;温度升高至260℃时,甲醇几乎完全转化。
4.1.2 产物分布
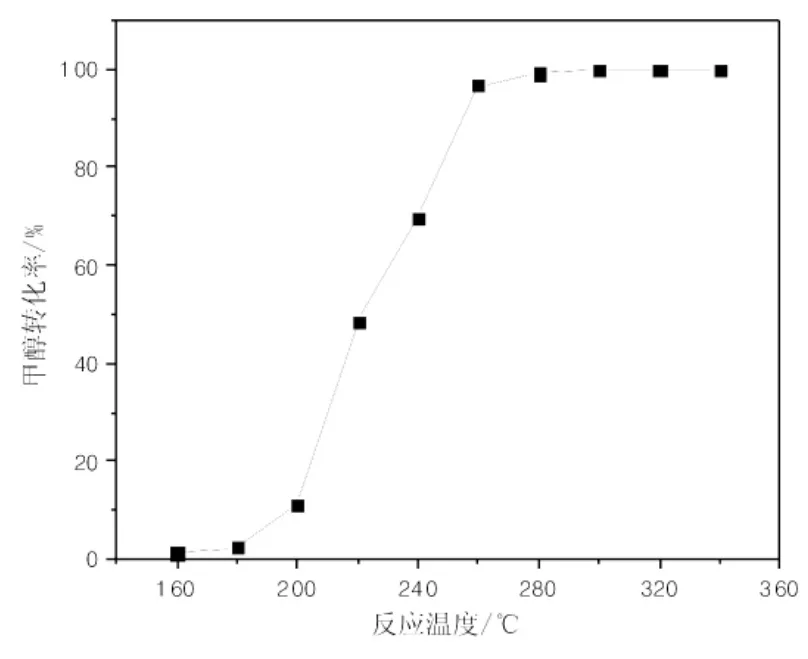
图3 反应温度与甲醇转化率的关系
同样以S10为甲醇制烯烃反应的催化剂,固定其他实验条件,改变反应温度,考察不同反应温度对产物分布的影响,其结果可见图4。从图4可知,反应温度低于330℃时,几乎没有乙烯产生,这是由于甲醇在较低反应温度下首先转化为二甲醚,而非直接转化为乙烯,这与甲醇制烯烃的反应机理有关;当反应温度高于330℃时,二甲醚开始转化为乙烯,且乙烯收率随反应温度的升高而增大;当反应温度为430℃时,乙烯收率可达最大90.65%;而后,乙烯收率随反应温度的升高反而降低。由此可见,在反应温度为430℃以下时,动力学条件是整个反应过程的控制因素,升高温度使反应速率增加,乙烯的收率相应提高;当反应温度高于430℃时,由于该反应为放热反应,热力学因素成为影响转化率的控制因素;同时升高温度,也加快了甲醇的炭化速率,乙烯的选择性就下降。故该反应的推荐反应温度为410~430℃。
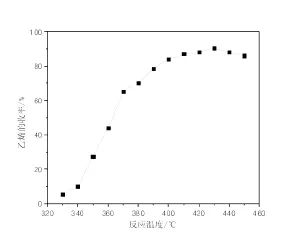
图4 反应温度与乙烯收率的关系
实验中发现,当反应温度达460℃时,乙烯收率极低,由此可推测,此时的催化剂几乎失活。目前知道催化剂失活的原因有多个方面[12-14]:(1)在催化合成反应中,系统内的水蒸气与催化剂表面的负载物SO接触,使其表面上的SO流失,导致催化剂表面的酸中心数减少,造成酸强度减弱,催化活性下降;(2)在反应过程中,甲醇分子等亲核基团或分子会进攻超强酸中心,与活性中心结合后分解从而导致催化剂表面硫物种的流失,同样降低了催化剂的催化活性;(3)在反应过程中,因反应温度的波动而脱水,或反应过程中吸水使B酸量和L酸量比例失调,使得B酸和L酸的协同效应下降;(4)在反应过程中,由于反应温度过高,催化剂直接被氧化而失活。
实验结束后,发现从反应装置中倒出的催化剂已成焦炭,说明当反应温度为460℃时,甲醇炭化,沉积在催化剂表面,使活性中心被覆盖,使得甲醇不易与活性中心接触,从而降低反应速率,甚至完全失活,故实验时需严格控制好反应温度,反应温度不能超过460℃。
4.2 反应物流量的影响
4.2.1 甲醇转化率
以S10为催化剂,在常压下,考察推荐反应温度430℃下反应物甲醇流量对甲醇转化率的影响,其结果如图5所示。
从图5中可看出,甲醇流量的大小对甲醇转化率影响不大,即在430℃高温下,甲醇几乎完全转化,甲醇转化率达98.8%以上。
4.2.2 产物分布
以S10为催化剂,在常压下,考察推荐反应温度430℃下乙烯收率随甲醇流量的变化而变化,其结果如图6所示。
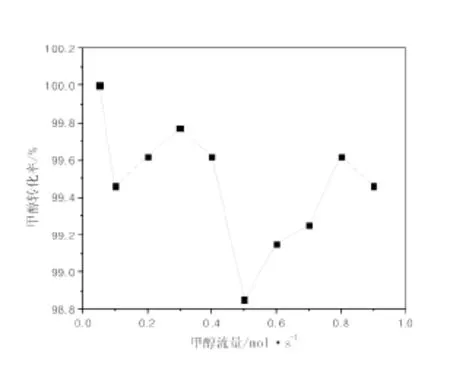
图5 甲醇流量与甲醇转化率的关系
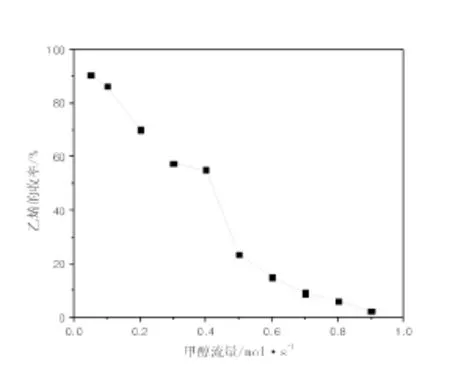
图6 甲醇流量与乙烯收率的关系
从图6可知,乙烯收率随着甲醇流量的增加而减少,在0.05~0.40 mol·s-1范围内,乙烯收率下降较缓慢;在0.40~0.50 mol·s-1时,其下降有加快的趋势;而在大于0.50 mol·s-1时,其下降趋势又变缓。因此,该反应推荐甲醇流量为0.05 mol·s-1,此时乙烯收率达90%以上。
5 结论
综上所述,实验表明:
⑵对于甲醇制烯烃反应,采用1.0 mol·L-1硫酸浸渍制备的催化剂时,410~430℃为推荐反应温度;
⑶上述反应超过460℃时,催化剂易失活。其主要原因是甲醇炭化,沉积在催化剂表面,从而使催化剂失活;
⑷430℃条件下的甲醇制烯烃反应,其推荐甲醇流量为0.05 mol·s-1。
[1]齐胜远.天然气制烯烃及GSMTO工艺进展[J].天然气化工,1999,24:44-46.
[2]齐国祯,马涛,刘红星,等.甲醇制烯烃反应动力学[J].化工学报,2005,56(12):2326-2328.
[3]曾昭槐.择形催化[M].北京:中国石化出版社,1994.
[4]柯丽,冯静,张明森.甲醇转化制烯烃技术的新进展[J].石油化工,2006,35(3):205-211.
[5]蒋文伟.超强酸催化剂的研究进展[J].精细化工,1997,3(1):46-49.
[6]车如心,高宏,赵宏滨,等.溶胶-凝胶技术的发展历史及现状[J].云南大学学报,2005,8(6):2-6
[7]苏碧桃,孙丽萍,孙巧珍,等.纳米二氧化钛催化剂的制备及其光催化性能[J].兰州大学学报:自然科学版,2000,36(6):75-78.
[8]李福颖,牛玉,朱启荣,等.纳米TiO2的制备及UV/TiO2体系光催化性能研究[J].三明学院学报,2013,30(2):58-60.
[9]蒋平平,卢冠忠.固体超强酸催化剂改性研究进展[J].现代化工,2002,22(7):13-21.
[11]华卫琦,周力,吴肖群,等.SO固体超强酸及其制备技术[J].石油化工,1997,26(8):553-560.
[12]张黎,王琳,陈建民.S2O固体超强酸的研究[J].高等学校化学学报,2000,21(1):116-119.
[13]YAMAGUCHI T.Recent progress in solid superacid[J].Appl Catal,1990,61:1-25.
[14]TSUCOMU Y,TUO J,KOZOT.Structure of acid sites in sulfur-promoted iron oxide[J].Journal of Physical Chemistry,1986,90(14):3148-3152.
LAI Hua-long
(Sanming Vocational Technical College,Sanming 365000,China)
The catalyst of SOwas prepared by sol-gel method.The catalyst was soak aged with different concentrations of sulfuric acid,the activity of catalyst was discussed and the optimal catalyst was chosen.Then effects of the reaction temperature and methanol flow on the performance of the catalyst and the reason for the deactivation of the catalyst were studied.The experiment results show that the activity of catalyst S10 was the best,the MTO reaction temperature was 410~430℃with 98.8%methanol conversion and 90.65%selectivity of ethylene,the methanol flow rate was 0.05mol·s-1.
MTO,catalyst,SO
TQ426.94
A
1673-4343(2013)04-0073-05
2013-04-10
赖华龙,男,福建上杭人,讲师。研究方向:清洁能源。

