氨基甲烷到氨基戊烷加、减电子对HOMO、LUMO的影响
姚树文,张艺川
(1.河南科技学院,河南新乡 453003;2.河南师范大学化学化工学院,河南新乡 453000)
1932年,美国化学家Mulliken RS和德国化学家Hund F提出了一种新的共价键理论—分子轨道理论(molecularorbital theory).分子轨道理论作为化学键理论的一个重要组成部分,已经成为处理双原子分子及多原子分子结构的有效近似方法.价键理论利用原子轨道的重组杂化成键来处理化学问题,而分子轨道理论则认为分子中的电子在整个分子中运动.由于分子轨道理论注意了分子的整体性,因此相对于其他理论,其更能描述多原子分子的结构[1-4].1951年,福井谦一提出分子的前线轨道理论,即分子的化学反应活性主要由分子的最高已占分子轨道(HOMO)和最低未占分子轨道(LUMO)决定,分子进行化学反应时,只和前线分子轨道有关,并由此获得了1981年诺贝尔化学奖[5-7].从分子轨道理论提出以来,使用这种理论能够解释很多化学反应,使化学工作者能够更深刻地理解化学反应的发生以及能够更好地预测化学反应[8-9].
本文采用经典Hartree-Fock(HF)方法,研究了从氨基甲烷到氨基戊烷物种氨基取代烷烃中,加电子或者减电子的位置.
1 计算方法
采用HF方法在STO-3G基组条件下,对氨基甲烷到氨基戊烷进行单点能计算,并分析其轨道信息,然后分别对每种取代烷烃的正离子和负离子进行计算,并分析其HOMO和LUMO轨道系数的变化,从而推断加电子和减电子的位置.所有计算均在Gaussian 03程序包中进行.
2 结果与分析
2.1 氨基甲烷
氨基甲烷的分子构型如下
根据要求选出正确的数据制作图1.

图1 氨基甲烷加一个电子和减一个电子后各原子轨道能量的变化Fig.1 Energy changes of each atom obitalafteraddingorsubstactingon electron foraminoethane
以图1纵坐标为HOMO或LUMO轨道能级数值,横坐标为底数序号1~15号,它们分别对应的轨道如表1所示.

表1 氨基甲烷中每个轨道序号所对应的原子轨道Tab.1 Serialnumber of atom orbitals in aminomethane
由图1和表1可知,①在氨基甲烷的U与其加电子后的O所作的轨道曲线上,序号为2、8、9、12、13、14、15的轨道上有稍微的差别,但曲线走向基本一致,基本符合加电子加载在最低非占据轨道上;②在氨基甲烷的O与其减电子后的U所作的轨道曲线上,只是序号3、5、11对应的轨道上减电子后会有少许变化,但并没有影响曲线的基本走向,由此可知,同样符合减电子是减在最高占据轨道上.
2.2 氨基乙烷
氨基乙烷分子构型如下
根据要求选出正确的数据制作图2.
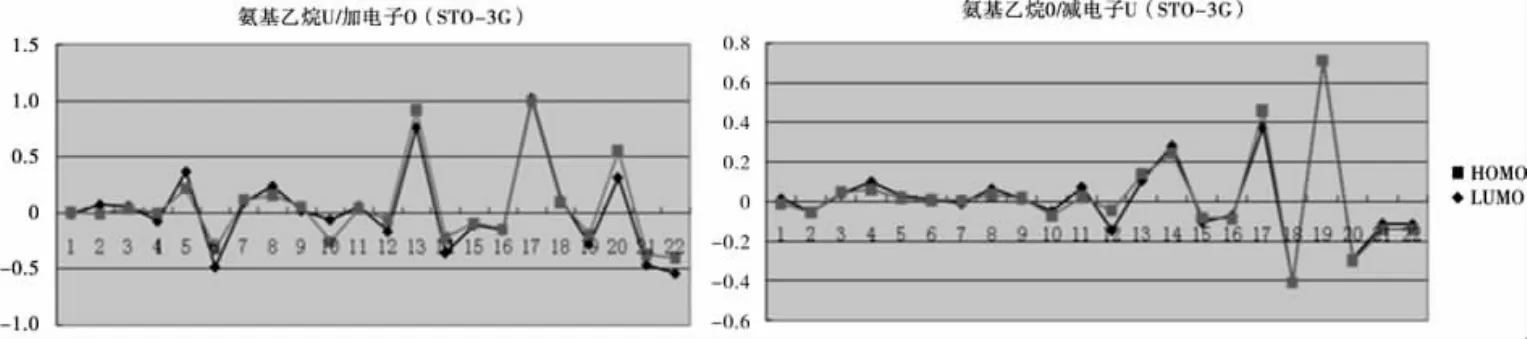
图2 氨基乙烷加一个电子和减一个电子后各原子轨道能量的变化Fig.2 Energy changes of each atom obitalafteraddingor substacting on electron foraminoethane
以图2纵坐标为HOMO或LUMO轨道能级数值,横坐标为底数序号1~22号,它们分别对应的轨道如表2所示.

表2 氨基乙烷中每个轨道序号所对应的原子轨道Tab.2 Serialnumber of atom orbitals in aminoethane
由图2和表2可知,①在氨基乙烷的U与其加电子后的O所作的轨道曲线上,序号为5、6、10、20、22的轨道上有稍微的差别,但曲线走向趋势基本一致,基本符合加电子加载在最低非占据轨道上;②在氨基乙烷的O与其减电子后的U所作的轨道曲线上,只是序号4、1、12、17对应的轨道上减电子后会有少许变化,但并没有影响曲线的基本走向,由此可知,同样符合减电子是减在最高占据轨道上.
2.3 氨基丙烷
氨基丙烷分子构型如下

根据要求选出正确的数据制作图3.

图3 氨基丙烷加一个电子和减一个电子后各原子轨道能量的变化Fig.3 Energy changes of each atom obitalafteradding orsubstactingoneelectron foraminopropane
以图3纵坐标为HOMO或LUMO轨道能级数值,横坐标为底数序号1~29号,它们分别对应的轨道如表3所示.

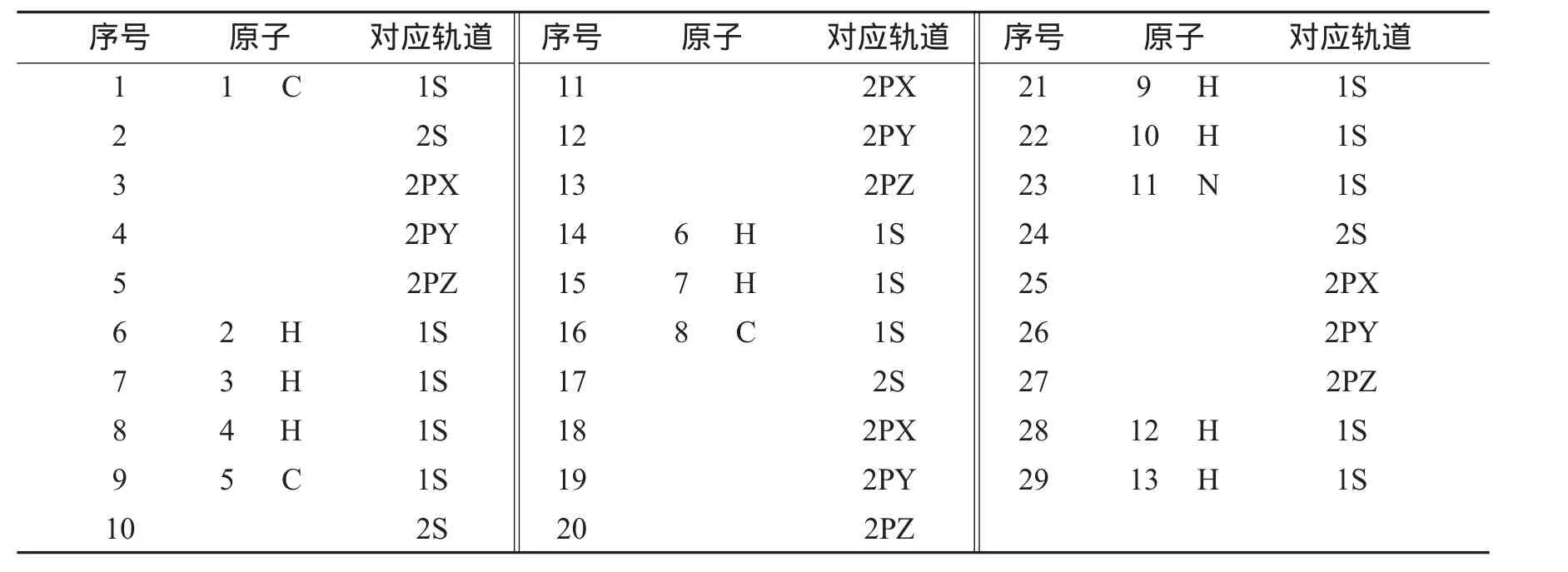
表3 氨基丙烷中每个轨道序号所对应的原子轨道Tab.3 Serialnumber of atom orbitals in aminopropane
由图3和表3可知,①在氨基丙烷的U与其加电子后的O所作的轨道曲线上,序号为10、12、17、18、25、26的轨道上有稍微的差别,但曲线走向趋势基本一致,基本符合加电子加载在最低非占据轨道上;②在氨基丙烷的O与其减电子后的U所作的轨道曲线上,只是序号11、18、24对应的轨道上减电子后会有少许变化,但并没有影响曲线的基本走向,由此可知,同样符合减电子是减在最高占据轨道上.
2.4 氨基丁烷
氨基丁烷分子构型如下
根据要求选出正确的数据制作图4.

图4 氨基丁烷加一个电子和减一个电子后各原子轨道能量的变化Fig.4 Energy changes of each atom obitalafteraddingor substacting one electron foraminobutane
以图4纵坐标为HOMO或LUMO轨道能级数值,横坐标为底数序号1~36号,它们分别对应的轨道如表4所示.

表4 氨基丁烷中每个轨道序号所对应的原子轨道Tab.4 Serialnumber of atom orbitals in aminobutane
由图4和表4可知,①在氨基丁烷的U与其加电子后的O所作的轨道曲线上,序号为5、8、12、24、25、33的轨道上有稍微的差别,但曲线走向趋势基本一致,基本符合加电子加载在最低非占据轨道上;②在氨基丁烷的O与其减电子后的U所作的轨道曲线上,只是序号13、20、26、27对应的轨道上减电子后会有少许变化,但并没有影响曲线的基本走向,由此可知,同样符合减电子是减在最高占据轨道上.
2.5 氨基戊烷
氨基戊烷分子构型如下

根据要求选出正确的数据制作图5
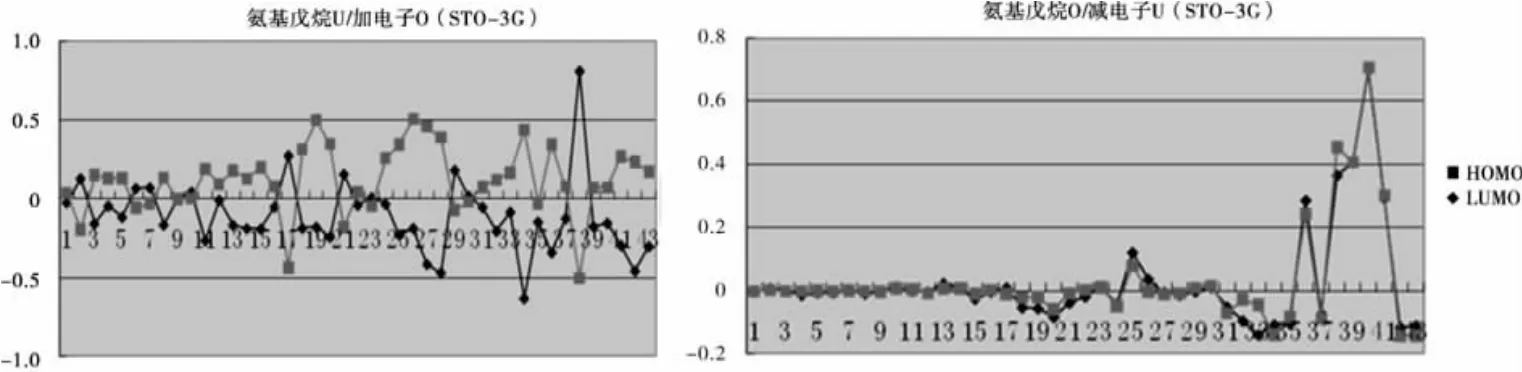
图5 氨基丁烷加一个电子和减一个电子后各原子轨道能量的变化Fig.5 Energy changes of each atom obitalafteradding orsubstactingoneelectron foraminopentane
以图5纵坐标为HOMO或LUMO轨道能级数值,横坐标为底数序号1~43号,他们分别对应的轨道如表5所示.

表5 氨基戊烷中每个轨道序号所对应的原子轨道Tab.5 Serialnumber of atom orbitals in aminopentane
由图5和表5可知,①氨基戊烷的U与其加电子后的O所作的轨道曲线走向趋势已经完全相反,但所谓的完全相反是正负号造成的,而电子密度与正负号无关,所以完全相反也是基本吻合的一种,因此同样符合加电子加载在最低非占据轨道上;②在氨基丁烷的O与其减电子后的U所作的轨道曲线上,只是序号32、33、36、38对应的轨道上减电子后会有少许变化,但并没有影响曲线的基本走向,由此可知,同样符合减电子是减在最高占据轨道上.
3 小结
本文分别对氨基甲烷到氨基戊烷等5种物质及它们加、减电子后的轨道能量进行了计算,并把原物质的U与加电子后的O、原物质的O与减电子后的U分别做曲线并比较,结合曲线与图表分析,对于各物质加电子能量计算,由其轨道分布得知加电子的轨道分布与物质本身的最低非占据轨道分布基本吻合,且减电子的轨道分布与物质其本身的最高占据轨道也同样吻合;结果表明各物质加电子是加载在最低非占据轨道上,减电子是减在最高占据轨道上.
综上所述,经过多次计算对比得出:该系列物质加电子是加载在最低非占据轨道上,减电子是减在最高占据轨道上.
[1]唐作华,万家义,毛治华.基础结构化学[M].成都:四川大学出版社,1996.
[2]徐光宪.物质结构[M].北京:高等教育出版社,1959:377.
[3]郭用猷.物质结构[M].北京:高等教育出版社,1985.
[4]杨金田.键级和化合价的分子轨道理论[J].湖州师范学院学报,1990(5):30-35.
[5]FukuiK,Yonezawa T,Shingu H J.Molecularorbital theory of reactivity in aromatic hydrocarbons[J].J.Chem.Phys.,1952,20:722.
[6]Kimura K,Katsumata S,Achiba Y,et al.Handbook of HeIPhotoelectron spectra of Fndamem~Organicmolecules[M].Tokyo:Japan Scientific Society,1981.
[7]Frisch M J,TrucksGW.Gaussian[M].Inc.,Pittsburgh PA,2003.
[8]李艳萍,刘翔宇,吉文欣,等.3,5-二碘水杨醛缩乙二胺席夫碱配合物的合成、理论研究及其与ct-DNA的实验研究[J].分子科学学报,2013,29(4):312-319.
[9]章日光,任军,凌丽霞,等.CuCl与SiO2-TiO2载体相互作用的密度泛函理论研究[J].化学学报,2010,68(9):851-857.

