含钴钠混合金属的一维链配合物的合成及其结构
王会生,潘志权
(武汉工程大学化工与制药学院 绿色化工过程教育部重点实验室,湖北 武汉 430074)/
0 引 言
自从2001年人们首次发现含有顺磁性离子的链状化合物具有单链磁体性质以来,对该领域的研究一直受到国内外科学家的重视,原因在于这类化合物在高密度信息存储设备、量子计算机及磁冰箱等方面存在潜在的应用[1-5].相比0维的单分子磁体化合物,一维的单链磁体化合物具有更高的能垒,这是由于单分子磁体的能垒除了与基态自旋值和负的磁各向异性有关外,还与链内重复单元间的磁交换导致的磁尺寸相关效应有关[6].为了合成更高能垒的单链磁体,人们使用不同的合成方法合成出许多含顺磁性离子的一维链化合物.
1 实验部分
1.1 试剂和仪器
本实验所用试剂均来源于试剂公司,为分析纯,没进一步提纯.C、N和H元素分析测试用的仪器为Perkin-Elmer 240C元素分析仪.IR红外光谱数据在VECTOR 22光谱仪上测定(KBr压片),测量范围为400~4 000 cm-1.
1.2 配合物的合成
取0.215 6 g(1.57 mmol)水杨醛肟、0.129 1 g(1.57 mmol)乙酸钠及0.048 4 g(0.74 mmol)叠氮钠并溶解在10 mL CH3OH中,然后与含有0.124 0 g(0.52 mmol)六水合氯化钴的5 mL CH3OH溶液混合,并继续搅拌5 min,溶液由紫色变成黑色,再搅拌30 min,过滤,滤液静置7 d后析出黑色块状晶体,过滤,并用无水乙醚洗涤3次,空气中干燥,依据Co的量产率约为70%.元素分析:按分子式C34H46Co2N7NaO14,计算值(%)C 44.50,H 5.05%,N 10.68;实验值(%)C 44.24,H 5.01,N 10.45.红外光谱IR(KBr,cm-1)3 278(m), 2086(s),1 640(m), 1 601(s), 1 552(m),1 446 (s),442(m),1 270(s),1 144(w),920(s),850(w),813(m),754 (s),734 (m),673(m),622(s),570(m),547(m),522(m).
1.3 配合物1·3CH3OH晶体结构的测定与解析
0.22 mm × 0.18 mm × 0.15 mm大小的单晶置于Bruker APEX CCD单晶衍射仪上,Mo/Kα辐射(0.071 073 nm)及φ-ω 扫描方式, 并用SMART 程序在室温下收集衍射数据,再用SAINT还原数据和SADABS程序进行经验吸收矫正[10].结构用直接法解出,对所有非氢原子采用全矩阵最小二乘法并基于F2精修,所有氢原子均为理论加氢并采用各向同性参数及跨式模型修正,且Uiso是母原子的1.2或1.5倍.需要指出的是,N3-上未配位的端基N7在晶胞内有一定范围的热扰动,所以如图1所示,其各向异性球显得比较大.配合物1·3CH3OH的晶体学数据和部分键长键角分别如表1和表2所示.
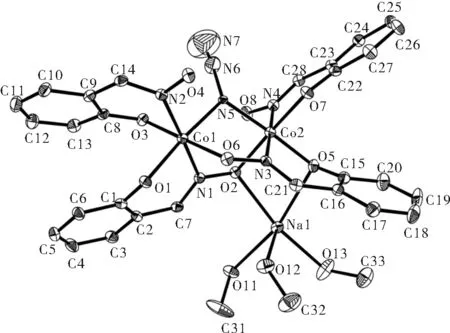
图1 一维链1·3 CH3OH的结构单元Fig.1 The structural unit of 1D chain 1·3 CH3OH
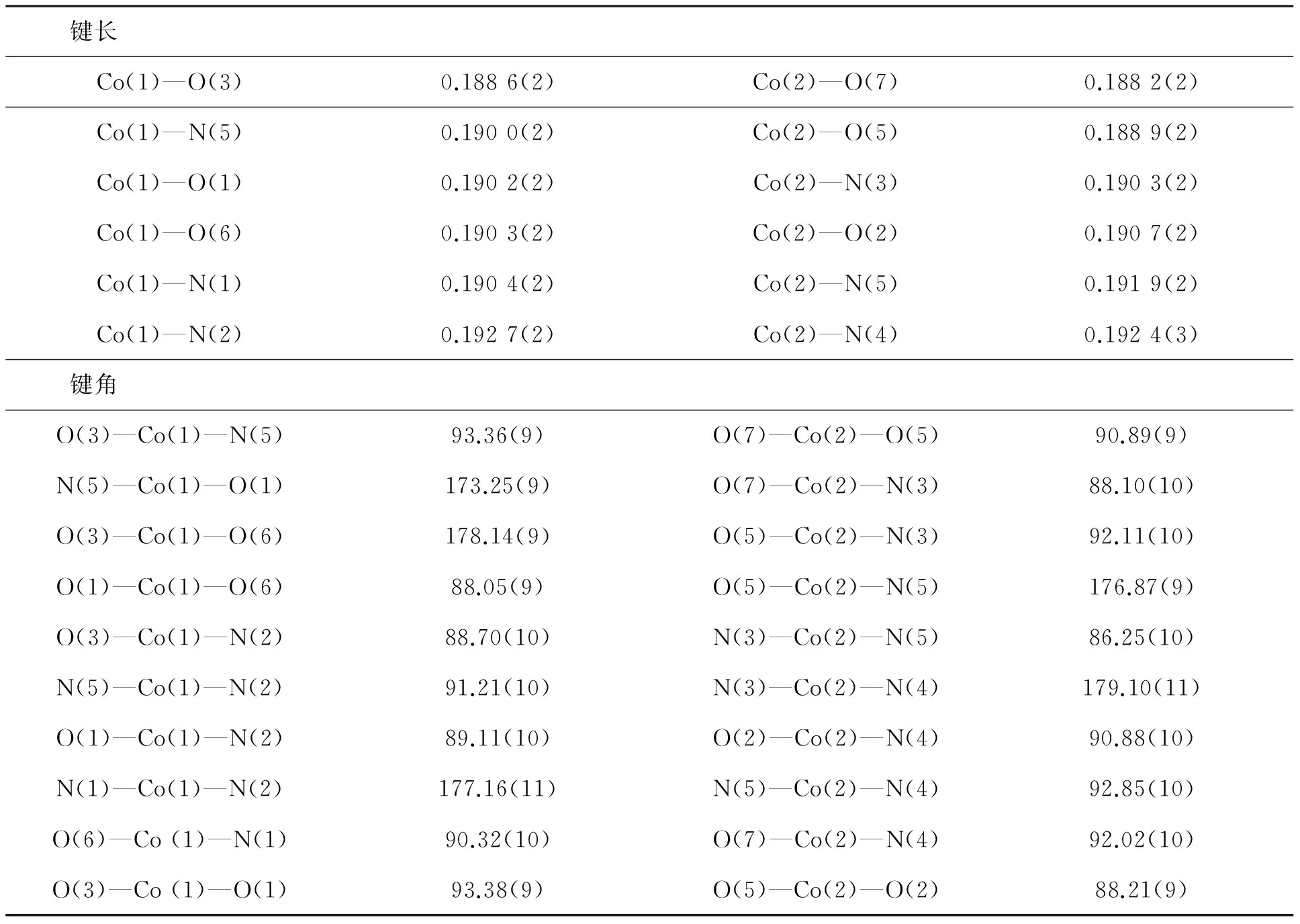
键长Co(1)—O(3)0.1886(2)Co(2)—O(7)0.1882(2)Co(1)—N(5)0.1900(2)Co(2)—O(5)0.1889(2)Co(1)—O(1)0.1902(2)Co(2)—N(3)0.1903(2)Co(1)—O(6)0.1903(2)Co(2)—O(2)0.1907(2)Co(1)—N(1)0.1904(2)Co(2)—N(5)0.1919(2)Co(1)—N(2)0.1927(2)Co(2)—N(4)0.1924(3)键角O(3)—Co(1)—N(5)93.36(9)O(7)—Co(2)—O(5)90.89(9)N(5)—Co(1)—O(1)173.25(9)O(7)—Co(2)—N(3)88.10(10)O(3)—Co(1)—O(6)178.14(9)O(5)—Co(2)—N(3)92.11(10)O(1)—Co(1)—O(6)88.05(9)O(5)—Co(2)—N(5)176.87(9)O(3)—Co(1)—N(2)88.70(10)N(3)—Co(2)—N(5)86.25(10)N(5)—Co(1)—N(2)91.21(10)N(3)—Co(2)—N(4)179.10(11)O(1)—Co(1)—N(2)89.11(10)O(2)—Co(2)—N(4)90.88(10)N(1)—Co(1)—N(2)177.16(11)N(5)—Co(2)—N(4)92.85(10)O(6)—Co(1)—N(1)90.32(10)O(7)—Co(2)—N(4)92.02(10)O(3)—Co(1)—O(1)93.38(9)O(5)—Co(2)—O(2)88.21(9)
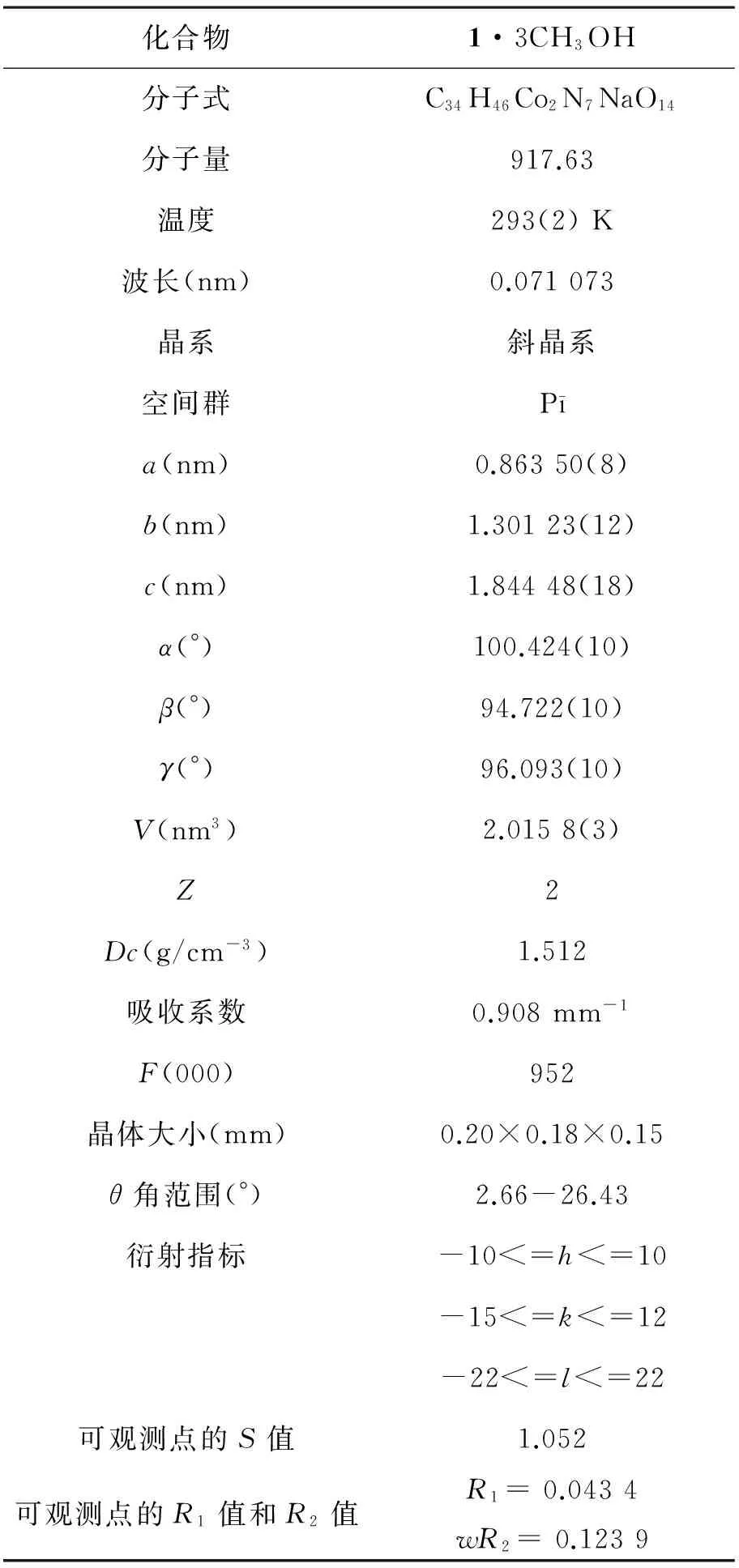
表2 一维链1·3CH3OH的晶体学数据
2 结果与讨论
2.1 合成
本实验水杨醛肟∶乙酸钠∶叠氮钠∶六水合氯化钴按物质的量比6∶6∶3∶2的比例进行混合并在甲醇溶液中反应.从下面结构讨论可知,晶体结构中没有醋酸根离子,如果重做去掉乙酸钠的实验,没有生长出晶体.可能原因是,在本实验中醋酸钠可作为弱碱参与水杨醛肟脱除酚羟基上的H原子.在以后的实验中,如果加入更强的碱如NMe4OH·5H2O可能会使得所有水杨醛肟上的酚羟基和肟基上的羟基都脱去H原子,丰富其配位模式,以便形成其它结构类型的化合物.
2.2 晶体结构

有趣的是,这四个水杨醛肟配位模式各不相同(如图3所示):a.第一种水杨醛肟上的肟基O6与Co1配位而肟基N3与Co2配位,酚羟基O5与Co2和Na1配位,其配位模式为η1∶η1∶η2, μ3;b.第二种水杨醛肟上的肟基O2与Co2和Na1配位, 而肟基N1和酚羟基O1都与Co1配位, 故其配位模式为η2∶η1∶η1, μ3; c.第三种水杨醛肟上的酚羟基O7和肟基N4均与一个Co2原子配位,肟基O8没参与配位,配位模式为η1∶η1, μ2;d.第四种水杨醛肟除了其上肟基O4参与链的结构单元桥连外,其它均与第三种水杨醛肟相同,故其配位模式为η1∶η1∶η1, μ2.调研文献发现,这是第一个水杨醛肟同时出现四种配位模式的配合物.
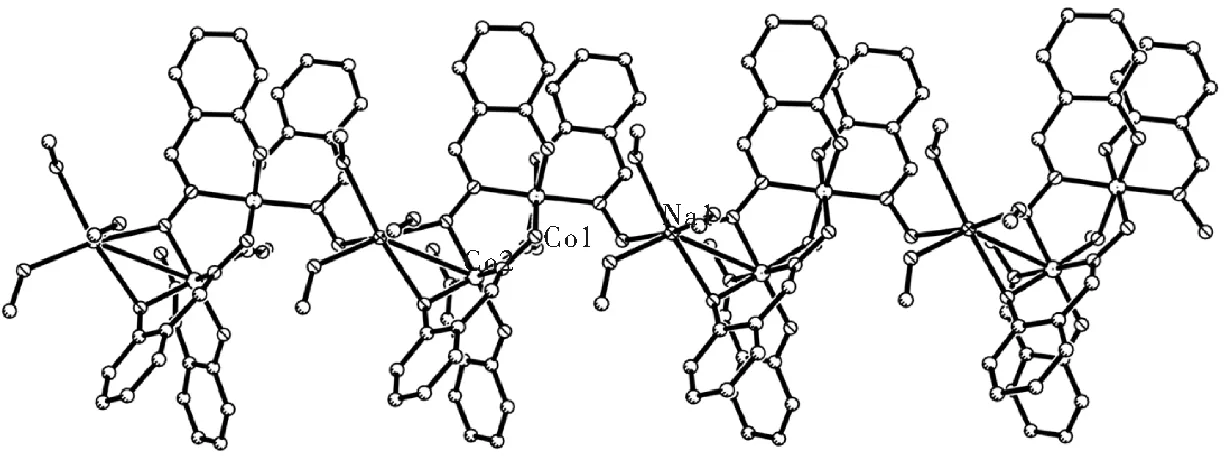
图2 1·3CH3OH的一维链结构Fig.2 The structure of 1D chain 1·3CH3OH
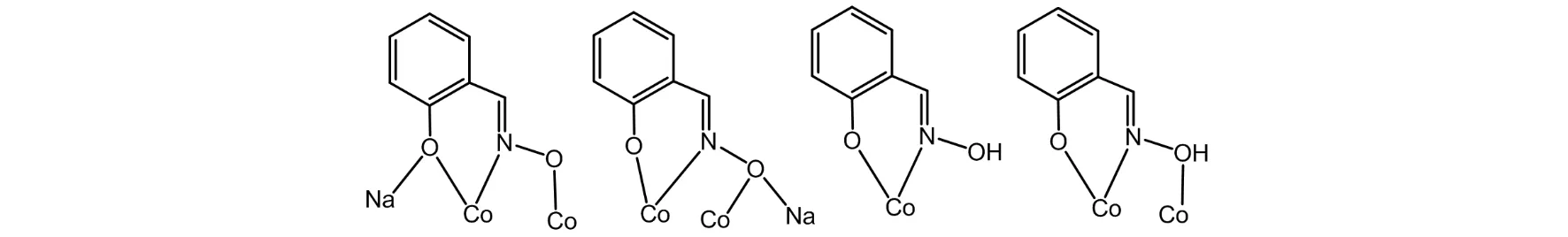
图3 一维链1·3CH3OH中水杨醛肟的四种配位模式Fig.3 Four coordination modes of salicylaldehyde oxime in the 1D chain 1·3CH3OH
配合物中,Co离子的价态和配体上O原子的质子化水平通过仔细检查键参数、价键和计算[11-12]和电荷平衡确认,结果表明,两个Co离子都是+3价的,配体上氧原子除O1、O2、O3、O5、O6和O7脱去质子外,其它所有氧原子都是没有脱去质子.结构单元中所有Co离子和Na离子都是六配位八面体构型.对于Co1和Co2,Co1-O和Co1-N键长范围分别为0.188 6(2)~0.190 3(2) nm和0.190 0(2) ~ 0.192 7(2) nm;Co2-O和Co2-N键长范围分别为0.188 2(2)~0.190 7(2) nm和0.190 3(2) ~ 0.192 4(3)nm,这些键长数据进一步说明Co1和Co2均是+3价的.Na1周围有六个配位O原子,八面体构型,Na1—O键长范围为0.230 5~0.249 1 nm,说明这些配位比较弱.

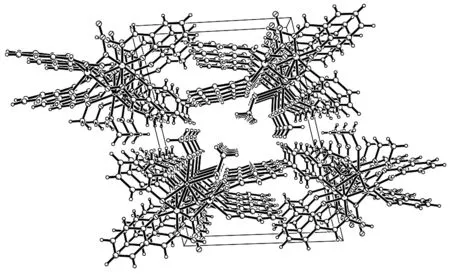
图4 一维链1·3CH3OH的晶胞堆积图Fig.4 Packing of the 1D chain 1·3CH3OH in a unit cell
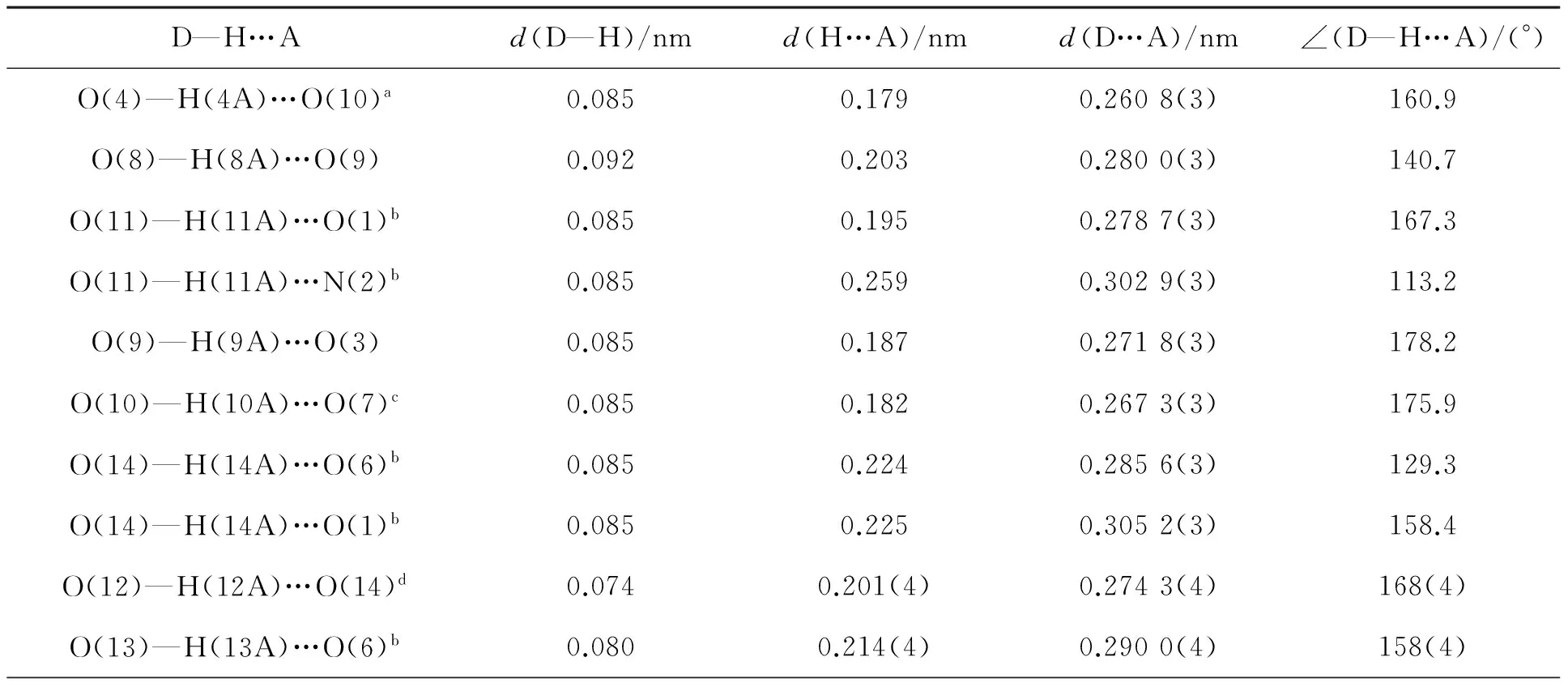
D—H…Ad(D—H)/nmd(H…A)/nmd(D…A)/nm∠(D—H…A)/(°)O(4)—H(4A)…O(10)a0.0850.1790.2608(3)160.9O(8)—H(8A)…O(9)0.0920.2030.2800(3)140.7O(11)—H(11A)…O(1)b0.0850.1950.2787(3)167.3O(11)—H(11A)…N(2)b0.0850.2590.3029(3)113.2O(9)—H(9A)…O(3)0.0850.1870.2718(3)178.2O(10)—H(10A)…O(7)c0.0850.1820.2673(3)175.9O(14)—H(14A)…O(6)b0.0850.2240.2856(3)129.3O(14)—H(14A)…O(1)b0.0850.2250.3052(3)158.4O(12)—H(12A)…O(14)d0.0740.201(4)0.2743(4)168(4)O(13)—H(13A)…O(6)b0.0800.214(4)0.2900(4)158(4)
注:对称操作码中a为x+1,y-1,z;b为x-1,y,z;c为x-1,y+1,z;d为x+1,y,z.
3 结 语
本研究首次使用水杨醛肟合成出一个以[Co2Na]为结构单元的一维链,链间不存在π—π堆积作用,晶胞内未配位的CH3OH分子也仅与近邻的链存在氢键作用,链间没有氢键作用,满足单链磁体链间作用较小的要求,然而,链内两个Co离子都是+3价的,是一抗磁性一维链.此外,这是第一个在一维链中水杨醛肟存在四个配位模式的配合物,说明该配体配位模式多样并适合构建单链磁体.今后将使用该配体构建其它顺磁性离子如Mn、Fe、Ni等一维链或构建过渡金属-稀土金属混金属一维链.
致 谢
感谢国家自然科学基金委和武汉工程大学科技处的资助.
参考文献:
[1] Gatteschi D, Sessoli R. Quantum tunneling of magnetization and related phenomena in molecular materials [J]. Angewandte Chemie International Edition, 2003, 42: 268-297.
[2] 胡学雷,姚瑜,肖莉,等. 双酚大环双核锰配合物的合成及其晶体结构 [J]. 武汉工程大学学报, 2013, 35(6): 7-11.
HU Xue-lei, YAO Yu, XIAO Li, et al. Crystal structure and characterization of new binuclear manganses(II) complex based on polyaza imino macrocyclic ligand [J]. Journal of Wuhan Institute of Technology, 2013, 35(6): 7-11. (in Chinese)
[3] Miyasaka H, Julve M, Yamashita M, et al. Slow Dynamics of the Magnetization in One-Dimensional Coordination Polymers: Single-Chain Magnets [J]. Inorganic Chemistry, 2009, 48: 3420-3437.
[4] 许公峰, 王庆伦, 廖代正, 等. 单链磁体及其研究进展 [J]. 化学进展, 2005, 17(6): 970-977.
XU Gong-feng, WANG Qing-lun, LIAO Dai-zheng,
et al. Single-Chain Magnets and their Research Progress [J]. Progress in Chemistry, 2005, 17(6): 970-977. (in Chinese)
[5] 王小波, 姜治平, 侯波涛, 等. 模板法合成大环单核铅及双核铜(II)配合物 [J]. 武汉工程大学学报, 2011, 33(4): 17-19.
WANG Xiao-bo, JIANG Zhi-ping, HOU Bo-tao, et al. Study on synthesis of new binuclear copper macrocyclic complex by template reaction involving lead ion as templating agent [J]. Journal of Wuhan Institute of Technology, 2011, 33(4): 17-19. (in Chinese)
[6] Feng X, Harris T D, Long J R. Influence of structure on exchange strength and relaxation barrier in a series of FeⅡReⅣ(CN)2single-chain magnets [J]. Chemical Science, 2011(2):1688-1694.
[7] Milios C J, Vinslava A, Wood P A, et al. A Single-Molecule Magnet with“Twist” [J]. Journal of the American Chemical Society, 2007, 129:8-9.
[8] Gass I A, Milios C J, Whittaker A. G, et al. A Cube in a Tetrahedron: Microwave-Assisted Synthesis of an Octametallic FeⅢCluster [J]. Inorganic Chemistry, 2006, 45: 5821-5283.
[9] Raptopoulou C P, Boudalis A K, Sanakis Y, et al. Hexanuclear Iron(III) Salicylaldoximato Complexes Presenting the [Fe6(μ3-O)2(μ2-OR)2]12+Core: Syntheses, Crystal Structures, and Spectroscopic and Magnetic Characterization [J]. Inorganic Chemistry, 2006, 45: 2317-2326.
[10] Bruker,SMART,SAINT,SADABS and SHELXTL[CP].Version 6.10.Madison:Bruker AXS Inc,2000.
[11] Liu W, Thorp H H. Bond valence sum analysis of metal-ligand bond lengths in metalloenzymes and model complexes. 2. Refined distances and other enzymes [J]. Inorganic Chemistry, 1993, 32: 4102-4105.
[12] Brown I D, Shannon R D. Empirical bond-strength-bond-length curves for oxides [J]. Acta Crystallographica, 1973, A29: 266-282.

