晚期非小细胞肺癌患者的营养状况及其对化疗的影响研究
韩东景,沈艳丽,赵 楠,李长生,任中海
恶性肿瘤患者往往具有较高的营养风险,目前研究表明,营养风险常导致患者治疗的并发症增多,死亡率增加,住院时间延长并可能影响到患者的生存[1]。原发性肺癌是我国常见的恶性肿瘤之一,化疗及化疗为主的综合治疗是晚期患者的主要治疗方法。本研究探讨了晚期非小细胞肺癌患者的营养状况及其对化疗的影响,以期为临床营养支持治疗提供依据。
1 资料与方法
1.1 一般资料 选取2010年3月1日—2012年9月30日南阳市中心医院肿瘤科收治的晚期非小细胞肺癌住院化疗患者87例,所有患者均经组织学检查确诊为非小细胞肺癌,并经全身ECT、胸和颅脑CT、腹部CT或B超确定为Ⅲb~Ⅳ期。其中男51例,女36例;年龄43~75岁,中位年龄64岁;鳞癌34例,腺癌49例,大细胞癌4例;Ⅲb期28例,Ⅳ期59例。纳入标准:无化疗禁忌证;预期生存期≥3个月;无脑转移;不伴有糖尿病和免疫系统疾病者。排除标准:昏迷患者;严重胸腹腔积液患者;依从性差,未能遵医嘱及时住院治疗者。
1.2 研究方法
1.2.1 化疗方案 所有患者化疗均采用TP方案:紫杉醇(TAX)175 mg/m2,静脉滴注,第1天;顺铂(PDD)25 mg/m2,静脉滴注,第1~3天;每3周重复1次,2次为1个疗程,复查并判断疗效。
1.2.2 营养风险筛查与营养不足的评定 采用欧洲肠外肠内营养学会(ESPEN)2002年制定的营养风险筛查2002(NRS2002)[2]进行营养风险筛查,包含营养状况受损评分(0~3分)、疾病严重程度评分(0~3分)和年龄评分,即在前两项评分基础上若年龄≥70岁加1分,总分为0~7分。当NRS2002评分≥3分时判断为有营养风险,需要营养支持治疗。体质指数(body mass index,BMI)采用陈春明[3]报告的标准,即BMI<18.5 kg/m2为低体质量,结合患者一般状况,如较差则评定为营养不足。
1.2.3 近期疗效和不良反应 近期疗效按照世界卫生组织(WHO)实体瘤客观疗效评价标准(1981年)[4]分为完全缓解(CR)、部分缓解(PR)、无变化(SD)和进展(PD),以CR+PR为有效(RR)。不良反应按照美国国立癌症研究所(NCI)不良反应分级标准(CTCAE)3.0[5]进行评价。
1.2.4 住院天数和化疗不良事件 从化疗第1天开始计算患者住院天数,化疗开始的第5天复查患者常规生化检查无异常、一般情况良好即认为达到出院标准,可以出院;不能出院者,对症治疗纠正后出院。在出现Ⅳ度骨髓抑制或粒细胞减少性发热时下一个周期化疗剂量递减20%,记录为1个不良事件;因其他毒性反应导致患者无法耐受化疗、化疗间歇期再入院或导致化疗延迟超过1周者,记录为1个不良事件,每例患者不重复记录[6]。
1.3 质量控制方法 营养评估数据由接受过统一标准化培训的专业营养师进行收集。化疗疗效由2名主治医师以上人员阅片判断。研究采用统一设计和方案,所有数据均经过核实。
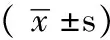
2 结果
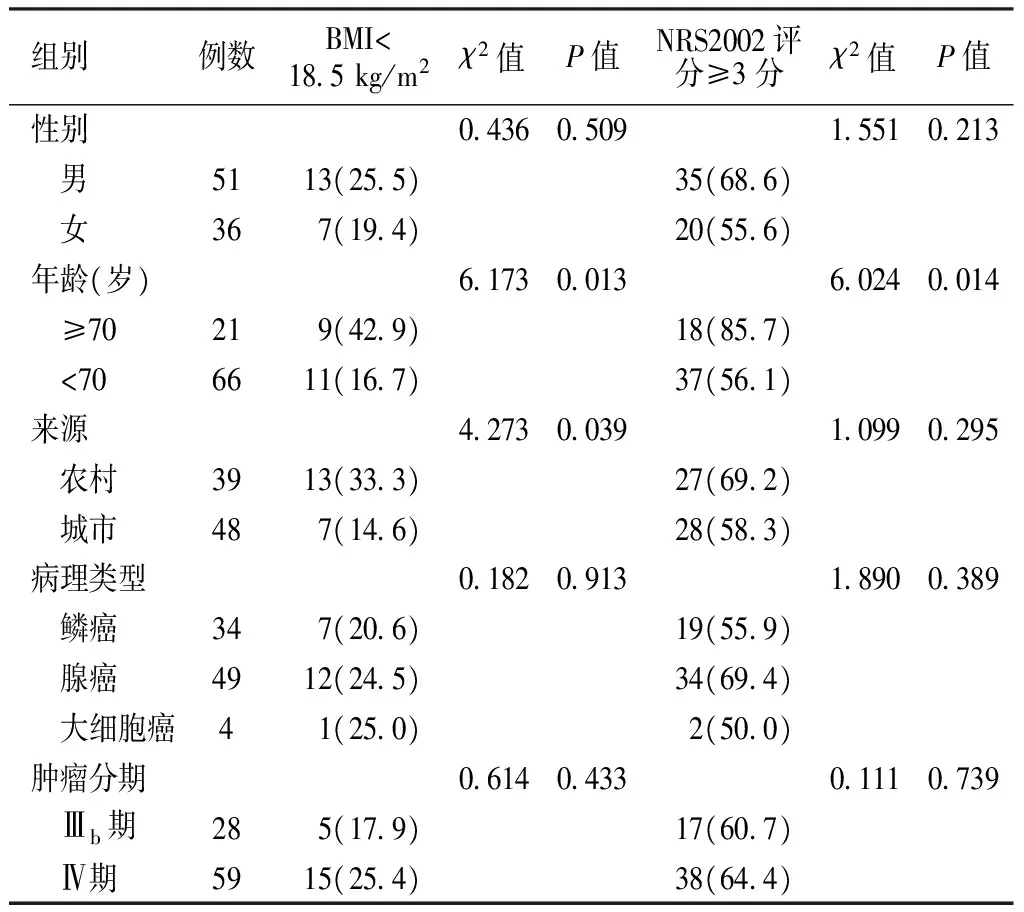
2.1 非小细胞肺癌患者的营养状况及其影响因素 87例患者中,BMI<18.5 kg/m2者20例,营养不足发生率为23.0%(20/87);BMI≥24.0 kg/m2(超重)者11例,为12.6%(11/87);无肥胖患者。NRS2002评分≥3分者55例,营养风险发生率为63.2%(55/87)。年龄≥70岁者营养不足和营养风险的发生率分别为42.9%和85.7%,与年龄<70岁者的16.7%和56.1%比较,差异有统计学意义(P<0.05)。农村患者营养不足发生率为33.3%,与城市患者的14.6%比较,差异有统计学意义(P<0.05);但两者营养风险发生率间差异无统计学意义(P>0.05)。不同性别、病理类型、肿瘤分期患者的营养不足和营养风险发生率比较,差异均无统计学意义(P>0.05,见表1)。
2.2 不同营养状况的非小细胞肺癌患者的近期疗效比较 87例患者中,CR 3例,PR 31例,RR率为39.1%(34/87)。不同营养状况患者的疗效比较,差异无统计学意义(P>0.05,见表2)。
2.3 不同营养状况的非小细胞肺癌患者的化疗不良反应比较 TP方案化疗主要毒性反应为消化道反应和血液学毒性。87例患者中,分别有14.9%(13/87)和37.9%(33/87)的患者出现了Ⅲ~Ⅳ级的消化道反应和血液学毒性,有19.5%(17/87)的患者出现了粒细胞减少性发热,需要减量化疗。营养不足与非营养不足患者的粒细胞减少性发热发生率比较,差异有统计学意义(P<0.05);有营养风险与无营养风险患者的血液学毒性、粒细胞减少性发热发生率比较,差异有统计学意义(P<0.05,见表3)。
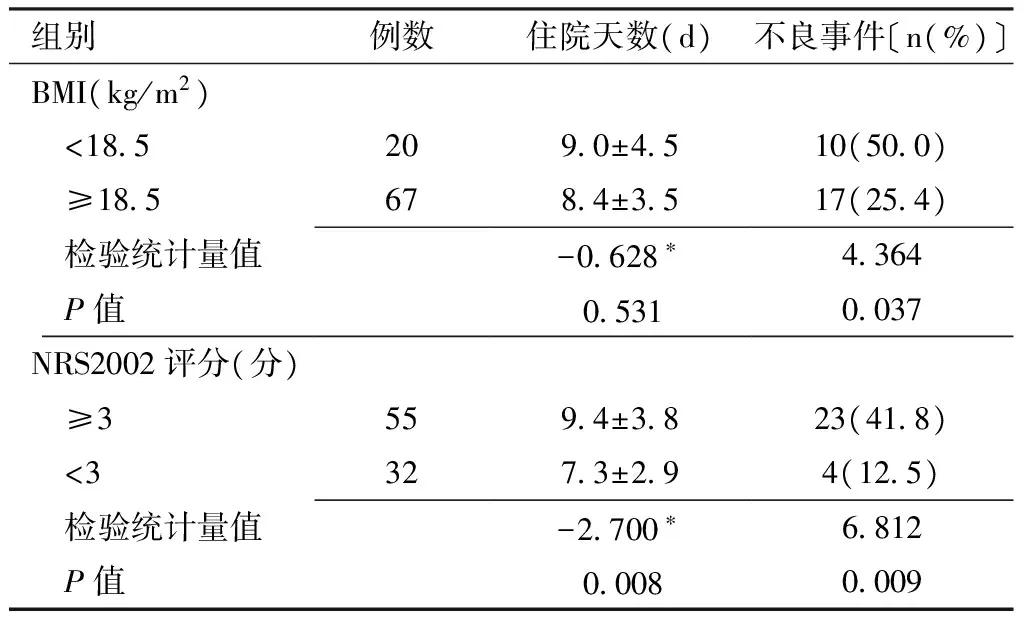
2.4 不同营养状况的非小细胞肺癌患者的住院天数和不良事件发生情况比较 全部患者化疗住院天数为5~16 d,平均(8.7±3.5)d。化疗过程中,共出现27个不良事件,包括17例粒细胞减少性发热,5例Ⅳ级粒细胞减少(未发热),但均需要减量,3例血小板减少化疗延迟,2例严重消化道反应不能耐受化疗弃用PDD。营养不足与非营养不足患者的不良事件发生率比较,差异有统计学意义(P<0.05);有营养风险与无营养风险患者的住院天数和不良事件发生率比较,差异有统计学意义(P<0.05,见表4)。
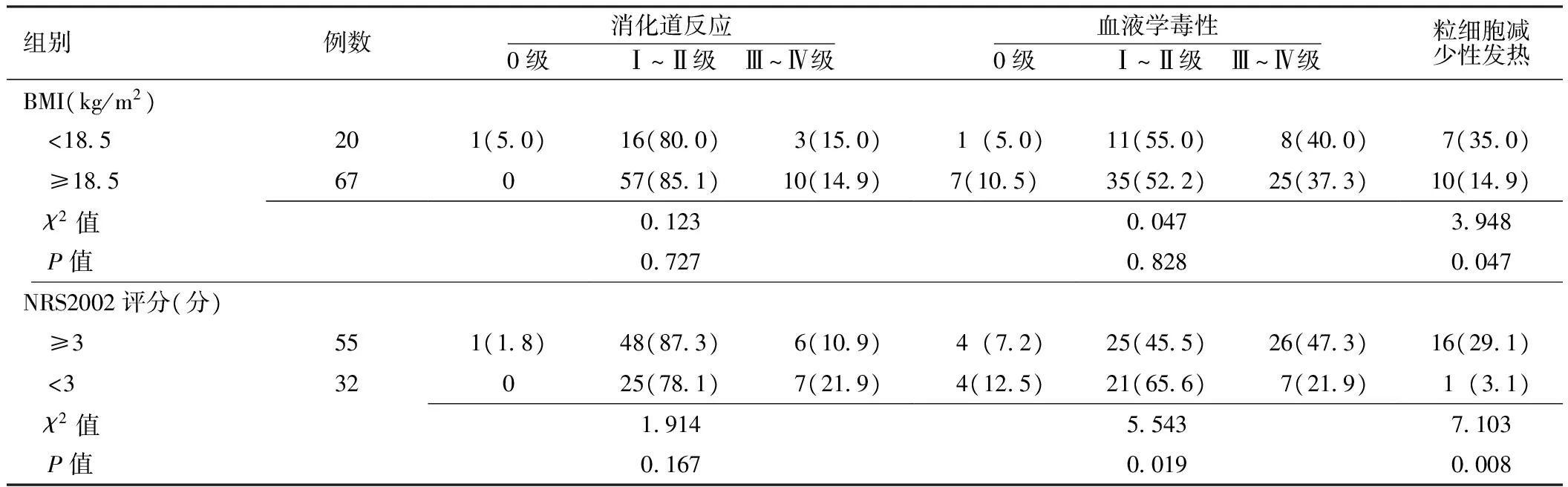
表3 不同营养状况的非小细胞肺癌患者的化疗不良反应比较〔n(%)〕
表1 非小细胞肺癌患者的营养状况及其影响因素〔n(%)〕
Table1 The nutritional status and its influencing factors among non-small cell lung cancer patients
组别例数BMI<185kg/m2χ2值P值NRS2002评分≥3分χ2值P值性别0436050915510213 男5113(255)35(686) 女367(194)20(556)年龄(岁)6173001360240014 ≥70219(429)18(857) <706611(167)37(561)来源4273003910990295 农村3913(333)27(692) 城市487(146)28(583)病理类型0182091318900389 鳞癌347(206)19(559) 腺癌4912(245)34(694) 大细胞癌41(250)2(500)肿瘤分期0614043301110739 Ⅲb期285(179)17(607) Ⅳ期5915(254)38(644)
注:BMI=体质指数,NRS2002=营养风险筛查2002
表2 不同营养状况的非小细胞肺癌患者的疗效比较〔n(%)〕
Table2 Comparison of therapy effect in non-small cell lung cancer patients with different nutritional status
注:CR=完全缓解,PR=部分缓解,SD=无变化,PD=进展
表4 不同营养状况的非小细胞肺癌患者的住院天数和化疗不良事件比较
Table4 Comparison of hospital stay and chemotherapy adverse events in non-small cell lung cancer patients with different nutritional status
组别例数住院天数(d)不良事件〔n(%)〕BMI(kg/m2) <1852090±4510(500) ≥1856784±3517(254) 检验统计量值-0628∗4364 P值 0531 0037NRS2002评分(分) ≥35594±3823(418) <33273±294(125) 检验统计量值-2700∗6812 P值 0008 0009
注:*为t值,余检验统计量值为χ2值
3 讨论
营养不良是恶性肿瘤患者常见的症状之一。调查显示,恶性肿瘤住院患者营养不足发生率为26.35%,营养风险发生率为45.56%[7],晚期患者的营养不良可达到47%[8],营养不良和具有营养风险是手术或化疗患者预后的不良因素[9]。因此,对于恶性肿瘤患者,必须重视其营养状况。
营养风险筛查的方法有多种,近年来比较可靠的方法有主观全面评定量表(SGA)、微型营养评定量表(MNA)、营养不良通用筛查工具(MUST)以及NRS2002等,每种方法各有其优缺点。NRS2002建立以来,因其有循证医学依据、简便易行等特点得到大家认可和广泛应用,并被ESPEN所推荐使用[10]。陈伟等[11]进行了NRS2002对中国住院患者营养风险筛查的可行性研究,结果证实结合中国人群BMI正常值情况下,将该方法应用于中国住院患者完全可行。与其他筛查工具相比,NRS2002更侧重于筛查住院患者所面临的营养风险,需要指出的是,营养风险并非营养不足,而是指现有的或潜在的与营养有关的因素导致患者出现不良结局的风险[2]。因此,准确筛查患者的营养风险,并给予对症处理,有可能影响患者的临床结局。
在本研究的87例晚期非小细胞肺癌患者中,BMI<18.5 kg/m2者20例,营养不足发生率为23.0%;NRS2002评分≥3分者55例,营养风险发生率为63.2%,说明晚期肺癌患者存在较高的营养不足和营养风险发生率,提示临床需要重视患者的营养状况。从患者营养状况的影响因素看,农村患者和城市患者营养不足发生率分别为33.3%和14.6%,可能与农村患者就诊时间偏晚有关,但两者营养风险相同;年龄≥70岁者营养不足和营养风险发生率为42.9%和85.7%,高于年龄<70岁的16.7%和56.1%,与文献报道一致[7]。说明年龄和城乡差异是晚期非小细胞肺癌患者营养状况的重要影响因素,对此必须加以重视。Ⅲb期和Ⅳ期患者无论是营养不足还是营养风险发生率均类似,说明对于晚期或局部晚期患者而言,分期已不再是影响患者营养状况的主要因素。研究还发现,患者性别和病理类型也不是患者营养状况的影响因素。
本研究中,全部患者治疗后CR 3例,PR 31例,RR率为39.1%。营养不足或具有营养风险患者RR率分别为35.0%和36.4%,低于无营养不足或营养风险者的40.3%和43.8%,但统计学未显示出差异,说明患者化疗疗效的影响因素比较复杂,营养状况只是影响因素之一。
目前研究已经表明,营养风险将影响恶性肿瘤手术或放疗患者的临床结局,但其对于化疗患者影响的研究很少[12-14]。在本研究TP方案化疗过程中,分别有14.9%和37.9%的患者出现了Ⅲ~Ⅳ级的消化道反应和血液学毒性,19.5%的患者出现了粒细胞减少性发热。在消化道反应上,有无营养学不良因素并不起决定作用;具有营养风险的患者出现了更多的Ⅲ~Ⅳ级血液学毒性,发生率为47.3%,明显高于无营养风险患者的21.9%;而营养不足患者Ⅲ~Ⅳ级血液学毒性发生率为40.0%,与无营养不足者的37.3%无明显差异,说明营养风险评估能更好地预测患者的化疗风险,而营养不足的评估可能由于过于强调BMI值,会导致很多具有营养风险的患者被归入营养良好组,从而不能预测化疗的风险。营养不足和具有营养风险的患者粒细胞减少性发热的发生率分别为35.0%和29.1%,高于无营养不足和营养风险者的14.9%和3.1%,说明营养状况是粒细胞减少性发热出现的重要影响因素。有研究表明,总体营养状况与生活质量有着密切联系,而对化疗不良反应未发现有必然的影响[15],与本研究结果似乎不相吻合,主要是其研究中使用SGA进行营养筛查,而SGA更侧重于患者已经存在的营养不良而非营养风险;本研究中,单纯依赖BMI和一般临床状况也不能很好地预测化疗的风险。
本研究中,具有营养不足或营养风险的患者化疗不良事件发生率分别为50.0%和41.8%,高于无营养不足或营养风险者的25.4%和12.5%;具有营养风险的患者,化疗住院时间也明显长于无营养风险者。
综上所述,晚期非小细胞肺癌患者有较高的营养不足和营养风险发生率,农村来源或者高龄患者发生率更高;营养不足或具有营养风险的患者化疗中将可能面临更高的化疗风险,并导致更多不良事件出现以及住院时间延长,应引起临床工作者的足够重视。NRS2002用于肺癌患者的营养风险筛查,可以很好地预测化疗发生严重血液学毒性反应和化疗相关不良事件的可能性。
1 Couch M,Lai V,Cannon T,et al.Cancer cachexia syndrome in head and neck cancer patients:Part I.Diagnosis,impact on quality of life and survival and treatment[J].Head Neck,2007,29(4):401-411.
2 Kondrup J,Allison SP,Elia M,et al.ESPEN guidelines for nutrition screening 2002[J].Clinical Nutrition,2003,22(4):415-421.
3 陈春明.中国成人体重指数分类的推荐意见简介[J].中华预防医学杂志,2001,35(5):349-350.
4 Miller AB,Hoogstraten B,Staquet M,et al.Reporting results of cancer treatment[J].Cancer,1981,47(1):207-214.
5 Andy T,Dimitrios C,Ann S,et al.CTCAE v3.0:Development of a comprehensive grading system for the adverse effects[J].Seminars in Radiation Oncology,2003,13(3):176-181.
6 National Cancer Institute.Common Terminology Criteria Adverse Events Version 3.0(CTCAE v3.0)[S].2006.
7 于康,周晓容,郭亚芳.恶性肿瘤住院患者营养风险和营养不足发生率及营养支持应用状况调查[J].肿瘤学杂志,2011,17(6):408-411.
8 李榕,马美丽,宋懿懿,等.初治晚期肺癌 132例患者营养状况调查[J].肿瘤,2008,28(4):353-356.
9 CSCO肿瘤营养治疗专家委员会.恶性肿瘤患者的营养治疗专家共识[J].临床肿瘤学杂志,2012,17(1):59-73.
10 Kyle UG,Kossovsky MP,Karsegard VL,et al.Comparison of tools for nutritional assessment and screening at hospital admission:A population study[J].Clin Nutr,2006,25(3):409-417.
11 陈伟,蒋朱明,张咏梅,等.欧洲营养风险调查方法在中国住院患者的临床可行性研究[J].中国临床营养杂志,2005,13(3):1372-1411.
12 Jie B,Jiang ZM,Nolan MT,et al.Impact of nutritional support on clinical outcome in patients at nutritional risk:A multicenter,prospective cohort study in Baltimore and Beijing teaching hospitals[J].Nutrition,2010,26(11-12):1088-1093.
13 唐大年,朱明炜,孙建华,等.有营养风险患者术后肠内、肠外营养支持模式与不经筛查术后全部应用肠外营养对结直肠癌患者结局的影响:60例回顾性分析[J].中华临床营养杂志,2011,19(6):355-359.
14 Paccagnella A,Morello M,Da Mosto MC,et al.Early nutritional intervention improves treatment tolerance and outcomes in head and neck cancer patients undergoing concurrent chemoradiotherapy[J].Support Care Cancer,2010,18(7):837-845.
15 袁玲,郭苗苗,许萍,等.胃肠肿瘤术后化疗患者的营养状况及对化疗不良反应的影响[J].中华护理杂志,2011,46(1):75-76.

