埃索美拉唑与瑞巴派特联合使用在预防非甾体抗炎药相关性胃黏膜损伤中的疗效研究
田笑笑,杜 浩,郑玉峰,周 清,张 瑜,白艳丽
非甾体抗炎药(NSAIDs)如阿司匹林、萘普生、布洛芬等因具有解热、镇痛、抗炎及抗凝等作用,已广泛应用于各种风湿性疾病、疼痛及软组织疾病的治疗以及心脑血管疾病的预防。随着NSAIDs在临床中的大量使用,其相关不良反应尤其是胃黏膜损伤的发生率逐年上升[1]。NSAIDs相关性胃黏膜损伤的表现可从无自觉症状、消化不良、黏膜糜烂溃疡直至出血或穿孔,临床常用的胃黏膜保护剂有H2受体阻断剂、质子泵抑制剂(PPI)、前列腺素衍生物以及近年来研发的作用于多靶点的细胞保护性药物,如瑞巴派特等。埃索美拉唑作为全世界第一个S-异构体的PPI,因其独特的代谢途径、高效持久的抑酸效果、不良反应少等优势[2],在NSAIDs导致的胃黏膜损伤领域受到普遍公认,其与不同作用机制黏膜保护剂联合使用的疗效也正受到越来越多的关注。
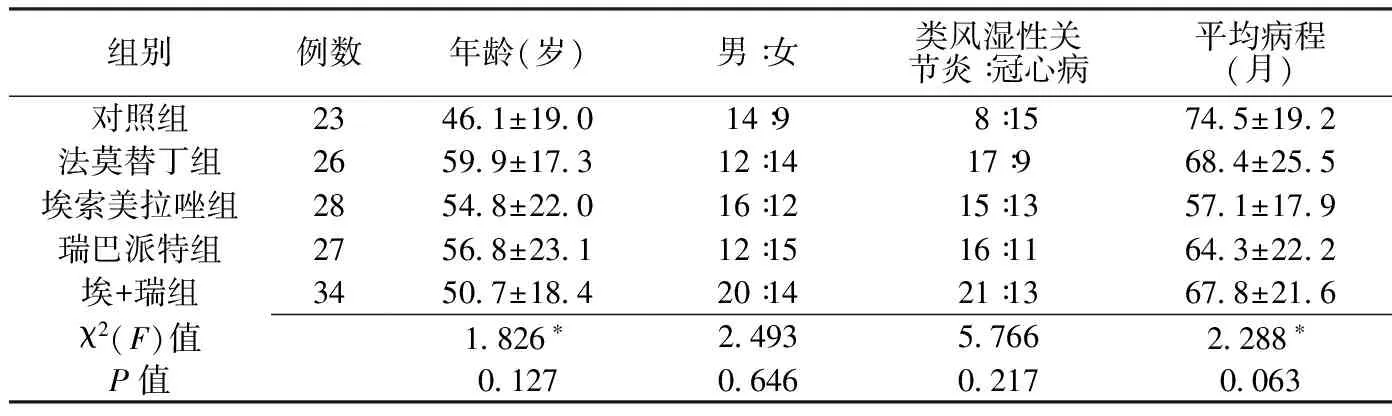
表1 各组患者一般资料比较
注:*为F值
本研究选择长期应用NSAIDs的患者作为研究对象,对照观察法莫替丁、埃索美拉唑、瑞巴派特及后两种药物联合应用在预防NSAIDs引起胃黏膜损伤中的疗效差异,从而指导临床选择合理药物进行治疗。
1 资料与方法
1.1一般资料选择2010年10月—2012年8月在本院消化内科、风湿免疫科及心血管内科就诊的患者。入选标准:(1)18岁以上的成年人;(2)已经服用NSAIDs 2周以上,由于原发疾病需要继续接受NSAIDs治疗,本研究入选的NSAIDs包括阿司匹林、氯诺昔康、双氯芬酸3种常用药物,均按常规剂量服用;(3)既往无幽门螺杆菌(H.pylori)感染史,或曾经感染已行正规H.pylori根除治疗。排除其他原因引起的胃黏膜损伤,且既往2周内未曾服用过胃黏膜保护药物者和心肝肾功能异常者。结果共入选138例患者,其中男74例,女64例;年龄25~78岁,平均(54.7±20.2)岁。将入选患者根据用药不同分为对照组23例、法莫替丁组26例、埃索美拉唑组28例、瑞巴派特组27例、埃索美拉唑+瑞巴派特组(埃+瑞组)34例,各组患者在年龄、性别等方面差异无统计学意义(P>0.05,见表1),具有可比性。
1.2方法对照组单独应用NSAIDs治疗原发性疾病;其余各组在应用NSAIDs治疗的基础上,法莫替丁组加用法莫替丁(商品名:高舒达,山之内制药公司产品)20 mg,2次/d;埃索美拉唑组加用埃索美拉唑(商品名:耐信,阿斯利康公司产品)20 mg,1次/d;瑞巴派特组加用瑞巴派特(商品名:膜固思达,浙江大冢制药有限公司生产)100 mg,3次/d;埃+瑞组加用埃索美拉唑+瑞巴派特〔(20 mg,1次/d)+(100 mg,3次/d)〕,每组疗程均为4周。4周后要求患者全部行胃镜检查,并对各组患者胃黏膜损伤发生情况,包括临床表现及损伤程度进行评估并比较。
1.3胃黏膜损伤的临床表现(1)消化不良症状:腹胀、胃灼热、恶心、反酸、上腹部疼痛、嗳气等;(2)上消化道出血、穿孔及幽门梗阻:以便隐血试验阳性或呕吐物隐血试验阳性者,确认为上消化道出血;(3)NSAIDs相关性溃疡[3]:多为无痛性溃疡,可能与NSAIDs本身具有镇痛作用有关,内镜下NSAIDs相关性溃疡的表现与传统的消化性溃疡不同,NSAIDs相关性溃疡多分布在胃底、胃窦和近幽门部,表现为形态多样、大小不等的多发性溃疡,其共同特点为浅表性溃疡。
1.4胃黏膜损伤程度评估标准参考改良Lanza标准:0分:无糜烂;1分:≤2个糜烂,局限于1个区域(胃底、胃体或胃窦);2分:3~5个糜烂,局限于1个区域(同上);3分:2个区域糜烂(每个区域的病灶数≤6个,整个胃内病灶数≤10个);4分:糜烂见于3个区域或整个胃内病灶数>10个。

2 结果
2.1各组入选者中法莫替丁组失访1例,瑞巴派特组失访1例,埃+瑞组失访2例。
2.2胃黏膜损伤临床表现5组患者胃黏膜损伤临床表现的发生率比较,差异有统计学意义(χ2=15.703,P<0.05)。其中法莫替丁组、埃索美拉唑组、瑞巴派特组及埃+瑞组患者胃黏膜损伤临床表现的发生率均较对照组低,且差异有统计学意义(P<0.05);法莫替丁组、埃索美拉唑组及瑞巴派特组患者胃黏膜损伤临床表现的发生率均较埃+瑞组高,且差异有统计学意义(P<0.05,见表2)。
2.3胃黏膜损伤程度评估5组患者胃黏膜损伤程度评估异常的发生率比较,差异有统计学意义(χ2=21.184,P<0.05)。其中法莫替丁组、埃索美拉唑组、瑞巴派特组及埃+瑞组患者的胃黏膜损伤程度评估异常的发生率均较对照组低,且差异有统计学意义(P<0.05);法莫替丁组、埃索美拉唑组及瑞巴派特组患者的胃黏膜损伤程度评估异常的发生率均较埃+瑞组高,且差异有统计学意义(P<0.05,见表3)。
表2各组患者胃黏膜损伤临床表现的发生率比较〔n(%)〕
Table2Comparison of incidence of the gastric mucosal lesion in each group

组别例数发生率对照组2312(52) 法莫替丁组256(24)∗△埃索美拉唑组286(21)∗△瑞巴派特组266(23)∗△埃+瑞组322(6)∗
注:与对照组比较,*P<0.05;与埃+瑞组比较,△P<0.05
表3各组患者胃黏膜损伤程度评估的比较
Table3Comparison of degree evaluation of the gastric mucosal lesion in each group

组别例数1分2分3分4分发生率〔n(%)〕对照组23532111(48) 法莫替丁组252210 5(20)∗△ 埃索美拉唑组282100 3(11)∗△ 瑞巴派特组262100 3(12)∗△ 埃+瑞组321000 1(3)∗
注:与对照组比较,*P<0.05;与埃+瑞组比较,△P<0.05
3 讨论
自从Roth于1986年首次提出NSAIDs相关性胃病的概念,与此有关的胃黏膜损伤机制及药物预防相关研究就不断增加,但随着NSAIDs在心血管、风湿关节病领域的应用日益广泛(统计表明全球每天有3 500万人在使用NSAIDs),NSAIDs导致的胃黏膜损伤发生率逐年提高。其发生的影响因素包括患者年龄、药物种类、剂量与用药时间、H.pylori感染以及高胃酸状态等多个方面,另外认为其发生的危险性还与吸烟及服用糖皮质激素有关[4]。加拿大一项针对长期服用阿司匹林的高危患者的调查表明[5],预防性使用黏膜保护剂的患者仅占35%,在我国这一比例甚至更低,所以对临床医师普及处方用NSAIDs的注意事项[6]及选择行之有效的预防性药物具有非常重要的意义。
NSAIDs导致胃黏膜损伤的机制主要包括:细胞毒作用直接损伤、抑制环氧合酶、产生自由基、诱导细胞凋亡等方面,其中,胃酸在NSAIDs导致胃黏膜损伤中扮演了重要角色,因此使用抑酸疗法控制胃内酸度和保护/修复黏膜屏障是治疗这类疾病的重点。防治药物中临床最常用的是PPI,包括奥美拉唑、泮托拉唑、兰索拉唑及埃索美拉唑等,埃索美拉唑作为新一代PPI正越发引起重视。与其他PPI一样,埃索美拉唑为胃壁细胞质子泵H+-K+-ATP酶的特异性抑制剂,在分泌胃酸的壁细胞或近酶区被转化为次磺酰胺的活化形式,然后与壁细胞上的H+-K+-ATP酶亚单位半胱氨酸残基上的硫基结合,使酶被氧化失活,使壁细胞的H+不能转运到胃腔,从而发挥抑制胃酸的作用。与其他PPI相比,埃索美拉唑的生物利用度更高,在肝脏内的清除效率更低,同样剂量条件下的血药浓度曲线下面积(AUC)更高,有更多药物到达壁细胞泌酸小管,具有更强的抑制质子泵泌酸作用。内源性羟自由基在NSAIDs导致的胃黏膜损伤中起重要作用,实验表明埃索美拉唑可阻断胃黏膜损伤时羟自由基、脂质过氧化和蛋白氧化产生,其抗氧化作用在防止损伤过程中起重要作用。Koch等[7]的实验表明,服用吲哚美辛的大鼠会出现黑便和体质量下降,死亡率达38%,这组大鼠胃内脂质过氧化物水平明显上升,而埃索美拉唑能逆转吲哚美辛诱导的脂质过氧化物水平增加效应,并提高胃内抗氧化物水平。黏膜细胞凋亡几乎存在于所有类型的胃黏膜损伤中,DNA损伤和断裂是黏膜细胞凋亡的征象,而埃索美拉唑可防止应激性DNA断裂以及羟自由基介导的氧化性DNA损伤。埃索美拉唑还有一些如抗炎症性因子、抗中性粒细胞浸润等作用,也在防治NSAIDs导致胃黏膜损伤中起重要作用。一项评价PPI预防NSAIDs相关性溃疡复发的临床疗效及安全性的荟萃分析显示,服用20 mg/d与40 mg/d的埃索美拉唑,对预防NSAIDs相关性溃疡复发的疗效相当(分别为4.4%与4.3%)[8],因此从经济学角度考虑,每日服用20 mg埃索美拉唑即可有效预防NSAIDs所致的胃黏膜损伤。
瑞巴派特是一种多靶点调节胃黏膜防御机制的细胞保护性药物,其不仅能作用于表皮生长因子(EGF)及其受体促进其表达,激活环氧化酶-2(COX-2)和丝裂原激活蛋白(MAP)激酶信号途径增加胃黏膜上皮细胞内源性前列腺素合成,还能清除激活的氧自由基[9]、抑制细胞凋亡、加强上皮屏障作用减少炎症因子产生从而促进胃黏膜损伤的愈合,除此之外,瑞巴派特下调细胞间黏附分子ICAM-1表达、抑制线粒体损伤的作用也有助于胃黏膜损伤的修复,所以瑞巴派特可直接针对NSAIDs所致胃黏膜损伤的多种机制发挥作用。临床研究亦证实,瑞巴派特可有效预防阿司匹林、吲哚美辛等导致的胃黏膜损伤。
NSAIDs相关性胃黏膜损伤被认为是一种酸相关性疾病,其预防疗效与胃酸被抑制的程度密切相关,埃索美拉唑能显著减少基础和餐后胃酸分泌,提高溃疡愈合率,在NSAIDs相关性胃黏膜损伤的预防和治疗中起主要作用,但单一依赖抑酸是不够的,前列腺素合成减少、细胞线粒体损伤因素等均可影响胃黏膜损伤修复的质量。本研究发现,埃索美拉唑与瑞巴派特联合使用治疗时患者腹胀、胃灼热、反酸的发生率最低,且该组无一例腹痛及消化道出血发生,内镜下检查仅有1例患者在胃窦部有单一的糜烂现象,无溃疡发生,无论与对照组,还是与法莫替丁组、埃索美拉唑组、瑞巴派特组患者相比较,埃+瑞组胃黏膜损伤临床表现的发生率及胃黏膜损伤程度评估异常的发生率均为最低。因此,单独应用PPI或黏膜保护剂远不及联合用药好,当NSAIDs激活众多致病因子共同作用并相互促进导致胃黏膜损伤时,联合用药既能阻断胃酸的直接损伤作用,又能通过增加前列腺素合成、阻断炎症信号转导、抑制促炎因子表达等作用减轻胃黏膜损伤,充分发挥药物的互补作用。
综上,NSAIDs相关性胃黏膜损伤的发生是由损伤与防御修复因素失平衡引发,临床对胃黏膜炎性损害性疾病的防治需要祛除损伤因子,同时选择黏膜保护剂增强防御与修复。埃索美拉唑与瑞巴派特联合使用以不同机制同时作用于损伤防御及修复的各个过程,能更好地兼顾损伤愈合的质量和速度,对NSAIDs所致胃黏膜损伤具有显著保护作用,二者联合使用具有广泛的临床应用前景。
1Morgner A,Miehlke S,Labenz J.Esomeprazole:prevention and treatment of NSAID-induced symptoms and ulcers[J].Expert Opin Pharmacother,2007,8(7):975-988.
2廖日斌,潘旻,刘晓敏.埃索美拉唑对防治非甾体类抗炎药致胃肠道黏膜损伤的研究进展[J].医学综述,2011,17(13):2030-2032.
3Matsui H,Shimokawa O,Kaneko T,et al.The pathophysiology of non-steroidal anti-inflammatory drug(NSAID)-induced mucosal injuries in stomach and small intestine[J].J Clin Biochem Nutr,2011,48(2):107-111.
4Tiihonen K,Tynkkynen S,Ouwehand A,et al.The effect of ageing with and without non-steroidal anti- inflammatory drugs on gastrointestinal microbiology and immunology[J].Br J Nutr,2008,100(1):130-137.
5Targownik LE,Metge CJ,Leung S.Underutilization of gastroprotective strategies in aspirin users at increased risk of upper gastrointestinal complications[J].Aliment Pharmacol Ther,2008,28(1):88-96.
6周淑新,王伟刚.处方用非甾体类抗炎药的注意事项[J].中国全科医学,2010,13(7):741-744.
7Koch TR,Petro A,Darrabie M,et al.Effects of esomeprazole magnesium on nonsteroidal anti-inflammatory drug gastropathy[J].Dig Dis Sci,2005,50(1):86-93.
8张颖,陈世耀,姚健凤.质子泵抑制剂预防非甾体抗炎药相关性溃疡复发的荟萃分析[J].中华消化杂志,2009,29(7):471-475.
9Miwa H,Osada T,Nagahara A,et al.Effect of a gastro-protective agent,rebamipide,on symptom improvement in patients with functional dyspepsia:a double-blind placebo-controlled study in Japan[J].J Gastroenterol Hepatol,2006,21(12):1826-1831.

