磷石膏热分解制备二氧化硫和氧化钙研究
郑绍聪,宁平,汪帆,成飞翔,胡粉娥
(1.曲靖师范学院化学化工学院,云南省高校煤资源开发利用及其污染控制重点实验室,云南曲靖 655011;2.昆明理工大学环境科学与工程学院)
磷石膏热分解制备二氧化硫和氧化钙研究
郑绍聪1,宁平2,汪帆1,成飞翔1,胡粉娥1
(1.曲靖师范学院化学化工学院,云南省高校煤资源开发利用及其污染控制重点实验室,云南曲靖 655011;2.昆明理工大学环境科学与工程学院)
摘要:在氮气氛下研究了碳还原分解磷石膏制备二氧化硫和氧化钙的反应特性,用烟气分析仪分析析出的气体成分,用X射线衍射仪(XRD)分析热分解固体样品。考察了煤颗粒尺寸、原料配比和反应温度对磷石膏热分解的影响。得到磷石膏热分解制备二氧化硫和氧化钙的最佳条件:煤粒径小于150 μm,碳与硫酸钙物质的量比为0.8,反应温度为1 000℃。在此条件下,可以得到二氧化硫最大体积分数为12.5%的分解炉气,分解固体样品中氧化钙质量分数达到65.32%,可以用作水泥原料或二氧化碳吸收剂。
关键词:磷石膏;热分解;二氧化硫;氧化钙
磷石膏是湿法磷酸生产过程中磷矿与硫酸反应生成的工业废渣,每生产1 t磷酸(P2O5)将产生4~5 t磷石膏[1],中国每年排放磷石膏近2 000万t。磷石膏中CaSO4·2H2O质量分数高达90%以上,是一种重要的再生石膏资源[2]。国内外对磷石膏的资源化利用做了大量的研究工作,成功开发了多种利用途径,其中研究热点之一就是利用磷石膏分解制SO2和CaO,分别用作制备硫酸和水泥的原料[3],实现磷石膏的资源化利用,同时减少磷石膏对环境的污染。
采用还原剂还原分解磷石膏,能最大程度地降低磷石膏的分解温度,有利于磷石膏的应用研究。已报道研究使用的还原剂主要有碳、CO、CH4、S等[4]。笔者选用无烟煤(碳)作为还原剂,通过热力学分析磷石膏的分解温度,在实验室采用高温电炉进行实验验证,为磷石膏热分解制备SO2提供理论数据。
1 磷石膏分解热力学分析
磷石膏的主要成分为CaSO4,碳还原分解磷石膏的过程可能会有少量氧气存在[5],会发生式(1)的磷石膏分解反应,也有可能发生式(2)的磷石膏分解成CaS,然后CaS与CaSO4反应生成SO2和CaO的反应历程:

碳还原分解磷石膏过程还可以发生下列反应过程:
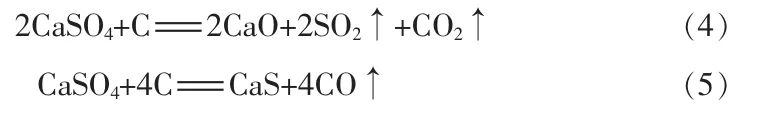
根据磷石膏的分解反应过程,查询相关热力学数据,计算反应式(1)~(5)的吉普斯自由能△rG与温度的关系式,结果见图1。
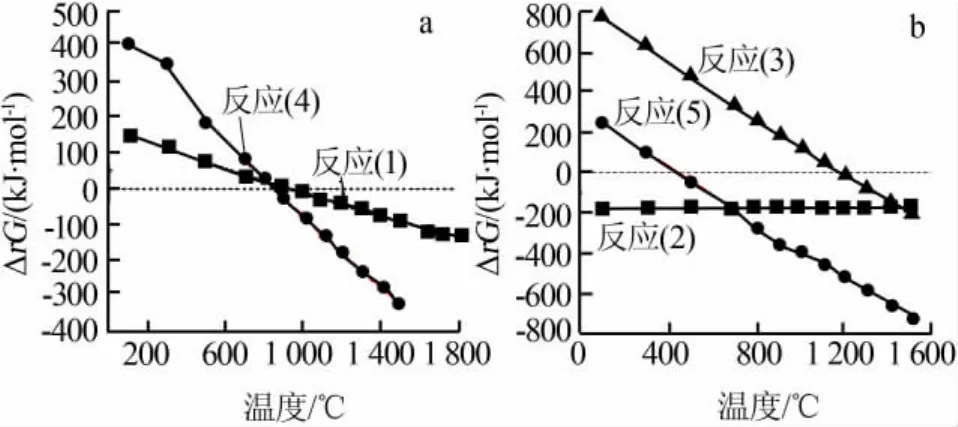
图1 不同反应的吉普斯自由能△rG随温度的变化
图1是不同温度下磷石膏分解反应的吉普斯自由能△rG随温度的变化曲线。图1a是C或CO还原剂还原分解磷石膏制备SO2和CaO的热力学数据。图1a结果表明,以碳为还原剂时,分解温度达到862℃时,反应式(4)的自由能△rG小于0,反应就可以进行,比CO为还原剂时低。图1b是磷石膏还原分解产生CaS的热力学数据及CaS和CaSO4反应生成SO2和CaO的热力学数据。图1b结果表明,磷石膏还原分解过程中会副产CaS,CaS在高温下通过反应式(3)生成SO2和CaO。所以,在随后的实验过程中拟在氮气保护条件下进行碳还原分解磷石膏制备SO2和CaO的实验研究。
2 实验部分
2.1实验原料
磷石膏取自云南云天化集团富瑞化工股份有限公司,经105℃烘干、粒径小于150 μm,样品化学成分见表1。无烟煤经预处理制成不同粒径的样品,样品化学组成见表2。N2,体积分数为99.99%。
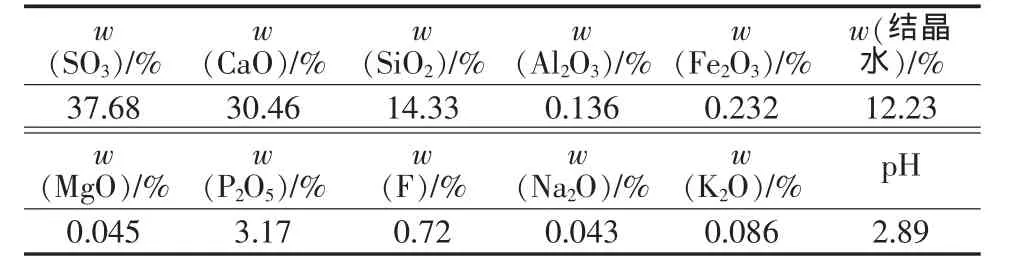
表1 磷石膏化学成分
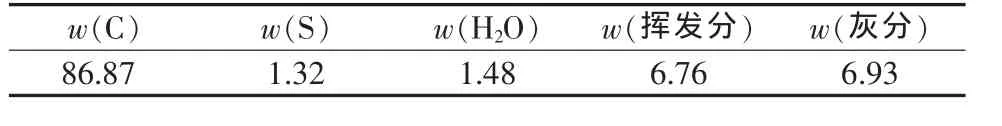
表2 煤化学成分%
2.2实验仪器
SK2-2-12管式电阻炉;KM9106综合烟气分析仪;D/max-2200型X射线衍射仪;AB204-S电子天平。
2.3实验方法
将磷石膏与无烟煤研磨均匀,按不同碳与硫酸钙物质的量比配料,分别称取5.0 g样品压片,放入石英管内,连接好实验装置。通入N2(10 mL/min)吹扫石英管,检测气体中无O2后开始实验,实验过程中保持N2流速稳定。磷石膏在不同实验温度下煅烧,至SO2不产生时停止实验,测定产生的气体中SO2的浓度以及固体产物的成分。
采用KM9106综合烟气分析仪分析析出的气体成分;采用D/max-2200型X射线衍射仪分析热分解固体成分;CaSO4和总硫的测定采用重量法。
3 实验结果与分析
3.1物料粒径、原料配比、反应温度对磷石膏热分解的影响
固定条件:煤与磷石膏的质量比为10∶1(碳与硫酸钙物质的量比接近1),磷石膏分解温度为1 000℃。考察煤的粒径对磷石膏热分解的影响,结果见图2。由图2可以看出,当煤的粒径从250 μm减小到150 μm时,炉气SO2体积分数从6.9%升高到10.1%;当煤的粒径继续由150 μm减小到75 μm的过程中,炉气SO2体积分数在10.1%浮动。实验结果说明,煤的粒径越大,反应接触面越小,越不利于磷石膏分解反应的进行;随着煤的粒径的减小,增加了反应的接触面积,反应过程进行得完全;当煤的粒径继续减小时,分解炉气增加不明显,说明煤的粒径减小到一定程度时,继续减小煤的粒径并不能从动力学角度增加磷石膏的分解反应。根据理论分析和实验结果,选择煤的粒径小于150 μm。
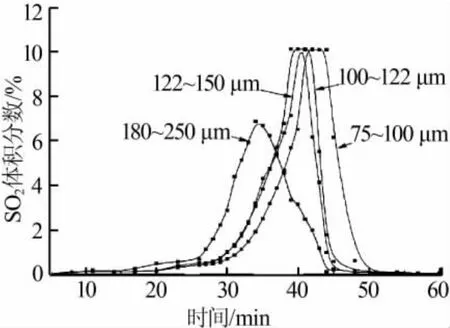
图2 不同煤粒径条件下SO2气体析出曲线
固定条件:煤的粒径小于150 μm,磷石膏分解温度为1 000℃。考察碳与硫酸钙物质的量比对磷石膏热分解的影响,结果见图3。由图3可知,当n(C)/ n(CaSO4)从0.5增加到0.8时,分解炉气SO2最大体积分数从6.3%增加到12.5%;当n(C)/n(CaSO4)从0.8增加到1.2时,分解炉气SO2最大体积分数从12.5%降低到8.8%。实验结果表明,磷石膏分解制备SO2炉气过程中,在弱还原气氛下磷石膏分解反应比较完全,因此选择n(C)/n(CaSO4)为0.8。
固定条件:煤的粒径小于150μm,n(C)/n(CaSO4)为0.8。考察分解温度对磷石膏热分解的影响,结果见图4。由图4可以看出,当分解温度为800℃时,分解炉气SO2最大体积分数为9.5%;温度升高到900℃时,分解炉气SO2最大体积分数升高到10.5%;分解温度升高到1 000℃时,分解炉气SO2最大体积分数升高到12.5%;分解温度升高到1 100℃时,分解炉气SO2最大体积分数升高到13.15%。实验结果说明,当分解温度达到1 000℃后,继续升高温度对磷石膏分解的影响不明显,所以选择磷石膏分解温度为1 000℃。
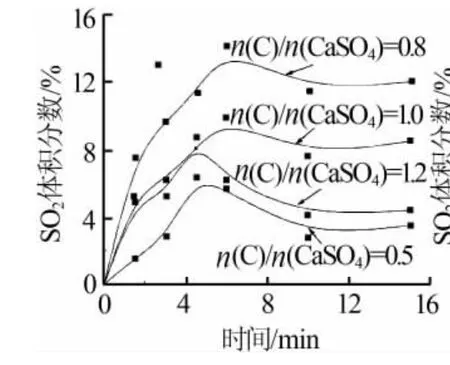
图3 不同原料配比条件下SO2气体析出曲线
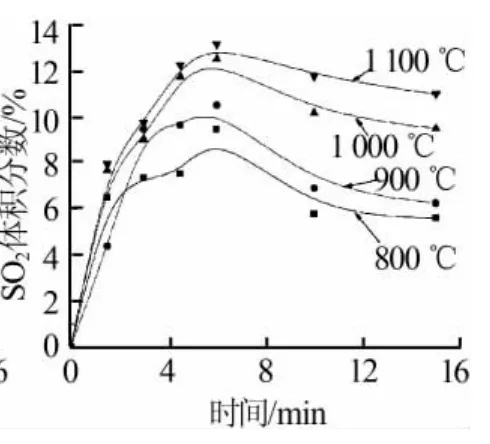
图4 不同反应温度条件下SO2气体析出曲线
3.2固体样品XRD分析
实验条件:煤的粒径小于150μm、n(C)/n(CaSO4)为0.8、分解温度为1 000℃。对分解渣进行XRD分析,结果见图5。由图5可以看出,分解样品XRD谱图中有CaO和CaS的特征峰,且CaO峰最强而CaS峰弱,说明分解后产物主要是CaO含有少量CaS;分解产物无CaSO4特征峰说明磷石膏中CaSO4几乎完全分解。分解产物中CaO质量分数为65.32%,SO3质量分数为4.21%,脱硫率为93.68%。磷石膏分解固体中CaO可用作水泥的原料。
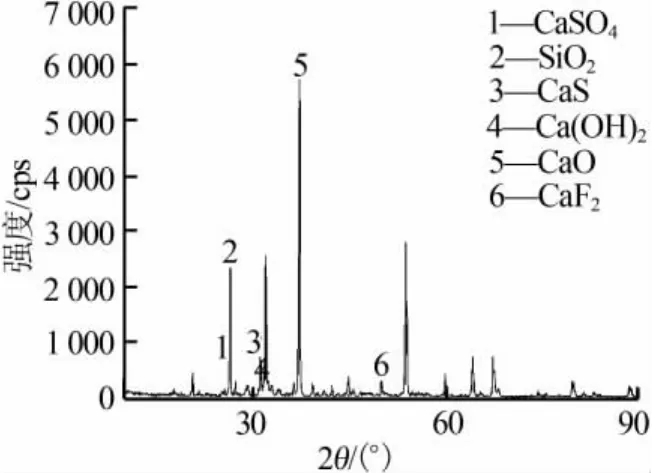
图5 分解固体样品XRD谱图
4 结论
分析磷石膏热分解反应过程,首先通过热力学分析讨论不同条件下磷石膏分解反应的工艺条件。在热力学理论研究基础上,通过实验验证磷石膏热分解制备SO2和CaO的反应过程,并确定最佳工艺条件:1)磷石膏热分解制备SO2和CaO的反应过程比较复杂,热力学分析结果表明,氮气保护气氛下进行碳还原分解磷石膏制备SO2和CaO的反应温度最低;2)煤的粒径影响磷石膏的热分解过程,大颗粒不易混匀,对磷石膏热分解反应不利,煤的粒径小于150 μm可满足磷石膏热分解制备SO2和CaO的工艺条件;3)原料配比是影响磷石膏分解反应过程、分解炉气浓度和分解固体成分的主要影响因素,在n(C)/n(CaSO4)为0.8时可以制得SO2最大体积分数为12.5%的分解炉气;4)在氮气保护条件下,碳还原分解磷石膏热分解制备SO2和CaO的最佳分解温度为1 000℃。在上述条件下磷石膏分解比较完全。
参考文献:
[1]Ma Liping,Ning Ping,Zheng Shaocong,et al.Reaction mechanism and kinetic analysis of the decomposition of phosphogypsum via a solid-state reaction[J].Ind.Eng.Chem.Res.,2010,49(8):3597-3602.
[2]Mariana Moreira Cavalcanti Canut,Vanusa Maria Feliciano Jacomino,Kari Bråtveit,et al.Microstructural analyses of phosphogypsum generated by brazilian fertilizer industries[J].Mater.Charact.,2008,59(4):365-373.
[3]刘少文,张茜,吴元欣,等.热分析在磷石膏制酸反应研究中的应用[J].化工进展,2008,27(5):761-764,785.
[4]梅毅,段东成,杨亚斌,等.磷石膏的综合利用及其竞争力分析[J].无机盐工业,2011,43(8):1-5.
[5]Ma Liping,Du Yalei,Niu Xuekui,et al.Thermal and kinetic analysis of the process of thermochemical decomposition of phosphogypsum with CO and additives[J].Ind.Eng.Chem.Res.,2012,51(19):6680-6685.
联系方式:zhshcong2008@sina.com
中图分类号:TQ125.14
文献标识码:A
文章编号:1006-4990(2013)09-0045-03
收稿日期:2013-03-17
作者简介:郑绍聪(1981—),男,博士,研究方向为固体废物资源化利用。
Study on preparation of sulfur dioxide and lime by thermal decomposition of phosphogypsum
Zheng Shaocong1,Ning Ping2,Wang Fan1,Cheng Feixiang1,Hu Fen′e1
(1.Y unnan Key Laboratory of University of Development,Utilization and Pollution Control of Coal Resources,College of Chemistry and Chemical Engineering,Qujing Normal University,Qujing 655011,China;
2.Faculty of Environmental Science and Engineering,Kunming University of Science and Technology)
Abstract:The reaction characteristics of the thermal decomposition of phosphogypsum with coal as reducing agent to prepare CaO and SO2were investigated in N2atmosphere.The output gas and the solid decomposition products were analyzed by gas analyzer and XRD,respectively.The influences of particle size of coal,mix ratio of raw materials,and reaction temperature on the thermal decomposition of phosphogypsum were studied.The results showed that the optimum conditions to produce SO2and CaO were:the coal particle size was less than 150 μm,the amount-of-substance ratio of C to CaSO4was 0.8,and the decomposition temperature was 1 000℃.Under optimum conditions,the maximum SO2volume fraction of the decomposition gas was 12.5%,and the CaO mass fraction of the solid product was 65.32%,which can be used as a raw material of cement or a CO2sorbent.
Key words:phosphogypsum;thermal decomposition;sulfur dioxide;calcium oxide

