改良固相萃取高效液相色谱法测定人血清中万古霉素浓度
宋新文 汪洋 许琼 刘炘 彭静
(武汉市妇女儿童医疗保健中心药学部,湖北 武汉430016)
改良固相萃取高效液相色谱法测定人血清中万古霉素浓度
宋新文 汪洋 许琼 刘炘 彭静
(武汉市妇女儿童医疗保健中心药学部,湖北 武汉430016)
目的:建立高效液相色谱法测定人血清中万古霉素浓度的方法。方法:以Hypersil C18柱(4.6 mm× 200 mm,10 μm)为色谱柱,流动相为乙腈-磷酸二氢钾缓冲液(9∶91),流速为0.8 mL/min,检测波长236 nm。血清样品采用固相萃取柱,以含20%乙腈的磷酸二氢钾溶液为洗脱剂,收集洗脱液直接进样测定。结果:万古霉素血清样品线性范围为0.8~120 mg/L,低、中、高3种不同浓度(4.33、19.40、77.60 mg/L)回收率分别为100.23%、102.11%、95.68%,日内、日间RSD均小于5%。结论:该方法准确性好、灵敏度高、操作简便,可满足临床万古霉素血药浓度检测的需要。
万古霉素;固相萃取;高效液相色谱法;人血清
万古霉素(Vancomycin)属糖肽类抗生素,临床上主要用于耐甲氧西林金黄色葡萄球菌(MRSA)的治疗[1]。为保证用药的安全性和有效性,减少耐药菌的产生,临床上往往需要检测其血药浓度,根据血药浓度检测结果调整用药方案[2]。因此,建立一种简便、快速、准确的检测万古霉素血药浓度方法具有十分重要的临床意义。目前国内临床上测定万古霉素血药浓度主要是通过蛋白沉淀法处理血清样品,取上清液直接进入高效液相色谱仪进行检测[3-5]。蛋白沉淀法处理血清样品具有快速、简便的特点,但由于血清蛋白沉淀不完全,大批次检测容易堵塞高效液相色谱仪管路。此外,加入的蛋白沉淀剂对血清样品的稀释作用以及蛋白沉淀物对万古霉素的吸附作用使得其提取回收率较低。张文娟等[6]建立了固相萃取(SPE)处理血清样品,高效液相色谱仪检测血清中万古霉素浓度的方法,但该方法所采取的洗脱液(10%冰醋酸-甲醇溶液)需在氮气流下水浴蒸干,实际操作中费时较长。本研究在此基础上通过改变固相萃取洗脱液成分,建立了一种快速、稳定、准确的万古霉素血药浓度检测方法。
1 仪器与材料
1.1 仪器
Agilent1260高效液相色谱仪,包括G1311C二元色谱泵、G1316A柱恒温箱(TCC)、G1315D二极管阵列检测器(DAD)、Agilent1260化学工作站;WH-1微型旋涡混合仪(上海沪西分析仪器厂);LDZ4-0.8A台式离心机(北京医用离心机厂);AB204万分之一电子分析天平(瑞士);Cleanert C18-SPE柱(规格:200 mg/支,批号:BL0061L0709)。
1.2 试药
万古霉素对照品(原中国药品生物制品检定所,批号 130360-200301);乙腈(色谱纯,国药集团化学试剂有限公司,批号T20100423);无水磷酸二氢钾(北京益利精细化学品公司,批号0902020);磷酸(天津市福晨化学试剂厂,批号 070425);正常空白人血清(实验室自制);0.9%氯化钠注射液(武汉滨湖双鹤药业有限责任公司,批号100704-201);20%乙腈-磷酸二氢钾溶液(配制方法:取色谱乙腈 20 mL与 80 mL磷酸二氢钾缓冲液混合);灭菌注射用水(安徽双鹤药业有限责任公司,批号11070920)。
2 方法与结果
2.1 色谱条件
色谱柱:Hypersil C18(4.6 mm×200 mm,10 μm);流动相为乙腈-磷酸二氢钾缓冲液(9∶91)(取磷酸二氢钾6.805 g,加入超纯水到1 000 mL使溶解,最后用磷酸调节 pH至 3.2左右,0.45 μm微孔滤膜过滤),流速 0.8 mL/min;柱温 25℃;检测波长为236 nm;进样量20 μL。
2.2 标准溶液的制备
精密称取万古霉素对照品12.4 mg于10 mL量瓶中,加灭菌注射用水制成1 240 mg/L储备液,再用灭菌注射用水稀释储备液,配制浓度为9.70、19.38、38.75、77.50、155.00、310.00、620.00 mg/L系列标准水溶液。
2.3 血清标本的处理
取血清样品0.5 mL置SPE小柱,待自然沥干后用0.9%氯化钠注射液2 mL上柱进行淋洗,弃去淋洗液,将SPE小柱于3 000 r/min离心1 min,精密量取 1 mL 20%乙腈-磷酸二氢钾溶液上柱进行洗脱,收集洗脱液,取 20 μL直接进样测定。
2.4 标准品和血清样品色谱图
分别取空白血清样品、含万古霉素血清样品及标准品进样测定,记录色谱图,见图1。结果显示色谱峰与血清中内源性杂质峰很好分离,无干扰峰出现,万古霉素的保留时间为11 min左右。
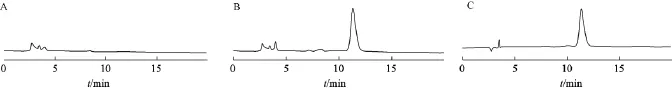
图1 万古霉素血清样品色谱A空白血清 B含万古霉素血清样品 C万古霉素标准液
2.5 线性关系考察
取空白血清1.0 mL,依次加入万古霉素系列标准水溶液及储备液0.1 mL,配制成万古霉素浓度分别为 0.88、1.76、3.52、7.04、14.09、28.18、56.36、112.72 mg/L的系列血清样品。取以上血清样品,按1.3项下的方法操作,取20 μL进样测定,记录色谱图,以样品的浓度(C)对峰面积(A)进行线性回归,得回归方程
C=0.117 2 A-0.205 2(r=0.999 1)
结果表明,万古霉素血药浓度在0.8~120 mg/L范围内线性关系良好,最低定量浓度为0.8 mg/L。
2.6 方法学回收率及精密度试验
取空白血清1.0 mL,加入0.1 mL万古霉素对照水溶液,配制成低、中、高浓度分别为 4.33、19.40、77.60 mg/L万古霉素血清样品各5份。按2.3项下的方法操作,连续测定3 d,以标准曲线方程计算样品实测浓度,与配制浓度比较,计算低、中、高各浓度方法学回收率及其日内、日间精密度。结果见表1。
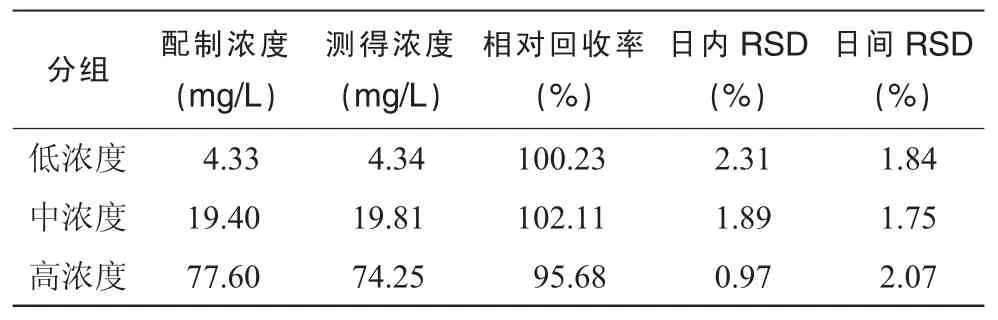
表1 万古霉素血清方法学回收率
2.7 临床标本检测结果
10例化脓性关节炎患儿,其中,男7例,女3例;年龄最小27天,最大9岁1个月,分别按40mg/kg.d,分3~ 4次,静脉滴注的用药方案治疗3 d后采集静脉血测定万古霉素血清峰浓度(静脉滴注完毕后60 min采血)及谷浓度(下次给药前5~10 min采血),结果见表2。

表2 10例化脓性关节炎患儿万古霉素血清浓度
3 讨论
本研究在实验过程中分别采用 10%、20%、 30%乙腈-磷酸二氢钾溶液作为洗脱剂。结果发现,10%乙腈-磷酸二氢钾溶液的洗脱能力有限,只能将约10%的万古霉素从SPE柱上洗脱,20%及30%乙腈-磷酸二氢钾溶液洗脱能力较好,可以将万古霉素完全洗脱。但30%乙腈-磷酸二氢钾溶液作为洗脱液,由于乙腈含量较高,所得色谱峰形前延现象严重,影响峰面积准确积分。Backes DW等[7]和Farin D等[8]分别采用0.05 M磷酸二氢钾-乙腈(30∶70)及0.05 M磷酸二氢钾-乙腈(50∶50)作为洗脱剂,这两种洗脱剂同样存在乙腈含量较高问题,故本研究采用20%乙腈-磷酸二氢钾溶液作为洗脱液。实验表明,所得色谱峰形对称性良好,符合实验要求。宋新文等[9]曾采用20%偏磷酸作为蛋白沉淀剂纯化血样测定万古霉素血清浓度,但由于蛋白沉淀物对万古霉素的部分吸附及内源性杂质干扰,该方法的最低检测限只能达2 mg/L,对于万古霉素血清谷浓度的检测有一定的局限性。本研究采用SPE法纯化血样,内源性杂质去除干净,将最低检测浓度提高到0.8 mg/L,尤其适合万古霉素血清谷浓度的测定。
SPE高效液相色谱法测定万古霉素血药浓度国内少有报道,国外文献[7-8,10]报道多采用洗脱液蒸干复溶后进样测定,实际操作中洗脱液蒸干极为困难,耗时较长。张文娟等[6]曾采用洗脱液(10%醋酸-甲醇溶液作为洗脱剂)蒸干复溶后进样测定,但耗时较长,需40~60 min才能将洗脱液蒸干。考虑到万古霉素血清峰浓度和谷浓度比较高,用2倍于血清量的洗脱液将万古霉素从SPE柱上洗脱后直接进样,虽然进样浓度稀释了1倍,但仍可被高效液相色谱仪检测出来,故本研究采用洗脱液直接进样测定,该方法简便、快速、准确,可以满足万古霉素血药浓度监测和药动学研究的需求。
[1] 李家泰.临床药理学[M].3版.北京:人民卫生出版社,2007:1024-1027.
[2] 万古霉素临床应用中国专家共识 (2011版)[J].中国新药与临床杂志,2011,30(8):561-573.
[3] 蒋硕民,戚双双,王增寿.高效液相色谱法测定人血浆中万古霉素的浓度[J].中国医院药学杂志,2006,26(11):1364-1366.
[4] 张虹,方昱,李英,等.反相高效液相色谱法测定临床联合用药时血浆中万古霉素浓度[J].药物分析杂志,2008,28(4):591-594.
[5] 林玉仙,苏煌财.高效液相色谱法测定万古霉素的血药浓度[J].中国医院药学杂志,2009,29(8):637-639.
[6] 张文娟,宋新文,汪洋,等.固相萃取高效液相色谱法测定万古霉素血药浓度[J].中国临床药理学杂志,2011,27(2):149-151.
[7] Backes DW,Aboleneen HI,Simpson JA.Quantitation of vancomycin and its crystalline degradation product(CDP-1)in humanserumbyhighperformanceliquidchromatography[J].JPharm Biomed Anal,1998,16(8):1281-1287.
[8] Farin D,Piva GA,Gozlan I,et al.A modified HPLC method for the determination of vancomycin in plasma and tissues and comparison to FPIA(TDX)[J].J Pharm Biomed Anal,1998,18(3):367-72.
[9] 宋新文,许琼,汪洋,等.HPLC法测定人血清中万古霉素的浓度[J].中国药房,2010,21(18):1663-1665.
[10] Zhang T,Watson DG,Azike C,et al.Determination of vancomycin in serum by liquid chromatography-high resolution full scan mass spectrometry[J].J Chromatogr B Analyt Technol Biomed Life Sci,2007,857(2):352-356.
Determination of the Concentration of Vancomycin in Human Serum by Modified Solid Phase Extraction and HPLC
Song Xinwen,Wang Yang,Xu Qiong,Liu Xin,Peng Jing (Pharmaceutical Department of Wuhan Medical Care Center for Women and Children,Hubei Wuhan 430016,China)
Objective:To establish a high performance liquid chromatography method for the determination of the concentration of vancomycin in human serum.Methods:The analysis was conducted with Hypersil C18column (4.6 mm× 200 mm,10 μm).Acetonitrile-potassium dihydrogen phosphate (9∶91)was served as mobile phase,the flow rate was 0.8 mL/min,and the detecting wavelength was at 236 nm.Serum sample was applied to solid phase extraction column.Taking the potassium dihydrogen phosphate solution containing 20%acetonitrile as eluent,and collecting the eluent which was determined by direct injection.Results:The linear range of vancomycin in serum was 0.8~120 mg/L.The recovery rate of low,moderate and high concentrations(4.33,19.40,77.60 mg/L)was 100.23%,102.11%,95.68%respectively.Both intra-day and inter-day RSDs were less than 5%.Conclusion:This method is accurate,sensitive,and simple.It is suitable for the determination of the concentration of vancomycin in human serum.
Vancomycin;Solid Phase Extraction;High Performance Liquid Chromatography;Human Serum
10.3969/j.issn.1672-5433.2013.02.005
宋新文,男,副主任药师。研究方向:临床药学。通讯作者E-mail:13797028603@126.com

