DIS探究催化剂对过氧化氢分解反应速率的影响
沈燕萍
(江苏省常州高级中学 江苏 常州 213003)
一、探究意图
苏教版教材《实验化学》专题4 的课题2 中设计了催化剂对过氧化氢分解反应速率的影响实验,这是采用传统中学化学实验手段对此实验进行的定量研究。通常判断过氧化氢分解速率的大小,可以通过观察比较过氧化氢溶液中析出气泡的快慢程度,或测定单位时间内过氧化氢分解放出氧气的体积。但催化剂对过氧化氢分解反应过程究竟是如何影响的? 该分解反应是什么规律? 反应速率曲线又是怎样的数学关系? 这些都是传统中学化学实验手段难以回答的。基于对这些问题的思考,我进行了本文的探究。
二、探究思路
为了准确、实时、快速和自动采集过氧化氢分解放出氧气的气压变化曲线,本实验选用了先进的DIS实验系统来完成。DIS(Digital Information System)即数字化信息系统,是将现代实验技术和以计算机为核心的信息技术融为一体的新型实验系统,由“传感器+数据采集器+实验软件包+计算机”构成。DIS 实验系统最根本的特点是将实验过程或现象转化为可检测的物理信号,进而利用物理信号反映或研究实验本质,这也是科学研究中非常重要的“转化”思想。传统的实验手段存在着误差大、数据采集慢(无法在很快的时间内采集很多组数据)、有的物理量无法直接测量、读数不方便等问题,更为重要的是数据处理手工完成,效率低,误差大。计算机和传感器的介入可以更快更准确地获得可连续的监测和采集实验数据,对于化学反应中许多“瞬时”的过程,我们也能将实验数据记录下来仔细分析了,测出来的数据以表格、图像、仪表等多种方式实时显示、分析、处理,更客观、真实地展现实验过程,更容易、更深刻地揭示客观世界隐藏的各种规律。因此利用DIS 实验系统可以探究问题的广度和深度都大大拓展,这对提高学生的探究能力很有益处。不仅能使学生加深理解和巩固学科知识,更重要的意义在于可以培养学生形成科学的思维方式,掌握科学的研究方法。
选用MnO2作催化剂,通过DIS 实验系统的压强传感器对过氧化氢分解放出氧气的气压进行实时测量,利用气压变化快慢与氧气放出速率大小成正相的关系,绘制在无催化剂和有催化剂两种情况下的“pt”曲线,外显出催化剂对过氧化氢分解反应的影响过程,揭示出该分解反应速率曲线的数学规律和反应的变化规律。
三、探究用品
压强传感器:用于测量气体压强,其读数为绝对压强值。使用时应保证被测气体与压强传感器前端的软管连接紧密。量程为0kPa~300kPa,分度0.1kPa。请注意勿将该传感器直接用于测量液体压强,不能超量程使用。
四、探究方案
1.组装实验装置,用数据线连接计算机、数据采集器、压强传感器,如图1 所示。

图1 实验装置图
2.打开DISLab V6.0实验软件系统,点击 “通用软件”,系统自动识别所接入的传感器,并显示当前压强值。观察压强示数是否稳定,如果示数有所下降,则说明装置漏气。
3.先用6%H2O2溶液作空白实验,监测体系中氧气生成速率。用注射器抽取3mL6%H2O2溶液并插入单孔橡胶塞,在具支试管上塞紧橡胶塞。
4.打开实验软件系统的“组合图线”功能,点击“采集控制”中“停止”按钮。点击“图线选择”中“添加”按钮,设定x 轴、y 轴分别为“时间”、“p”,点击“确定”,即添加“p-t”曲线。
5.点击“开始”,迅速注入3mL6%H2O2溶液并抵按住注射器活塞。观察60s 内实验过程中气压随时间的变化曲线,后点击“停止”。
6.点击界面下方“选择区域”图标,分别选择图线上反应开始时的起点和终点。根据实验所获得的曲线形状,对曲线的分布规律作出初步的判断。点击“图线分析”的“拟合”按钮,选择相应的拟合工具加以验证,即得到基于该工具的拟合曲线及其图线方程。观察拟合曲线与“p-t”曲线的吻合程度,可为推断该“p-t”曲线符合何种数学规律提供有力的佐证。
7.加入0.2gMnO2于洗净的具支试管中,用注射器抽取3mL6%H2O2溶液并插入单孔橡胶塞,在具支试管上塞紧橡胶塞。重复以上4-6 步操作,得到“p-t”曲线,找出此曲线的数学规律。
五、数据分析与讨论
1.室温下不加催化剂:如图2 是做空白实验时绘制的“p-t”曲线,点击“开始”时压强为101.1kPa,迅速注入3mL6%H2O2溶液后体系的压强迅速升到110.2kPa,此后60s 内压强变化不明显,说明H2O2溶液在不加催化剂的情况下分解很慢。根据此“p-t”曲线的分布规律选择“线形拟合”工具,得到如图3 所示的拟合图线,图线方程为y=0.0075x+108.9855,拟合曲线与“p-t”曲线完全吻合,可推断此“p-t”曲线符合线性关系。斜率为0.0075 而不是0,说明体系的压强还是在缓慢增加的,从试管壁上附着一些小气泡也验证了这一点,这可能由于试管壁的粗糙表面或有杂质促使H2O2溶液在缓慢分解,也说明该DIS 实验系统的压强传感器的灵敏度非常高。

图2

图3
2.室温下加催化剂:如图4 是加入0.2g MnO2(粉末) 时绘制的 “p-t” 曲线,点击 “开始” 时压强为101.1kPa,迅速注入3mL6%H2O2溶液后体系的压强迅速升到110.1kPa,此后压强开始快速增加,反应约40s后压强增加缓慢,60s时压强上升到209.1 kpa。这说明H2O2溶液在催化剂的存在下迅速分解,当反应进行到40s 后反应速率逐渐减缓。同时可观察到试管内H2O2溶液产生大量气泡,触摸试管壁有热量放出。根据此“p-t”曲线的分布规律选择 “对数拟合”工具,得到如图5 所示的拟合图线,图线方程为y=25.8809lnx+107.1113,拟合图线与“p-t”曲线基本吻合,可推断此“p-t”曲线基本符合对数函数规律,从而外显出催化剂对过氧化氢分解反应的影响过程,揭示出该分解反应的变化规律。
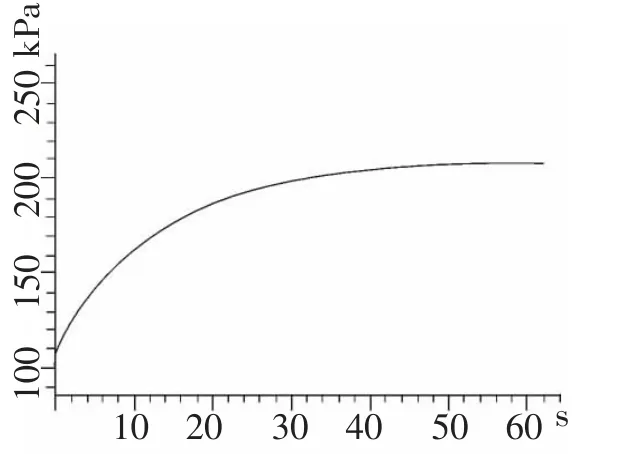
图4

图5
六、实验优点
1.创新性
采用先进的DIS 实验技术来进行该探究实验,这充分体现了新课程背景下的实验面向现代化的特点,对于帮助学生了解现代实验技术能够起到积极的作用。创新性的体现不仅仅在于采用了先进的DIS 实验系统,而是设计了全新的探究思路、探究装置和探究方案,在信息技术与传统实验的整合方面有所创新。
2.过程性
利用DIS 实验软件包的相关数学工具进行数据分析,充分利用各种科学探究中的统计方法,让我们能透过反应现象看清反应本质,能动态显示出实验过程的细节,使我们从原来关注实验现象转变成关注实验过程与原理,使我们得出的结论更加科学,使我们对问题的解释更加客观、真实、有效。
3.探究性
既可以观察到实验现象,又可以清晰地看到过氧化氢迅速分解反应速率曲线的绘制过程,还可以用手触感到过氧化氢迅速分解所产生的热量。从而体验科学研究的过程,强化科学探究意识,利于培养学生创新精神和实践能力,充分体现新的化学课程理念。
4.灵活性
除MnO2外,还可用CuO、Fe2O3等作H2O2分解的催化剂。该实验方案和实验装置基本不变,只需将MnO2换成其他的催化剂,即可探究不同催化剂对过氧化氢分解反应速率的影响,使得探究的问题范围和深度都大大拓展。
5.实用性
该实验装置简单、材料易得、操作简便、效果明显,易于推广。传统实验中测定单位时间内过氧化氢分解放出氧气的体积时,极短的时间内很容易造成体积误读,而DIS 实验系统测量的数据显示来得直接和准确,能很好地适应演示实验的要求。
6.安全性
压强传感器的使用要求是在密闭系统中测定,但密闭系统中产生压强过大容易引起爆炸等危险,所以实验装置设计中采用的注射器既是加入反应物的容器,又是整个体系的减压装置。一旦体系的压强过大,超过压强传感器量程,即可松开注射器活塞,达到减压目的,确保实验安全。
七、注意事项
1.双氧水有强腐蚀性,强氧化性,与皮肤接触会有强烈的烧灼感,使局部皮肤和毛发发白,产生刺痛、瘙痒。在使用过程中应注意避免与眼睛、皮肤接触,以防灼伤。
2.装置使用前要检查气密性,以防实验过程中漏气,导致数据不准确。
3.实验要采用同一个实验装置,以保证实验的公平和可比性。
4.MnO2的用量以及颗粒直径大小均会影响H2O2分解的速率。
5.选用6%的H2O2溶液是因为DIS 压强传感器很敏感,如果浓度大虽然反应剧烈,一方面数据波动也会较大,不利于精确测定;另一方面在密闭系统测定时,压强过大容易引起爆炸等危险。
6.清洗具支试管或向其中加入药品时,应注意不要将水或药品流入具支试管的支口,以免沾污压强传感器软管。
[1] 上海市中小学数字化实验系统研发中心,山东省远大网络多媒体有限责任公司.朗威数字化信息系统实验室V6.0:化学、生命科学用户手册.2007

