离子色谱法测定盐酸阿扎司琼氯化钠注射液中亚硫酸氢钠的含量
杨丽珍,杨伟峰,,石云峰
(1.浙江工业大学化材学院,杭州 310014;2.浙江省食品药品检验研究院,杭州 310004)
离子色谱法测定盐酸阿扎司琼氯化钠注射液中亚硫酸氢钠的含量
杨丽珍1,杨伟峰1,2,石云峰2
(1.浙江工业大学化材学院,杭州 310014;2.浙江省食品药品检验研究院,杭州 310004)
目的 建立一种离子色谱法准确快速测定盐酸阿扎司琼氯化钠注射液中抗氧化剂亚硫酸氢钠含量的方法。方法 采用AS-11阴离子分析柱(4.6 mm×250 mm,5 μm) 对样品进行分离,以20 mmol·L-1氢氧化钾溶液为淋洗液,流速1.0 mL·min-1,抑制型电导检测器检测。样品用0.4%甲醛溶液稀释后直接进样。结果 NaHSO3线性范围为4.07~30.51 μg·mL-1,r=0.999 7;Na2SO4线性范围为1.59~159.0 μg·mL-1,r=0.999 8;NaHSO3、Na2SO4样品平均回收率(n=9)分别为98.82%,98.24%。结论 本方法操作简便、灵敏、稳定、选择性高,可用于盐酸阿扎司琼氯化钠注射液中亚硫酸氢钠含量的检测。
离子色谱;盐酸阿扎司琼;亚硫酸氢钠
盐酸阿扎司琼氯化钠注射液是一种用于放疗、细胞毒素药物化疗引起的恶心呕吐及手术后患者恶心呕吐的止吐药物,部分生产企业加入亚硫酸氢钠作为抗氧化剂。与口服不同的是,静脉给药的亚硫酸盐过敏反应发病快、病情严重。因为口服亚硫酸盐在肠道吸收经门静脉进人肝脏,被肝内亚硫酸氧化酶氧化成无毒的硫酸盐由尿液排出体外,静脉给药的亚硫酸盐绕过肝脏解毒环节直接进人血液循环,毒性更强。注射剂中亚硫酸盐常用剂量为0.1%~1.0%[1],准确测定出注射剂中亚硫酸盐的含量是控制药品质量,保证用药安全的一大途径。采用氧化还原法[2]、分光光度法[3]、化学发光法[4]等方法测定盐酸阿扎司琼氯化钠注射液中的亚硫酸氢钠含量方法较为烦琐,空白干扰较大,需样品量大。文献[5]报道了以碳酸钠、碳酸氢钠混合溶液为淋洗液,三乙醇胺为稳定剂的离子色谱法测定卡络磺钠氯化钠注射液中亚硫酸氢钠的含量。本实验在此基础上,研究了以氢氧化钾为淋洗液,甲醛为稳定剂测定盐酸阿扎司琼氯化钠注射液中亚硫酸氢钠含量的方法。
1 仪器与试剂
ICS-3000离子色谱仪(美国戴安,配有EG发生器和抑制型电导检测器);Mettler XS205DU电子分析天平(瑞士梅特勒)。硫酸钠对照品(国药集团化学试剂有限公司,批号:20120910,纯度>99%);亚硫酸氢钠对照品(湖南尔康制药有限公司,批号:101120120601,含量:90.57%),国内3家企业生产的盐酸阿扎司琼氯化钠注射液4批(正大天晴药业集团有限公司,批号:111209;扬子江药业集团有限公司,批号:120911,120945;四川三精升和制药有限公司,批号:20120515)。试验用水为 Milli-Q系统制备,甲醛为分析纯。
2 方法
2.1 0.4%甲醛溶液的配制
取4.0 mL甲醛溶液,置1 000 mL量瓶中,加水稀释,摇匀,即得。
2.2 对照品溶液的配制
2.2.1 亚硫酸氢钠对照品溶液的配制 精密称取亚硫酸氢钠对照品0.101 7 g 置100 mL 量瓶中,加少量水溶解,并用水稀释至刻度,精密量取2.0 mL置100 mL量瓶中,用0.4%甲醛溶液稀释至刻度,摇匀,即得。
2.2.2 硫酸钠对照品溶液的配制 精密称取硫酸钠对照品0.106 0 g 置100 mL 量瓶中,加少量水溶解,并用水稀释至刻度,精密量取10.0 mL置100 mL量瓶中,用0.4%甲醛溶液稀释至刻度,摇匀,即得。
2.3 供试品溶液的配制
精密量取本品2.0 mL,置20 mL量瓶中,用0.4%甲醛溶液稀释至刻度,摇匀,即得。
2.4 色谱条件
色谱柱:AG-11阴离子保护柱和AS-11阴离子分析柱(4.6 mm×250 mm,5 μm戴安公司);淋洗液:20 mmol·L-1氢氧化钾(在线淋洗液发生器生成),流速:1.0 mL·min-1,抑制型电导检测器,抑制电压:50 mV,进样量:25 μL。
3 结果
3.1 专属性试验
在选定的色谱条件下,SO32-峰形尖锐,对称性好,保留时间约为7.35 min,SO42-的保留时间约为7.90 min,两者之间分离度为1.65,见图1。
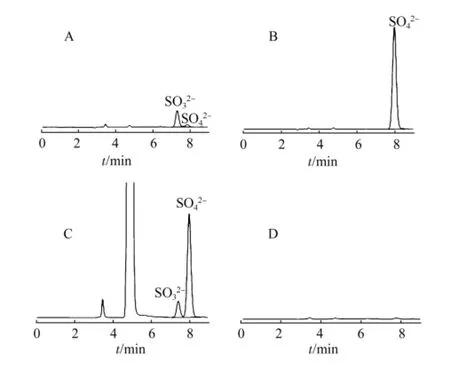
图1 离子色谱图A-亚硫酸氢钠对照品;B-硫酸钠对照品;C-样品;D-空白溶液Fig 1 Ion chromatograms A-sodium bisulfite standard solution; B-sodium sulfate standard solution; C-samples; D-blank
3.2 线性关系考察
3.2.1 亚硫酸氢钠线性关系考察 精密量取适量亚硫酸氢钠对照品溶液,用0.4%甲醛溶液稀释制成浓度为30.51,24.41,20.34,16.27,12.20,8.140,4.07 μg·mL-1的系列浓度对照品溶液,按“2.4”项下色谱条件进样测定峰面积,以浓度为横坐标,峰面积为纵坐标,绘制标准曲线,得回归方程Y=0.080 4X-0.082 9,r=0.999 7,结果表明亚硫酸氢钠在4.07~30.51 μg·mL-1内呈良好线性关系。
3.2.2 硫酸钠线性关系考察 精密量取适量硫酸钠对照品溶液,用0.4%甲醛溶液稀释制成浓度159.0,127.2,106.0,84.80,63.60,42.40,21.20,1.590 μg·mL-1的系列浓度对照品溶液,按“2.4”项下色谱条件进样测定峰面积,以浓度为横坐标,峰面积为纵坐标,绘制标准曲线,得回归方程Y=0.140 8X+0.067 7,r=0.999 8。结果表明硫酸钠在1.59~159.0 μg·mL-1内呈良好线性关系。
3.3 仪器精密度试验
分别精密吸取亚硫酸氢钠对照品溶液25 μL,连续进样6次,结果其峰面积的RSD为0.53%。
3.4 重复性试验
取盐酸阿扎司琼氯化钠注射液(批号:1210105),按“2.3”项下方法平行制备6份供试品溶液,测定峰面积,计算含量和RSD。结果该批盐酸阿扎司琼氯化钠注射液中亚硫酸氢钠的平均含量为0.02%,RSD为0.45%,硫酸钠的平均含量为0.065%,RSD为0.28%,表明方法重复性良好。
3.5 定量限试验
精确配制亚硫酸氢钠系列浓度的溶液,分别进样,按峰高为基线噪声的10倍计算得亚硫酸氢钠定量限为0.78 μg·mL-1(n=6,RSD%为2.3%),硫酸钠定量限为1.15 μg·mL-1(n=6,RSD%为1.68%)。
3.6 回收率试验
3.6.1 亚硫酸氢钠回收率 A公司的1102141批盐酸阿扎司琼氯化钠注射液样品中未添加亚硫酸氢钠辅料,故以该批样品分别配制亚硫酸氢钠含量为16.95,20.34,25.43 μg·mL-1低(80%)、中(100%)、高(120%)浓度的共 9份模拟样品,按“2.3”项下方法制备,按“2.4”项下色谱条件进样,测定其峰面积,并计算回收率,得平均回收率为98.82%,RSD%为1.08%。由此可知,使用本方法测定NaHSO3含量准确率较高。
3.6.2 硫酸钠回收率 以A公司1102141批盐酸阿扎司琼氯化钠注射液样品分别配制硫酸钠含量为88.33,106.0,132.5 μg·mL-1低(80%)、中(100%)、高(120%)浓度的共 9份模拟样品,按“2.3”项下方法制备,按“2.4”项下色谱条件进样,测定其峰面积,并计算回收率,得平均回收率为98.24%,RSD%为0.64%。由此可知,测定Na2SO4含量使用本方法准确率较高。
3.6.3 不同浓度甲醛溶液对亚硫酸氢钠回收率的影响 以A公司1102141批盐酸阿扎司琼氯化钠注射液样品,分别用0.1%,0.2%,0.4%,1.0%甲醛溶液配制亚硫酸氢钠含量为20.34 μg·mL-1的模拟样品,按“2.3”项下方法制备,按“2.4”项下色谱条件进样,测定其峰面积,并计算回收率,结果见表1。由此可知,采用0.4%甲醛溶液作为稳定剂时,测定NaHSO3含量使用本方法准确率较高。

表1 不同浓度甲醛溶液对回收率的影响Tab 1 The influence of different concentration of formaldehyde solution for the recovery

?
3.7 稳定性试验
按“2.2.1”项下方法配制亚硫酸氢钠对照品溶液,分别于 0,1,2,4,6,8 h 进样测定,记录峰面积,RSD为 1.6%。结果表明亚硫酸氢钠对照品溶液在8 h内基本稳定。
3.8 样品分析
对4批样品进行测定,以亚硫酸氢钠对照品溶液和硫酸钠对照品溶液的峰面积按外标法分别计算样品中亚硫酸氢钠和硫酸钠的含量,因硫酸钠是加入的亚硫酸氢钠在生产和贮存期间氧化而来的,故按式(1)将其折算成亚硫酸氢钠的含量,结果见表2。
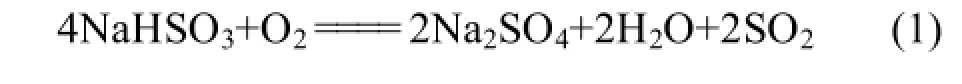

表2 亚硫酸氢钠含量测定结果Tab 2 Results of the content of sodium bisulfite
4 讨论
盐酸阿扎司琼氯化钠注射液中加入亚硫酸氢钠作为抗氧化剂,在生产和贮存期间,部分亚硫酸氢钠被氧化,生成硫酸钠,所选择的色谱条件须能使SO32-和SO42-达到良好的分离;为准确测定初始加入盐酸阿扎司琼氯化钠注射液中亚硫酸氢钠的含量,需同时测定硫酸钠的含量,折算成亚硫酸氢钠来确定总亚硫酸氢钠的含量。
中国食品药品检定研究院尚无亚硫酸氢钠对照品提供,本实验使用湖南尔康制药有限公司生产的亚硫酸氢钠作为对照品。实验中发现,该公司生产的亚硫酸氢钠已部分被氧化,故须采用建立的离子色谱法先测定硫酸钠含量后通过计算确定亚硫酸氢钠含量。
采用建立的方法测得4批样品,均符合国家药监部门推荐的限度(0.1%)[2],而其中一批未检出,说明该方法能很好的检测注射液中亚硫酸氢钠含量,有助于药监部门对药品质量的监管,保证用药安全。
本方法采用在线淋洗液生成器和水自动生成20 mmol·L-1氢氧化钾作为淋洗液,简便、快捷,且能使SO32-和SO42-的分离度达到要求;实验中若不加稳定剂,两针平行样相差15%左右,这是由于亚硫酸氢根不稳定,容易转化为硫酸根。根据文献报道[6],甲醛是亚硫酸氢钠的很好的稳定剂。通过考察不同浓度的甲醛溶液的影响,发现0.4%的甲醛溶液能使SO32-峰面积基本稳定,且样品的加样回收率达到99.07%。
REFERENCES
[1] ZHENG C, MEI D , WANG L, et al. Adverse effect of excipients in pharmaceutical products [J]. Chin Pharm J(中国药学杂志), 2005, 40(9): 644-649.
[2] HU R R. Control and determination of antioxidant in amino acid injection [J]. Acad J Guangdong Coll Pharm(广东医学院学报), 2011, 4(17): 283-284
[3] ZHANG S D. Quantitation of sodium bisulphite in dobutamine hydrochloride injection by spectrophotometry [J]. China Med Pharm(中国医药科学), 2011, 1(17): 45-48.
[4] LIU Z C, YANG F Z, SHAN Y F. Quantitation of sodium bisulphite in injection liquid by chemiluminescence method [J]. J Hebei Norm Univ(河北师范大学学报), 2010, 1(34): 80-85.
[5] RONG Y H, ZHOU G R, SHAN Y F, et al. IC determination of sodium bisulfite of carbazochrome sodium sulfonate chloride injection [J]. Chin J Pharm Anal(药物分析杂志), 2011, 31(1): 160-162
[6] LU K P. Simultaneous determination of Cl-and SO42-in 30% sodium bisulfite solution samples by ion chromatography [J]. Chin J Chromatogr(色谱), 2005, 23(3): 205-208.
Determination of Sodium Bisulfite in Azasetron Hydrochloride and Sodium Chlodide Injection by Ion Chromatography
YANG Lizhen1, YANG Weifeng1,2, SHI Yunfeng2
(1.College of Chemical Engineering and Materials Science, Zhejiang University of Technology, Hangzhou 310014, China; 2.Zhejiang Insititue for Food and Drug Control, Hangzhou 310004, China)
OBJECTIE To establish an ion chromatography method for rapid and precise determination of the content of antioxidant sodium bisulfite in azasetron hydrochloride and sodium chlodide injection. METHODS The AS-11 anion analytical column(4.6 mm×250 mm, 5 μm) was adopted to separate the samples with the eluent of 20 mmol·L-1potassium hydroxide. The flow rate was 1.0 mL·min-1, and the suppressed conductivity detector was adopted. Samples were diluted with 0.4% formaldehyde solution followed by direct injection. RESULTS This method exhibited excellent regression(r=0.9997) in the range of 4.07-30.51 μg·mL-1for NaHSO3and regression(r=0.999 8) in the range of 1.59-159.0 μg·mL-1for Na2SO4, the average recovery (n=9) was 98.82%, 98.24%, respectively for NaHSO3and Na2SO4. CONCLUSION The method is simple, accurate, stable and precise, and can be userd for the determination of sodium bisulfite in azasetron hydrochloride and sodium chlodide injection.
ion chromatography; azasetron hydrochloride; sodium bisulfite
R917.101
B
1007-7693(2013)10-1116-04
2013-01-05
杨丽珍,女,硕士生 Tel: (0571)86459422 E-mail: 15807975068@163.com

