羟丙基-β-环糊精包合双氯芬酸钠注射液的制备
庄婕,呼海涛,乔燕萍
(上海医药集团股份有限公司,上海 201203)
羟丙基-β-环糊精包合双氯芬酸钠注射液的制备
庄婕,呼海涛,乔燕萍
(上海医药集团股份有限公司,上海 201203)
目的 制备适合临床用药浓度和稳定性的双氯芬酸钠(DS)注射液。方法 采用羟丙基-β-环糊精对DS进行包合,通过相溶解度图确定包合比例,并对抗氧剂种类以及灭菌条件进行筛选。结果 当羟丙基-β-环糊精浓度>0.067 7 mol·L-1时,可以实现对DS的完全包合;以硫代甘油作为抗氧剂,注射液性质稳定;终端灭菌不宜采用热压灭菌法。结论 羟丙基-β-环糊精可以增加DS在水中的溶解度,使其达到有效治疗浓度。制备得到的注射液性质稳定,满足临床用药要求。
双氯芬酸钠;羟丙基-β-环糊精;抗氧剂;稳定性
双氯芬酸钠(diclofenac sodium,DS)是一种衍生于苯乙酸类的非甾体消炎镇痛药(NSAIDS),其良好的解热镇痛效果带动了众多剂型的开发上市,目前除了注射剂之外,均为口服剂型和局部给药剂型[1]。DS注射液主要为不能口服的住院患者解除疼痛和退热。然而,由于DS在水中溶解度较小(25 mg·mL-1,25 ℃)[2],达不到制剂浓度要求,而DS的分子结构中尚含有易氧化基团,如将其制成注射液后,可使药物的稳定性下降[3],因此寻找合适的溶剂系统以及提高制剂稳定性成为研究的关键问题。本实验采用羟丙基-β-环糊精(HP-β-CD)对DS进行包合,并对包合比例、抗氧剂的种类以及灭菌条件分别进行考察,以制备具有较高溶解度和稳定性的DS注射液。
1 材料与仪器
1.1 材料
DS(河南东泰制药有限公司,批号:110401,纯度:99.8%);羟丙基-β-环糊精(西安德立生物化工有限公司,批号:120723);其他试剂均为分析纯。
1.2 仪器
85-2型恒温磁力搅拌器(上海司乐仪器有限公司);Agilent1260型高效液相色谱仪(美国Agilent公司);UV9200型紫外分光光度计(北京瑞利分析仪器厂);PB-10 pH计(Sartorious);G154DW高压灭菌锅(Zealway);DSC204/1/G动态热流式差示扫描仪(德国Phoenix公司)。
2 方法
2.1 包合物的制备
制备有效治疗浓度37.5 mg·mL-1的DS注射液。首先量取60%的注射用水,加入HP-β-CD 0.2 mol·L-1,60 ℃水浴加热溶解,冷却至室温,加入一定量的抗氧剂,搅拌至溶解,用盐酸调节溶液的pH值至4.5。再加入DS使其达相应浓度,室温下继续搅拌1 h,补足余量水,得HP-β-CD包合DS注射液:DS-HP-β-CD。
用3‰的活性炭过滤后,用0.22 μm滤膜过滤,充氮,灌封,主客体分子的摩尔比为1∶2。
2.2 包合物的鉴定
采用差示扫描量热分析法(DSC)对包合物的形成进行鉴定。各取5 mg的DS、HP-β-CD、DS和HP-β-CD的物理混合物(摩尔比1∶2)及其包合物样品,填充于铝坩埚,压盖后打孔,将其放于高温炉。以空白坩埚作为参比,升温扫描。扫描范围为50~400 ℃,升温速度为10 ℃·min-1,气氛为氮气,流速为100 mL·min-1。
2.3 包合物含量测定
2.3.1 DS包合物的紫外吸收峰位确定 根据文献[4]报道,包合物形成与否对DS的紫外吸收没有影响,游离态药物的吸收光谱与包合态药物完全重叠,因此可采用紫外分光光度法直接测定DS溶液的吸收光谱来确定包合物中DS的吸收峰位。
分别称取DS与HP-β-CD适量置量瓶中(DS用微量甲醇溶解),用水稀释至合适浓度,进行紫外扫描。
2.3.2 标准曲线的绘制 精密称取干燥至恒重的DS对照品适量,加微量甲醇溶解后,用水稀释配制成不同浓度的溶液,浓度分别为2.5,5,12.5,20,25 µg·mL-1,于276 nm波长处测定其吸光度(A),绘制标准曲线,得回归方程:A=0.031 7C+ 0.011 2,r=1。
2.4 包合比例的确定-相溶解度图的制备
量取20 mL水,分别加入0,0.02,0.04,0.08,0.1,0.2 mol·L-1的HP-β-CD,室温搅拌溶解,用HCl调节pH值至4.5,加入过量DS搅拌12 h后,取0.5 mL,8 000 r·min-1离心5 min,测定上清液中DS的量。
2.5 抗氧剂的筛选
将制备的DS-HP-β-CD注射液分成6组,分别加入不同的抗氧剂,配好后过滤、灌装、充氮、封口,于40 ℃及光照条件下(4 500±500) lx放样10 d,观察注射液的变色情况,测定pH值的变化,并用HPLC测定注射液的有关物质及含量。
2.6 DS-HP-β-CD注射液中DS含量测定方法
2.6.1 色谱条件 用十八烷基硅烷键合硅胶为填充剂,以0.02 mol·L-1磷酸二氢钾溶液(磷酸调pH值为2.5)-甲醇(32∶68)为流动相;检测波长为276 nm。理论板数按DS峰计算不低于3 000。
2.6.2 测定方法 取40 ℃及光照条件下(4 500± 500)lx放样10 d的样品适量,8 000 r·min-1离心5 min,取上清液,用甲醇稀释至合适浓度,用HPLC测定DS的含量。
2.7 DS-HP-β-CD注射液有关物质测定方法
2.7.1 色谱条件 用十八烷基硅烷键合硅胶为填充剂;以0.02 mol·L-1磷酸二氢钾溶液(磷酸调pH值为2.5,B)与甲醇(A)按1∶1混合均匀,混合后的溶液与甲醇按80∶20作为初始比例进行梯度洗脱,梯度洗脱程序见表1;检测波长为240 nm,流速为1 mL·min-1,柱温为25 ℃。
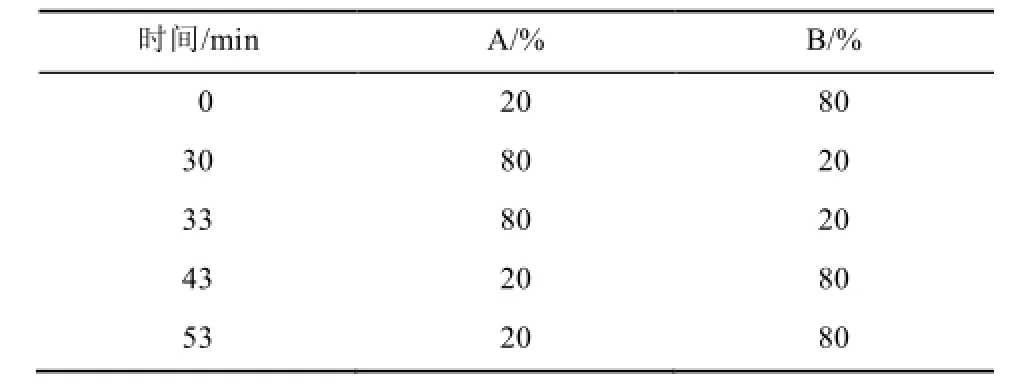
表1 梯度洗脱程序Tab 1 Program of gradient elution
2.7.2 测定法 同“2.6.2”含量测定方法。
2.8 活性炭吸附对药液pH值及含量的影响
取所制备的DS-HP-β-CD注射液两份,一份加入3‰的活性炭,于室温搅拌20 min后过滤;一份不加活性炭,分别测定药液的pH值和含量。
2.9 时间对注射液的影响
取所制备的DS-HP-β-CD注射液两份,一组不加抗氧剂作为对照组,一组加入0.5%的硫代甘油(MTG)作为抗氧剂,分别于121 ℃灭菌15 min和30 min,考察灭菌前后注射液的变色情况、pH值、含量及有关物质的变化。
3 结果
3.1 包合物的鉴定
由DS、HP-β-CD、二者的物理混合物(摩尔比1∶2)及其包合物的DSC图谱可知,DS在290 ℃表现出强烈的吸热峰,而HP-β-CD在约350 ℃处有显著的吸热峰,物理混合物中也可观察到DS和HP-β-CD的吸热峰,但是包合物中仅在约350 ℃处观察到HP-β-CD的吸热峰,DS的吸热峰消失,这表明DS以分子形式包裹于环糊精中,无结晶型存在,形成了包合物。DSC图谱见图1。
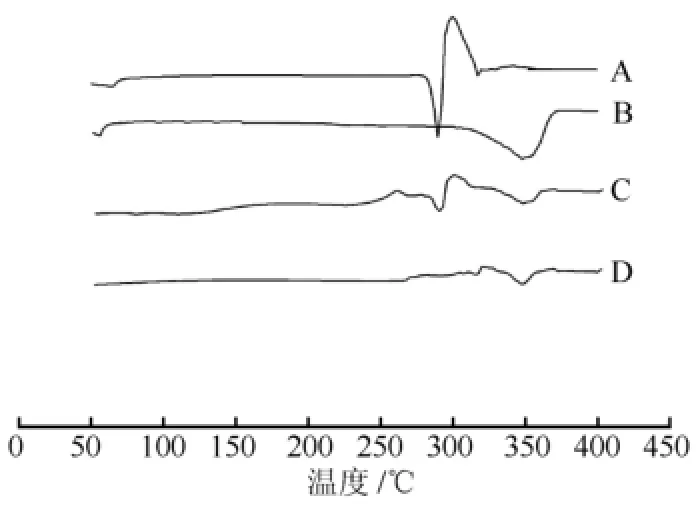
图1 DSC图谱A-DS;B-HP-β-CD;C-物理混合物;D-包合物Fig 1 DSC chromatograms A-DS; B-HP-β-CD; C-physical mixture of DS and HP-β-CD; D-DSHP-β-CD inclusion complex
3.2 DS包合物紫外吸收峰位的确定
通过紫外扫描图谱可知,DS在276 nm处有强吸收峰,而HP-β-CD在此处没有干扰。
3.3 包合物中主客体分子比例的确定
参照文献相溶解度图法[5],以DS溶解度对HP-β-CD的浓度做图,并进行线性回归,当固定DS的浓度为37.5 mg·mL-1(0.118 mol·L-1),所需HP-β-CD的浓度为0.067 7 mol·L-1。因此,当HP-β-CD的浓度大于0.067 7 mol·L-1时,可以实现对DS的完全包合,结果见图2。

图2 DS在HP-β-CD中的相溶解度图(n=3)Fig 2 Phase solubility diagram of DS in HP-β-CD(n=3)
3.4 抗氧剂的筛选
3.4.1 注射液的变色情况 分别于40 ℃及光照条件下(4 500±500)lx放样10 d。结果显示在40 ℃下放样10 d,不加抗氧剂和加抗氧剂组溶液的外观均没有发生变化,依然澄清透明,说明高温对该注射液的影响较小;在光照条件下放样10 d,除以亚硫酸钠、亚硫酸氢钠和硫代甘油作为抗氧剂组,其余各组颜色均发生不同程度的变黄,说明该注射液对于光照较为敏感,光照加速了原料药DS的氧化。结果见表2。

表2 40 ℃及光照条件下放样10 d注射液的变色情况Tab 2 Color changes of DS-HP-β-CD injection at 40℃ and light condition for 10 days
3.4.2 注射液的pH值变化 分别于40 ℃及光照条件下(4 500±500) lx放样10 d,测注射液的pH值变化。在40 ℃及光照条件下放样10 d,注射液的pH值均发生不同程度的下降,主要是由于原料药DS氧化后产生吲哚类的酸性降解产物[6];除不加抗氧剂组外,其余各组pH值仍在质量标准范围内(6.5~8.5),结果见表3。
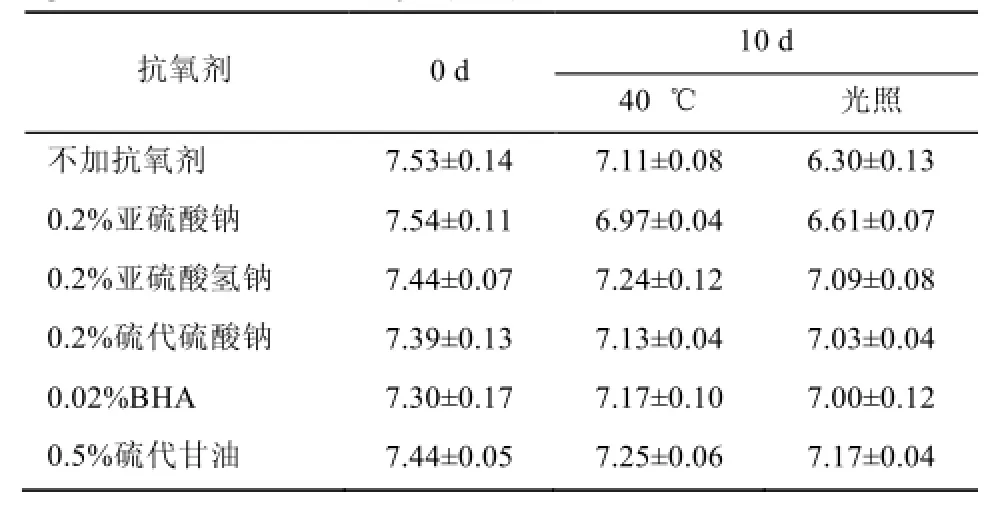
表3 40 ℃及光照条件下放样10 d注射液的pH值变化(n=3)Tab 3 pH changes of DS-HP-β-CD injection at 40℃ and light condition for 10 days (n=3)
3.4.3 注射液的含量变化 分别于40 ℃及光照条件下(4 500±500) lx放样10 d。在40 ℃及光照条件下放样10 d,各组注射液含量变化不明显,仍在质量标准范围内(93.0%~107.0%),结果见表4。

表4 40 ℃及光照条件下放样10 d注射液的含量变化(n=3)Tab 4 Assay changes of DS-HP-β-CD injection at 40 ℃and light condition for 10 days (n=3)

?
3.4.4 注射液有关物质变化 分别于40 ℃及光照条件下(4 500±500)lx放样10 d,注射液有关物质的单个杂质峰面积占主峰面积的百分比(A)见表5。
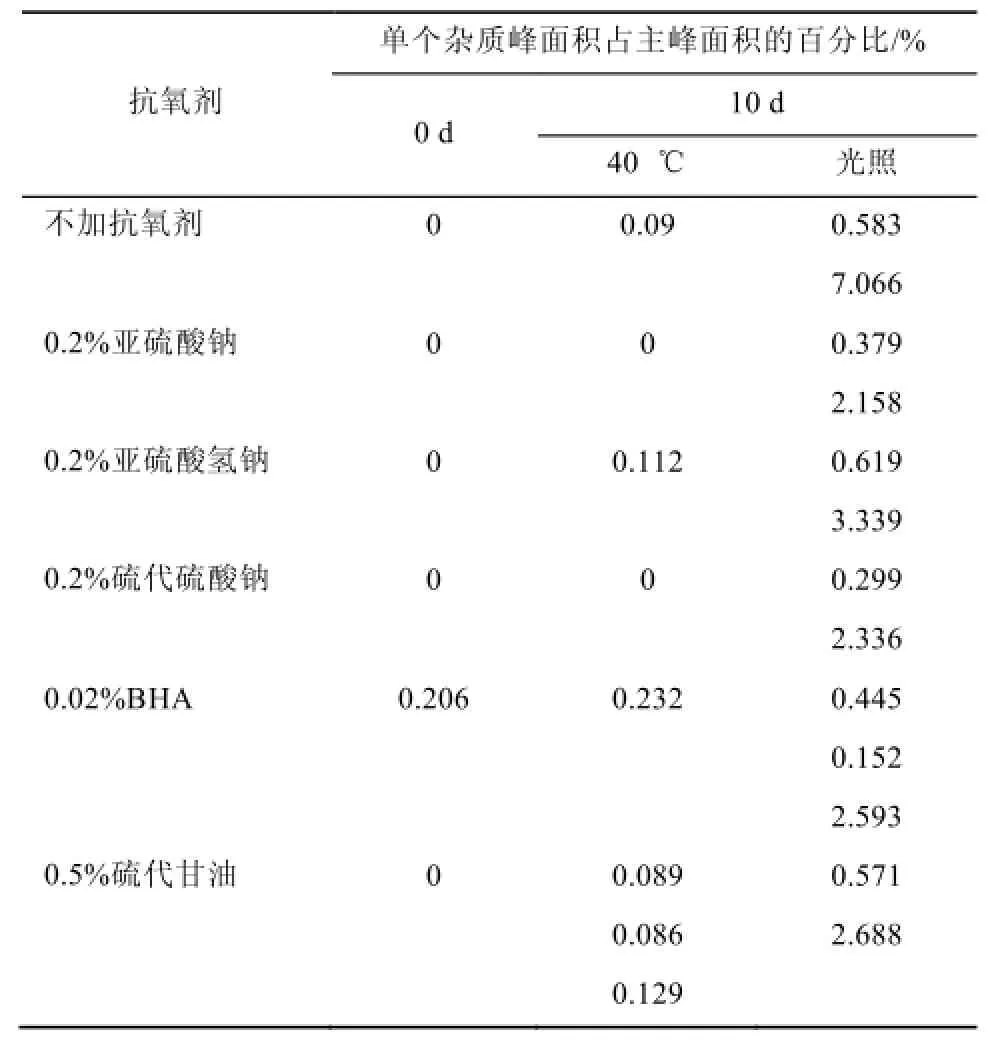
表5 40 ℃及光照条件下放样10 d注射液的有关物质变化Tab 5 Related substances of DS-HP-β-CD injection at 40 ℃ and light condition for 10 days
于40 ℃放样10 d,各组有关物质基本没增加(<0.3%),再次证明高温对该注射液影响较小;在光照条件下放样10 d,不加抗氧剂组出现7%的较大杂质峰,其余各组有关物质也略有增加,最大不超过3.5%。
3.5 活性炭吸附对注射液pH值及含量的影响
活性炭吸附对注射液的pH值基本无影响,含量下降2%,结果见表6。

表 6 活性炭吸附前后注射液pH值及含量的变化(n=3) Tab 6 pH and assay changes of DS-HP-β-CD injection before and after activated carbon adsorption (n=3)
3.6 时间对注射液外观的影响
3.6.1 不同灭菌条件下注射液的变色情况 分别于121 ℃灭菌15,30 min,加0.5%的硫代甘油组略变黄色,少量沉淀;不加抗氧剂组121℃灭菌15 min后,颜色变黄,灭菌30 min后,变成红棕色,并出现絮状沉淀。产生的絮状沉淀为DS的热压降解产物,成分复杂,有脱羧脱氢物以及多分子聚合物等,而非单一成分。
3.6.2 不同灭菌条件下注射液pH值的变化 分别于121 ℃热压灭菌15,30 min,注射液的pH值升高,可能是由于热压条件下,DS生成碱性降解产物所致,结果见表7。

表7 不同灭菌条件下注射液pH值的变化(n=3)Tab 7 pH changes of DS-HP-β-CD injection under different sterilization conditions (n=3)
3.6.3 不同灭菌条件下注射液含量的变化 分别于121 ℃热压灭菌15,30 min,注射液的含量基本没有变化,结果见表8。

表8 不同灭菌条件下注射液含量的变化(n=3)Tab 8 Assay changes of DS- HP-β-CD injection under different sterilization conditions (n=3)
3.6.4 不同灭菌条件下注射液有关物质的变化分别于121 ℃热压灭菌15,30 min,热压灭菌后,注射液的有关物质略有增加,最大不超过3%,结果见表9。

表9 不同灭菌条件下注射液有关物质的变化Tab 9 Related substances changes of DS-HP-β-CD injection under different sterilization conditions
4 讨论
DS是一种离子型化合物,为了提高包合效率,首先将溶液的pH调至酸性,使DS盐转化为双氯芬酸,双氯芬酸的脂溶性较强,与环糊精内腔的疏水性结构亲和力强,更容易被包合在HP-β-CD的空腔内,从而提高包封效率。相溶解度图显示,随着HP-β-CD浓度的增加,DS的溶解度也随之增加,但是由于HP-β-CD在体内具有一定的毒性,所以笔者选择适合注射的浓度来制备DS包合物。
稳定性结果表明,硫代甘油是DS注射液的最佳抗氧剂,这可能与硫代甘油中巯基的易氧化程度高有关,巯基的存在能在很大程度上争夺溶液中所存在的氧气,从而保护双氯芬酸不被氧化,从而提高了样品的稳定性。
除热原的常用方法就是使用活性炭或超滤的方法,而超滤本身的成本很高,操作复杂,批量小,所以在工业生产中活性炭除热原得到了广泛的应用。但是活性炭对药物略有吸附,通过活性炭吸附热原后,含量下降约2%,但仍在质量标准范围内(93.0%~107.0%);但对药液的pH值基本无影响。因此,在产业放大过程中,我们仍然可以考虑采用活性炭对药液进行除热原。
随着热压灭菌时间的延长,有关物质增加,且pH也随之升高,颜色加深,所以DS在热压灭菌时仍然存在降解的可能,目前在研究过程中采用过滤除菌法,在以后的研究和生产中,需要进一步选择合适的灭菌条件,完善整个注射剂的生产工艺。
REFERENCES
[1] QIAO M Y. Summary of development of diclofenac sodium preparation in our country [J]. Pract Pharm Clin Remed(实用药物与临床), 2010, 13(5): 379-380.
[2] MCCORMARK P L, SCOTT L J. Diclofenac sodium injection(Dyloject): in postoperative pain [J]. Drugs, 2008, 68(1): 123-130.
[3] PENKLER L J. Stable injectable diclofenac compositions: USA, 20050238674A1 [P]. 2005-10-6.
[4] ZHANG M J, WANG Z Q, WU J Y. Preparation of inclusion compound of diclofenac sodium-β-cyclodextrin [J]. Strait Pharm J(海峡药学), 2008, 20(10): 28-30.
[5] LU B. New Dosage Form and Technology of Drugs (药物新剂型与新技术) [M]. 2nd ed. People’s Medical Press, 2005: 41.
[6] KORODI T, BUKOWSKI K, LACHMANN B. Evaluation of a short stability-indicating HPLC Method for diclofenac sodium gels [J]. Pharmazie, 2012, 67(12): 980-983.
Injectable Solution of Diclofenac Sodium Cyclodextrin Inclusion
ZHUANG Jie, HU Haitao, QIAO Yanping
(Shanghai Pharmaceuticals Holding Co. Ltd., Shanghai 201203, China)
diclofenac sodium; hydroxypropyl-β-cyclodextrin; antioxidant; stability
R944.11
B
1007-7693(2013)10-1097-05
2013-02-01
庄婕,女,博士,助理研究员 Tel: (021)61871700 Email: zhuangj@pharm-sh.com.cn
ABSTRACT:OBJECTIVE To prepare diclofenac sodium injection with therapeutic concentration and high stability. METHODS Hydroxypropyl-β-cyclodextrin was used to form the inclusion complex with diclofenac sodium. The compounding rate was measured by phase solubility diagram. The optimal antioxidant and sterilization condition were selected. RESULTS The analysis showed the inclusion complex could be formed when the concentration of hydroxypropyl-βcyclodextrin was more than 0.067 7 mol·L-1. Monothioglycerol was a suitable antioxidant to stabilize the injection. Filtration should be used for terminal sterilization. CONCLUSION Hydroxypropyl-β-cyclodextrin could increase the aqueous solubility of diclofenac sodium to reach the effective therapeutic concentration. The diclofenac sodium injection prepared was stable enough to satisfy the clinical requirement.

