3种药物联合治疗晚期胃癌疗效及安全性评估
董陈诚,钟 漓,王振冉,田小林
(桂林医学院附属医院胃肠外科,广西桂林541001)
胃癌是中国发病率最高的恶性肿瘤,位居世界高发恶性肿瘤第4位[1],严重危害着人类的健康。胃癌早期症状不具有特异性,不易引起患者及医生的重视,早期诊断率较低,较大部分患者在确诊时已为晚期,错过了手术最佳时机或已无法行胃癌根治术。因此,胃癌患者晚期多采有化学治疗,胃癌对化学治疗相对敏感,可是迄今为止,对晚期胃癌尚无公认的、规范的统一化学治疗方案[2]。临床实践表明,晚期胃癌患者化学治疗效果差,复发治疗者更差[3]。因此,开发新的药物、设计新的方案已成为国内、外胃癌领域研究的热点和重点。国外许多文献报道表明,卡培他滨联合奥沙利铂是治疗胃肠恶性肿瘤疗效较好且不良反应轻的两种新药[4],近年来,国内也有不少报道已证实卡培他滨联合奥沙利铂方案治疗晚期胃癌效果显著。而贝伐单抗作为一种分子靶向药物,对其在晚期胃癌中的应用效果及安全性报道少见。本文旨在通过对38例胃癌患者采用贝伐单抗与卡培他滨联合奥沙利铂方案治疗,以观察其临床疗效及安全性,为临床晚期胃癌的科学合理用药提供参考。
1 资料与方法
1.1 一般资料 选取本科自2008年10月至2011年10月收治的38例晚期胃癌患者,其中,男22例,女16例;年龄34~65岁,平均 (54.4±13.5)岁;纳入标准:胃镜下活检及细胞学、病理学检查确诊为胃癌,根据UICCI 1997年分期均为Ⅳ期;在本次研究之前无任何放身、化学治疗;Kamofsky评分大于80分,预计生存期不低于5个月;无肿瘤相关的出血病史,且血常规检查显示,血红蛋白大于100g/L;无严重肝肾功能不全及严重心肺疾病。病理类型:低分化癌10例,高分化癌8例,黏液腺癌6例,菅状腺癌6例,中分化癌4例,印戒细胞癌3例,未分化癌1例。转移情况:肝转移10例、肺转移6例、腹腔转移3例、淋巴结转移2例,其中7例存在2个或2个以上的病灶转移。手术史:10例有1次手术史、1例有2次手术史,27例无手术史。将38例患者分为两组,19例患者采用卡培他滨联合奥沙利铂方案化学治疗,作为对照组;另外19例患者在对照组基础上加用贝伐单抗化学治疗,作为观察组,两组患者一般资料比较差异无统计学意义,具有可比性。
1.2 方法 对照组患者:第1~14天,卡培他滨2 000 mg/m2,每天分2次口服。第1天奥沙利铂130mg/m2静脉滴注,其后,每3周重复1次[5]。化学治疗前常规使用5-HT3拮抗剂及维生素B12(1 000g/d),前者可止呕,后者可保护周围神经功能。用奥沙利铂当天禁冷[6]。观察组患者:在对照组基础上第1天以7.5mg/kg贝伐单抗静脉滴注,每3周重复1次[7]。治疗期间每周监测患者血常规及肝肾功能等,每21天为1个周期,所有患者均至少连续用药2个周期。
1.3 评价标准 按照WHO实体肿瘤近期客观疗效评定标准进[8]行客观疗效评定,完全缓解(CR):肿瘤完全消失大于1个月;部分缓解(PR):肿瘤最大直径及最大垂直直径乘积缩小程度大于50%,其他病灶无明显增大;稳定(SD):肿瘤最大直径及最大垂直直径乘积缩小程度小于50%或增加小于25%;进展(PD):肿瘤最大直径及最大垂直直径乘积增加大于50%。近期客观总有效率(RR)=CR(%)+PR(%)。毒性反应按照WHO抗癌药物急性与恶急性不良反应和分级标准[8]进行判定。
1.4 统计学处理 采用SPSS17.0软件进行统计学分析处理,计量资料以±s表示,采用χ2检验,以P<0.05为差异有统计学意义。
2 结 果
2.1 两组患者近期疗效比较 观察组近期有效率为84.20%,对照组为52.63%,观察组近期有效率明显高于对照组,两组间CR、PR、SD、PD、RR比较差异均有统计学意义(P<0.05),见表1。
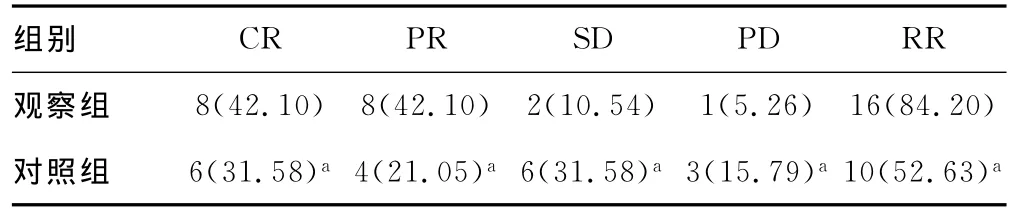
表1 两组患者近期疗效比较[n(%),n=19]
2.2 两组患者不良反应比较 两组患者不良反应均表现为骨髓抑制、口腔炎、消化道不适及周围神经毒性等,两组不良反应发生情况比较,差异无统计学意义(P>0.05),但观察组患者3例发生腹痛、腹泻,且1例腹痛明显者经相关检查确诊为胃肠穿孔,对照组患者无明显腹痛腹泻症状。观察组不良反应发生情况见表2,严重程度由轻至重按WHO抗癌药急性及亚急性毒性反应分级标准,分为0°~Ⅳ°。

表2 观察组患者不良反应发生情况(n)
3 讨 论
肿瘤的发生、发展及转移与肿瘤的血管生成密切相关[9],因此,抑制肿瘤血管生成即可对肿瘤产生抑制作用。血管内皮生长因子(VEGF)可诱导血管形成,其高水平表达与肿瘤转移及疾病预后不良密切相关[10-11]。贝伐单抗是重组人源化抗VEGF的单克隆抗体靶向制剂,可识别并结合人VEGF受体样的结合部位,发挥血管抑制作用,诱导肿瘤细胞凋亡[12]。研究表明,贝代单抗应用于晚期胃癌治疗时,不仅可抑制瘤体生长,而且还为其他化学治疗方案的治疗争取了更多的时间[13]。
目前新的有效的胃癌化学治疗方案以紫杉醇、伊立替康、卡培他滨及奥沙利铂等新药为主,口服卡培他滨抗肿瘤效果类似于氟尿嘧啶的持续输注,卡培他滨应用于晚期胃癌患者的治疗,在达到与氟尿嘧啶同等疗效的同时,避免了静脉穿刺引起的各种并发症,易被患者接受。奥沙利铂为新一代铂类衍生物,可通过产生烷化物抑制DNA的合成与复制,最终抑制肿瘤细胞增殖[14]。而奥沙利铂联合卡培他滨可发挥良好的协同作用,增强抗肿瘤效果[15-16]。
从本组研究结果可以看出,对照组患者近期总有效率(52.63%)。明显高于观察组患者近期总有效率为84.20%,差异具有统计学意义(P<0.05)。从对两组患者用药后药物毒副反应的比较结果可以看出,两组患者骨髓抑制现象差异无统计学意义(P>0.05),但观察组患者胃肠道反应明显高于对照组,主要表现为恶心、呕吐及腹痛、腹泻,观察组患者中共3例发生腹痛,且1例为3度腹痛,经相关检查确诊为胃肠穿孔。关于贝伐单抗应用时引起胃肠穿孔并发症国外已有学者报道。因此,在采用贝代单抗联合其他化学治疗方案治疗晚期胃癌时应密切观察患者症状与体征,尽早发现患者持续性腹痛症状,以便及时停药。
综上所述,贝伐单抗与卡培他滨联合奥沙利铂治疗晚期胃癌的近期疗效确切,但由于贝伐单抗可引起严重的消化道不适反应,在用药过程中,应加强病情观察,避免严重并发症的发生。
[1]王爱英,张毛讲.卡培他滨联合奥沙利铂治疗晚期胃癌的临床观察[J].中国医药导报,2012,9(6):58-59.
[2]关丽莉.卡培他滨联合奥沙利铂治疗老年人晚期胃癌36例[J].肿瘤研究与临床,2010,22(6):423-425.
[3]王卫星.卡培他滨联合奥沙利铂治疗晚期胃癌疗效观察[J].吉林医学,2011,32(16):3237-3238.
[4]田姗,李曾.卡培他滨联合奥沙利铂治疗晚期胃癌临床效果对比分析[J].中国实用医药,2011,9(4):48-50.
[5]田姗,李曾.替吉奥与卡培他滨联合奥沙利铂治疗晚期胃癌效果对比分析[J].中国老年保健医学,2011,9(4):48-50.
[6]黄小兵,崔德利.卡培他滨联合奥沙利铂治疗晚期胃癌[J].中国医药科学,2012,2(1):109-110.
[7]赵文英,陈冬云,齐全.伊立替康或奥沙利铂联合卡培他滨治疗晚期胃癌的疗效比较[J].中华肿瘤杂志,2011,33(4):295-298.
[8]蒋代文,蔡君,李爽,等.奥沙利铂联合卡培他滨治疗晚期胃癌的临床观察[J].现代肿瘤医学,2010,18(5):972-973.
[9]陆锡燕,周长芳,陈雷.紫杉醇联合奥沙利铂和卡培他滨治疗晚期胃癌的临床观察[J].临床肿瘤学杂志,2010,15(11):1023-1025.
[10]Liu SV,Gollard R,Iqbal S.Case report of perforation of an ileal neobladder after treatment of rectal Cancer with bevacizumab and comment on mechanisms of intestinal perforation associated with bevacizumab[J].J Clin Pharm Ther,2012,37(5):607-609.
[11]王磊,胡冰,季楚舒,等.XELOX与FLO方案治疗晚期胃癌的近期疗效及毒副反应比较[J].安徽医药,2011,15(3):329-330.
[12]倪田根,关泉林,王娜,等.贝伐单抗联合化疗一线治疗转移性结直肠癌有效性和安全性的系统评价[J].肿瘤,2010,30(3):232-238.
[13]赵静,李航,张力,等.四例贝伐单抗所致肾损害临床和病理特征分析[J].中国医学科学院学报,2012,34(2):153-158.
[14]赵静,张文,李文桦,等.贝伐单抗联合化疗治疗晚期结直肠癌的临床观察[J].中国癌症杂志,2011,21(10):799-802.
[15]Díaz-Rubio E,Gómez-España A,MassutíB,et al.Firstline XELOX plus bevacizumab followed by XELOX plus bevacizumab or single-agent bevacizumab as maintenance therapy in patients with metastatic colorectal Cancer:The phase III MACRO TTD study[J].Oncologist,2012,17(1):15-25.
[16]袁媛,于静,张昊,等.小剂量奥沙利铂联合卡培他滨治疗老年晚期胃癌患者疗效观察[J].山东医药,2010,50(52):52-53.

