高分子化学教学中有机化学知识的融通实践
陈静侯文华
(1南京工业大学理学院应化系 江苏南京210009;2南京大学化学化工学院 江苏南京210093)
高分子化学是研究高分子化合物合成和化学反应的一门科学[1]。其中,合成部分涉及高分子化合物的合成反应和机理以及高分子的分子结构、相对分子质量及其分布等;而化学反应部分则涉及高分子的化学反应。高分子化学作为化学、化工、材料及相关专业的一门专业必修课或选修课,通常在大三或大四开设。从课程内容看,它与之前的有机化学和物理化学课程密切相关。因此,学好高分子化学,不仅有助于学生对已学过的有机化学和物理化学课程的理解和把握,夯实所学的基础知识,而且还可进一步加强和充实所建的知识框架,为今后的学习和工作打下良好的基础。鉴于此,在高分子化学课程教学中,我们注意通过从学生已有基础知识点切入,与所授高分子化学知识融通,提高学生的学习兴趣。通过强调课程间的相互联系,充分发挥学生已学过的有机化学和物理化学等先期课程的优势,即,利用学生在以前课程中学到的知识,使学生能快速、深入理解本课程内容,并将所学知识进行交叉融合、融会贯通、触类旁通,而不仅仅是将知识局限在每一门具体的课程中,从而培养学生的创新思维。本文根据作者多年来的教学实践和经验,介绍在高分子化学课程教学中进行相关的有机化学知识融通的一些做法和体会。
1 有机官能团和聚合反应
高分子化合物通常由单体(有机小分子)通过聚合反应制备而得。聚合反应有缩聚和加聚两大类。通过缩聚反应可得缩聚物,如对苯二甲酸和乙二醇合成聚对苯二甲酸乙二醇酯(涤纶)、己二酸和己二胺合成聚己二酰己二胺(尼龙-66),都是带有官能团的单体之间经多次缩合去小分子而成。通过加聚反应可得加聚物,如氯乙烯合成聚氯乙烯、苯乙烯合成聚苯乙烯,都是通过烯类单体的双键进行加成聚合而成。在授课时,首先通过系统复习与两类单体相关的有机化学基础知识,以便学生充分了解此类有机化合物的结构和性质,再进一步讲清楚两类单体在聚合反应中的应用特性,使学生很快理解并掌握聚合反应的特点和实质。缩聚和加聚是两类不同性质的聚合反应,所得聚合物的结构和性能也不相同。缩聚是由含二个或二个以上官能团的单体通过各种缩合反应,去掉某些小分子而成,为平衡反应,属于逐步聚合,要有高的基团反应程度(>98%)才可得到高分子化合物,有副反应;而加聚是烯类单体在引发剂或光照等的作用下,通过双键断裂(即π键打开)相互加成而得,聚合反应中无小分子生成,属于连锁聚合,一旦引发,即能很快形成高分子化合物,但需提高反应的转化率,且所得聚合物多属于碳链聚合物。如,常见的缩聚物有玻璃钢(单体为马来酸酐和乙二醇)、聚碳酸酯(单体为光气和乙二醇),它们的合成均是由含两个官能团的单体,通过去除某些小分子缩合而得。而常见的加聚物则有有机玻璃(单体为α-甲基丙烯酸甲酯)、聚四氟乙烯(单体为四氟乙烯)、聚丙烯腈(单体为丙烯腈),它们均由烯类单体经过加聚而得。
接着,在此基础上,进行应用拓展。如,导电高分子聚乙炔的合成及导电原理,其聚合属于加聚还是缩聚?所得聚合物的顺式和反式两种异构体结构是什么样的?导电高分子聚乙炔是通过由一个σ键和两个π键组成的乙炔三键的π键打开加聚而成,其形成的顺、反式异构体见图1,其导电原理是聚乙炔主链上含有交替的单键和双键,从而形成了大的共轭π体系。π电子的流动产生了导电的可能性。
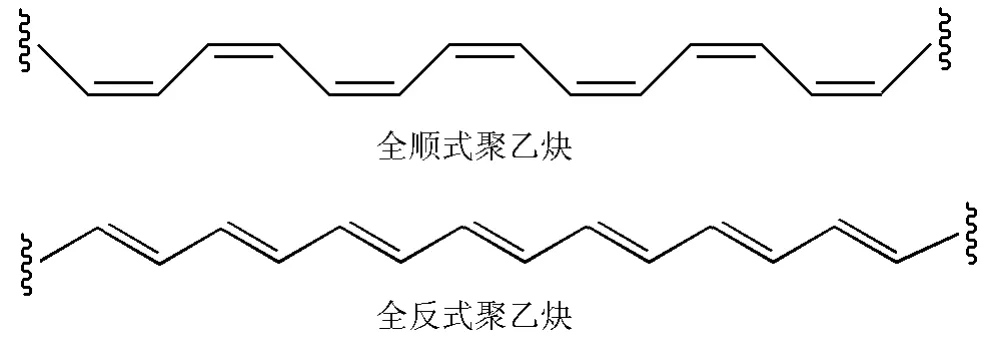
图1 聚乙炔的顺式和反式异构体
再如可降解的生物塑料聚乳酸(PLA)的合成和应用。聚乳酸的合成有化学合成法和微生物发酵法两种,化学直接缩聚合成反应式见图2。
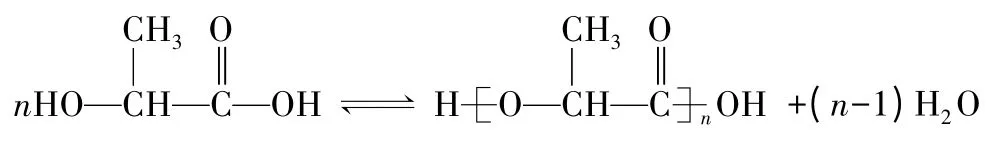
图2 聚乳酸直接缩聚合成反应
从反应式可以看出,聚乳酸的合成是通过乳酸(2-羟基丙酸)分子间脱水缩聚成酯而成,水的有效脱除是形成聚合物的关键。由于聚乳酸是通过酯键形成而得,故其降解也是以酯键断裂为基础的[2]。通常高分子化合物具有电绝缘性和不可降解性。上述实例可开阔学生的眼界。
通过上述的系统学习、对比讲授及相关实例的拓展,学生学习兴趣和热情大增,对高分子学科的基本知识也有了初步的认识。最后,通过作业,进一步让学生复习和巩固所学的有机化学和高分子化学知识,从而达到融通的效果。选择的作业有:(1)以丙酮为原料合成有机玻璃的单体α-甲基丙烯酸甲酯,并写出相应的聚合反应方程式;(2)以1,3-丁二烯为原料合成尼龙-66的单体——己二酸和己二胺,并写出相应的聚合反应方程式;(3)写出聚乙炔的聚合方程式,所得聚合物有顺式和反式两种,请写出其结构式,并解释其导电原理。
2 电子效应和单体的聚合机理
在自由基聚合章节中,烯类单体对聚合机理的选择性涉及到单体分子结构中双键所连基团的电子效应。电子效应包括共轭效应和诱导效应。通常连有吸电子基团的烯类单体(如硝基乙烯)易进行阴离子聚合;而连有给电子基团的烯类单体(如烷基乙烯基醚和异丁烯)则易进行阳离子聚合;由于卤素的弱吸电子性,连有卤素的烯类单体(如氯乙烯)易进行自由基聚合;而苯乙烯和1,3-丁二烯则由于基团的共轭特性,3种机理均可。
课程开始后,首先让学生回忆有机化学课程中学过的电子效应概念。大部分学生反应较茫然,少部分只是有点印象,而具体内容已不是很清楚了。于是,我们引导学生比较苯甲醚、苯、甲苯、氯苯及硝基苯进行亲电取代反应的活性,学生很快得到了活性次序:苯甲醚>甲苯>苯>氯苯>硝基苯。因为在此前的有机化学课程学习中,这部分内容是重点,于是,进一步分析。由于取代基团的给电子性能,苯甲醚和甲苯均较苯容易发生亲电取代反应。甲氧基具有p-π共轭给电子效应,其给电子效应很强;甲基是通过超共轭效应给电子,其给电子效应较甲氧基要弱。硝基则具有强的吸电子诱导效应和共轭效应,故硝基苯较苯难于发生亲电取代反应。氯苯中氯原子的情况比较特殊,由于氯的电负性大于碳,具有吸电子诱导效应,但氯上的未共用p电子对又具有p-π共轭给电子效应,两者相抵后,氯表现为弱吸电性,导致氯苯较苯更难发生亲电取代反应,但比硝基苯容易[3-4]。
以上结果正好解释烷基乙烯基醚和异丁烯由于双键所连基团的给电子性能,使带正电的活性中心稳定,从而易发生阳离子聚合。硝基的吸电子性使带负电的活性中心稳定,故硝基乙烯易发生阴离子聚合。而氯的弱吸电性既不能使带正电的活性中心稳定,也不能使带负电的活性中心稳定,只能使自由基活性中心稳定[1],故氯乙烯适合自由基聚合。而在苯乙烯和1,3-丁二烯中,由于基团苯和双键的共轭特性,正电、负电及自由基的活性中心均稳定,故3种机理均可。
通过融入上述生动的有机化学实例,不仅使学生巩固了有机化学知识,拓展了电子效应的应用,而且还提高了学生对高分子单体聚合机理的选择判断能力。最后,再通过补充例子,如异戊二烯(自由基、阴离子、阳离子3种机理均可,原因同1,3-丁二烯),氟乙烯(自由基聚合,原因同氯乙烯),偏二氯乙烯(自由基、阴离子聚合,两个—Cl使吸电子诱导效应增强[5]),丙烯腈(自由基、阴离子聚合,原因是—CN为吸电子基团),偏二腈乙烯(阴离子聚合,两个—CN的吸电倾向过强,同硝基乙烯[1]),丙烯(比较特殊,不能进行自由基、阴离子、阳离子聚合,只能进行特殊的配位聚合。因为只有一个甲基给电子,作用弱,不能进行阳离子聚合,如采用自由基聚合,则因自由基容易从丙烯分子中夺取氢原子,形成稳定的低活性烯丙基自由基,故只能得到低聚物[6]),指导学生举一反三,从而使学生能很快地掌握该部分内容。
3 高分子化合物的合成与改性
高分子化合物的改性是高分子化学课程中的重要教学内容之一。改性的主要目的是提高高分子材料的性能和引入功能,制备新的聚合物,扩大应用范围。常用的改性方法有共聚、聚合物的化学改性等,其中涉及到很多与有机化学相关的知识,且融有很多新要素,是有机化学知识在高分子学科中的应用和拓展。
例如,在共聚合章节中,第一单体通过与第二、第三单体的共聚,可以改进高分子的结构和性能,增加品种,从而满足人们的多种需要。聚合物性能改变的程度与共聚单体的种类、数量以及排列方式有关。以聚氯乙烯为例,其为一种脆性材料,塑性差,且存在抗老化能力弱、热成型变色等问题。将氯乙烯与醋酸乙烯酯共聚可得氯-醋共聚物。若共聚了5%的醋酸乙烯酯,则增加了材料的柔性,产品可用作制管、薄板;共聚了13%的醋酸乙烯酯,增加了塑性和溶解性能,产品可用作塑料和涂料;共聚了50%的醋酸乙烯酯,产品可用作人造革。若与40%的丙烯腈共聚,产品的极性、耐油性和耐溶性增加,可用作过滤材料;与丙烯共聚,热稳定性增加,可用于无毒包装材料;与85%偏二氯乙烯共聚,可提高气密性,用作阻透塑料。综上,通过共聚,可减少聚氯乙烯的缺陷,增加产品的种类,扩大应用范围[1,6]。从有机化学的角度来看,由于新单体的引入,即引入了新的有机官能团,它们本身各有特性,通过共价键与单体氯乙烯相互连接,能够改善聚氯乙烯大分子的结构和性能。此外,若将丁二烯与苯乙烯无规共聚,可得到丁苯橡胶;若进行嵌段共聚,则得到SBS热塑性弹性体。即共聚单体在形成聚合物大分子中的排列方式不同,也会影响产品的性能。
共聚还可将一些自身难以均聚的单体作为共聚单体,从而扩大合成聚合物的原料范围。如顺丁烯二酸酐为1,2-双取代烯类,由于位阻效应加上结构对称,极化程度低,难以均聚,但却易与苯乙烯共聚,制备苯乙烯-顺丁烯二酸酐无规共聚物,用作工程塑料;亦可改变合成条件,制备交替共聚物,用作悬浮聚合的分散剂。从有机化学的电子效应不难理解,在共聚反应中,单体苯乙烯由于苯基的共轭特性,很容易进行阳离子、阴离子及自由基聚合形成均聚物;但在与顺丁烯二酸酐的共聚中,主要是利用了苯环的给电子效应和顺丁烯二酸酐的吸电子效应,即极性效应相匹配,而一般极性相匹配的单体易于共聚。
以上知识融通的实例,能使学生充分了解有机官能团分子结构的特性、电子效应及空间效应在高分子合成与改性中的作用。有机小分子单体的结构和分子特性与所合成的聚合物的性能密切相关。通过控制共聚物的组成与结构,根据小分子单体的结构特性,可以设计合成新的聚合物材料。学生可从中体会到有机小分子与高分子材料之间的关联和奥妙,有助于提高学习兴趣。
具有特殊性能的立构规整的等规聚丙烯、间规聚苯乙烯及顺丁橡胶聚合物等的合成,更是与有机化学密切相关,一些内容在有机化学课程的烯烃和二烯烃章节中有相关介绍[3-4]。等规聚丙烯、间规聚苯乙烯及顺丁橡胶是通过著名的Ziegler-Natta催化剂进行定向聚合而得(Ziegler和Natta因此获得了诺贝尔化学奖)。由丙烯和苯乙烯聚合而得的聚合物属于对映异构,而由1,3-丁二烯聚合而得的聚合物属于几何异构(顺反异构)。对于丙烯和苯乙烯单体,由于含有平面双键,有对称面,为非手性分子。但一旦聚合成聚合物,双键打开,就有手性中心(C*,即不对称碳)产生,因此高立构规整的等规聚丙烯、间规聚苯乙烯必须用特殊的催化剂才能得到就不难理解了。对于1,3-丁二烯聚合生成顺丁橡胶,由于1,3-丁二烯为共轭体系,单体可进行1,2-和1,4-加成,可能会有顺、反1,4-和全同、间同1,2-聚丁二烯4种立体构型异构体。要想得到有序的顺1,4-加成聚合物,即顺丁橡胶,同样需要使用特殊的催化剂才能实现。由于学习这部分内容需要很强的空间思维想象能力,加上手性、光学活性、顺反异构、几何异构等一些特殊概念的引入,学生往往不容易学懂。对映异构内容一直是有机化学的教学难点之一,配位定向聚合同样也是高分子化学教学的难点。所以,如能结合有机化学中的基础知识和概念进行讲授,学生就会学得有兴趣,学得有感觉。因为,从聚合产物来说,得到了一类具有特殊功能的高分子材料;就聚合方法来说,是一种特殊的定向配位聚合;就单体结构和聚合产物来说,从无立体异构的小分子合成得到了具有一定光学或几何异构的立构规整高分子。
在聚合物的化学反应章节中,也涉及到高分子化合物的改性,同样融有很多新知识。首先,以聚乙烯醇的合成为例。由于乙烯醇不稳定,易发生酮式、烯醇式重排生成乙醛,故不能直接合成,必须先合成聚醋酸乙烯酯,再经过醇解或水解来制备。其次,所得聚乙烯醇含有大量的羟基,具有一定的亲水性,能溶胀,要将其制备成重要的维尼纶织品,须将其羟基缩醛化,以降低它的亲水性。在此处给学生布置相关的作业:以乙炔为原料合成聚醋酸乙烯酯;从聚醋酸乙烯酯到维尼纶纤维,需要经过哪些反应?其目的是什么?并写出相应的反应方程式。
再如纤维素的改性。在有机化学课程的碳水化合物章节中有关于纤维素改性的介绍[4],但由于纤维素属于多糖,且有机化合物的授课重点主要在单糖的结构和反应性能上,故对纤维素往往是一带而过,导致学生印象很淡,容易遗忘。而在高分子化学的教材上[1],纤维素只是以—OH代替,并未写出其是由β-D-葡萄糖通过β-1,4-苷键相连而成的直链聚合物(见图3)。这样会使学生学得有些茫然,只知道纤维素富含羟基,可通过羟基进行改性,与酸作用成酯,制备硝化纤维和醋酸纤维,成醚得羧甲基纤维素等。在课程接近尾声时,学生通过之前的有机化学知识复习,已感觉大不一样了。因此,我们要求学生通过复习相关的有机化学内容,自己来讲解纤维素的结构,何为D?何为β?何为1,4-苷键?实际上,在开链式中,单糖分子中距离羰基最远的不对称碳原子与D-(+)-甘油醛的不对称碳原子构型相同时,称为D型糖;反之,称为L型。在开链式结构转化成六元环半缩醛氧环式结构时,既可形成α-异头体,又可形成β-异头体,而分别得到α-D-葡萄糖和β-D-葡萄糖(图4)。通过这样的授课实践,可使学生既巩固了知识,又培养了创新意识。
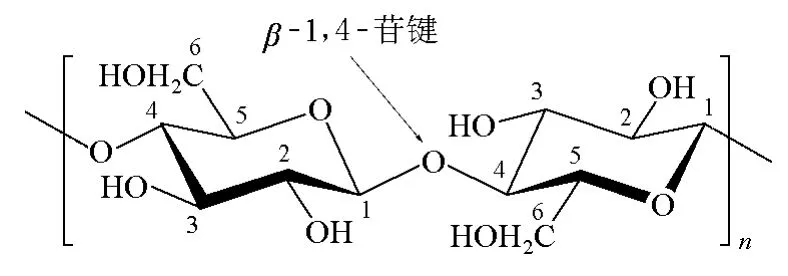
图3 纤维素的单体结构
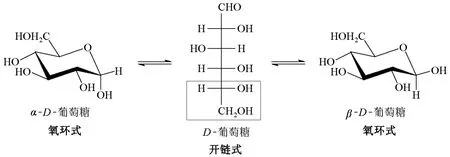
图4 D-葡萄糖的开链式和氧环式结构
总之,通过在高分子化学课程教学中融通相关的有机化学知识,激发了学生的学习兴趣和动力,进一步夯实了之前所学的有机化学基础知识,有效地提高了教学效果。
[1]潘祖仁.高分子化学.第5版.北京:化学工业出版社,2011
[2]李凡,王莎,刘巍峰,等.微生物学报,2008,48(2):262
[3]邢其毅,徐瑞秋,周政,等.有机化学.第2版.北京:高等教育出版社,1993
[4]徐寿昌.有机化学.第2版.北京:高等教育出版社,2002
[5]贾红兵.高分子化学导读与题解(与第4版配套).北京:化学工业出版社,2010
[6]张兴英,程珏,赵京波.高分子化学.北京:中国轻工业出版社,2000

