医疗器械溶血性能三种评价方法的比较
国家食品药品监督管理局济南医疗器械质量监督检验中心;山东省医疗器械生物学评价重点实验室(济南市 250101)
人体血液是由55%~60%的血浆和40%~45%的血细胞(红细胞、白细胞、血小板)组成的。红细胞的机能是运送氧气到身体各部,并将代谢产生的二氧化碳送到肺部随呼气而排出体外。血浆中的90%是水,其余为白质、钠、钾、激素、酶等人体新陈代谢所需要的物质,维持人体正常生命活动。红细胞胞质内充满血红蛋白,约占红细胞质量的33%,它具有结合与运输O2和CO2的功能,红细胞的渗透压与血浆相等,使出入红细胞的水分维持平衡。当血浆渗透压降低时,过量水分进入细胞,细胞膨胀成球形,甚至破裂,血红蛋白逸出,丧失其功能,称为溶血。引起溶血的原因有机械力如压力和流变以及生物化学等方面的因素,溶血的发生在临床上可能带来一些不利影响,如可能导致肝脏和肾脏的严重损伤及血栓的形成,对脑或其他器官产生继发损害。
ISO-10993.4[1]中指出溶血是一项很有意义的筛选试验。在试验操作规范的情况下,血浆血红蛋白量升高指示溶血并反映出在与材料和器械接触中红细胞膜的易破裂性。与循环血液接触的器械或器械部件常规需要进行溶血性能的评价,能够评价溶血的方法有很多种,有体内、半体内和体外与血液或血液成分接触方法,但常见的是采用体外法。体外试验一般用于评价红细胞损伤,有直接法和间接法。直接法可测定由于物理和化学因素对红细胞影响导致的溶血,间接法测定试验样品浸提物导致的溶血。ISO-10993.4 中列出了溶血试验的总则、可选择的血红蛋白总量测定和血浆或上清液血红蛋白浓度的测定方法,但并没有具体描述试验过程以及选择试验方法的原则,所以各个医疗器械检测和评价机构根据自己实验室的检测水平选择的检测方法有所不同。
目前国际上明确的、公认的用于评价医疗器械或医疗器械材料的溶血性能的方法主要有三种:NIH(National Institutes of Health,国家健康机构)法[2]、ASTM(American Society for Testing and Materials,美国材料与试验协会)F756-2008[3]和MHLW(日本劳动健康福利局)[4]的溶血方法。本文对此三种方法方法进行总结比较,分别列出了他们在处理样品、检测原理、检测方式等一些指标方面的特点。
1.一般情况比较
三种方法都是通过分光光度计法,在波长540nm 或545nm 处测定试验样品或其浸提液接触的血液上清液的吸光度值,通过计算溶血率来评价溶血的程度。对比参照方面三者有些不同:NIH 采用0.1%碳酸钠溶液与生理盐水作为阳性与阴性对比参照,ASTM 方法和MHLW 方法都采用注射用水作为阳性对照,但采用的阴性对照则不同:前者是CMF-PBS,后者是生理盐水。实验试剂方面:NIH 方法不采用其他实验试剂,ASTM 方法采用血红蛋白标准品与氰化正铁血红蛋白作为试剂,MHLW 方法采用Drabkin’s Reagent 作为试剂。具体情况见表1。

表1.三种溶血试验方法一般情况比较
2.血源比较
三种方法都要求采用新西兰白兔,MHLW 对白兔的要求更为细致,但三种方法所使用的抗凝剂和对血液的处理完全不同。NIH 采用8mL 兔血,用草酸盐抗凝,并用10ml 生理盐水进行稀释,通过测定其与碳酸钠混合物的吸光度判断其可用性。ASTM 方法要求3 只兔子分别抽取5ml 血液进行混合,用柠檬酸盐抗凝,需要对血液的血红蛋白含量进行测定和调整。MHLW 方法对血源要求较具体,对兔子的种类、月龄、体重和健康状况等要求详细,并且要对血液进行处理使其去纤维蛋白,通过测定吸光度判断去纤维蛋白血源的可用性。具体情况见表2。

表2.三种溶血试验方法的血源比较
3.样品处理方法比较
三种方法的试验温度都是37 ±2℃。NIH 和ASTM 都有直接接触和间接接触两种方法,可以根据器械本身和其将来使用的条件选择试验,而MHLW 则直接采用间接接触法。采用间接接触方法进行试验时的浸提液制备方法都按照ISO-10993.12 执行。ISO-10993.12 是国际标准委员会制定的关于医疗器械生物学评价样品制备和参照样品的指导性标准。直接接触法时,NIH 一般采用5g 样品10ml 生理盐水的比例,ASTM 则采用42cm2或21cm2或1.4g 样品加7ml CMF-PBS 的比例。浸提时间方面:NIH 方法浸提时间最短,与血液接触的时间是60min,ASTM 的接触时间是至少3h,而MHLW 方法与其他两种最大的区别是样品与血液接触时间为4 个时间点,分别是1h、2h、3h 和4h。结果测定:对于NIH 方法规定阳性对照的吸光度值应≥ 0.850,阴性对照的吸光度值应<0.100,否则应重新试验。其他两种方法未做要求,但是都要用到特定的试剂。具体情况见表3。

表3.三种溶血试验样品处理方法比较
4.结果计算和判定方法比较
NIH 法和MHLW 比较相似,同时测定阴性对照和阳性对照的吸光度值,换算出标准化的溶血率,根据溶血率大小判断器械或其浸提液是否具有溶血特性。只是在NIH 的间接接触法应用时去除了浸提液(不与血液接触)的本底值。ASTM 方法通过测定样品吸光度和接触样品前全血的吸光度,同时去除空白管的吸光度值而计算出溶血率,实际计算出的结果是游离血红蛋白的含量占总的血红蛋白的百分比。三者的具体计算方式和结果判定方法见表4,可以看出MHLW 法在结果判定方面较其他两种方法分级多,分为5级,且溶血率的分级区间也比较大。具体情况见表4。
综合以上比较结果可以看出:NIH 法在应用方面因为试验时间短,没有应用特定试剂而最省时省力,且节约成本。而且使用间接接触法测定结果时,因为去除了浸提液(不与血液接触)的本底值,这样可以去除医疗器械或材料浸提物颜色的干扰,客观评价这类器械或材料的溶血性能。MHLW 方法除了在血源方面的处理和孵育时间方面与其他两种方法有差异外,其与NIH 方法基本相似。ASTM 方法对血浆血红蛋白进行定量测量,试验过程较其他两种方法复杂,应用了血红蛋白标准品和氰化正铁血红蛋白试剂,为所有使用该法的实验室提供了可比性。该方法的主要缺点是使用氰化物溶液存在潜在的健康风险。氰化试剂在各种接触方式下都具有毒性,并且遇酸释放 HCN,试剂和产品的处置比较麻烦而且费用较高。
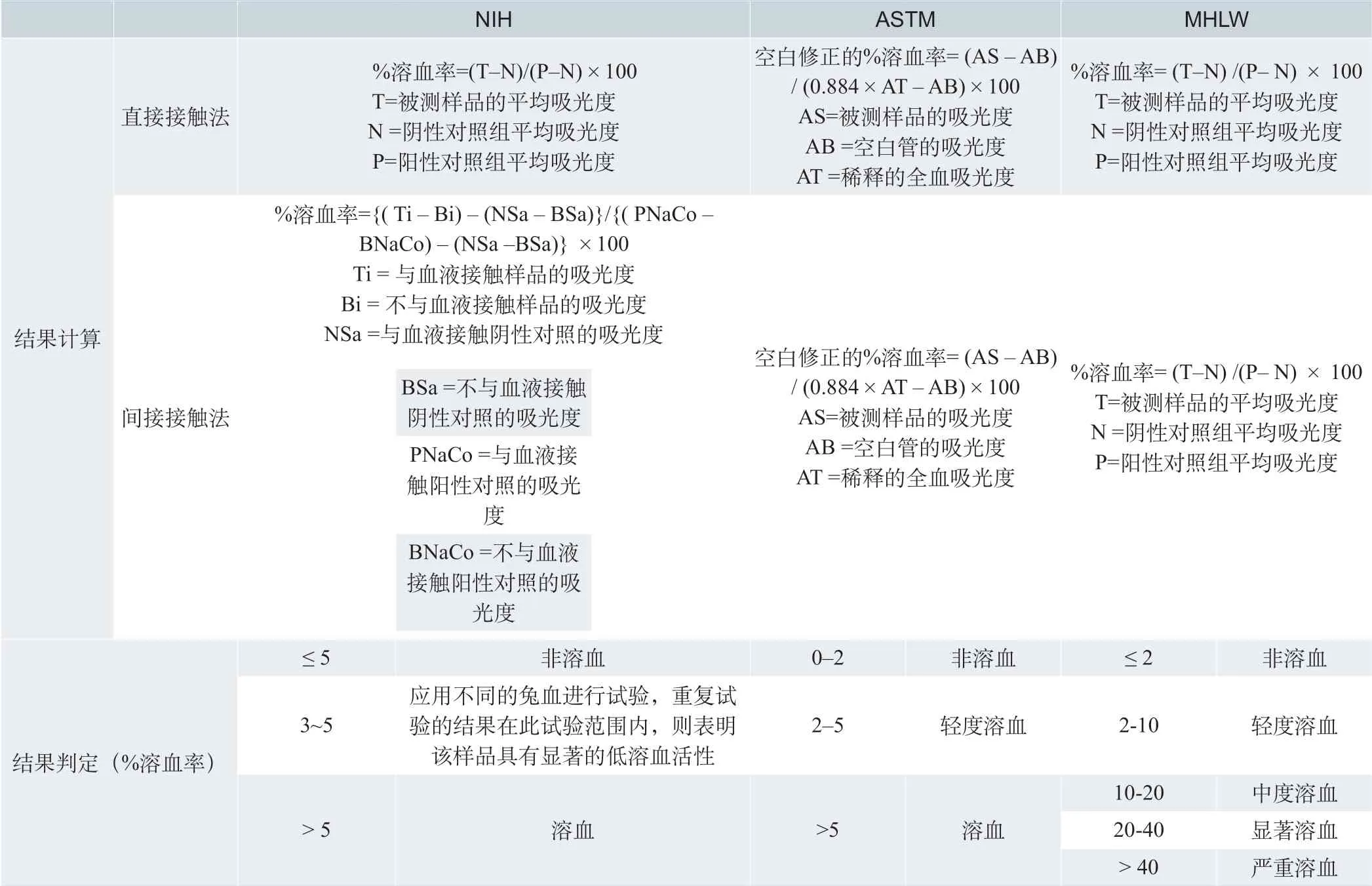
表4.三种溶血试验结果计算和判定方法比较
以上对三种方法的比较是基于目前公认的试验步骤而进行的,在实际被各个实验室应用的过程中会有一些轻微变动如对于血液的收集,有报道[6]称ASTM 方法采用一只兔的血液是可行的,再如NIH 法的阳性对照采用注射用水或者是对血液的处理进行简化,只对阳性和阴性对照的吸光度范围做出要求[7~8]。
虽然三种方法在国际上应用比较广泛,但是使用标准材料对这三种方法的比较研究是不完全的或不存在的。为了给这三种方法结果的互换性提供全面的比较信息,ISO/TC194 工作组正在组织国际上影响力较大的实验室(Nelson、NAMSA、WuXi AppTec、Caridian BCT、Gambro、BD 、日本和我中心)进行溶血比对试验(Round-robin)[9]。由工作组总结讨论影响试验结果的各项因素,对三种试验方法的细节进行优化、规定,决定采用统一的材料(高、中、低溶血性材料)、统一的浸提条件(温度、时间、浸提比例和浸提介质)、统一的血液来源(兔血和人血)、统一的抗凝剂等方面的因素来进行这次比对试验。此次比对试验通过使用共同的医疗器械(公认的非溶血、低溶血和溶血性材料)和对照材料,比较三种试验方法的结果是否一致,是否符合材料的溶血性能预期,同时也比较各个试验方法和血源(兔或人血)及不同实验室之间的一致性问题。最终会将此三种方法的具体过程列入新一版的ISO-10993.4 中,能更直接明确地指导医疗器械或医疗器械材料的溶血性能评价。
[1]ISO 10993-4:2002/Amd 1:2006.Biological evaluation of medical devices -Part 4:Selection of tests for interactions with blood.
[2]National Institutes of Health.Evaluation of hemodialyzers and dialysis membranes.Report of a Study Group for the Artificial Kidney-Chronic Uremia Program NIAMDD-1977.Chapter two.In vitro characterization of hemodialyzers.ArtifOrgans 1977;1(2):59-77.
[3]ASTM F 756-08.Standard Practice for Assessment of Hemolytic Properties of Materials.
[4]Ministry of Health,Labour and Welfare(MHLW),Japan:Testing Methods to Evaluate Biological Safety of Medical Devices, Notice from the office medical devices evaluation number 36,2003
[5]ISO 10993-12,Biological evaluation of medical devices -Part 12:Sample preparation and reference materials
[6]张伶俐, 朱蔚精,谭言飞,等.生物材料溶血性标准化评价方法比较:溶血率法和氰化高铁血红蛋白法[J].生物医学工程学杂志,2004,21( 1):111-114
[7]GB/T 16175-1996,Organic silicone material for medical use -Biological evaluation test methods.
[8]GB/T 14233.2-2005 医用输液、输血、注射器具检验方法 第2 部分:生物学试验方法
[9]ANSI/AAMI/ISO 10993-4:2002(R2009)&A1:2006(R2009)Biological Evaluation of Medical Devices-Part 4:Selection of tests for the interaction with blood.Association for the Advancement of Medical Instrumentation.Arlington,VA.Hemolysis Round Robin Draft Protocol

