孔结构渐变聚己内酯/羟基磷灰石仿生骨材料
唐 俊,周 斌,杜 艾,张志华,沈 军,夏 琰,许硕贵
(1.同济大学上海市特殊人工微结构材料与技术重点实验室,上海200092; 2.上海市第二军医大学附属长海医院骨科,上海200433)
孔结构渐变聚己内酯/羟基磷灰石仿生骨材料
唐 俊1,周 斌1,杜 艾1,张志华1,沈 军1,夏 琰2,许硕贵2
(1.同济大学上海市特殊人工微结构材料与技术重点实验室,上海200092; 2.上海市第二军医大学附属长海医院骨科,上海200433)
为获得具有类似人骨的渐变孔结构、力学性能良好的羟基磷灰石(hydroxyapatite,HA)/聚己内酯(polycaprolactone,PCL)仿生骨材料,采用水热法制备了HA粉末,通过溶剂共混法将其与PCL复合,并采用浇铸/NaCl微粒浸出法制备了多孔状HA/PCL复合材料.通过控制造孔剂NaCl的粒径和用量得到了不同孔径、不同孔隙率的HA/PCL复合材料及具有渐变孔结构的HA/PCL复合材料.利用光学显微镜观察了其孔结构,结果为孔径在100~300 μm,最大孔隙率达到80%.同时研究了它们在人体体温附近(37±5)℃的力学性能,结果表明渐变孔结构的HA/PCL复合材料的力学性能较单一孔结构的HA/PCL复合材料有了很大的提高.通过梯度造孔不仅可获得与人骨极为类似的多孔仿生材料,同时还可大幅提高多孔材料的力学性能.关键词:复合材料;羟基磷灰石;聚己内酯;孔结构;仿生;力学性能
羟基磷灰石(hydroxyapatite,HA)是人骨中的主要无机成分,具有优良的生物活性和生物相容性[1],广泛应用于骨骼系统修复和重建,然而纯的HA脆性大、易断裂、加工难,限制了其作为硬组织修复与替代材料的应用.为克服HA的上述缺点、提高材料的可塑性及力学性能,将其与有韧性的医用高分子材料复合,制备生物活性无机/有机纳米复合材料受到了人们的广泛关注,尤其是可生物降解的羟基磷灰石/聚合物复合生物材料[2-3].医用高分子材料聚己内酯(PCL)具有优越的生物可降解性[4-5]、良好的生物相容性,同时还具备优越的力学性能,因此是优良的高分子复合材料.有关HA与PCL的复合,一般而言,在不考虑复合材料力学性能的前提下,HA颗粒在复合材料中分散越均匀、含量越高,材料的生物活性就越好[6].
多孔状结构可以增加材料的表面积,在材料植入体内后有利于材料和体液充分接触,加快材料的降解,同时多孔材料也为种植细胞提供较大的粘附面,有利于细胞粘附,为大量种植细胞和生长提供足够的空间,并允许血管和组织向内生长[7],因此,多孔材料在组织再生和修复工程中具有其独特的优势.然而,随着多孔结构的引入,材料的力学性能必然发生相应的改变.动物实验表明,高孔隙率和大孔径有利于骨长入,但同时也降低了材料的力学性能[8].实际上,天然骨是一种具有梯度结构的纳米级多孔复合材料,外层是起支撑作用的密质骨,逐渐向髓腔过渡是孔径从几百微米到几毫米的松质骨,天然骨的这种梯度结构,使其在保持良好生物学活性的同时,具有优秀的生物力学性能.因此,基于仿生的理念,制备具有梯度渐变孔隙结构的复合材料,并研究它们的力学性能有非常重要的实际意义.
本文采用浇铸/NaCl微粒浸出法制备了不同孔隙率、不同孔径的多孔状HA/PCL复合材料,研究了它们在人体体温附近(37±5)℃的力学性能,同时制备了具有类似天然骨渐变孔隙结构的HA/PCL复合材料,以提高材料的力学性能.
1 试验
1.1 试剂与仪器
四水硝酸钙(纯度98%)、二甲基乙酰胺(DMAC,纯度98%)、氯化钠(纯度99.5%)、磷酸氢二铵(纯度99%)、聚乙二醇(PEG6000,纯度99%)、氨水(纯度99%)和无水乙醇(纯度99.7%)均购自国药集团化学试剂有限公司.聚己内酯(Mn=80 000,纯度99.5%,Sigma公司).
JEM-2100F场发射透射电镜(TEM),Philips XL30FEG场发射扫描电镜(FESEM),DMA800型动态力学分析仪,光学显微镜,FA1104型电子天平(上海天平仪器厂),80-2B型低速离心机(上海菲恰尔分析仪器有限公司),恒温油浴锅、磁力搅拦器(上海实验仪器厂),PH030型恒温干燥箱(上海实验仪器厂).
1.2 试验过程
1.2.1 羟基磷灰石(HA)的制备
制备HA的反应方程式为Ca(NO3)2+ (NH4)2HPO4→Ca10(PO4)6(OH)2.
称取3.96 g磷酸氢二铵((NH4)2HPO4),溶于25 mL去离子水中,向其中滴加氨水(NH3·H2O)调节其pH至10以上,称取11.8 g四水硝酸钙(Ca(NO3)2·4H2O),将其溶于37.5 mL去离子水中,并向其中加入25 mL二甲基乙酰胺(N,N-dimethylacetamide,DMAC,分散剂).在加热至60℃并搅拌的条件下,将略带碱性的磷酸氢二铵溶液缓缓地加入到硝酸钙溶液中,然后让混合溶液自然冷却,陈化24 h,再分别用去离子水和无水乙醇离心洗涤,在100℃下干燥24 h,经研磨得到HA粉末.
1.2.2 HA/PCL复合材料的制备
取上一步所得浆液17.5 mL,向其中加入20 mL溶剂二甲基乙酰胺和 1 g聚乙二醇(PEG6000,分散剂),升温至100~120℃脱水,然后向其中加入2.3 g聚己内酯(Sigma,Mn= 80 000),在140~160℃下搅拌复合直至溶剂基本蒸发完全,取出试样,用热去离子水洗涤4次,无水乙醇洗涤3次,然后在55℃下干燥48 h,得到HA/PCL复合材料(含HA质量分数30%).改变加入的PCL的质量依次为1.5、1.0、0.67 g,即可以得到含HA质量分数为40%、50%、60%的HA/PCL复合材料.
1.2.3 多孔HA/PCL复合材料的制备
将NaCl分成100~200 μm和200~300 μm的颗粒备用.取一定质量的HA/PCL复合材料,加热熔融,并向其中加入适量溶剂二甲基乙酰胺,加热至120℃并搅拌使HA/PCL复合材料与溶剂混合成粘稠溶液状,按NaCl颗粒与HA/PCL复合材料的质量比为6∶1向其中加入NaCl,搅拌均匀并逐渐蒸发溶剂,将试样取出加入塑料模具中,压制成型,冷却后取出放入去离子水中浸泡,每24 h换水一次,换水3~4次,最后在40℃下干燥,即得到固态的三维多孔HA/PCL复合材料.改变NaCl颗粒与复合材料的质量比可改变材料的孔隙率,用不同粒径的NaCl颗粒造孔可得到不同孔径的多孔材料.
1.2.4 渐变孔结构的HA/PCL复合材料的制备
采用多孔HA/PCL复合材料的制备方法,首先用200~300 μm的NaCl颗粒造孔,得到6 mm的柱体作为材料的最内层,用100~200 μm的 NaCl颗粒造孔,压制成内、外径分别为6、8 mm的环形作为材料的中间层,将未造孔的HA/PCL复合材料压制成内、外径分别为8、10 mm的环形,最后将三者嵌套在一起,溶去NaCl,即得到具有类似人骨的渐变孔结构HA/PCL复合材料.
1.2.5 材料的测试与表征
采用透射电子显微镜(TEM)对纳米HA粉末进行形貌分析,用扫描电子显微镜(SEM)观察HA/PCL复合材料的表面形貌,用EDS分析复合材料表面的化学成分,采用DMA8000动态力学分析仪测试HA/PCL复合材料的压缩模量.比较造孔前后 HA/PCL复合材料的密度差求得多孔HA/PCL复合材料的孔隙率,采用光学显微镜观察多孔HA/PCL复合材料的孔结构.
2 结果与讨论
2.1 纳米羟基磷灰石(HA)的TEM分析
图1(a)是60℃下合成的HA的TEM图,(b)是60℃合成、并经水浴处理2 h的HA粉末的TEM图.从图1(a)可以看出,60℃合成的纳米HA形貌为针状,尺寸约10 nm×50 nm,这与自然骨中的无机矿物相HA极为相似而具有很好的生物活性.而图1(b)表明,经水浴处理2 h的HA的尺寸变大,约为40 nm×300 nm,形状为棒状,说明水浴处理会影响合成的纳米HA的形貌和尺寸[9-10],使得纳米HA的尺寸变大、结晶度提高.

图1 HA粉末的TEM图
2.2 复合材料的表面微观分析与力学性能
2.2.1 复合材料的形貌和表面微观分析
图2中(f)是含HA质量分数60%的复合材料表面的EDS图,可以看到明显的钙和磷的成分,说明复合材料表面存在HA的成分.(a)~(e)分别是纯PCL、含HA质量分数30%、含HA质量分数40%、含HA质量分数50%、含HA质量分数60%的HA/PCL复合材料表面的SEM照片.从图中可以看出,复合材料表面存在大量的纳米羟基磷灰石颗粒.随着HA含量的增加,裸露在PCL基底外的HA颗粒也就越多.含HA质量分数30%的复合材料表面仅有少量的HA颗粒裸露在PCL,而含HA质量分数60%的复合材料表面则有大量的HA暴露在表面.这些裸露在复合材料表面的羟基磷灰石颗粒直接关系着材料的生物学性能,材料表面的羟基磷灰石越多,植入体内后细胞的反应就越明显,材料表面越容易形成新的骨成分,从而表现出更好的生物活性[11].
2.2.2 HA/PCL复合材料的力学性能
采用DMA8000动态力学分析仪测试了不同温度下纯PCL及不同HA含量的HA/PCL复合材料的压缩模量,如图3所示,来表征材料的刚度和弹性.从图3可以看出,随着温度的升高,复合材料和纯PCL的压缩模量均略有下降.说明随着温度的升高,材料逐渐软化,刚度下降,弹性增大.然而,复合材料植入人体后,只需要考虑在人体体温附近(37±5)℃复合材料的抗压模量是否满足要求即可.比较图中5条曲线可以发现,掺入了HA的复合材料,其压缩模量比纯PCL要大.而且随着HA掺入量的增大,复合材料的压缩模量也随之增大.HA的掺入提高了纯PCL的刚度,使得复合材料更好地具备作为硬组织替代材料所必需的强度,同时使得复合材料具备了一定的生物活性.复合材料的PCL基体解决了纯HA脆性大、易断裂、加工难等问题,综合了HA与PCL二者各自的优点.在不考虑力学性能的前提下,HA含量越高,复合材料的生物活性越好,越适合作为硬组织修复与替代材料.然而,天然的人骨不仅具备很高的硬度,还拥有一定的弹性,所以对于生物骨材料也同样要求不仅有一定的强度,还要具备一定的弹性.HA在复合材料中的含量增加时,复合材料的刚度增加而弹性减小.当HA的质量分数达到60%时,复合材料的压缩模量超过了100 MPa,失去了作为骨材料所必须的弹性.因此,为保证HA/PCL复合材料同时具备优良的生物学性能和力学性能,成为理想的骨材料,HA在HA/PCL复合材料中的质量分数最好为50%~60%,而不宜超过60%.

图2 不同HA含量的HA/PCL复合材料表面SEM图片和EDS分析结果
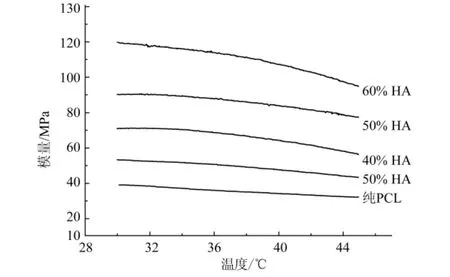
图3 不同HA质量分数的复合材料的压缩模量随温度变化曲线
2.3 多孔HA/PCL复合材料的结构与力学性能
分析
通过改变造孔剂的用量与粒径制备了不同孔径、不同孔隙率的多孔HA/PCL复合材料,如表1所示.从表中数据可以看到,随着NaCl与PCL质量比越大,材料的孔隙率也越大,由此可以说明能够通过造孔剂的用量来控制材料的孔隙率.高孔隙率的多孔支架具有大的比表面积,有利于材料的降解,同时能为大量细胞的种植及生长提供足够的空间.图4显示了采用不同粒径的造孔剂制得的多孔材料的孔结构图.从图中可以看出,所用的造孔剂的粒径越大,所得到的多孔材料的孔径也就越大,因而可以通过造孔剂的粒径来控制多孔材料的孔径.孔径的大小是影响纤维组织血管内生的重要因素,对新生骨的长入有重要影响,合适的孔径为100~600 μm,过大或过小均不利于组织和细胞的长入[8].

表1 不同粒径、不同用量的造孔剂制得的多孔HA/PCL材料的孔隙率比较

图4 不同孔径的NaCl造孔的多孔材料
对于不同孔径、不同孔隙率的多孔材料,同样采用DMA8000动态力学分析仪对其压缩模量进行测量,结果如图5所示.图中a、b、c分别为200~300 μm孔径,62.5%孔隙率;100~200 μm孔径,77.1%孔隙率;200~300 μm孔径,80.8%孔隙率的多孔材料的压缩模量随温度的变化曲线.与未造孔的HA/PCL复合材料相比,多孔结构的引入使其压缩模量大幅下降.比较a与c可以发现对于相同的孔径,孔隙率越大的多孔材料其压缩模量越小.同样比较b与c可知,相同孔隙率下孔径小的多孔材料其压缩模量较大.因此,虽然高孔隙率的材料更有利于细胞及组织的长入,具有更好的生物学性能,然而,孔隙率越高,材料的压缩模量越小,强度下降而不再具备优良的力学性能.因此,用作骨修复与替代材料的多孔材料,同样应充分考虑生物学性能与力学性能两方面的因素.
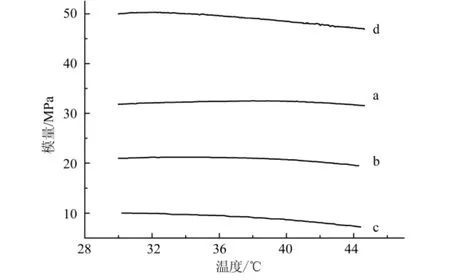
图5 不同孔隙率、不同孔径的多孔材料的压缩模量随温度变化曲线
2.4 渐变孔结构的多孔复合材料的结构与力学性
图6是具有渐变孔结构的多孔复合材料的孔结构图.由图6可以看到,材料从里到外孔结构具有明显的变化,最内层为200~300 μm的孔径,是最为疏松的结构,相当于人骨的骨髓,中间一层为100~200 μm的孔径,最外层由无孔HA/PCL复合材料构成,是致密的结构,相当于人骨最外层的密质骨.
由于最外层的致密结构,由图5中曲线d可知,在37℃下其压缩模量约49.4 MPa,相对于单一孔结构的多孔材料有了很大提高.由此可以说明,具有类似人骨的渐变孔结构的复合材料不仅具有多孔材料所具有的优异生物学性能,其力学性能较单一孔结构的多孔材料也有了很大提高.

图6 具有渐变孔结构的复合材料的孔结构图
3 结论
1)采用水热法制备了羟基磷灰石粉末,并通过溶剂共混法将其与聚己内酯复合,制备了不同HA含量的HA/PCL复合材料,并研究了它们在体温附近(37±5)℃的力学性能.结果表明HA含量越高,材料的压缩模量越大.当HA的质量分数达到 60%时,复合材料的压缩模量达到了100 MPa以上.
2)采用浇铸/NaCl微粒浸出法制备了多孔状HA/PCL复合材料.通过造孔剂的粒径和用量来控制材料的及孔隙率,并对不同孔隙率、不同孔径的材料在体温附近(37±5)℃的力学性能进行研究,结果显示孔隙率越大、孔径越大,材料的压缩模量越小.当孔径为200~300 μm,孔隙率达到80.8%时,材料的压缩模量仅为10 MPa左右.
3)基于仿生的理念,在多孔材料制备的基础上制备了具有类似人骨的渐变孔结构的HA/PCL复合材料,对其研究的结果显示,具有渐变孔结构的材料不仅具备单一孔结构材料所具有的多孔结构,而且由于最外面的致密层,其压缩模量提高到了49.4 MPa,力学性能相对于单一孔结构材料得到了显著的提高.
[1] ZHAO J,GUO L Y,YANG X B,et al.Preparation of bioactive porous HA/PCL composite scaffolds[J].Applied Surface Science,2008,255:2942-2946.
[2] 于婷,刘娅,王宇,等.改性纳米羟基磷灰石/PLGA复合材料的制备及生物活性[J].高等学校化学学报,2009,30(7):1439-1444.YU Ting,LIU Ya,WANG Yu,et al.Preparation and bioactivity of the composite of PLGA and hydroxyapatite nanocrystals surface-grafted with L-lactic acid oligomer[J].Chemical Journal of Chinese Universities,2009,30(7):1439-1444.
[3] 陈广美,黄毅萍.羟基磷灰石含量对纳米粒子-聚己内酯复合材料性能的影响[J].安徽大学学报,2011,35(5):73-79.CHEN Guang-mei,HUANG Yi-ping.Effect of the HA content on the properties of nanoparticle-polycaprolactone composites[J].Journal of Anhui University,2011,35(5):73-79.
[4] 戴炜枫,杜征臻,何月英,等.官能团化己内酯与丙交酯无规共聚物的合成与降解性能[J].高等学校化学学报,2009,30(10):2076-2081.DAI Wei-feng,DU Zheng-zhen,HE Yue-ying,et al.Synthesis,characterization and degrade-ability of P (LA-co-ACL)copolymer bearing pendant N-substituted acyla mine group[J].Chemical Journal of Chinese Universities,2009,30(10):2076-2081.
[5] JOSHUA R P,ANDREW H,KETUL C P.Biodegradable polycaprolactone nanowires for bonetissue engineering applications[J].Biomaterials,2009,30:780-788.
[6] 肖凤娟,张颖,王少辉,等.硅掺杂羟基磷灰石生物活性微粉对人血清白蛋白的吸附特性[J].复合材料学报,2009,26(2):149-154.XIAO Feng-juan,ZHANG Yin,WANG Shao-hui,et al.Characterization and mechanism of the adsorption of human serum albumin on silicon-substituted hydroxyapatite[J].Acta Materiae Compositae Sinica,2009,26(2):149-154.
[7] 王晶.引导骨组织长入植入物狭长腔洞的技术研究[D].武汉:武汉理工大学,2010.WANG Jing.The research of a method for inducing bone tissue Growth into narrow cavity in bone implant[D].Wuhan:Wuhan University of Technology,2010.
[8] 严宁,侯铁胜.材料孔隙结构对骨长入的影响[J].中国生物医学工程学报,2008,27(4):611-614.YAN Ning,HOU Tie-sheng.Porosity of biomaterials and bone in growth[J].Chinese Journal of Biomedical Engineering,2008,27(4):611-614.
[9] 王扬,王宇明,李海东.纳米羟基磷灰石的制备及工艺优化[J].长春工业大学学报,2009,30(2):137-141.WANG Yang,WANG Yu-ming,LI Hai-dong.Preparation processing optimization of nano-hydroxyapatite[J].Journal of Changchun University of Techonology,2009,30(2):137-141.
[10] 隋岩峰,李子燕,解田,等.纳米羟基磷灰石制备方法的研究进展[J].贵州化工,2011,36(4):6-8.SUI Yan-feng,LI Zi-yan,XIE Tian,et al.The progress study on method of producing nano-hydroxyapatite[J].Guizhou Chemical Industry,2011,36(4):6-8.
[11] 黄勇,王迎军,宁成云,等.微弧氧化法制备含铈羟基磷灰石生物活性膜层[J].材料科学与工程学报,2008,26(1):80-83.HUANG Yong,WANG Ying-jun,NING Cheng-yun,et al.Preparation and properties of Cerium-containing hydroxyapatite coating on commercially pure titanium by micro-arc oxidation[J].Journal of Material s Science&Engineering,2008,26(1):80-83.
Bionics materials of hydroxyapatie/poly(ε-caprolactone) with gradual change pore structure
TANG Jun1,ZHOU Bin1,DU Ai1,ZHANG Zhi-hua1,SHEN Jun1,XIA Yan2,XU Shuo-gui2
(1.Shanghai Key Laboratory of Special Microstructure Technology,Tongji University,Shanghai 200092,China; 2.Department of Orthopaedics,Changhai Hospital Second Military Medical University,Shanghai 200433,China)
To get hydroxyapatite(HA)/polycaprolactone(PCL)bionic bone material with gradual changing pore structure similar to the bone structure and good mechanical properties,HA powder was prepared by hydrothermally synthesized method,and it had been compounded with PCL via solvent blending method,then vesicular HA/PCL composite were prepared with cast/sodium chloride particle-leaching technique.On this basis,HA/PCL composite with different pore size,different porosity rate and HA/PCL composite with gradual changing pore structure were achieved via changing the particle size and the quantity of sodium chloride.The pore structures were observed by optical microscope,and the pore size is from 100~300 μm,the maximum porosity rate is of 80%.What’s more,the mechanical properties had been studied near the body temperature (37±5)℃,and the results indicated that the mechanical properties were greatly improved compared to the HA/PCL composite with single pore structure.
composite;hydroxyapatite;poly(ε-caprolactone);pore structure;bionics;mechanical property
TB33 文献标志码:A 文章编号:1005-0299(2012)06-0023-06
2011-11-25.
上海市纳米专项(1052nm03100);国家自然科学基金资助项目(51102184,51172163);教育部博士点基金资助项目(20090072110047,20100072110054).
唐 俊(1988-),男,博士研究生.
周 斌,E-mail:zhoubin863@tongji.edu.cn.
(编辑 程利冬)

