CoMo/Al2O3-TiO2 催化剂上加氢脱除苯并噻吩宏观动力学研究
吴 楠,廖尾英,郝玉翠
(1.唐山学院 环境与化学工程系,河北 唐山 063000;2.唐山工业职业技术学院 机械工程系,河北 唐山 063000)
随着经济高速发展,我国对原油的需求量日益增大,但由于石油资源有限,国产原油产量已经不能满足市场需求,越来越多地依赖进口。而进口原油,尤其是中东油含硫量高,品质相对较低,这对我国的石油加工技术提出了更高的要求。加氢脱硫(HDS)是柴油深度脱硫最为有效的方法之一[1],而新型载体的研制及高效HDS催化剂的开发是目前国内外研究的热点。
Vanrysselberghe等[2]以 DBT,MDBT及 DMDBT为模型物,在模拟溶剂或轻循环油中,采用三相高压滴流床,在排除内外扩散情况下进行了HDS动力学试验,在综合考虑反应物在催化剂上的吸附与脱附的基础上,建立了反应网络中各步反应的L-H型动力学方程组,回归计算出吸附平衡常数、吸附热、反应活化能、指前因子等参数。Froment和Pillu[3]共同开发出一组苯并噻吩(BT)的反应动力学模型,模型综合考虑了H2S,H2和苯并噻吩在催化剂上的竞争吸附关系。
本文以含苯并噻吩的二甲苯溶液为模型化合物在气液固三相等温滴流床中反应,拟合了在CoMo/Al2O3-TiO2催化剂上加氢脱硫反应动力学模型,进一步研究了该反应的动力学特性。
1 实验部分
1.1 催化剂制备与模型化合物的配制
催化剂的制备:硝酸铝溶液与氨水、钛酸四丁酯混合,经过陈化、结晶、过滤、干燥焙烧制得Al2O3-TiO2复合载体;将硝酸钴和钼酸铵以Co/Mo摩尔比为0.4混合,在恒温水浴条件下浸渍到复合载体上,经过773K高温焙烧制成。为保证动力学实验数据的一致性和准确性,动力学实验所采用的催化剂为同一批次制得。
模型化合物的配制:将含一定量的苯并噻吩化合物溶解在二甲苯溶液中,制得含硫约为1 000ppm(质量分数)的模型化合物溶液(药品均为AR级)。
1.2 实验流程
含硫模型化合物经过平流泵增压与氢气(浓度99.9%)混合进入反应器进行反应。反应产物从反应器流出后进入冷凝器冷凝,然后进入高压分离器中进行气液分离,分离后的液体经缓冲罐取出进行气相色谱检测,尾气进入KOH溶液瓶进行无害处理。
1.3 分析方法
实验过程中定时收集冷凝下的液相产物,并经气相色谱分析其组成。气相色谱采用FPD(火焰光度)检测器,色谱柱采用的是长度×内径×膜厚为50m×0.25mm×0.5μm的毛细管石英柱。色谱使用分离条件为进样口:553K,分流比100∶1,进样量1μL,柱温393K-0min-1.5K/min-408 K/min-0min-10K/min-543K-5min。根据不同硫化合物出峰时间不同判断硫化合物种类(见图1),苯并噻吩保留时间为17.723min,通过外标法计算得出每种含硫物在反应前后的硫含量Cin及Cout。

图1 模型溶液的色谱分析图
1.4 催化剂的预硫化和老化
钴钼基催化剂的活性成分为钴钼硫化物,因此在实验前需要对催化剂进行预硫化处理[4]。在温度653K,总压3 MPa,质量空速5.16h-1和氢油比1 500V/V条件下采用含3%CS2的环己烷溶液对催化剂预硫化5h。硫化结束后,在553K,总压3MPa,质量空速15.48h-1和氢油比750V/V条件下老化5h,以使催化剂活性达到稳定状态,而后进入反应动力学实验。
2 结果与讨论
2.1 动力学模型
在加氢脱硫过程中,加氢速率和直接脱硫速率都会由于原料或产物中某些抑制剂的存在而下降,对此许多学者做过研究,主要包括H2S对催化剂的抑制和失活影响、对含氮化合物的影响以及对各种溶剂的影响[5-7]。
本文采用动力学模型方程为

其中,-r为 HDS反应速率,mol·h-1·gcat-1;k为反应速率常数,mol·h-1·gcat-1;KBT,KH2,KH2S分别为苯并噻吩、氢气和硫化氢的吸附平衡常数,mol/mol,它们都是关于温度的函数。
此模型方程综合考虑了氢气、硫化氢和苯并噻吩在催化剂上的竞争吸附关系。
kBT为反应速率常数符合Arrhenius方程,可以写成

其中kBT,0为苯并噻吩反应速率的指前因子,mol·h-1·gcat-1;Ea为活化能,J/mol;R 为气体常数,8.314J/(mol·K);T 为反应温度,K。

其中T为反应温度;珚T是平均温度,本试验设定为525K;a,b为待定系数。
催化剂的加氢脱硫反应速率可以用下式表示,其中F为含硫模型化合物的摩尔流速,mol/h;F0为模型化合物的摩尔流速,mol/h;w为催化剂质量,g;Ci为硫化物摩尔浓度,mol/mol。
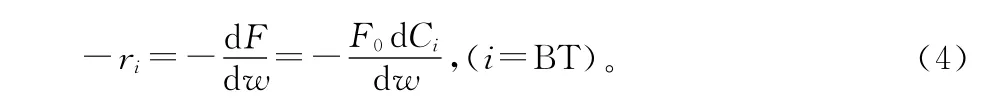
2.2 模型参数
在实验压力和温度下,氢气在模型溶液中溶解度由文献查得[8],由拉格朗日差值法计算所需压力温度下氢气溶解度。二甲苯、苯并噻吩和二苯并噻吩的浓度由质量浓度换算为摩尔浓度。
考虑硫化氢为加氢脱硫产物,根据质量守恒硫化氢的浓度可以由下式计算出来,CBT,in为苯并噻吩的进口浓度,mol/mol;CBT,out为苯并噻吩的出口浓度,mol/mol。

方程(1)(4)和反应器的入口条件组成了一阶常微分方程组的初值问题,只要给定动力学模型参数的初值,就可由相应的数值计算方法求得反应器出口处的物料组成。然后,利用反应器出口各组分浓度(分压)实验值与计算值之间的偏差信息,以适当的方法对模型参数进行修正和优化,就可获得满足一定精度要求的动力学模型参数的估计值。笔者采用四阶龙格库塔法解微分方程(1)(4),将动力学数据(见表1)代入方程中,并采用全局通用算法结合马夸特算法对模型参数进行修正优化,以苯并噻吩和二苯并并噻吩为关键组分,它们出口浓度的计算值和实验值的残差平方和为参数估值目标函数。
计算得到加氢脱除苯并噻吩动力学模型参数为:

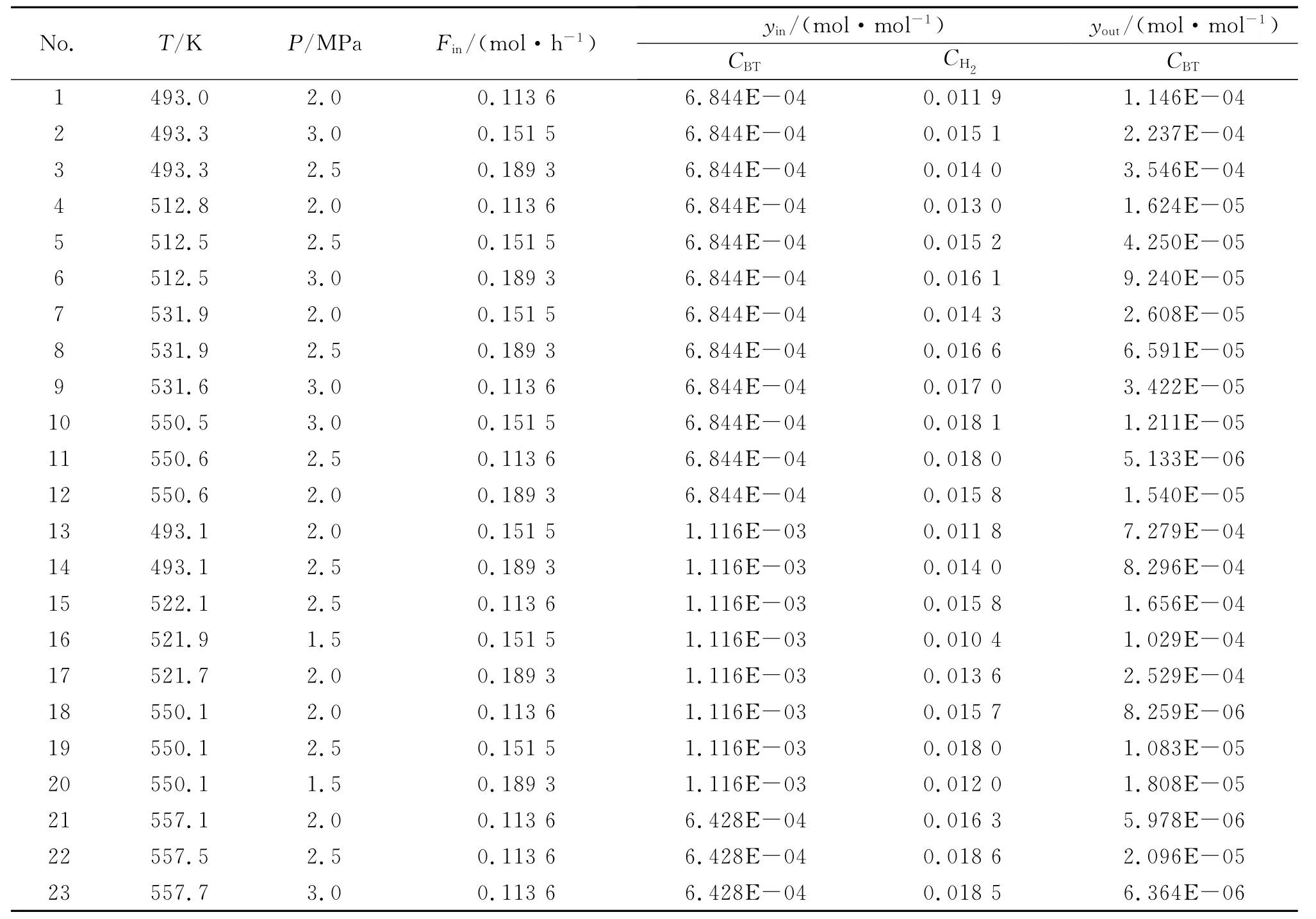
表1 双曲线动力学模型数据

2.3 模型参数验证
对拟和的动力学参数进行统计验证,见表2。

表2 动力学统计检验结果
F为回归均方和与模型残差均方和之比,ρ2为决定性指标。

M为试验次数,Mp为参数个数。一般认为ρ2>0.9,F>10F0.05时,动力学方程是适合的。实验测得的苯并噻吩摩尔浓度和计算出的摩尔浓度比较见图2,计算值和实验测量值基本吻合。
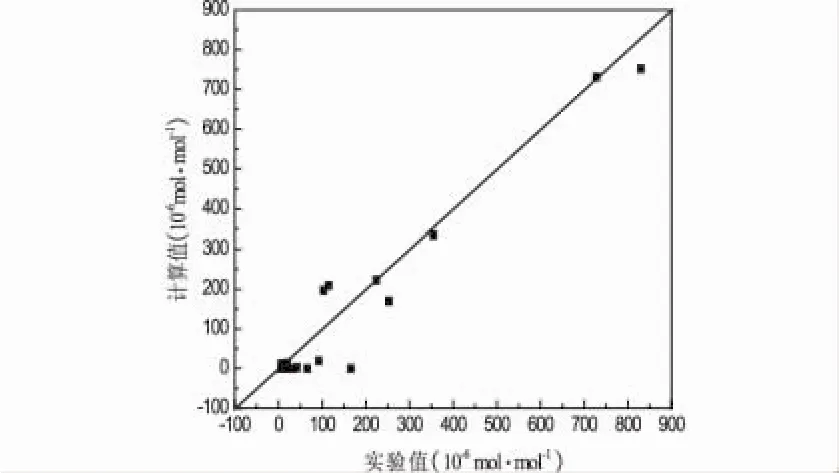
图2 苯并噻吩摩尔浓度实验值和计算值比较
3 结论
本文采用龙格库塔法数值计算一阶微分方程,采用全局通用算法结合马夸特算法拟合出模型化合物硫组分的双曲线型动力学方程,计算出苯并噻吩的活化能为5.219 9×104J/mol。通过残差检验和统计学考察,模型计算结果和实验数据吻合良好。
[1] 马叶勇,吴楠,马骁驰,等.燃料油加氢深度脱硫催化剂及工艺技术进展[J].工业催化,2007,15(12):
[2] Vanrysselberghe V,Gall R L,Froment G F.Hydrodesulfurization of 4-Methyldibenzothiophene and 4,6-dimethyldibenzothiophene on a Co-Mo/A1203catalyst:Reaction network and kinetics[J].Ind Eng Chem Res,1998,37(4):1235-1242.
[3] Gilbert F Froment,Guy A Depauw,Valerie Vanrysselberghe.Kinetic modeling and reactor simulation in hydrodesulfurization of oil fractions[J].Ind Eng Chem Res,1994,33,2975-2988.
[4] 黄海涛,齐艳华,石玉林,等.催化裂化柴油深度加氢脱硫反应动力学模型的研究[J].石油炼制与化工,1999,30(1):55-59.
[5] Topsae H,Clausen B S,Massoth F E.Hydrotreating catalysis in Catalysis:Science and Technology[M].New York:Springer,1996.
[6] W hitehurst D D,Isoda T,Mochida I,et a1.Present state of the art and future challenges in the hydrodesulfurization of polyaromatic sulfur compounds[J].Adv Catal,1998,42:345.
[7] Girgis M J,Gates B C.Reactivities,reaction networks,and kinetics in high-pressure catalytic hydroprocessing[J].Ind Eng Chem Res,1991,30(9):2021-2058.
[8] 赵亮富,赵玉龙,吕超辉.氢气和一氧化碳在混二甲苯中的溶解度[J].化学反应工程与工艺,2000,16(4):396-400.

