对氨基水杨酸对利福平血药峰浓度的影响
黄学锐,戈启萍,高微微,杜亚东,陆 宇
(首都医科大学附属北京胸科医院,北京 101149)
对氨基水杨酸对利福平血药峰浓度的影响
黄学锐*,戈启萍,高微微#,杜亚东,陆 宇
(首都医科大学附属北京胸科医院,北京 101149)
目的:探讨肺结核患者口服对氨基水杨酸异烟肼片时对氨基水杨酸对利福平血药峰浓度的影响。方法:采取同一患者自身前后对照,同时服用对氨基水杨酸异烟肼片和利福平胶囊为观察组,同时服用异烟肼片和利福平胶囊为对照组,分别检测2组异烟肼和利福平的血药峰浓度,观察对氨基水杨酸对利福平血药峰浓度的影响。结果:口服异烟肼片和利福平胶囊后1.5 h异烟肼和利福平平均血药浓度分别为(4.88±2.32)μg·mL-1和(6.49±3.40)μg·mL-1,而口服对氨基水杨酸异烟肼片和利福平胶囊后1.5 h两者平均血药浓度分别为(2.62±2.34)μg·mL-1和(5.84±2.74)μg·mL-1。2组利福平血药峰浓度比较,差异无统计学意义(P>0.05);2组异烟肼血药峰浓度比较,差异有统计学意义(P<0.05)。结论:对氨基水杨酸异烟肼片中的对氨基水杨酸未对利福平血药峰浓度产生明显影响。
肺结核;抗结核药物;血药峰浓度;氨基水杨酸异烟肼片;对氨基水杨酸;利福平
对氨基水杨酸异烟肼(Pa)片、异烟肼(INH,H)片和利福平(RFP,R)胶囊是一线抗结核药物。Pa是H和对氨基水杨酸(PAS)的结合物,其目的是使PAS竞争性抑制H的乙酰转移酶,使H在体内代谢延缓,从而达到提高H体内组织中的浓度。在临床上,为了个体化治疗需要,常有Pa与R合用者。据文献报道[1],PAS和R同时应用,PAS可降低R吸收达50%,两药联用时服药应间隔6~8 h。Pa片每片含H 47.3 mg、PAS 52.7 mg,其中的PAS能否影响到R血中药物浓度,对此我们存有一定的疑虑。由于没有文献做过类似的研究,为此,我们考察肺结核患者同服Pa和R后的血药峰浓度,并选H作为对照,初步探讨常态口服Pa或H对R血药峰浓度的影响,以便指导临床用药。
1 资料
1.1 仪器
Waters-600系列高效液相色谱仪,包括600四元梯度泵、4200紫外检测器、717自动进样器、Empower色谱工作站(美国Waters公司)。
1.2 药品
H片(上海信谊药厂有限公司,批号:090401);R胶囊(上海信谊药厂有限公司,批号:090201);Pa片(重庆华邦制药股份有限公司,批号:2009003);甲醇为色谱纯,其余试剂均为分析纯。
1.3 选择对象与标准
选取2009年4月-2010年1月在首都医科大学附属北京胸科医院结核科住院的肺结核患者15例,诊断均为初治肺结核,见肺结核诊断标准[2]。其中男性4例,女性11例;肝肾功能正常,血尿常规正常;年龄18~66岁,平均年龄(32.87±13.87)岁;体重40~74 kg,平均体重(54.13±8.72)kg。H片、R胶囊2种药物常规为每日清晨空腹顿服;Pa因服用片数多(0.9 g·d-1),常规每日分3次口服。
病例排除标准:<18岁和>70岁,合并肺外结核病、心肺严重合并症和并发症、乙肝和丙肝抗体阳性、酒精性肝病、脂肪肝、糖尿病、肾功能不全、贫血、营养不良、低蛋白血症等有明确消化系统疾病者,或服用过可能影响结果的药品的患者。
2 方法
2.1 色谱条件及处理方法
2.1.1 H:血浆0.5 mL,经衍生化及去蛋白处理后进样测定,色谱柱为Waters Symmetry ShieldTMRP18(3.9 mm×150 mm,5 μm),进样量为40μL,流动相为0.01 mol·L-1磷酸盐缓冲液(Na2HPO4+KH2PO4)(pH 7.7)∶甲醇(52∶48),检测波长为335 nm,流速为1 mL·min-1。
2.1.2 R:血浆0.5 mL,经去蛋白处理后进样测定,色谱柱为Waters Symmetry ShieldTMRP18(3.9 mm×150 mm,5μm),进样量为40μL,流动相为0.01 mol·L-1磷酸盐缓冲液(KH2PO4+Na2HPO4)(pH 4.8)∶甲醇(35∶65),检测波长为336 nm,流速为1 mL·min-1。
2.2 试验方案
采取Pa片或H片自身前后对照方法,设H片为Pa片的对照,经患者知情同意,服药后第7天抽血1次,每次抽静脉血3 mL,同时测H、R 2种药物,前后共测2次。分别检测2种药物Pa或H在常规口服情况下(常态下)分别对R的血药峰浓度的影响。其中一组(R+H~R+Pa)8例口服H片0.3 g·d-1、R胶囊0.45 g·d-1,第7天晨起空腹口服上述药物,服药时饮水200 mL,在1.5 h抽血测定血浆中H、R血药峰浓度;检测后的第2天把H片改为Pa片0.3 g(分每天3次服),第7天再次晨起空腹口服Pa片0.3 g、R胶囊0.45 g,服药时饮水200 mL,在1.5 h抽血,检测血浆中H、R血药峰浓度。另一组(R+Pa~R+H)7例先口服Pa胶囊0.3 g(分每天3次服)、R 0.45 g·d-1,第7天同样方法,检测血中H、R药物峰浓度,次日把Pa改为H片0.3 g·d-1,第7天同样方法再次检测H、R药物峰浓度。
2.3 统计学处理
采用SPSS 13.0软件包对数据进行统计学分析,试验数据用均数±标准差表示,均数比较采用t检验,P<0.05为差异有统计学意义。
3 结果
3.1 H、R血浆中药物浓度
15例口服H片、R胶囊治疗后,血浆中H药物浓度在1.57~8.72μg·mL-1之间,其中>3μg·mL-113例,占86.7%;R药物浓度在1.25~14.38μg·mL-1之间,>3μg·mL-113例,占86.7%。口服Pa片、R胶囊治疗后,血浆中H药物浓度在0.75~7.64μg·mL-1之间,>3μg·mL-13例,占20.0%;R药物浓度在2.52~10.64μg·mL-1之间,>3μg·mL-112例,占80.0%。2组比较显示Pa对R血浆中的药物峰浓度影响不大;Pa片0.3 g剂量中H的药物峰浓度不如单纯H片0.3 g剂量,与Pa片分次服用有关,见表1。
由表1可以看出,第8例患者用H片、R胶囊7 d和Pa片、R胶囊7 d血浆中H、R峰浓度较高,此例患者在抗结核治疗40 d左右出现明显的精神症状,不能控制情绪,停用H片后,症状逐渐好转;第4例为最高体重者,H的血药峰浓度最低,但R的血药峰浓度未见最低。
3.2 R、H血浆中药物峰浓度均数比较
对15例肺结核患者的H、R血药峰浓度检测结果用SPSS13.0进行统计分析,t检验分析R+Pa组和R+H组的前、后R自身对照平均血药峰浓度,2组差异无统计学意义(t=0.575,P=0.570>0.05);用t检验分析R+Pa组中的H平均血药峰浓度和R+H组的H平均血药峰浓度,2组差异有统计学意义(t=2.66,P=0.013<0.05),见表2。
4 讨论
Pa化学名称为4-吡啶甲酰肼-4-氨基水杨酸,是H和PAS的化学合成物。PAS可延缓和阻滞H在体内的乙酰化过程,因此Pa可在血液中维持较高、较久的H浓度[3]。有文献报道[4],Pa高于最低抑菌浓度作用时间可达12 h。另有文献报道[5,6],Pa对耐H和/或PAS的结核菌株仍显示一定程度的敏感,是临床常用的抗结核药物之一。如何合理使用Pa,特别是其与R的相互作用,是临床医师关心的问题之一。

表1 15例患者血浆中H、R药物峰浓度的比较Tab 1 Comparison of peak blood concentrations of R and H among 15 patients
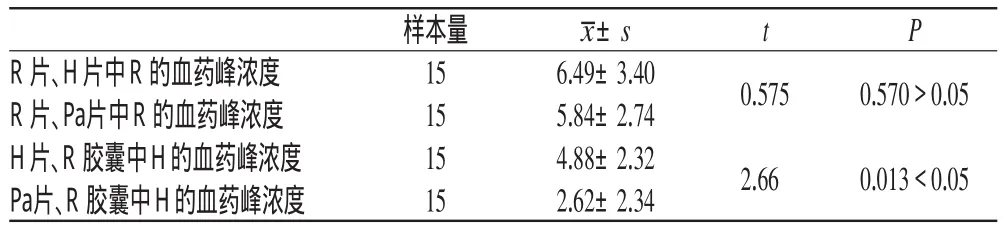
表2 15例患者血浆中R、H药物峰浓度均数比较Tab 2 Comparison of mean peak blood concentrations of R and H among 15 patients
本文通过简易的、便于患者接受的、贴近临床常用、非正规药物研究的方式,采取唯一1个点的采血,观察常规口服剂量Pa片中的PAS对R的血药峰浓度的影响。文献报道[7],H 0.3 g的峰浓度为2.5~6.1µg·mL-1,达峰时间1~2 h;R 0.6 g的峰浓度为7~9 mg·mL-1,达峰时间1.5~4 h;Pa片因分次服用,达峰时间无文献报道。因此,笔者根据以往测定血药浓度的经验和文献报道[8~10]选择Pa合适的抽血时间。
检测结果显示,口服H片、R胶囊后1.5 h平均血药浓度为(4.88±2.32)µg·mL-1和(6.49±3.40)µg·mL-1,而口服Pa片、R胶囊后1.5 h二者的平均浓度(2.62±2.34)µg·mL-1和(5.84±2.74)µg·mL-1,基本与文献报道血浆中峰浓度的结果相近。因此,通过与对照组结果比较,提示常规口服剂量Pa片中的PAS对R的血药峰浓度无明显影响(P>0.05)。故不需要两药隔开服用,即早晨Pa片常规口服剂量可与R胶囊同服。然而,我们考察的仅仅是在Pa 0.3 g时对R 0.45 g的影响,而非Pa片一天0.9 g的总量对R胶囊顿服0.45 g的影响,因此,本试验有一定的局限性和缺陷,只代表所测药物H、R的血药峰浓度,而并不代表血药浓度。本文检测结果仅说明临床医师在常规剂量使用下,不必担心Pa中PAS会降低R的血药峰浓度。
另外,2组中H平均峰浓度比较差异有统计学意义(P<0.05),是因为Pa片为分服所致。这种给药方法虽单次剂量小,但在1.5 h我们所测定的H平均药物浓度为(2.62±2.34)µg·mL-1,也能达到抗结核作用,既能减少患者的胃肠道反应,也符合临床医师常用的用药方法。
检测结果显示,15例患者中个别患者的个体差异较大,体现在各患者的血药峰浓度相差可达倍数关系,可能与我们仅选1个点(服药后1.5 h)抽血有关,或也可能与患者体重有关。本组最高体重者,H的血药峰浓度最低,但R的血药峰浓度未见最低,见表1第4例患者。文献报道[11],R血药浓度受体重的影响,与本项观察不相符,可能受样本量或R达峰时间的影响。R达峰时间有报道[1]在2~4 h,本组检测服用R胶囊后1.5 h的抽血时间略有提前,主要是照顾了H的血药峰浓度的影响,以尽可能减少抽血次数。本文表1第8例患者在2组中H和R血峰浓度最高,此患者在抗结核治疗40 d左右出现明显精神症状,经停用H片、对症治疗后,症状逐渐好转,提示本项简易的血药峰浓度的检测可发现特殊的病例,对临床指导个体化治疗是有益处的。因此,临床应针对特殊体重或特殊症状等特殊人群通过检测药物浓度,以指导临床用药。
[1] 贾公孚,谢惠民.药物联用禁忌手册[M].北京:中国协和医科大学出版社,2001:100.
[2] 中华医学会.临床诊疗指南——结核病分册[M].第1版.北京:人民卫生出版社,2005:附录(一)、附录(二).
[3] 岳志华,牛秀华.HPLC法测定对氨基水杨酸异烟肼中的含量及有关物质的研究[J],药物分析杂志,2005,25(12):1 553.
[4] 屠德华,万利亚.现代结核病控制与实践[M].北京:现代教育出版社,2009:128.
[5] 许 申,邝荔香,鲁义东,等.结核清联用方案治疗难治肺结核32例的疗效观察及血药浓度的检测[J].中国防痨杂志,1999,21(3):169.
[6] 孙 丽,席家宁,康丽君,等.对氨基水杨酸异烟肼对耐INH及PAS结核菌株的耐药实验观察[J].中国防痨杂志,2001,23(2):110.
[7]Johnson JL,Hadad J,Boom WH,et al.Early and extended early bactericidalac tivityo flevofloxacin,gatifloxacin and moxifloxacin in pulmonary tuberculos[J].Am J Respir Crit Care Med,2008,178(11):1 180.
[8] 高微微,段连山,黄学锐,等.合并糖尿病肺结核与无糖尿病结核病人的三种抗结核药物药代动力学观察[J].中国防痨杂志,2003,25(2):72.
[9] 李艳静,韩喜琴,高微微,等.糖尿病对异烟肼和利福平血药浓度影响的研究[J].中华临床医师杂志,2011,18(1):18.
[10] 曾德贵,刘玉琴.异烟肼人体血药浓度测定及药代动力学研究[J].药物研究,2011,20(3):6.
[11] 吴启秋,段连山,林 羽,等.脊椎结核患者寒性脓肿及血液中三种抗结核药物浓度的比较[J].中华结核和呼吸杂志,1998,21(10):617.
Effects of Aminosalicylic Acid on Peak Blood Concentration of Rifampicin
HUANG Xue-rui,GE Qi-ping,GAO Wei-wei,DU Ya-dong,LU Yu
(Beijing Chest Hospital Affiliated to Capital Medical University,Beijing 101149,China)
OBJECTIVE:To investigate the effects of aminosalicylic acid on peak blood concentration of rifampicin in pulmonary tuberculosis patients receiving Isoniazid aminosalicylate tablets.METHODS:Taking the same patients before-after controlled method,observation group
Isoniazid aminosalicylate tablets and Rifampicin capsules,and control group received Isoniazid tablets and Rifampicin capsules.The peak blood concentrations of isoniazid and rifampicin were detected in 2 groups.The effects of Isoniazid aminosalicylate tablets on peak blood concentration of rifampicin were observed.RESULTS:The mean blood concentrations of isoniazid and rifampicin after taking drugs for 1.5 hours were(4.88±2.32)μg·mL-1and(6.49±3.40)μg·mL-1in control group,(2.62±2.34)μg·mL-1and(5.84±2.74)μg·mL-1in observation group.There was no significant difference in peak blood concentration of rifampicin between two groups(P>0.05),and there was significant difference in peak blood concentration of isoniazid between two groups(P<0.05).CONCLUSION:Aminosalicylic acid of Isoniazid aminosalicylate tablets has no obvious effect on peak blood concentration of rifampicin.
Tuberculosis;Antituberculous drugs;Peak blood concentration;Isoniazid aminosalicylate tablets;Aminosalicylic acid;Rifampicin
R969.1;R979.5
A
1001-0408(2012)30-2839-03
DOI 10.6039/j.issn.1001-0408.2012.30.22
*主任医师。研究方向:结核病诊断和治疗。电话:010-89509321。E-mail:huangxr2004@yahoo.com.cn
#通讯作者:主任医师。研究方向:结核病诊断和治疗。电话:010-89509029。E-mail:gwwjys@sina.com
2012-03-07
2012-03-28)
*主管药师,硕士。研究方向:临床药学。电话:0898-68642533。E-mail:kittyruling2002@126.com

