组织运动三尖瓣环位移自动追踪技术评价房间隔缺损患者右心室功能的研究
王慧英,李天亮,胡新玲,张晓丽,高明兰,王仲朝
组织运动瓣环位移自动追踪技术(tissue motion annular displacement,TMAD)是基于斑点追踪技术而发展起来的一项新技术,目前文献报道中多用于研究二尖瓣环位移以评价左心功能。TMAD技术用于研究三尖瓣环位移及右心室功能尚少见报道。房间隔缺损(atrial septal defect,ASD)患者常存在异常分流,影响右心室功能。故本研究采用TMAD技术测量ASD患者及正常人的三尖瓣环位移(tricuspid annular displacement,TAD),探讨其在评价ASD患者右心室收缩功能方面的临床应用价值。
1 资料与方法
1.1 研究对象 病例组为2011年3月—2011年10月明确诊断的ASD患者36例,其中男8例,女28例,年龄8岁~69岁(43.7岁±10.8岁)。经胸超声心动图测量ASD最大直径为10mm~47mm(28.1mm±10.9mm)。对照组为2011年3月—2011年10月健康体检者23例,其中男8例,女15例,年龄21岁~55岁(39.2岁±18.5岁)。两组间年龄、性别匹配,所有病例组观察对象检查时均为窦性心律,并排除右心室流出道梗阻、肺动脉瓣狭窄及三尖瓣器质性病变、右心起搏器植入术后、右心室心肌梗死、心肌病及其他心脏畸形等疾患[1]。
1.2 方法
1.2.1 仪器与方法 采用Philips iE33型彩色多普勒超声诊断仪,S5-1探头,频率(1~5)MHz。所有受检者均取左侧卧位,连接同步心电图,平静呼吸,心率稳定后胸骨旁左室长轴切面测量右心室前后径(right ventricular,RV),大动脉短轴切面测量主肺动脉内径(main pulmonary artery,MPA),心尖四腔切面测量右心房左右径(right atrium,RA),Simpson法测量右心室射血分数(right ventricular ejection fraction,RVEF)。并记录心尖四腔切面二维动态图像,脱机后进行分析。
1.2.2 TAD的测量 将心尖四腔切面图像输入Qlab7.0工作站,进入TMAD模式,分别于三尖瓣环右心室游离壁处、室间隔处及右室心尖部心内膜下标记取样点,系统将使用半自动跟踪法,描绘出三尖瓣环两个点相对于心尖部的运动曲线,并计算出三尖瓣环右室游离壁处、室间隔处及二者连线中点处相对于右室尖部的收缩期峰值位移即T1、T2、Tm。
1.3 统计学处理 采用SPSS17.0软件分析,计量资料以均数±标准差(x±s)表示,采用独立样本t检验。
2 结 果
病例组与对照组相比,两组间年龄及RVEF差异无统计学意义(P>0.05)。病例组 MPA、RA、RV内径大于对照组(P<0.05);病例组T1及Tm较对照组明显减低(P<0.05),T2在两组间无统计学意义。详见表1、表29。
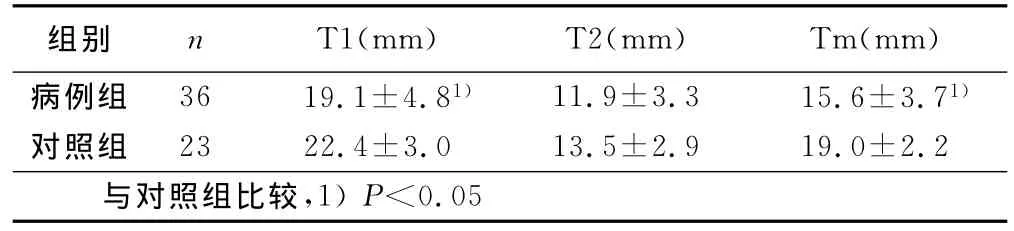
表2 病例组与对照组T1、T2及Tm比较(x±s)
3 讨 论
ASD患者常存在左向右分流,极易导致右心容量负荷过重,进而右心功能衰竭甚至死亡[2]。右心室对于维持心脏排血量、有效血容量及整体血流动力学都有重要的意义[3,4]。但右心室特殊的解剖位置及复杂的形态结构等影响了其功能的准确评价。新近发展的实时三维超声技术能较准确评价右心室收缩功能[5]。ASD患者右心室局部及整体收缩功能均较正常人减低[6]。王东光等[7]在研究房间隔缺损介入封堵术前后右心室功能变化中发现,ASD患者RVEF明显低于正常人,实时三维超声心动图可以较准确地评价ASD患者的右心室收缩功能。但目前来说,实时三维超声心动图仍有其自身缺点,如对图像质量要求较高,易受声窗和呼吸运动的限制,显示内膜不及二维图像清晰,且操作费时费力等,不适合于临床常规应用。
TMAD技术使用半自动法跟踪瓣环相对于心尖部的运动,通过定量分析瓣环运动参数来评价心室收缩功能[8]。Carlsson等[9]的研究表明,右心室纵向运动对于右心室收缩功能的贡献约为75%,径向运动为25%,认为测定右心室长轴收缩功能即可代表右心室的整体射血功能。三尖瓣环收缩期位移各参数与实时三维超声所测RVEF之间均呈显著正相关关系[10]。吴卫华等[11]应用斑点追踪显像技术评估扩张型心肌病患者右心室收缩功能,TAD各测值与三维超声所测RVEF相关性良好。
本研究结果显示,与正常人比较,ASD患者T1、Tm均显著减低,提示ASD患者右心室收缩功能减低;T2在两组之间的差别无统计学意义,这可能是由于T2不可避免地要受到左心室运动影响的结果,不能完全代表右心室功能。RVEF在ASD患者与正常人之间无显著差异,这可能是因为:①RVEF反应的是右室容积的相对变化,不能直接反应右室心肌的舒缩变化,不可避免地会受到右心室前后负荷及容量等因素的影响,此外,右心室形态结构极不规则,且内膜面不光滑,肌小梁丰富,故简单的假设几何模型不能准确代表右心室实际容积;②本研究未对病例进行分组,可能轻、重病例之间相互混杂,使得在统计中出现RVEF在ASD患者与正常人无统计学意义。值得注意的是,本研究中,在未分组的情况下,ASD患者的TAD已较正常人减低,由此说明,对于反映右心室收缩功能变化,TMAD技术测量TAD能较传统的Simpson法测量RVEF更灵敏,且采用TMAD技术测量TAD只需在三尖瓣环右心室游离壁处、室间隔处及心尖部心内膜下标记好取样点,系统将自动描绘出三尖瓣环两个点相对于右室心尖部的运动曲线,并计算出三尖瓣环右室游离壁处、室间隔处及二者连线中点处相对于心尖部的收缩期峰值位移,整个过程简便、迅速,可重复测量,人为因素干扰较小,比较适合临床操作。
本研究具有一定的局限性,样本量偏小,且仅限于ASD患者与正常人的对比,而ASD患者术前、术后TAD是否具有差异还有待探讨。另外,本研究未对ASD患者进行分组,若按照肺动脉收缩压进行轻、中、重度分组后,TAD是否会在组间呈现阶梯性变化,也有待于在进一步的研究中证实。
TMAD技术测量TAD可用于评价ASD患者的右心室收缩功能,或可成为临床常规评价右心室收缩功能的新方法。
[1] 赵利辉,黄灿亮,陈静婉,等.三尖瓣环收缩期位移评价肺动脉高压患者右心室功能的研究[J].中国医学影像学杂志,2011,19(2):87-91.
[2] Tomar M,Khatri S,Radhakrishnan S,et al.Intermediate and long-term followup of percutaneous device closure of fossa ovalis atrial septal defect by the Amplatzer septal occluder in a cohort of 529patients[J].Ann Pediatr Cardiol,2011,4(1):22-27.
[3] 朱丽敏.先天性心脏病右心功能的研究[J].国外医学:心血管疾病分册,2003,30(5):289-291.
[4] Webb G,Gatzoulis MA.Atrial septal defects in the adult:Recent progress and overview[J].Circulation,2006,114(15):1645-1653.
[5] Chen G,Sun K,Huang G.In vitro validation of right ventricular volume and mass measurement by real-time three-dimensional echocardiography[J].Echocardiography,2006,23(5):395-399.
[6] 方凌云,谢明星,王新房,等.实时三维超声心动图评价房间隔缺损患者右室整体及局部容积与功能[J].中国超声医学杂志,2008,24(5):428-431.
[7] 王东光,卢启秀.房间隔缺损介入封堵术前后右心室功能变化的超声评价研究[J].中国民康医学,2009,21(8):818;859.
[8] 张婷婷,李天亮.组织运动二尖瓣环位移自动追踪技术对正常人左心室收缩功能的评价[J].中西医结合心脑血管病杂志,2011,9(4):414-416.
[9] Carlsson M,Ugander M,Heiberg E,et al.The quantitative relationship between longitudinal and radial unction in left,right,and total heart pumping in humans[J].Am J Physiol Heart Circ Physiol,2007,293(1):636-644.
[10] 张琳,张军,苏海砾,等.斑点追踪技术测量三尖瓣环位移评价2型糖尿病患者右心室收缩功能[J].中国医学影像技术,2011,27(4):718-722.
[11] 吴卫华,黄艳,谢晓奕,等.斑点追踪显像检测三尖瓣环位移评估右心室收缩功能的应用价值[J].中华超声影像学杂志,2009,18(12):1034-1036.

