天然藻蓝蛋白对SD大鼠的长期毒性研究
宋璐非 刘 冰 赵 勇 田景振 秦 松
1.山东中医药大学药学院,山东济南 250355;2.中国科学院烟台海岸带研究所生物资源实验室,山东烟台 264003;3.烟台大学生命科学学院,山东烟台 264000
天然藻蓝蛋白对SD大鼠的长期毒性研究
宋璐非1刘 冰2赵 勇3田景振1秦 松2
1.山东中医药大学药学院,山东济南 250355;2.中国科学院烟台海岸带研究所生物资源实验室,山东烟台 264003;3.烟台大学生命科学学院,山东烟台 264000
目的 研究天然藻蓝蛋白对SD大鼠的长期毒性。 方法 将天然藻蓝蛋白水溶液分为高、中、低3个剂量与蒸馏水对照,对80只SD大鼠连续灌胃12周,恢复4周。除观察动物一般状态外,第12、16周分别对给药末期大鼠及恢复期结束的大鼠进行连续处死,检测血常规、血生化指标,精密量取心、肝、脾、肺、肾等重要脏器,计算其脏器系数,并进行常规病理检查。 结果 天然藻蓝蛋白对大鼠的一般状态、血常规、血生化指标、主要脏器质量系数及组织病理均无明显影响。停药4周后上述结果未见明显异常。与空白对照组比较,未见与天然藻蓝蛋白相关的明显异常。结论大鼠长期毒性试验表明天然藻蓝蛋白口服无毒性。
天然藻蓝蛋白;SD大鼠;长期毒性
藻蓝蛋白(Phycocyanin)是从螺旋藻中提取的天然捕光色素蛋白,属于藻胆蛋白(Phycobiliprotein)的一种。Romay等[1]第一次报道从蓝藻中提取的藻蓝蛋白具有抗氧化和抗炎作用,藻蓝蛋白还能抑制肝脏微粒脂过氧化物生成(IC50=12 mg/mL)。此外藻蓝蛋白和藻红蛋白的抗氧化活性也相继被证实[2-4]。Morcos等[5]首先发现了藻蓝蛋白的激光致细胞毒作用并对骨髓造血具有刺激作用。现已证实藻蓝蛋白能在适宜波长光的激发下,产生单线态氧和其他的氧自由基[6]用于肿瘤细胞光动力治疗。最近报道显示藻蓝蛋白对人肺腺同样有抑制作用[7]。在国内,刘宇峰等[8]证明螺旋藻藻蓝蛋白(C-PC)对K562(白血病)细胞的抑制效果良好。关燕清等[9]发现固定在聚苯乙烯(PSt)基板上藻蓝蛋白对体外肝癌细胞7402有抑制作用。目前对藻蓝蛋白的各种药理药效学研究已经积累了大量数据可供参考并且展示了开发成各种功能食品及药物的良好前景,但对其毒理学研究鲜见报道。本试验用自提天然藻蓝蛋白对SD大鼠进行长期毒性试验研究,为以后开发藻蓝蛋白为主要成分的功能食品和药物提供依据。
1 材料与仪器
1.1 受试药物的制备
食品级螺旋藻粉购自江苏赐百年公司,藻蓝蛋白从螺旋藻中提取[10],纯度 1.0(A620/A280)。
1.2 受试动物与饲养条件
SPF级SD大鼠购自绿叶制药[SCXK(鲁)20090009]。80只,雌雄各半,6~9周龄。适应性喂养一周,动物身体健康,无异常状况,试验开始时体质量差异不超过±20%。
饲养条件:饲养于塑料笼(350mm×24 mm×170 mm)内,每笼 1只。室温(22±2)℃,相对湿度 50%~70%,控制光 12 h,黑暗12 h。自由取水和食料,定期更换垫料。
1.3 设备与试剂
CA-500血球计数仪(AITAIKE),溶血素(山东兰桥医学科技有限公司),稀释液 (烟台卓越生物技术有限公司),TBA-40FR全自动生化分析仪(东芝,日本),检测试剂(中生北控生物科技股份有限公司)。
2 试验方法
2.1 动物分组
将80只SD大鼠按体重随机分为蒸馏水对照组与高、中、低三个剂量组,共4组,每组20只,雌雄各10只。
2.2 给药途径与剂量设计
灌胃,每次口服容量 1mL/(100 g·d)。
根据天然藻蓝蛋白经口急性毒性试验结果,12 g/kg无毒性反应和预试验结果,确定SD大鼠天然藻蓝蛋白长期毒性试验高剂量组为4.00 g/kg,中剂量组为0.40 g/kg,低剂量组为0.12 g/kg,对照组为蒸馏水。
2.3 检测指标
检测指标及时间见表1。
2.4 统计学方法
采用统计软件SPSS 11.5对实验数据进行分析,计量资料数据以均数±标准差()表示,采用方差分析,两两比较采用LSD-t检验。以P<0.05为差异有统计学意义。
3 结果
3.1 对大鼠一般状况及体质量的影响
各组动物发育良好,皮毛光泽,行为正常,大小便与对照组无差异,眼、鼻无异常分泌物,摄食正常。恢复期4周内无异常表现。连续给药12周及恢复期4周各组体质量逐周增加,各组体质量增长量差异无统计学意义(P>0.05)。给药12周及停药4周,各给药组大鼠的进食量与空白对照组比较差异无统计学意义(P>0.05)。
3.2 对大鼠外周血常规的影响
给药12周末次给药24 h后,连续处死大鼠,腹腔动脉取血。血常规各项指标均在正常值范围内,给药组与对照组比较差异无统计学意义(P>0.05)。结果见表2、3。恢复期4周末次给药24 h后,重复以上试验差异无统计学意义(P>0.05)。
3.3 对大鼠血液生化指标的影响
给药12周末次给药24 h后连续处死大鼠,腹腔动脉取血后静置30min,3 000 r/min离心10 min后去上清液,得到血清进行血液生化指标检查。结果与对照组比较,天门冬氨酸氨基转移酶(AST)、丙氨酸氨基转移酶(ALT)、碱性磷酸酶(ALP)、血清尿素氮(BUN)、总胆固醇(T-CHO)、血糖(GLU)、总蛋白(TP)、白蛋白(ALB)、肌酐(CREA)、总胆红素(TBIL)等含量差异无统计学意义(P>0.05)。见表4、5。恢复期4周末次给药24 h后,重复以上试验差异无统计学意义(P>0.05)。

表1 检测时间及指标
表2 天然藻蓝蛋白对大鼠血常规的影响(,n=6)

表2 天然藻蓝蛋白对大鼠血常规的影响(,n=6)
组别 剂量(g/kg) 雌性给药12周RBC(1012/L) Hb(g/L) PLT(109/L) WBC(109/L) N(%) L(%)蒸馏水对照组藻蓝蛋白低剂量组藻蓝蛋白中剂量组藻蓝蛋白高剂量组-0.12 0.40 4.00 8.16±1.00 7.86±1.62 9.07±1.70 8.83±1.27 161.64±19.30 157.89±21.56 150.37±24.98 172.43±26.77 876.55±139.39 913.36±159.58 826.93±148.63 896.50±123.39 6.02±1.54 5.22±1.95 5.89±1.23 5.13±2.01 75.93±15.73 83.58±17.65 79.35±16.08 80.78±20.01 20.31±15.43 22.40±17.02 19.21±16.88 25.34±20.10
表3 天然藻蓝蛋白对大鼠血常规的影响(,n=6)

表3 天然藻蓝蛋白对大鼠血常规的影响(,n=6)
组别 剂量(g/kg) 雄性给药12周RBC(1012/L) Hb(g/L) PLT(109/L) WBC(109/L) N(%) L(%)蒸馏水对照组藻蓝蛋白低剂量组藻蓝蛋白中剂量组藻蓝蛋白高剂量组-0.12 0.40 4.00 9.20±1.08 9.77±1.49 8.20±1.38 9.53±1.36 169.54±29.22 173.81±22.79 155.63±32.12 168.53±27.12 935.30±166.19 850.52±183.37 822.30±176.54 900.00±170.82 7.70±2.75 7.58±2.89 8.03±3.08 8.14±3.25 76.53±15.67 79.78±17.84 80.82±18.33 88.72±18.79 24.39±15.29 21.57±13.67 19.76±16.69 28.50±19.24
表4 天然藻蓝蛋白对雌性大鼠血液生化指标的影响(,n=6)
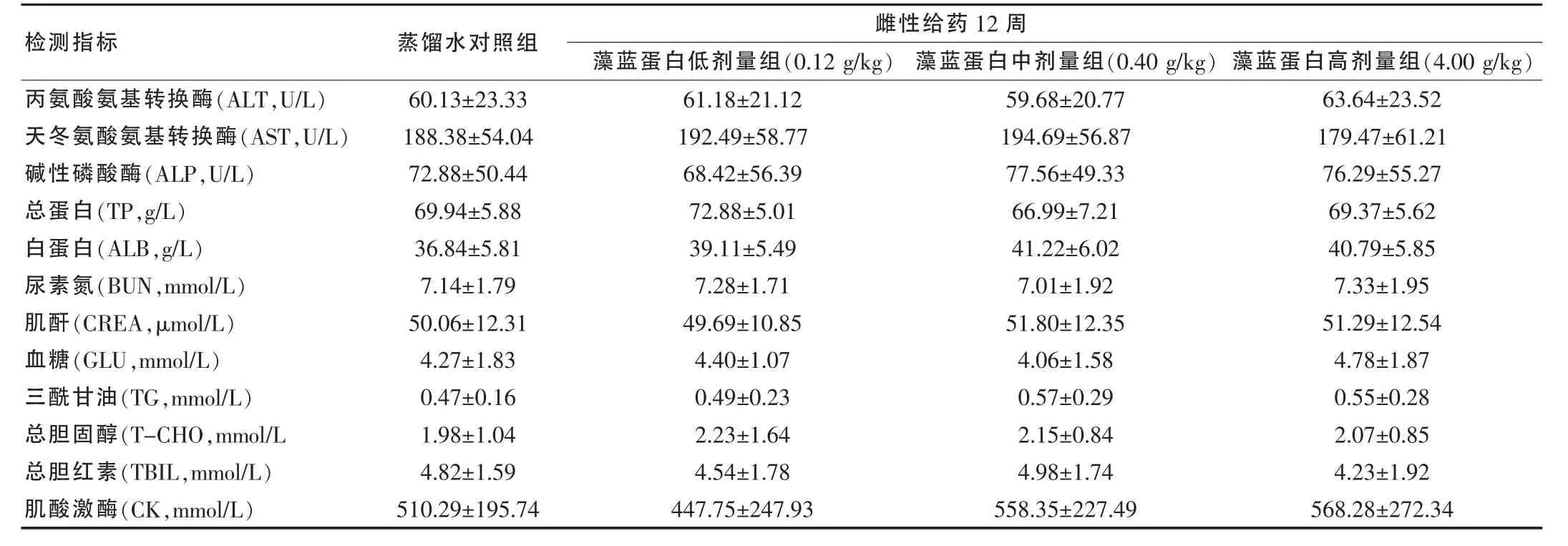
表4 天然藻蓝蛋白对雌性大鼠血液生化指标的影响(,n=6)
检测指标 雌性给药12周藻蓝蛋白低剂量组(0.12 g/kg) 藻蓝蛋白中剂量组(0.40 g/kg)藻蓝蛋白高剂量组(4.00 g/kg)蒸馏水对照组丙氨酸氨基转换酶(ALT,U/L)天冬氨酸氨基转换酶(AST,U/L)碱性磷酸酶(ALP,U/L)总蛋白(TP,g/L)白蛋白(ALB,g/L)尿素氮(BUN,mmol/L)肌酐(CREA,μmol/L)血糖(GLU,mmol/L)三酰甘油(TG,mmol/L)总胆固醇(T-CHO,mmol/L总胆红素(TBIL,mmol/L)肌酸激酶(CK,mmol/L)60.13±23.33 188.38±54.04 72.88±50.44 69.94±5.88 36.84±5.81 7.14±1.79 50.06±12.31 4.27±1.83 0.47±0.16 1.98±1.04 4.82±1.59 510.29±195.74 61.18±21.12 192.49±58.77 68.42±56.39 72.88±5.01 39.11±5.49 7.28±1.71 49.69±10.85 4.40±1.07 0.49±0.23 2.23±1.64 4.54±1.78 447.75±247.93 59.68±20.77 194.69±56.87 77.56±49.33 66.99±7.21 41.22±6.02 7.01±1.92 51.80±12.35 4.06±1.58 0.57±0.29 2.15±0.84 4.98±1.74 558.35±227.49 63.64±23.52 179.47±61.21 76.29±55.27 69.37±5.62 40.79±5.85 7.33±1.95 51.29±12.54 4.78±1.87 0.55±0.28 2.07±0.85 4.23±1.92 568.28±272.34
表5 天然藻蓝蛋白对大鼠血液生化指标的影响(,n=6)

表5 天然藻蓝蛋白对大鼠血液生化指标的影响(,n=6)
检测指标 雄性给药12周藻蓝蛋白低剂量组(0.12 g/kg) 藻蓝蛋白中剂量组(0.40 g/kg) 藻蓝蛋白高剂量组(4.00 g/kg)蒸馏水对照组丙氨酸氨基转移酶(ALT,U/L)天冬氨酸氨基转移酶(AST,U/L)碱性磷酸酶(ALP,U/L)总蛋白(TP,g/L)白蛋白(ALB,g/L)尿素氮(BUN,mmol/L)肌酐(CREA,μmol/L)血糖(GLU,mmol/L)三酰甘油(TG,mmol/L)总胆固醇(T-CHO,mmol/L)总胆红素(TBIL,mmol/L)肌酸激酶(CK,mmol/L)73.69±24.12 175.89±47.88 104.07±46.98 70.13±6.12 36.96±5.12 7.27±1.87 47.25±16.51 4.28±0.93 0.55±0.15 1.87±0.56 4.43±2.17 743.53±242.56 74.69±22.17 181.43±48.64 110.58±43.94 67.12±5.95 38.25±5.70 7.40±1.92 45.71±16.98 4.17±0.98 0.59±0.18 1.77±0.58 4.76±2.04 710.53±293.06 75.79±25.41 169.69±50.34 117.09±47.15 69.54±6.17 36.84±5.92 7.45±1.97 45.00±17.62 4.09±1.02 0.66±0.23 1.75±0.61 4.55±2.11 684.50±310.54 72.11±23.62 173.32±43.75 117.88±48.60 70.33±5.80 37.51±5.83 7.36±1.98 48.50±16.68 4.40±1.13 0.64±0.21 1.91±0.62 4.58±2.09 773.53±294.24
3.4 对大鼠脏器系数的影响
大鼠给药第12周后和恢复至16周时,解剖取心、肺、肝、脾、肾、脑、肾上腺、胸腺、睾丸/卵巢和前列腺/子宫,称其绝对重量并计算以上器官各占100 g体质量的相对重量。结果表明,藻蓝蛋白不影响动物脏器重量。
3.5 对大鼠重要脏器病理组织学检查
第12周解剖时,取心、肺、肝、脾、肾、脑、甲状腺、肾上腺、胸腺、副睾、前列腺/子宫和睾丸/卵巢、胃、十二指肠、回肠、结肠、胰腺、眼球及视神经、胸骨和骨髓,肉眼观察其外观和形态,与对照组比较差异无统计学意义(P>0.05)。HE染色后,光镜下观察各剂量给药组大鼠器官组织结构未发现组织萎缩、增长和炎症细胞浸润,未见明显的与受试物相关的病理性损伤。恢复至16周时各给药组以上组织器官与对照组比较差异无统计学意义(P>0.05)。
4 讨论
本研究用自提天然藻蓝蛋白对SD大鼠进行系统的长期毒性试验研究。结果显示,天然藻蓝蛋白以4.00、0.40、0.12 g/kg的剂量,对SD大鼠连续灌胃给药12周,对大鼠的体质量、饮食、饮水无不良影响;定期检测的RBC、PLT、WBC血常规以及 ALT、AST、ALP、TBIL、CREA 等血液生化指标都在正常范围内,并且与灌胃样品量无剂量依赖相关性,无明显的血常规毒性;对肝、脾、肾等重要脏器组织结构以及主要脏器系数的观察,未见明显肿胀、坏死以及炎症反应,综合以上结果表明样品口服无肝脏毒性。经过4周恢复期后检测上述各指标均未见明显异常,并且高、中、低剂量组数据与蒸馏水对照组比较差异无统计学意义(P>0.05),提示上述指标在停止灌胃后未见其他明显的后遗效应和继发毒性变化。对比已有的相关文献报道,结合大鼠长期毒性试验结果表明,天然藻蓝蛋白口服无毒性,属于实际无毒物,具有进一步开发成为功能食品和药物的价值。
[1]Romay C,Armesto J,Remirez D,etal.Antioxidant and anti-inflammatory properties of C-phycocyanin from blue-green algae [J].Inflamm Res,1998,47(1):36-41.
[2]俞丽君,李永明,陈艳丽,等.钝顶螺旋藻藻胆蛋白的纯化及其清除氧自由基的作用[J].台湾海峡,1999,18(2):172-176.
[3]Bermejo P,Pinero E,Ma A.Villar Iron-chelating ability and antioxidant properties of phycocyanin isolated from a protean extract of Spirulina platensis[J].Food Chemistry,2008,110:436-445.
[4]Manconia M,Pendas J,Ledon N,et al.Fadda Phycocyanin liposomes for topical anti-inflammatory activity:in-vitro in-vivo studies[J].Journal of Pharmacy and Pharmacology,2009,61:423-430.
[5]Morcos NC,Berns M,Henry WL.Phycocyanin:laser activation,cytotoxic effects,and uptake in human atherosclerotic plaque[J].Lasers Surg Med,1988,8(1):10-17.
[6]He JA,Hu YZ,Jiang LJ.Photodynamic action of phybiliproteins in situ generation of reactive oxygen species[J].J Biochim Biophys Acta:Bioenergetics,1997,1320(1):165-174.
[7]Zhang X,Li JY,Gong XG.Isolation of C-PC subunits from spirulina platensis and inhibitory effect on SPC-A-1 cell line [J].Journal of Zhejiang University:Science Edition,2010,37(3):319-323.
[8]刘宇峰,程霓.螺旋藻藻蓝蛋白对人血癌细胞K562生长的影响[J].南京大学学报:自然科学版,2000,36(5):640-642.
[9]关燕清,徐和德,郭宝江.光固定化藻蓝蛋白对体外肝癌细胞7402的抑制作用[J].离子交换与吸附,2000,16(6):547-552.
[10]吴蕾,庞广昌,陈庆森.螺旋藻藻蓝蛋白的规模化提取和色谱纯化技术研究进展[J].食品科学,2008,29(4):461-463.
Chronic toxicity study of Phycocyanin on Sprague Daw ley rats
SONG Lufei1 LIU Bing2 ZHAO Yong3 TIAN Jingzhen1 QIN Song2
1.School of Pharmacy,Shandong University of Traditional Chinese Medicine,Shandong Province,Ji′nan 250355,China;2.Biological Resources Laboratory,Yantai Institute of Coastal Zone Research,Chinese Academy of Sciences,Shandong Province,Yantai 264003,China;3.College of Life Sciences,YantaiUniversity,Shandong Province,Yantai 264000,China
Objective To investigate the chronic toxicity induced by oral administration of Phycocyanin to Sprague Dawley rats.MethodsRats were randomly divided into four groups:control group,which
the distilled water,and three treatmentgroups,which received oral administration of high,medium and low doses of Phycocyanin.Totally 80 SD ratswere continuously administrated for 12 weeks,and then recovered for 4 weeks.Except for general factors such as bodyweight,food consumption and daily behavior,the routine biochemical blood indictors,the organ/bodyweight rate,the pathological changes of important organs such as heart,liver,spleen,lung,kidney,brain were also detected after 12 weeks and 16 weeks.The viscera coefficientwas calculated,and pathologicalwas examed routinely.ResultsThere was no significant influence of Phycocyanin on the blood routine,serum indictors and organ/bodyweight rate of the three dose group rats.ConclusionTheResultsof long-term toxicity experiment show that oral administration of Phycocyanin is safe.
Phycocyanin;SD Rats;Chronic toxicity
R948
A
1673-7210(2012)11(c)-0015-04
国家海洋局海洋公益性行业科研专项经费项目(项目编号:201205027)。
宋璐非(1985-),男,山东济南人,硕士研究生,主要从事中药新药、新剂型的研究。
田景振,教授,博士生导师;秦松,研究员,博士生导师。
2012-06-27 本文编辑:卫 轲)

