正丙苯的合成研究
郑行行,王蕊娜,李效军
(河北工业大学 化工学院,天津 300130)
正丙苯的合成研究
郑行行,王蕊娜,李效军
(河北工业大学 化工学院,天津 300130)
以苯和丙酸为起始原料,经酰氯化、Freidel-Crafts酰基化和沃尔夫-克斯尼尔-黄鸣龙还原反应合成了正丙苯。采用1H NMR方法分析了产物结构。表征结果显示,中间产物及最终产物为目标化合物。考察了反应物的摩尔比、反应温度和反应时间对各反应的影响。实验结果表明,合成中间产物丙酰氯、苯丙酮和最终产物正丙苯的各反应的优化条件分别为:n(氯化亚砜)∶n(丙酸)=1∶1.1,120 ℃反应6 h;n(丙酰氯)∶n(AlCl3)∶n(苯)=1∶1.1∶8.5,50 ℃反应2 h,80 ℃反应4 h;n(苯丙酮)∶n(水合肼)∶n(KOH)=1∶4∶2,120 ℃反应2 h,160 ℃反应4 h。在优化的反应条件下,丙酰氯、苯丙酮和正丙苯的收率分别可达73.5%,90.1%,95.6%。
正丙苯;苯丙酮;丙酰氯;Freidel-Crafts酰基化;沃尔夫-克斯尼尔-黄鸣龙还原
烷基苯是重要的化工产品,可直接作为溶剂,也是合成其他重要化工原料的中间体[1]。正丙苯可用于纺织染料、印刷、醋酸纤维溶剂及合成聚丙烯成核剂(双-1,3,2,4-(4’-丙基亚苄基)-1-丙基山梨醇[2])的中间体,该成核剂具有成核效率高、透明度大、生物适应性好和气味小等优点[3-4]。
以烯烃[5]、1-氯代烷烃[6]或一级醇为烷基化试剂与苯反应时,这些烷基化试剂在酸催化作用下形成的碳正离子易发生重排,得到的产物通常以异烷基苯为主。因此需开发反应过程短、操作简单且能避免碳正离子重排的高纯度正丙苯的合成路线。
本工作以苯和丙酸为主要起始原料,经酰氯化反应[7-8]、Freidel-Crafts酰基化反应[9]以及沃尔夫-克斯尼尔-黄鸣龙还原反应[10-11]合成了正丙苯,并考察了反应物的摩尔比、反应时间和反应温度对产物的收率及纯度的影响。
1 实验部分
1.1 仪器和试剂
BEIFEN-SP3420型气相色谱仪:北京北分瑞利分析仪器集团;AC-400型核磁共振仪:400 MHz,Brucker公司。
丙酸、氯化亚砜、苯、无水AlCl3:分析纯,天津市江天化工技术有限公司;水合肼、一缩二乙二醇:分析纯,天津大学科威公司;KOH:纯度不小于85.0%(w),天津博迪化工股份有限公司。
1.2 实验方法
1.2.1 丙酰氯的合成
向装有球形冷凝管(连接尾气干燥吸收装置)、温度计和磁力搅拌的250 mL四口瓶内加入0.55 mol丙酸,搅拌下,于1~2 h内自恒压滴液漏斗中缓慢滴加0.5 mol氯化亚砜(滴加温度低于20℃);滴毕,迅速升温至120 ℃回流,搅拌反应6 h;反应完毕,将反应液冷却至25 ℃,常压蒸馏,收集78~81 ℃的馏分,产物为无色或淡黄色液体。
1.2.2 苯丙酮的合成
向装有球形冷凝管(连接尾气干燥吸收装置)、温度计和磁力搅拌的250 mL四口瓶内加入0.22 mol无水AlCl3和1.4 mol苯,搅拌冷却下,滴加含0.2 mol丙酰氯的苯溶液0.28 mol约1.5 h;滴毕,升温至50 ℃反应2 h;再加热至80 ℃反应4 h;反应结束后,冷却,滴加80 mL蒸馏水至白色沉淀完全溶解,静置分液;水相用苯萃取两次,合并有机相,经碱洗、水洗,常压蒸出苯,再减压收集120~130 ℃(-0.09 MPa)的馏分,产物为无色或淡黄色透明液体。
产物的1H NMR (400 MHz,CDCl3)表征结果(化学位移δ):7.936~7.959(d,2H,CH);7.273~7.449(m,2H,CH);7.506~7.545(m,1H,CH);2.947~3.002(m,2H,CH2);1.192~1.238(m,3H,CH3)。1H NMR表征结果显示,产物与目标化合物苯丙酮的结构相符。
1.2.3 正丙苯的合成
向装有球形冷凝管、温度计和机械搅拌的250 mL四口瓶内加入0.6 mol KOH、8.4 g H2O、苯丙酮、一缩二乙二醇;加热搅拌待KOH全部溶解后,加入33 mL 80%(w)的水合肼,升温至120 ℃反应2 h;加分水器在160 ℃下保温分水4 h,反应结束。常压蒸馏收集150~160 ℃的馏分,产物为无色透明状液体。
产物的1H NMR (400 MHz,CDCl3)的表征结果(δ):7.148~7.200(d,3H,CH);7.248~7.285(m,2H,CH);2.559~2.598(m,2H,CH2);1.611~1.667(m,2H,CH2);0.919~0.956(m,3H,CH3)。1H NMR表征结果显示,产物与目标化合物正丙苯的结构相符。
2 结果与讨论
2.1 丙酰氯的合成
2.1.1 合成丙酰氯的反应机理
丙酰氯由丙酸和氯化亚砜经酰氯化反应合成(见式(1))。丙酸与氯化亚砜反应生成混酸酐,由于羟基为易离去的基团从而使羰基碳上的正电荷数增加,亲核试剂(Cl-)进攻羰基碳生成丙酰氯。该反应的优点:产物中的HCl和SO2都为气体,容易分离,因此是合成丙酰氯的通用方法之一。2.1.2 反应物摩尔比的影响

丙酰氯易水解,一般通过蒸馏方法将其他产物或未反应完的反应物与其分离。氯化亚砜的沸点(76 ℃)与丙酰氯的沸点(80 ℃)相近,后处理时分离较困难。通过实验初步确定丙酸过量有利于反应。n(氯化亚砜)∶n(丙酸)对丙酰氯收率的影响见表1。由表1可看出,当n(氯化亚砜)∶n(丙酸)=1∶1.0时,不能反应完全,收率不高;当n(氯化亚砜)∶n(丙酸)=1∶1.1时,收率最高;丙酸用量继续增加,收率反而降低,因为过量的丙酸会与生成的丙酰氯发生副反应生成副产物酸酐。选择n(氯化亚砜)∶n(丙酸)=1∶1.1较适宜。

表1 n(氯化亚砜)∶n(丙酸)对丙酰氯收率的影响Table 1 Influence of n(sulfoxide chloride)∶n(propanoic acid) (r1)on the yield of propionyl chloride
2.1.3 反应时间的影响
反应时间对丙酰氯收率的影响见表2。由表2可看出,随反应时间的延长,收率增加,当反应时间为6 h时收率最高,可达73.5%;此后继续延长反应时间,收率反而降低。这是因为反应物中的丙酸是过量的,反应时间太长,过量的酸会与生成的丙酰氯发生副反应,使收率降低;且反应时间过长也会使丙酰氯少量挥发。反应时间为6 h较适宜。
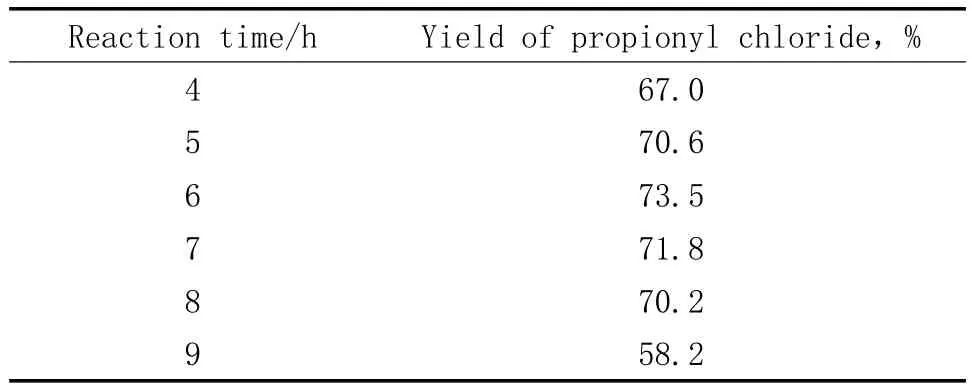
表2 反应时间对丙酰氯收率的影响Table 2 Influence of reaction time on the yield of propionyl chloride
2.2 苯丙酮的合成
2.2.1 合成苯丙酮的反应机理
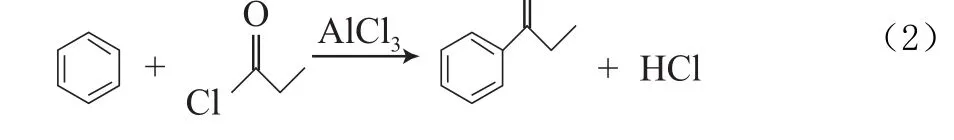
苯丙酮由丙酰氯在无水AlCl3的催化下与苯经Freidel-Crafts酰基化反应合成(见式(2))。丙酰氯先与AlCl3结合得到复合物R(O),复合物中的碳正离子再进攻苯环得到酮与AlCl3的络合物,络合物经水解得到相应的酮。该反应的优点:由于酰基是一个间位定位基,当苯环上的一个氢原子被酰基取代后,该苯环会自行终止反应,不会出现生成多元取代混合物的现象,因此反应收率一般都很高,且生成的副产物HCl为气体,容易分离。
2.2.2 催化剂用量的影响
为提高转化率,催化剂AlCl3的用量应比理论值稍多。n(丙酰氯)∶n(AlCl3)对苯丙酮的收率及纯度的影响见表3。

表3 n(丙酰氯)∶n(AlCl3)对苯丙酮的收率和纯度的影响Table 3 Influences of n(propionyl chloride)∶n(AlCl3) (r2) on the yield and purity of propiophenone
由表3可看出,当n(丙酰氯)∶n(AlCl3)=1∶1.0时,纯度和收率均较低;当n(丙酰氯)∶n(AlCl3)=1∶1.1时,收率和纯度最高;继续增加AlCl3的用量,收率呈下降趋势,可能因为过量的AlCl3与苯丙酮形成络合物的量增加,后处理时分解不彻底,导致收率下降。选择n(丙酰氯)∶n(AlCl3)=1∶1.1较适宜。
2.2.3 苯用量的影响
在合成苯丙酮的反应中,苯既是反应物又是溶剂。n(丙酰氯)∶n(苯)对苯丙酮的收率及纯度的影响见表4。由表4可看出,随苯用量的增加,收率和纯度均增大;当n(丙酰氯)∶n(苯)=1∶8.5时,收率和纯度最高;此后继续增加苯的用量,收率和纯度变化不大。选择n(丙酰氯)∶n(苯)=1∶8.5较适宜。
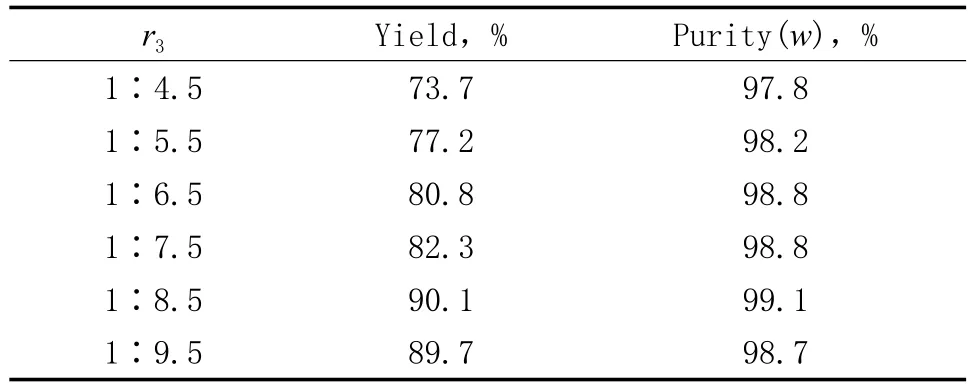
表4 n(丙酰氯)∶n(苯)对苯丙酮的收率和纯度的影响Table 4 Influences of r3 on the yield and purity of propiophenone
2.2.4 反应时间的影响
反应时间对苯丙酮收率和纯度的影响见表5。

表5 反应时间对苯丙酮的收率和纯度的影响Table 5 Influences of reaction time on the yield and purity of propiophenone
由表5可看出,随反应时间的延长,收率和纯度均增大;当反应时间为4 h时,收率达90%以上,纯度可达99.1%(w);继续延长反应时间,纯度虽稍有提高,但收率下降。其原因可能是反应时间过长,AlCl3与苯丙酮生成络合物的量增加,后处理时水解不彻底,导致苯丙酮的回收有所损失。综合考虑,80 ℃下反应时间以4 h为宜。
2.3 正丙苯的合成
2.3.1 合成正丙苯的反应机理
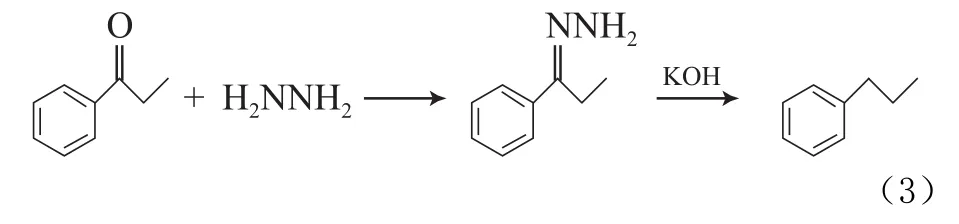
正丙苯由苯丙酮与水合肼经沃尔夫-克斯尼尔-黄鸣龙还原反应合成(见式(3))。将酮还原成亚甲基化合物的方法通常有两种:克莱门森还原反应,即在酸性条件下用锌汞齐作还原剂,该反应的缺点是会产生大量的重金属副产物污染环境;沃尔夫-克斯尼尔-黄鸣龙还原法相对清洁,其反应机理是醛或酮和肼反应生成腙,腙在碱催化剂的作用下发生质子的可逆加成和消除反应,形成偶氮化合物的负离子,负离子在高温下分裂出N后和质子结合形成亚甲基化合物。对于脂肪基醛酮或芳基醛酮,中间体腙在碱催化下可生成和反应物结构一致的还原产物。
2.3.2 KOH用量的影响
n(苯丙酮)∶n(KOH)对正丙苯的收率及纯度的影响见表6。由表6可看出,当n(苯丙酮)∶n(KOH)=1∶2时,收率和纯度均较好;继续增加KOH的用量,纯度虽有所增加,但收率降幅较大。选择n(苯丙酮)∶n(KOH)=1∶2较适宜。

表6 n(苯丙酮)∶n(KOH)对正丙苯的收率及纯度的影响Table 6 Influences of n(propiophenone)∶n(KOH)(r4) on the yield and purity of n-propylbenzene
2.3.3 反应时间的影响
在合成正丙苯的反应中,120 ℃下苯丙酮与80%(w)水合肼先生成腙,然后升温至160 ℃腙发生分解反应得苯丙酮。反应时间对正丙苯的收率和纯度的影响见表7。
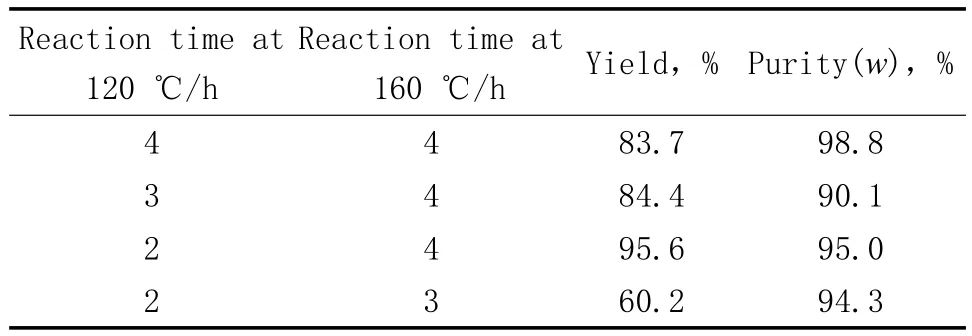
表7 反应时间对正丙苯的收率及纯度的影响Table 7 Influences of reaction time on the yield and purity of n-propylbenzene
由表7可看出,在120 ℃反应2 h,然后在160 ℃反应4 h时,收率达95.6%,纯度达95.0%(w);在120 ℃下即使反应时间延长,收率和纯度也不再提高。160 ℃下的反应时间如缩短至3 h,收率和纯度均降低,因为在此阶段如反应时间太短则生成的腙不能完全分解,导致收率降低。120 ℃下反应2 h然后160 ℃下反应4 h较适宜。
3 结论
(1)合成丙酰氯适宜的反应条件为:n(氯化亚砜)∶n(丙酸)=1∶1.1、反应时间6 h。在此条件下,丙酰氯收率可达73.5%。
(2)合成苯丙酮适宜的反应条件为:n(丙酰氯)∶n(AlCl3)∶n(苯)= 1∶1.1∶8.5,50 ℃反应2 h、80 ℃反应4 h。在此条件下,苯丙酮的收率为90.1%,纯度为99.1%(w)。
(3)合成正丙苯适宜的反应条件为:n(苯丙酮)∶n(水合肼)∶n(KOH)=1∶4∶2;120 ℃反应2 h、160 ℃反应4 h。在此条件下,正丙苯的收率为95.6%,纯度为95.0%(w)。
[1] 高志成. 二十四烷基苯的制备[J]. 石油化工,1991,20(8):571 - 574.
[2] Milliken & Company. Dibenzylidene Sorbitol(DBS)-Based Compounds,Compositions and Methods for Using Such Compounds:US,7662978B2[P]. 2010-02-16.
[3] 张友强,梁勇芳. 聚丙烯成核剂的研究与发展[J]. 工程塑料应用,2010,38(2):85 - 88.
[4] Xu T,Lei H,Xie C S. The Effect of Nucleating Agent on the Crystalline Morphology of Polypropylene(PP)[J].Mater Des,2003,24(3):227 - 230.
[5] 雷志刚,陈标华,李成岳. 苯与烯烃烷基化反应的研究进展[J]. 化学反应工程与工艺,2002,18(1):1 - 5.
[6] 王莉. 苯与氯乙烷烷基化制乙苯的研究[D]. 北京:北京化工大学,2011.
[7] 喻名强,刘广义,尹兴荣,等. 酰氯的合成方法及其应用新进展[J]. 精细化工中间体,2011,41(4):1 - 7.
[8] 信建峰,马吉海,张树芬,等. 酰氯制备方法综述[J]. 河北化工,2006,29(11):16 - 20.
[9] Universal Oil Products Company. Process for the Acylation of Aromatic Hydrocarbons:US,3883594[P]. 1975-05-13.
[10] 陶风岗,许临晓,邵黎明,等. 黄鸣龙还原法中溶剂作用的讨论[J]. 有机化学,1983,9(1):25 - 28.
[11] Taber D F,Stachel S J. On the Mechanism of the Wolff-Kishner Reduction[J].Tetrahedron Lett,1992,33(7):903 -906.
(编辑 邓晓音)
Synthesis of n-Propylbenzene
Zheng Xingxing,Wang Ruina,Li Xiaojun
(School of Chemical Engineering and Technology,Hebei University of Technology,Tianjin 300130,China)
n-Propylbenzene was synthesized from benzene and propionic acid by acyl chlorination,Friedel-Crafts acylation and Wolff-Kishner-Huang Minlon reduction. The structures of the intermediates and product were tested and verified by means of1H NMR. The effects of the mole ratios of the reactants,reaction temperatures and reaction times on the reactions were investigated.The results indicate that under the optimum reaction conditions for the propionyl chloride synthesis ofn(sulfoxide dichloride)∶n(propionic acid) 1∶1.1,reaction temperature 120 ℃ and reaction time 6 h,for the propiophenone synthesis ofn(propionyl chloride)∶n(AlCl3)∶n(benzene) 1∶1.1∶8.5,reaction temperature 50 ℃ for 2 h and then 80 ℃ for 4 h,and for then-propylbenzene synthesis ofn(propiophenone)∶n(hydrazine hydrate)∶n(KOH) 1∶4∶2,reaction temperature 120 ℃ for 2 h and then 160 ℃ for 4 h,the yields of propionyl chloride,propiophenone andn-propylbenzene can reach 73.5%,90.1% and 95.6%,respectively.
n-propylbenzene;propiophenone;propionyl chloride;Friedel-Crafts acylation;Wolff-Kishner-Huang Minlon reduction
1000 - 8144(2012)09 - 1056 - 04
TQ 241.14
A
2012 - 02 - 27;[修改稿日期]2012 - 05 - 30。
郑行行(1988—),女,河南省驻马店市人,硕士生,电话 022 - 60202469,电邮 zheng.xing1988@163.com。联系人:李效军,电话 022 - 26582469,电邮 lixiaojun@hebut.edu.cn。

