Baeyer–Villiger重排反应的研究进展
武 宁, 孙晓云, 岳 爽, 臧树良
(1. 辽宁石油化工大学, 辽宁 抚顺 113001; 2. 沈阳航空航天大学,辽宁 沈阳110136; 3. 辽宁大学,辽宁 沈阳110036)
综合评述
Baeyer–Villiger重排反应的研究进展
武 宁1, 孙晓云2, 岳 爽3, 臧树良1
(1. 辽宁石油化工大学, 辽宁 抚顺 113001; 2. 沈阳航空航天大学,辽宁 沈阳110136; 3. 辽宁大学,辽宁 沈阳110036)
介绍了近些年Baeyer-Villiger反应中氧化方面的研究情况,主要介绍常用的催化剂,包括酸类和具有碱性的水滑石类、过渡金属离子的分子筛类、微生物酶类及过渡金属配合物类,同时介绍了离子液体在Baeyer-Villiger氧化反应中的应用现状。
Baeyer-Villiger重排反应;催化剂;离子液体
Baeyer-Villiger是将酮氧化成相应的酯的一类氧化反应,也叫做Baeyer–Villiger重排[1,2]。Adolf Baeyer等第一次于1899年报道了Baeyer–Villiger重排反应,他们选择过硫酸钠和浓硫酸为氧化剂,进行了薄荷酮等的Baeyer-Villiger氧化反应。此后,此类反应在天然产物等的合成中发挥着重要的意义。对于此反应中常见的氧化剂,冯小明等[3]曾作过系统的综述,常规的B-V反应通常用三氟过氧乙酸、过氧苯甲酸等作为氧化剂,但用三氟过氧乙酸、过氧苯甲酸等作为氧化剂会对环境造成严重的污染,工业上已经很少被使用,新型的Baeyer-Villiger反应氧化剂以环境友好的H2O2和O2为主。
在对Baeyer–Villiger重排反应的研究中,催化剂方面的研究一直是热点。同时,离子液体作为一类新型的绿色溶剂,近几年来也开始被应用于Baeyer–Villiger氧化反应。
1 Baeyer–Villiger氧化反应5类催化剂
1.1 酸类
酸类催化剂作为一类高效催化剂在Baeyer-Villiger重排反应中应用广泛。由于过酸在作为氧化剂的同时也具有很好的催化性能,所以也可以把过酸类催化体系归于酸催化体系中。事实上,在很多反应体系中,酸催化剂的存在会大大提高反应活性。张研等[4]发现,在以乙酸酐为介质的Baeyer–Villiger重排反应中,可以用过碳酸钠(Na2CO3﹒H2O2)作氧化剂,将环酮或酮氧化成相应的内酯或酯。Berkessel等[5]报道了环己酮等的Baeyer–Villiger重排反应,反应中他们选择以酸作催化剂、以环境友好的H2O2为氧化剂。在温度、溶剂等条件相同的情况下,与不加催化剂的空白试验进行对照,加入酸类催化剂时的反应转化率和产率都有很大的提高。同时,他们在试验中还发现,该类Baeyer–Villiger重排反应中存在溶剂效应,在相同条件下,以1,1,1,3,3,3-六氟-2-丙醇(HFIP)为溶剂时,转化率和产率较其他溶剂都高,所以选择合适的溶剂也是该类重排反应中的研究重点。
Lewis酸类如SnCl4等能够与酮羰基之间发生络合作用,进而活化酮羰基,使H2O2、O2等氧化剂更容易进攻酮羰基,促进重排反应的进行。所以很多Lewis酸类也常用作Baeyer–Villiger重排反应中的催化剂。
1.2 碱性的水滑石类
固体水滑石及类水滑石对Baeyer–Villiger重排反应具有比较高的催化活性。Kanda等[6-10]研究发现,在以层状水滑石等水滑石类作为催化剂催化的Baeyer–Villiger重排反应中,不仅反应中的产率较高,而且催化剂在反应后可以很好的分离回收再利用。Kanda等认为, Baeyer–Villiger重排反应的活性中心恰好是水滑石的碱性中心,这个碱性中心可以促进过酸把氧传递给酮这个重要过程的进行。所以,碱性的水滑石类催化剂才会对Baeyer–Villiger重排反应有着很高的催化活性。
Kanda等还认为,由于 Fe3+,Cu2+等变价金属离子可以和水滑石类的碱性中心发生协同作用,所以Fe3+,Cu2+等变价金属离子的加入能明显提高Baeyer–Villiger重排反应的转化率和产率[11]。
1.3 过渡金属离子的分子筛类
过渡金属离子的分子筛在Baeyer–Villiger重排反应中的应用十分广泛。Bhaumik等[12]第一次报道了在催化氧化Baeyer–Villiger重排反应中应用TS—1分子筛。Corma等[13]的研究结果表明,掺杂金属离子Sn的β分子筛类,可以选择地活化酮上的羰基,从而能够有效的促进Baeyer–Villiger重排反应有效进行,反应产物中相应内酯的比例可达到98%。并且反应中的选择性也很高,对于不饱和酮,也能生成单一的目标酯或内酯,无环氧化物等副产物。他们还以对甲氧基苯甲醛为底物,以Sn—β分子筛等作催化剂,催化氧化对甲氧基苯甲醛生成甲酸酯,进一步水解生成酚,其效果也较好[14-15]。
以Sn—β分子筛作催化剂的Baeyer–Villiger重排反应过程有如下优点:首先,由于此类催化剂催化的Baeyer–Villiger重排反应中没有由醛生成的相应的酸的过程,因此提高了重排反应的原子经济性;其次,无论是从反应的温度还是从溶剂的量来看,其温和的反应条件和较少的溶剂用量都使得Sn—β分子筛类催化剂有着较好的工业应用前景。
1.4 微生物酶类
微生物酶是指起着催化生物体系中特定反应的、由微生物活细胞产生的蛋白质。作为催化剂的微生物酶,它可以加速三种反应:水解反应、氧化反应和合成反应。微生物酶可以在活细胞内进行催化作用,也可以透过细胞作用细胞外的物质;前者称内酶,后者称外酶。酶的催化过程是一个两步反应: E + S→ ES→ E + P 酶基质 复合物 酶 底物酶具有专一性。酶的活性受环境条件的影响十分显著,主要的物理环境条件有:温度、需氧量和pH值,这些条件是废水生物处理过程中的最重要因素。
微生物酶在氧化反应中的催化活性较高。此类催化剂催化氧化的Baeyer–Villiger重排反应可在室温中性或接近中性的条件下进行,这样温和的反应条件会减低反应中发生重排的几率,而且无论是从绿色化学还是从能源节约的角度考虑,微生物酶类催化剂都明显优于其他类型的催化剂。最早被应用于催化氧化Baeyer–Villiger重排反应的微生物酶为CHMO(环己酮单氧酶),近几十年来,应用于Baeyer–Villiger重排反应的单酶有20多种。常见的微生物酶催化剂[16,17]有:E.coli Top 10 [pQR 239]、NCIMB9871,环戊酮单过氧化酶(CPMO)、以及4-羟基苯己酮单过氧化酶(HAPMO)等催化活性较高的微生物酶类。从反应的立体选择性的角度来讲,微生物酶催化的Baeyer–Villiger重排反应较化学法更高。目前,该方法由于在反应中有代谢副产物的生成,所以应用于工业化生产还有一定的局限性。近年来,基因工程酵母菌成为了人们研究的新热点,基因工程酵母菌在Baeyer–Villiger重排反应中的应用不仅可以降低毒性,还可以提高催化活性,为微生物酶类催化的Baeyer–Villiger重排反应的工业化应用起到很好的促进作用。
1.5 过渡金属配合物类
在Baeyer-Villiger重排反应催化剂的研究中,过渡金属配合物类的应用也很广泛。按反应体系可分为均相催化剂和非均相催化剂两类,其中固体酸、硅胶负载的钛配合物和硒等属于非均相催化剂;均相催化剂主要基于铂、锆、铼、硒、砷和钼等,此催化体系中通常采用的氧化剂为分子氧,此外,还常加入醛类作为体系的共氧化剂[18]。
1978 年,Jacobson等首次将过渡金属Mo的配合物应用于Baeyer-Villiger反应, 随后又发展了一系列过渡金属( Cu , W , Re , Mn ,Pt , Sc , Ti 等)的配合物,它们在光学活性化合物的合成中应用较广。1994年,Bolm第一次报道了环己酮和环庚酮的不对称的Baeyer-Villiger重排反应。他们选择镍和铜的金属配合物作催化剂,将环酮类氧化成了目标的内酯。但试验结果不太理想,而且此类催化体系在很大程度上受到溶剂种类的制约[19]。于此同时,Strukul等以手性铂作催化剂催化不对称的Baeyer-Villiger重排反应[20]。Tatsuya等接着又以Co(Ⅲ)(salen)作催化剂、催化手性的3-取代的环丁酮生产相应的内酯,同样取得了较好的产率和e.e.值[21-25]。
2 离子液体的应用
离子液体即完全由正负离子组成的室温下为液体的盐,由于阴阳离子数目相等,因而整体上显中性。又称室温离子液体或者室温熔融盐,也称非水离子液体、液态有机盐等。简而言之,离子液体是指在室温或室温附近温度下呈液态,并由阴阳离子组成的物质。与熔盐相比,离子液体的熔点低于100 ℃;与固态物质相比,它是液态;与传统的液态物质相比,它是离子型,离子液体具有不挥发、热稳定性较高、便于反应操作处理和易于回收等特点,近年来倍受关注。此外,通过阴阳离子的设计,可调节其对无机物、有机物、及聚合物的溶解性,并且其酸度可调至超酸。最初的离子液体主要用于电化学的研究,近年来在作为环境友好的溶剂方面有很大的潜力。目前,应用于催化氧化Baeyer-Villiger重排反应中的离子液体大多作为反应溶剂,比较常用的是[bmim]BF4[26],此外,还有HmimOAc[27]等。
2.1 [bmim]BF4
近年来,Roberta Bernini等将离子液体[bmim]BF4(图1)应用于Baeyer-Villiger重排反应,建立了一种以离子液体作溶剂,催化氧化Baeyer-Villiger重排反应的新的催化体系。

图1 [bmim]BF4离子液体的结构Fig.1 The structure of ionic liquid [bmim]BF4
MTO(甲基三氧化铼)在化学领域应用最多最广的是作为多种有机化学的催化剂使用。Roberta Bernini等以MTO为催化剂,在离子液体[bmim]BF4中催化环丁酮等生成相应的内酯,获得了较高的产率和转化率。从绿色化学的角度讲,此催化体系在较温和的反应条件下进行(室温或者40 ℃),此外,此催化体系可循环使用,而且在循环5次内得到的产率没有明显降低。此反应机理如图2。
Bernini等还在MTO(甲基三氧化铼)上负载聚4-乙烯基吡啶,以丁醇为溶剂,以H2O2为氧化剂氧化甲基化的4′,5,7-三羟黄烷酮和和5,7,3′三羟基-4′甲氧基黄烷酮生成相应的酯,产率也较高。上述反应体系虽然达到了较高产率和转化率,但反应的选择性不是很好,而且催化剂循环使用次数也有限。
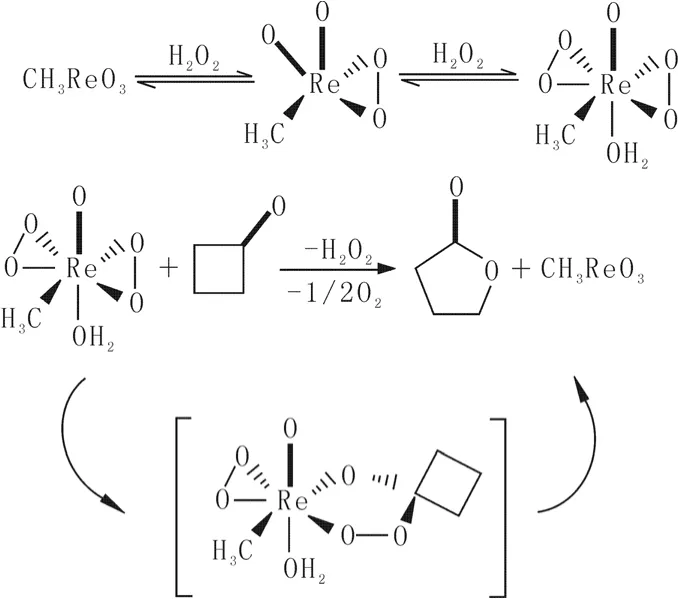
图2 离子液体中MTO催化氧化机理Fig.2 Pathway of cyclobutanone oxidation catalyzed by MTO
2.2 HmimOAc等
最近,Anna Chrobok等以过硫酸氢钾为氧化剂,以各种离子液体为溶剂,在40 ℃的条件下,研究了各种离子液体在此体系中对Baeyer-Villiger氧化反应的影响。实验结果表明,此体系中效果最好的离子液体是[bmim]BF4和HmimOAc。随后将这两种离子液体应用于其它内酯和酯的合成中,都获得了较高的产率(65%~95%);这两种离子液体被循环使用3次后,催化活性无较大的损失。该实验体系虽然获得了较高的产率和较好的选择性,但是此体系中离子液体的循环使用次数有限。
3 结束语
几十年来,在重排反应的体系中,各种各样的催化剂已广泛应用于催化氧化Baeyer-Villiger重排反应。在Baeyer-Villiger重排反应中,液态的过酸做氧化剂,加入苯甲醛等醛类做助催化剂的反应体系不利于实现重排反应的原子经济性,因此,上述介绍的5种催化体系中,固体酸和过渡金属离子的分子筛类催化剂有着很好的工业应用前景。从近几年对Baeyer-Villiger重排反应催化剂的研究现状来看,催化体系中催化活性、反应的原子经济性以及将Baeyer-Villiger重排反应应用于不对称合成中等方面将是以后值得关注的重点方向。随着人们的研究,绿色化学已经深入到化学界的各个领域,离子液体作为一种新型绿色溶剂逐渐被人们认识,在很多化学反应中都开始尝试使用离子液体来代替传统的有机溶剂,它在增加反应速率、提高催化性能和循环使用等方面有很大的潜力,因此将更多新型、功能型的离子液体应用于Baeyer-Villiger重排反应也将成为一种绿色环保的好方法。
[1] Paul D M. Molecular Rearrangements.Part One[M].New York:Interscience Publishers a Division of John Wiley & Sons,1963 :577-589.
[2] Strukul G. Transition Metal Catalysis in the Baeyer-Villiger Oxidation of Ketones[J]. Angew Chem Int Ed Engl,1998,37(9):1198-1209.
[3] 冯小明,彭云贵,蒋耀忠. Baeyer-Villiger反应中的氧化剂[J].合成化学,1999,7 ( 4 ) :374-381.
[4] 张研,胡辉,方屹,等.过碳酸钠—醋酸酐作用下的Baeyer-Villiger反应[J].有机化学,1996,16(1):64-67.
[5] Berkessel A,Andreae M R M. Efficient Catalytic Methods for the Baeyer-Villiger Oxidation and Epoxidation with Hydrogen Peroxide[J].Tetrahedron Lett,2001,42(12): 2293-2295.
[6] Kanda K,Yamaguchi K,Mori K,et al. Catalyst Design of Hydrogentalcite Compound for Efficient Oxidations[J].Catal Surv Jpn,2000,4(1):31-38.
[7] Kanda K,Ueno S, Imanaka T. Catalysis of Transition Metal—Functionalized Hydro talcites for the Baeyer-Villiger Oxidation of Ketones in the Presence of Molecular Oxygen and Benzaldehyde[J]. J Mol.Catal A:Chem ,1995,102(3): 135-138.
[8] Kanda K,Yamashita T.Heterogeneous Baeyer-Villiger Oxidation of Ketones Using m-Chloroperbenzoic Acid Catalyzed by Hydrocalciteas[J]. Tetrahedron Lett,1996,37(26):4555-4558.
[9] Nnikrishnan R P,Demessie E S.Sn—Exchanged Hydrocalciteas as Catalysts for Clean and Selective Baeyer-Villiger Oxidation of Ketones Using Hydrogen Peroxide[J]. J Mol.Catal A:Chem,2003,191(1):93-100.
[10] Ueno S,Ebitani K,Ookubo A,et al.The Active Sites in the Heterogeneous Baeyer-Villiger Oxidation of Cyclopentanone by Hydrotalcite Catalysts[J].Appl Surf Sci,1997,121-122:366-371.
[11] Fukuda O,Sakaguchi S,Ishii Y.A New Strategy for Catalytic
Baeyer-Villiger Oxidation of KA—Oil with Molecular Oxygen Using N—Hydroxyphthalimide[J]. Tetrahedron Lett,2001,42(20): 3479-3481.
[12] Bhaumik A,Kumar P,Kumar R. Baeyer-Villiger Rearrangement Catalysed by Titanium Silicate Molecular Sieve (TS-1)/H2O.System[J].CatalLett,1996,40:47-50.
[13] Corma A,Nemeth L T,Renz M,et al.Sn¬¬Zeolite Beat as a Heterogeneous Chemoselective Catalyst for Baeyer-Villiger oxidations[J].Nature,2001,412(6845): 423-425.
[14] Corma A,Fornes V ,Iborra S,et al.One-Pot Synthesis of Phenols from Aromatic Aldehydes by Baeyer-Villiger Oxidation with H2O2Using Water—Tolerant Lewis Acids in Molecular Sieves[J].J Catal ,2004,221(1):67-76.
[15] Nnikrishnan R P,Demessie E S.Sn-Exchanged Hydrotalcites as Catalysts for Clean and Selective Baeyer-Villiger Oxidation of Ketones Using Hydrogen Peroxide[J]. J Mol.Catal A:Chem,2003,191(1):93-100.
[16] Gutierrez M C,Alphand V,Furstoss R. Microbiological Transformations 52;Biocatalysed Baeyer-Villiger Oxidation of 1-IndanoneDerivatives[J]. J Mol.Catal B:Enzym,2003,21(4-6): 231-238.
[17] Wang S Z,Kayser M M,Iwaki H,et al.Monooxygenase-Catalyzed Baeyer-Villiger Oxidations:CHMO Versus CPMO[J]. J Mol.Catal B:Enzym,2003,22(3-4):211-218.
[18] Lei Ziqiang,Zhang Qinghua,Luo Jujie.Baeyer-Villiger Oxidation of Ketones with Hydrogen Peroxide Catalyzed by Sn--Palygorskite[J].Tetrahedron Lett,2005,46(20):3505-3508.
[19] Boronat M ,Corma A ,Renz M ,et a1.A Multisite MolecularMechanism for Baeyer-Villiger Oxidations on Solid Catalysts Using Environmentally Friendly H2O2as Oxidant[J]. Chem Eur J,2005,11(23):6 905-6 915.
[20] Corma A,Navarro M T,Renz M. Lewis Acidic Sn(Ⅳ)Centers-Grafted onto MCM -41 -as Catalytic Sites for the Baeyer-Villiger Oxidation with Hydrogen Peroxide[J].2003,219(1):242-246.
[21] Palazzi C ,Pinna F,Strukul G.Polymer-Anchored Platinum Complexesas Catalysts for the Baeyer-Villiger Oxidation of Ketones:Preparation an d Catalytic Properties[J]. J Mol Catal A :Chem,2000,151(1-2):245-252.
[22] Bolm C,Beckmann O.Zirconium -M ediated Asymmetric Baeyer-Villiger Oxidation[J].Chirality,2000,12(5-6):523-525.
[23] Muranhashi S I,Oda Y,Naota T. Fe2O3-Catalyzed Baeyer-Villiger Oxidation of Ketones with Molecular Oxygen in the Presence of Aldehydes[J]. Tetrahedron Lett,1992,33(49):7557-7560.
[24] Inokuchi T,Kanazaki M,Sugimoto T,et al. Baeyer-Villiger Type Oxidation in a Dioxygen-Arenecarbaldehyde-Rhthenium Dioxide or Manganese Dioxide System[J].Synlett,1994,(12):1037-1038.
[25] Brink G J,Auends I W C E,Sheldon R A.The Baeyer-Villiger Reaction:New Developments Toward Greener procedures[J].Chem Rev,2004,104(9):4 105-4 124.
[26] Bernini R, Coratti A, Fabrizi G, et al. CH3ReO3/H2O2in room temperature ionic liquids:an homogeneous recyclable catalytic system for the Baeyer–Villiger reaction[J].Tetrahedron Lett,2003,44(50):8991-8994.
[27] Chrobok A.The Baeyer–Villiger oxidation of ketones with Oxone in the presence of ionic liquids as solvents[J]. Tetrahedron, 2010 ,66:6212-6216.
Research Progress of Baeyer-Villiger Rearrangement Reaction
WU Ning1,SUN Xiao-yun2,YUE Shuang3,ZANG Shu-liang1
(1. Liaoning Shihua University, Liaoning Fushun 113001,China;2. Shenyang Aerospace University, Liaoning Shenyang 110036,China; 3. Liaoning University, Liaoning Shenyang 110036,China)
Research situation of oxidation reaction in Baeyer-Villiger was introduced.Common catalysts were discussed, including acid and alkaline hydrotalcite-like compounds, zeolites with transition metal ions, microbial enzymes and transition metal complex. At last, application of ionic liquids in Baeyer-Villiger oxidation reaction was also introduced.
Baeyer-Villiger rearrangement; Catalyst; Ionic liquids
O 6
A
1671-0460(2012)02-0152-04
国家自然科学基金,项目号:N SFC (21071073);国家青年科学基金项目,项目号:NSFC (21101084)
2011-12-20
武宁(1986-),女,辽宁营口人,在读硕士,辽宁石油化工大学分析化学专业,研究方向:离子液体的合成及应用。E-mail:wuning618@126.com。
臧树良(1951-),男,教授,博士,研究方向:分析化学。

