应急管理理论在基层药监执法工作中的应用
北京市药品监督管理局朝阳分局 段志永 刘建军 蔚冬红
“应急管理”一词在20世纪引入我国,现在普遍认为2003年的“非典”是我国应急管理建设的转折点[1]。我国及时总结抗击“非典”的经验和教训,提出应对突发公共事件的“一案三制”(法制、体制、机制以及预案)建设,应急管理工作逐步走上了规范化、法制化的轨道[2]。
目前,我国药品安全突发事件应急管理方面的“一案三制”体系已初步形成。特别表现在预案体系上,以《国家突发公共事件总体应急预案》[3]为总纲,制定了《药品和医疗器械突发性群体不良事件应急预案》[4]、《国家突发公共卫生事件应急预案》[5]等。省市县三级药品安全突发事件应急预案也相继制定。近年来,我国药品安全事件呈现比较平稳的态势。药监分局处在药品执法监管一线,处理着大量的群众投诉举报及各类威胁药品安全的违法违规事件。但是,国家、省级应急预案中定义的突然发生、造成严重的群体健康损害的药品安全突发事件极少发生或只占很小的比例。因此,国家、省级应急预案对基层药监部门的执法实践并没有很强的借鉴、指导意义。如何将应急管理理念应用到药监日常管理的程序和体系中来?能否建立相应的处理程序,以便在一线执法实践中高效甄别药品安全风险预警,预防或缓解事故发生?笔者在本文中从基层药监稽查工作的角度探讨这些内容。

▲北京市药监局朝阳分局工作人员对可疑药品抽检
1 药监稽查工作的应急特质
应急管理的本质在于:消除潜在隐患,阻止或减缓正在发生的危害,减轻事故后果,通过经验总结和信息反馈为下一步管理提供依据。药监部门稽查办公室的工作职责是:负责本行政区域内药品、医疗器械、保健食品、化妆品方面的执法监督工作,依法查处有关违法案件,受理有关投诉和举报。可以看出,稽查办公室工作性质和职责在于保障“三品一械”质量安全,消除隐患,查处违法行为[6]。
1.1 预警,即案件受理阶段 应急管理运行机制的“预警”,指的是相关部门针对各种可能发生的突发公共事件,进行信息采集,开展风险分析,并根据预测分析结果,对其危害程度、范围做出估计,必要时向决策者建议发出危机警报,启动危机处理程序。药品安全预警一般定义为:发现、评估、理解和预防药品研发、生产、流通、使用过程中与药物有关问题的科学和活动。对药品安全风险进行预警的目的在于做到“早发现、早报告、早处置[7]”。
在案件受理阶段,稽查受理人员依据法律法规对举报投诉信息进行甄别、判断,对属于本部门管辖、主管的举报投诉予以受理。这些涉及药品研究、生产、经营、使用环节的个案,存在着引发药品安全危机的可能性,需要充分重视,采取措施降低危机发生的概率;另一方面,如若危机已经发生,则应努力调查原因,减轻事故造成的负面影响。
1.2 应急响应,即案件办理阶段 应急响应是应急管理运行的核心部分,指的是应急指挥部门及时启动相关预案,统一指挥或指导有关地区、部门,开展应对突发公共事件的处置工作。
1.2.1 信息报告 受理部门依据《北京市药品监督管理局受理违法案件举报暂行规定》,将受理的案件统一编号、登记后,当日报请主管局长。信息报告还包括事中报告和结案报告。
1.2.2 分级响应 稽查办公室根据《北京市药品监督管理局受理违法案件举报暂行规定》、《药品监督行政处罚程序规定》承办举报案件,并于7日内展开调查。
1.2.3 应急升级 现场调查符合立案条件的,报主管领导批准立案。调查发现案件超出药监分局控制处置职责范围的,及时请示市药监局或区(县)政府,并按照上级批复精神,组织开展处置工作。
1.2.4 应急措施 在药监稽查执法过程中,采取的应急措施包括:责令暂停问题产品的生产、经营、使用,责令召回产品,对现场涉案产品抽检,对涉案物品、证据采取查封扣押、先行登记保存等。必要时,通报卫生、公安等相关部门,联合执法。
1.3 后期处置 应急管理运行的后期处置是指在应急结束后进行的善后处置、调查与评估、恢复重建等工作。稽查办公室对举报、案件的后期处置主要包括以下两方面:①报告和归档。即制作相关文书、报告、案卷,报送相关领导或部门;②评估反馈。稽查办公室及时将查处企业信息通报相关监督科室。
综上所述,稽查办公室的工作在内容上、流程上合乎应急处置工作运行程序,同时印证和践行了应急处置中“减少危害、快速反应、注重预防”的原则。
2 药监稽查案件分级管理与响应
2.1 案件分级管理与响应 目前北京市药监系统每年受理举报投诉案件达数千件。案件信息来源大致有以下几类:①群众举报;②上级机关批转;③日常监督或专项检查发现;④其他单位移送或协查;⑤检验机构检验发现;⑥新闻媒体曝光;⑦其他途径。药监分局受理的各类举报、案件数量大、来源广、情况杂,因此,监管任务重,监管力量严重不足,举报案件办理呈现疲于应对的局面。
当前,《北京市药品监督管理局受理违法案件举报暂行规定》将案件分为了一般情况和紧急情况两级。“紧急情况”的标准是“需药品监督管理部门立即制止违法行为或参与协助其他相关行政部门的”,而未就具体情形进行表述,实践指导性存在欠缺。本文结合工作实践,参照各级应急管理预案,提出案件分级管理与响应原则。
2.1.1 按照上述原则将分局稽查办公室受理的举报、案件分为四级。
Ⅰ级:①已经或者可能造成药品安全突发事件的;②卫生部门通报的非法行医致人死亡或伤残的案件。
Ⅱ级:①有证据表明涉案药品造成举报投诉人人身伤害,举报投诉人要求赶赴现场的;②涉及药品生产环节的、证据较为翔实的举报;③涉及血液制品、疫苗、生物制品等高风险品种或麻醉药品、精神药品、毒性药品、放射性药品等特殊管理药品的举报;④新闻媒体已报道,社会影响较大的;⑤上级要求紧急调查处理的其他举报投诉事项。
Ⅲ级:①检验机构检验发现不合格产品的;②未取得药监部门行政许可,非法从事相关生产经营活动的;③需要及时到现场抽检取证的。
Ⅳ级:除Ⅰ级、Ⅱ级、Ⅲ级以外的其他举报投诉事项。
2.1.2 分级响应 对应案件级别,将响应级别分为Ⅰ级、Ⅱ级、Ⅲ级、Ⅳ级。
Ⅰ级:需立即启动分局应急预案,按分局应急工作领导小组统一部署,开展调查及信息上报工作。Ⅰ级是最为紧急的情况,要求执法人员严守时限,接到命令立即赶赴现场,进行调查、产品控制及抽样,并在时限内上报信息。Ⅱ级、Ⅲ级、Ⅳ级由稽查办公室分级处理。
Ⅱ级:情况紧急,需稽查执法人员立即赶赴现场展开调查。
例如,2010年6月,北京市药品监督管理局紧急转发河北省食品药品监督管理局通报的假药“洛汀新”在北京市的流向,各分局稽查办公室立即行动,对辖区药品经营企业展开调查,责令召回问题批号药品,对库存涉案药品查封扣押,及时、有效遏制了可能发生的药害事件。
Ⅲ级:情况比较紧急,需稽查执法人员及时出现场调查。如2010年9月,北京市药监局朝阳分局接到群众举报,反映辖区某药店销售的某批次复方丹参滴丸涉嫌存在质量问题。执法人员接到举报后及时到该药店,对涉及批号的复方丹参滴丸抽样送检,消除可能发生的药品质量风险。
Ⅳ级:此级案件由稽查执法人员按时限依法调查处理。
主要包括:①情节较轻、危害较小的违法行为和一般违规行为,如零售药店未凭处方销售处方药;②举报人无法提供问题产品详细信息、相关票据、证据等情况;③经初步核实,违法主体不存在或违法地址无法查找的情形;④违法行为已被控制,需要进一步调查核实情况的,如北京市药监局朝阳分局经常接到的外省市药监局请求协查标示紫竹药业、双鹤药业生产药品真伪的函,及有关企业资质的核查等。

▲北京市药监局朝阳分局工作人员查获假药窝点
2.2 分级管理与响应中应注意的问题
2.2.1 了解案情,明确需求 充分了解案情是分级管理的基础和依据。将调查前置,在受理阶段充分与举报人交流,了解案情细节,如涉案产品名称、批号、厂家、来源、地址信息,能否提供实物,是否有相关票据,举报诉求等。
2.2.2 了解法律,明确权限 依法行政的前提是知法、懂法。对案情依法做出研判,是案件查处过程中的关键环节。在此过程中,对超出管辖或主管权限的情况及时移送,而对于处在法律边缘的情况要多请示、多汇报,切忌不履行职责或不当履职。
2.2.3 了解事态,洞察发展 各类举报、案件反映的是群众快速增长的药品安全需求与当前依然严峻的药品安全形势的矛盾。因此,在案件处理过程中,执法人员一定要密切关注事件发展的趋势和范围,若发现药品存在安全隐患,采取措施及时清除;另一方面,如果已经发生药品使用危害,做好产品控制、抽检、溯源工作,敦促企业履行责任,减轻危害后果。
2.2.4 判断形势,灵活应对 对发生在首都重点地区,以及举办全国“两会”或重大政治活动等特殊时期发生的案件,相应提高响应级别,确保迅速、有效控制事件,维护社会和谐稳定。
3 北京市药监局朝阳分局的稽查工作模式
北京市药监局朝阳分局每年受理举报案件近700件,稽查办公室在岗执法人员9人,分为3个执法组,不包括每年的各类专项检查,每年度每组出现场200余次,监管任务重与监管力量不足的矛盾十分突出。当前,该分局稽查办公室沿袭奥运期间的监管模式,将辖区按地域划分为北、中、南三片,每个片区由一个执法组负责。稽查办公室负责人接到主管局长批转的案件,依据监管区域分配到各执法组办理,重大、复杂的案件则统筹科室力量,指定人员重点办理。从主管局长—稽查办公室负责人—执法组,层级把关,力争最大限度地控制药品安全风险,确保监管到位。
笔者依据本文提出的分级管理和响应原则对北京市药监局朝阳分局稽查办公室2008~2010年受理的案件进行统计。该分局受理案件的年度总量分别为:2008年660件,2009年702件,2010年694件,统计各级案件所占比例(见附表)。
由附表可以看出,虽然每年受理举报案件数量、情况不尽相同,但三年来每一级案件所占比例却基本稳定。从Ⅰ级到Ⅳ级,案件比例成金字塔型分布,Ⅰ~Ⅱ级是需要执法人员立即赶赴现场的情况,占总量的2%~3%,Ⅰ~Ⅲ级比例之和接近30%,这是高风险举报案件所占的比重,Ⅳ级占到70%以上,说明大部分案件可以按规定时限依法调查处理。
4 延伸的思考
本文从应急管理的角度分析基层药监稽查执法工作,提出案件分级管理与响应原则,提高执法效率,降低药品安全风险。研究药监稽查工作的应急特质,还应考虑完善程序细则、深化案源管理等方面的问题。
4.1 完善程序细则 目前我国已搭建起“一案三制”药品安全应急管理框架。完善的细则有利于使工作规范化,促进快速反应、科学决策和有条不紊地应对紧急、突发事件的发生。这方面美国FDA完善的应急程序规定值得我国药品监管部门借鉴。
4.2 深化案源管理 北京市各药监分局稽查办公室基本已建立举报案件台账,数字稽查系统的运用也使全市药品举报案件有据可查。但目前大家的关注点主要集中于立案查处的案件,而对于大量的未立案案件缺少汇总分析。实际上,对每年度固定时间段的举报情况及趋势进行分析,可以发现群众关注的热点、监管薄弱点,以及执法难点(未立案案件中包含法律边缘问题、受执法手段局限无法继续调查等问题),这是药品安全预警信息的重要组成部分。完善这些信息的采集分析,有助于发现药品安全风险点,从而采取相应措施,防止其进一步演化为危机事件。
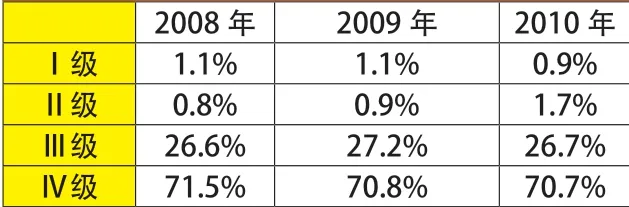
附表 2008~2010年北京市药监局朝阳分局稽查办公室受理案件分级情况统计
4.3 重视人的因素 任何先进的系统、程序,最终运行离不开人的操作,人的因素是一个老生常谈的问题。本文探讨的是应急工作,除了人员素质培养、结构构成等问题外,还需强调两点:①战时的执行力,应急情况下一线人员的执行力尤为重要,只有快速、坚决地贯彻上级决策,严谨细致,依法履职,才能尽快消除或缓解危机;②培育质疑的精神,执法人员平时要养成思考的习惯,对于可能对药品安全产生不利后果的现象、活动、决策要提高警惕,鼓励和重视不同的意见,通过思维的多元化来避免群体思维误区。

