5-氟尿嘧啶作用人肝癌细胞系SMMC-7721后残存细胞中肿瘤干细胞比例增加
朱雯静,杨 玥,郝溥辰,李德龙,赵 森,陈培琼,俞 亮,薛 冉,史 亮,王子乾,吕福东,冯骥良
1.首都医科大学附属北京佑安医院病理科,北京 100069;2.首都医科大学七年制研究生;3.中国人民解放军第306医院;4.西北民族大学医学院;5.首都医科大学病理学教研室
肝细胞癌(hepatocellular carcinoma,HCC)是世界上第六大多发癌症,死亡率居肿瘤死亡率第三位[1]。42.5%的原发性肝癌发生在中国大陆,它已成为我国第二位恶性肿瘤病因[2]。近年来,肿瘤干细胞学说的提出为肿瘤研究与治疗带来了希望。该学说认为[3-5],肿瘤中存在一小群表达干细胞特性的细胞,具有无限增殖和调控肿瘤生长的能力。这些细胞能够逃避常规治疗方案的杀伤作用,从而导致疾病的复发和转移[6-7]。肿瘤干细胞具有和成体干细胞相似的自我更新和自我分化潜能,应用正常干细胞与肿瘤干细胞的这一相似之处,人们开始以正常干细胞的标志分子来筛选肿瘤干细胞。已报道的存在肿瘤干细胞的组织类型肿瘤有急性髓性白血病、神经系统肿瘤、乳腺癌和前列腺癌等[8-11]。
肿瘤干细胞学说可能是一种具有普遍性的肿瘤发生机制,以往研究证实肝癌中也存在肝癌干细胞[12-13]。它们与正常肝干细胞共同表达一些表面标志物,如 AFP、CD133、ABCG2、CK7、Thy-1、上皮细胞黏附分子(EpCAM)、CD44等[14-18]。我们以往的研究发现5-FU作用BEL-7402肝癌细胞后细胞间黏附分子-1/CD54和神经细胞黏附分子(NCAM)/CD56阳性细胞比例增加,且通过克隆形成实验证实ICAM-1和NCAM可能成为肝癌干细胞的候选标志物[19]。但是肝癌具有明显的异质性[15],不同肝癌临床病例和不同肝癌细胞系中肿瘤细胞之间的细胞生物学特性不同,对药物作用的反应也不相同。我们在5-FU作用BEL-7402细胞系的模型中发现肿瘤干细胞的富集现象,并推测在临床治疗中十分常见的5-FU化疗后耐药所引起的肿瘤复发,很有可能与肝癌干细胞逃逸5-FU的单药物杀伤有关。但5-FU在其他肝癌细胞系中是否也具有同样作用还不得而知。
本研究中我们选择了SMMC-7721细胞系。与BEL-7402细胞系比较,虽然两者形态学特点相似,染色体个数相近,AFP均阳性表达,且两者接种裸鼠均可形成瘤结节,但BEL-7402在裸鼠移植成瘤实验中需要的瘤细胞数目更少且生长速度更快[20-21]。这些证据表明,与BEL-7402细胞系比较,SMMC-7721细胞系可能恶性转化自较成熟的肝细胞。因此,本研究采用了SMMC-7721细胞系,同时引入了更多的肿瘤干细胞标志物,如 NCAM、ICAM-1、EpCAM、CD133及 ABCG2,旨在进一步探讨肝癌干细胞逃避药物杀伤与临床化疗失败的关系,为肝癌的治疗提供新的思路。
1 材料与方法
1.1 材料
1.1.1 细胞系:人肝癌细胞系SMMC-7721由我校基础医学院安威教授惠赠。
1.1.2 试剂:RPMI-1640细胞培养基购于 Gibco公司,胎牛血清购自杭州四季清公司,CCK-8细胞计数试剂盒购自日本同仁化学研究所,5-FU试剂购自上海旭东海普药业公司。
1.1.3 抗体:ICAM-1-异硫氰酸荧光素(FITC)、Ep-CAM-藻红蛋白(PE)、NCAM-Cy5单克隆荧光抗体购自美国ABCAM公司,CD133-FITC单克隆荧光抗体购自北京博奥森生物技术有限公司
1.2 方法
1.2.1 检测5-FU对SMMC-7721细胞系增殖的影响:取对数生长期的SMMC-7721肝癌细胞株,0.25%胰蛋白酶消化后以每孔1×104个细胞接种于96孔细胞培养板中,设置6组不同5-FU浓度的实验组,每组每个时间点设置四个复孔。调节5-FU终浓度分别为0.1、1、10、25、50 μg/mL。同时设不加任何药物的对照组。5%CO2,37℃培养箱中培养。分别在培养12、24、36、48 h加入CCK-810 μL/孔,继续培养2 h后以450 nm波长检测每孔吸光度值。计算药物5-FU对SMMC-7721细胞增殖的影响。
1.2.2 测定5-FU作用SMMC-7721细胞系后对细胞周期的影响:取对数生长期的 SMMC-7721细胞,0.25%胰蛋白酶消化,1000 r/min离心 10 min,用含10%胎牛血清培养基RPMI-1640配成细胞悬浮液,稀释至5×104个细胞/mL。以5-FU终浓度为10 μg/mL的RPMI-1640培养基进行细胞培养,同时设置不含药物的对照组。48 h后取106~107个细胞4℃ 70%冷乙醇固定,加入含2%RNase和1‰Triton×100的PBS缓冲液1 mL,水浴30 min,PI染色,流式细胞仪检测细胞周期。
1.2.3 SMMC-7721细胞系表面标志物阳性细胞表达率的检测:取培养48 h的实验组及对照组细胞,培养方法与1.2.2相同。0.25%胰蛋白酶消化,离心,PBS稀释至细胞密度为2×106/mL。取流式细胞检测加样管10支,每支加入10 μL HEPES溶液,20 μL 灭活胎牛血清,其中5支每支加入实验组细胞悬液100 μL,另5支加入对照组细胞悬液100 μL。实验组和对照组均分别加入EpCAM-PE荧光抗体3 μL,NCAM-Cy5荧光抗体 1 μL,ICAM-1-FITC 荧光抗体 4 μL,CD133-FITC荧光抗体10 μL和 ABCG2-PE荧光抗体2 μL,1500 r/min离心两次,每次3 min。500 μL PBS悬浮,400目滤网过滤,流式细胞仪检测。
1.3 统计学处理 统计数据用SPSS 13.0软件进行处理,所有数据用均数±标准差()表示,n≥3,细胞周期及表面标志物检测采用独立样本t检验,增殖曲线经Mauchly“球对称”检验后采用重复测量数据方差分析,检验水准均为α=0.05。
2 结果
2.1 5-FU处理前后细胞增殖能力的变化 CCK-8试剂盒细胞增殖实验Mauchly“球对称”检验结果P=0.57,接受“球对称”假设。各时间点之间吸光度相比,差异有统计学意义(P=0.000);组间相比较,差异有统计学意义(P=0.000);药物浓度与药物作用时间之间存在交互作用(P=0.000)。说明5-FU的药物毒性使SMMC-7721细胞系增殖明显减弱,5-FU对各实验组的细胞增殖水平的抑制作用具有时间依赖性以及剂量依赖性,即随着浓度的增加和作用时间的延长而增强(见图1)。
2.2 5-FU药物处理前后细胞周期的变化(n=3) 使用10 μg/mL的5-FU浓度进行细胞周期与阳性细胞比例变化的研究,作用时间为48 h。流式细胞仪细胞周期测定实验表明,5-FU处理使SMMC-7721细胞的细胞周期分布变化明显,实验组G0/G1期细胞比例为 83.917% ±12.996%,较对照组 46.617% ±18.857%明显升高,S期细胞比例由对照组的50.510% ±16.405% 下降至实验组的 15.360% ±13.517%,G2/M期细胞比例由对照组的2.872% ±2.824%下降至实验组的0.722% ±0.711%。表明5-FU对SMMC-7721细胞周期各期细胞比例均有影响,G0/G1期、S期和G2/M期在5-FU作用前后差异均有统计学意义(P<0.05),G0/G1期阻滞明显(见图2、图3)。

图1 不同浓度的5-FU作用于SMMC-7721细胞系后细胞生长曲线的变化Fig 1 Treatment with 5-FU on the growth of SMMC-7721 cells with different concentrations

图2 10 μg/mL 5-FU作用SMMC-7721细胞前后对照组及实验组细胞周期变化 A:对照组细胞周期分布:G0/G1期:46.617% ±18.857%;S 期:50.510% ±16.405%;G2/M 期:2.872% ±2.824%;B:实验组细胞周期分布:G0/G1期:83.917% ±12.996%;S 期:15.360% ±13.517%;G2/M 期:0.722% ±0.711%Fig 2 Effects of 5-FU on the cell cycle distribution of SMMC-7721 with the concentration of 10 μg/mL for 48 h
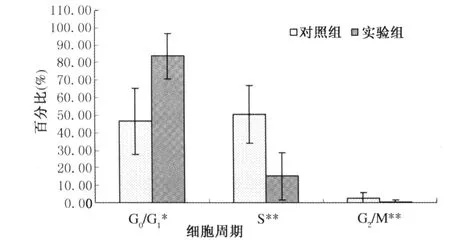
图3 10 μg/mL 5-FU作用48 h处理前后,SMMC-7721细胞细胞周期分布变化(*P <0.05,**P <0.01)Fig 3 Treatment with 5-FU on the cell cycle distribution of SMMC-7721 cells with the concentration of 10 μg/mL for 48 h
2.3 5-FU药物处理前后细胞表面标志物表达比率变化 流式细胞仪特定表面抗原测定实验表明,5-FU处理使SMMC-7721细胞表面的干细胞标志物阳性细胞表达率变化明显。实验组 NCAM、ICAM-1、EpCAM、CD133、ABCG2阳性细胞比例分别为7.2% ±0.1%,94.6% ±0.1%、5.4% ±0.3%、17.5% ±0.4%、1.8% ± 0.1%。较对照组分别为 0.6% ± 0、78.0% ±0.9%、3.9% ±0.1%、8.2% ± 0.6%、0.3% ± 0.1%,均明显升高,差异具有统计学意义(P<0.05)。表明5-FU处理能够提高残存细胞中表达这些标志物的细胞比例(见图4、图5)。

图4 10 μg/mL 5-FU作用SMMC-7721细胞48 h后,几种肝癌干细胞标志物阳性细胞的表达变化(*P<0.05,**P<0.01)Fig 4 Effects of 5-FU on the positive cells proportion of SMMC-7721 with the concentration of 10 μg/mL for 48 h
3 讨论
5-FU是临床上治疗肝癌的一线化疗药物。以往研究表明,5-FU可以诱导肿瘤细胞凋亡并抑制细胞增殖[22-25],但在临床肝癌治疗中对5-FU的耐药现象比较普遍,分子机理尚不明确。本研究发现5-FU对细胞增殖的抑制作用存在时间依赖性和剂量依赖性,但实验组各浓度5-FU均无法完全抑制SMMC-7721细胞的生长,始终会有部分细胞逃逸药物的杀伤作用。在这些残存的肿瘤细胞中,肿瘤干细胞表面标志物NCAM、ICAM-1、EpCAM、CD133阳性细胞比例均较未加药对照组明显升高,表明同5-FU作用BEL-7402肝癌细胞模型一样[19],一定剂量5-FU作用 SMMC-7721细胞后,残存细胞中的肿瘤干细胞的比例明显增加。NCAM、ICAM-1、EpCAM是三种细胞黏附分子,在肿瘤侵袭和转移中作用十分重要[26-28]。CD133是一种肿瘤干细胞的广谱标志物,尤其是在分化差的肿瘤组织中CD133表达更强。通过对两细胞系比较研究发现,虽然各细胞系5-FU单药物作用前后上述4种表面标志物阳性细胞比例存在显著差异,但在BEL-7402与SMMC-7721两细胞系之间,处理前后细胞表面标志物表达率存在不同程度变化。不同生物学特性的肿瘤细胞系之间其肿瘤干细胞的比例和种类可能是不同的。正是由于肿瘤干细胞异质性的存在而导致了临床上肝细胞癌不同患者之间肿瘤的侵袭、转移的能力不同。这提示未来对肿瘤的个体化治疗具有重要意义。

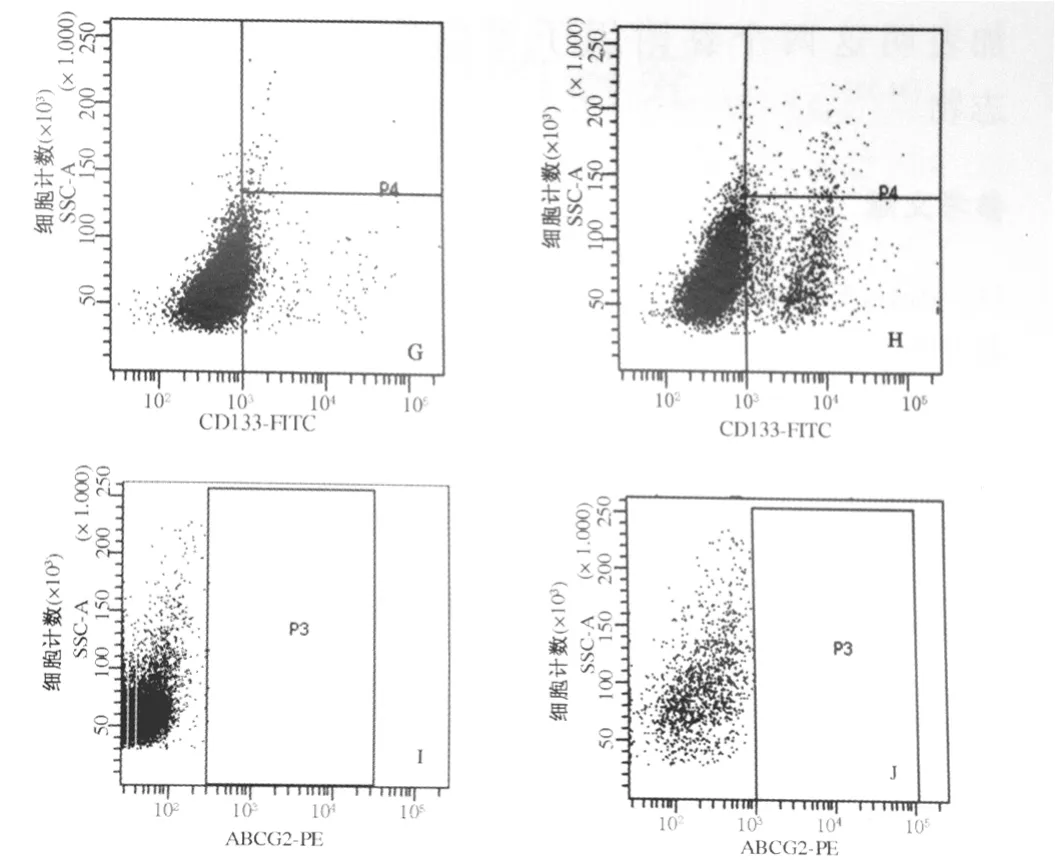
图5 10 μg/mL 5-FU作用SMMC-7721细胞48 h处理前后对照组及实验组细胞表面标志物阳性率比较A、B:NCAM;C、D:ICAM-1;E、F:EpCAM;G、H:CD133;I、J:ABCG2;A、C、E、G、I:对照组;B、D、F、H、J:实验组Fig 5 Several surface markers expression profiles in control and test group treated with 5-FU with the concentration of 10 μg/mL for 48 h
通过分析5-FU作用后的残存细胞的周期分布发现,静息期(G0/G1期)细胞在细胞群中比例明显上升。5-FU主要通过抑制细胞内胸腺嘧啶核苷酸合成酶(TS)的活性,阻断尿嘧啶脱氧核苷向胸腺嘧啶脱氧核苷的转变,从而影响细胞内的DNA与RNA的合成[22]。它对细胞周期中的各期都有毒性作用,尤其是S期,残存细胞多处于G0/G1期[29]。大量研究表明,肿瘤干细胞与人正常干细胞相似,处于静息的G0期。ABCG2属于ABC转运蛋白家族成员之一,在许多组织类型的正常干细胞膜上高表达,通过“ABCG2泵”排出药物以避免药物对自身的杀伤作用[30]。5-FU作用SMMC-7721后残存肿瘤细胞中ABCG2阳性细胞比例增加提示残存细胞群体具有肿瘤干细胞特性。同时,残存细胞群体中ICAM-1和NCAM阳性细胞比例的增加表明这两个黏附因子可以作为肝癌干细胞标志物[31-32]。
[1]Parkin DM,Bray F,Ferlay J,et al.Global cancer statistics,2002[J].CA Cancer J Clin,2005,55(2):74-108.
[2]Wu MC.Progress on treatment of primary carcinoma of liver[J].China Medical News,2002,1:10-11.吴孟超.原发性肝癌治疗的进展[J].中华医学信息导报,2002,1:10-11.
[3]Reya T,Morrison SJ,Clarke MF,et al.Stem cells,cancer,and cancer stem cells[J].Nature,2001,414(6859):105-111.
[4]Al-Hajj M,Clarke MF.Self-renewal and solid tumor stem cells[J].Oncogene,2004,23(43):7274-7282.
[5]Scadden DT.Cancer stem cells refined[J].Nat Immunol,2004,5(7):701-703.
[6]Morgan J,Jackson JD,Zheng X,et al.Substrate affinity of photosensitizers derived from chlorophyll-a:the ABCG2 transporter affects the phototoxic response of side population stem cell-like cancer cells to photodynamic therapy[J].Mol Pharm,2010 Sep1.
[7]Sell S.Cellular origin of hepatocellular carcinomas[J].Semin Cell Dev Biol,2002,13(6):419-424.
[8]Al-Hajj M,Wicha MS,Benito-Hernandez A,et al.Prospective identification of tumorigenic breast cancer cells[J].Proc Natl Acad Sci U S A,2003,100(7):3983-3988.
[9]Singh SK,Clarke ID,Hide T,et al.Cancer stem cells in nervous system tumors[J].Oncogene,2004,23(43):7267-7273.
[10]Collins AT,Berry PA,Hyde C,et al.Prospective identification of tumorigenic prostate cancer stem cells[J].Cancer Res,2005,65(23):10946-10951.
[11]Bonnet D,Dick JE.Human acute myeloid leukemia is organized as a hierarchy that originates from a primitive hematopoietic cell[J].Nat Med,1997,3(7):730-737.
[12]Mishra L,Banker T,Murray J,et al.Liver stem cells and hepatocellular carcinoma[J].Hepatology,2009,49(1):318-329.
[13]Sell S,Leffert H.Liver cancer stem cells[J].J Clin Oncol,2008,26(17):2800-2805.
[14]Yang XR,Xu Y,Yu B,et al.High expression levels of putative hepatic stem/progenitor cell biomarkers related to tumour angiogenesis and poor prognosis of hepatocellular carcinoma[J].Gut,2010,59(7):953-962.
[15]Zen Y,Fujii T,Yoshikawa S,et al.Histological and culture studies with respect to ABCG2 expression support the existence of a cancer cell hierarchy in human hepatocellular carcinoma[J].Am J Pathol,2007,170(5):1750-1762.
[16]Yamashita T,Forgues M,Wang W,et al.EpCAM and alpha-fetoprotein expression defines novel prognostic subtypes of hepatocellular carcinoma[J].Cancer Res,2008,68(5):1451-1461.
[17]Durnez A,Verslype C,Nevens F,et al.The clinicopathological and prognostic relevance of cytokeratin 7 and 19 expression in hepatocellular carcinoma.A possible progenitor cell origin[J].Histopathology,2006,49(2):138-151.
[18]Yang ZF,Ho DW,Ng MN,et al.Significance of CD90+cancer stem cells in human liver cancer[J].Cancer Cell,2008,13(2):153-166.
[19]Yang Y,Li DL,Zhu WJ,et al.The effect of 5-fluorouracil on enriching cancer stem cells of hepatoma cell line BEL-7402[J].Chin J Hepatol,2011,19(9):105-109.杨玥,李德龙,朱雯静,等.5-氟尿嘧啶对肝癌细胞系BEL-7402中肿瘤干细胞的富集作用[J].中华肝脏病杂志,2011,19(9):105-109.
[20]Chen RM,Zhu DH,Ye XZ,et al.Establishment and characteristic of BEL-7402[J].Chinese Science Bulletin,1975,(9):434-436.陈瑞铭,朱德厚,叶秀珍,等.人体肝癌体外细胞株(BEL-7402)的建立及其特征[J].科学通报,1975,(9):434-436.
[21]董荣春,周荣华,吕发度,等.SMMC-7721人体肝癌细胞株的建立及其生物学特性的初步观察[J].第二军医大学学报,1980,(1):5-9.
[22]Violette S,Poulain L,Dussaulx E,et al.Resistance of colon cancer cells to long-term 5-fluorouracil exposure is correlated to the relative level of Bcl-2 and Bcl-X(L)in addition to Bax and p53 status[J].Int J Cancer,2002,98(4):498-504.
[23]Jiang J,Liu J,Zhu J,et al.Mechanism of apoptotic effects induced by 5-fluorouracil on human liver carcinoma Bel7402 cell line[J].Chin Med J(Engl),2002,115(7):968-971.
[24]Tseng YS,Tzeng CC,Chiu AW,et al.Ha-ras overexpression mediated cell apoptosis in the presence of 5-fluorouracil[J].Exp Cell Res,2003,288(2):403-414.
[25]Yang L,Wu D,Luo K,et al.Andrographolide enhances 5-fluorouracil-induced apoptosis via caspase-8-dependent mitochondrial pathway involving p53 participation in hepatocellular carcinoma(SMMC-7721)cells[J].Cancer Lett,2009,276(2):180-188.
[26]Yamashita T,Ji J,Budhu A,et al.EpCAM-positive hepatocellular carcinoma cells are tumor-initiating cells with stem/progenitor cell features[J].Gastroenterology,2009,136(3):1012-1024.
[27]Terris B,Cavard C,Perret C.EpCAM,a new marker for cancer stem cells in hepatocellular carcinoma [J].J Hepatol,2010,52(2):280-281.
[28]Xu XL,Xing BC,Han HB,et al.The properties of tumor-initiating cells from a hepatocellular carcinoma patient’s primary and recurrent tumor[J].Carcinogenesis,2010,31(2):167-174.
[29]Hodgson GS,Bradley TR.Properties of haematopoietic stem cells surviving 5-fluorouracil treatment:evidence for a pre-CFU-S cell[J].Nature,1979,281(5730):381-382.
[30]Sarkadi B,Homolya L,Szakacs G,et al.Human multidrug resistance ABCB and ABCG transporters:participation in a chemoimmunity defense system[J].Physiol Rev,2006,86(4):1179-1236.
[31]Hu J,Li J,Wang M,et al.Isolation of side population cells from gallbladder carcinoma of human being and the expression of ABCG2 gene[J].Chinese-German Journal of Clinical Oncology,2007,6(5):469-473.
[32]Monzani E,Facchetti F,Galmozzi E,et al.Melanoma contains CD133 and ABCG2 positive cells with enhanced tumourigenic potential[J].Eur J Cancer,2007,43(5):935-946.

