黄柏化学成分研究
李行诺,翟文丰,周孟宇,沈培强,葛志伟,颜继忠
(1.浙江工业大学 药学院,浙江 杭州310032;2.正大青春宝药业有限公司,浙江 杭州310023;3.浙江大学 药学院,浙江 杭州310058)
黄柏为芸香科植物黄皮树PhellodendronchineseSchneid的干燥树皮,性苦、寒,具有清热燥湿、泻火除蒸和解毒疗疮的功效[1].现代药理学表明黄柏具有较强的广谱抗菌性,对葡萄球菌有较强的抑制作用,同时具有抗溃疡、降压、抗心律失常等作用[2].为进一步研究其化学成分,现利用硅胶柱色谱,反相中压制备色谱仪,制备液相色谱等分离手段,从黄柏中分离得到6个化合物,通过波谱数据鉴定了其结构,分别为异阔果芸香碱(Ⅰ),γ-花椒碱(Ⅱ),茵芋碱(Ⅲ),铁屎米酮(Ⅳ),阿魏酸(Ⅴ),5-O-阿魏酰基奎宁酸(Ⅵ).
1 实验部分
1.1 仪器与试剂
美国Agilent 1100制备型高效液相色谱仪(色谱柱为ZORBAX SB-C18,21.2×250mm,7μm),HP chemstations处理软件(安捷伦科技有限公司,美国);Waters 2695分析型高效液相色谱仪;BRUKER AVANCE-III型磁共振波谱仪(TMS为内标,瑞士 Bruker公司);Mill-Q 超纯水器(Mllipore公司);柱色谱硅胶(100—200目)和薄层色谱硅胶均为青岛海洋化工厂产品.甲醇为色谱纯,购自德国Merck公司,其他溶剂均为分析纯.黄柏药材取自杭州正大青春宝药业有限公司,由楚楚博士鉴定为PhellodendronchineseSchneid,留样保存于浙江工业大学药学院.
1.2 提取与分离
黄柏干燥树皮4.0kg,经70%的乙醇溶液回流提取两次,每次2h,合并提取液,减压浓缩得稠浸膏.所得浸膏用去离子水溶解,过滤,分别用石油醚,乙酸乙酯,正丁醇萃取.各部分分别经硅胶柱色谱层析,再经过高效制备液相色谱纯化,流速8mL/min,甲醇-水梯度洗脱.乙酸乙酯部分以石油醚-乙酸乙酯(20∶1~1∶1)洗脱,浓缩洗液,经制备高效液相色谱(甲醇-水为流动相)分离、纯化得化合物化合物Ⅳ(20mg),Ⅴ(132mg).正丁醇部分以二氯甲烷-甲醇(30∶1~1∶1)洗脱,浓缩洗脱液,经制备高效液相色谱(甲醇-水为流动相)分离、纯化得化合物Ⅰ(50mg),化合物Ⅱ(20mg),化合物Ⅲ(22mg),化合物Ⅵ(45mg).化合物Ⅰ-Ⅵ结构为
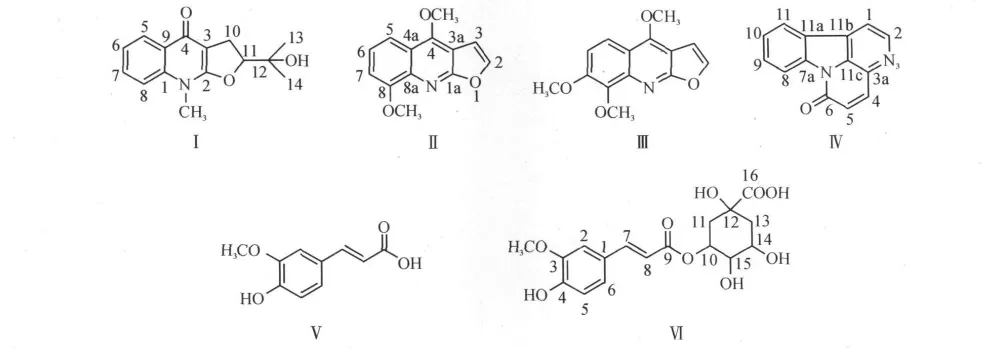
2 结构鉴定
化合物Ⅰ淡黄色固体.1H-NMR(CDCl3,500 MHz)δ:8.35(1H,br.d,J=7.5Hz,H-5),7.53(1H,br.t,J=7.5Hz,H-7),7.30(1H,br.t,J=7.5Hz,H-6),7.26(1H,br.t,J=7.5Hz,H-8),4.81(1H,t,J=8.5Hz,H-11),3.65(3H,s,N-C H—3),3.22(2H,d,J=8.5Hz,H-10),1.35(3H,s,H-14),1.26(3H,s,H-13);13C-NMR (CDCl3,125MHz)δ:173.6(C-4),161.6(C-2),138.6(C-1),131.0(C-7),126.4(C-9),126.2(C-6),123.2(C-5),114.1(C-8),99.6(C-3),92.0(C-11),71.5(C-12),31.3(N-C—H3),27.6(C-10),25.6(C-13),24.5(C-14).其波谱数据与文献报道的异阔果芸香碱[3-4]一致,故鉴定该化合物为异阔果芸香碱.
化合物Ⅱ无色晶体.1H-NMR(CD3OD,500 MHz)δ:7.66(1H,d,J=2.5Hz,H-2),7.58(1H,dd,J=1.0,8.5Hz,H-5),7.20(1H,dd,J=7.5,8.5Hz,H-6),7.11(1H,d,J=2.5Hz,H-3),7.00(1H,br.d,J=7.5Hz,H-7),4.31(3H,s,4-OC H—3),3.95(3H,s,8-OC H—3);13C-NMR(CD3OD,125 MHz)δ:164.3(C-1a),158.4(C-4),155.2(C-8),144.9(C-2),137.9(C-8a),124.5(C-6),120.5(C-4a),115.1(C-5),109.1(C-7),106.1(C-3),104.8(C-3a),59.8(C4-O C—H3),56.2(C8-O C—H3).其波谱数据与文献报道的γ-花椒碱[5-6]基本一致,故鉴定该化合物为γ-花椒碱.
化合物Ⅲ浅黄色晶体.1H-NMR(CD3OD,500MHz)δ:8.02(1H,d,J=9.0Hz,H-5),7.74(1H,d,J=2.5Hz,H-2),7.35(1H,d,J=9.0Hz,H-6),7.30(1H,d,J=2.5Hz,H-3),4.46(3H,s,4-O C—H3),4.00(3H,s,8-O C—H3),3.92(3H,s,7-O C—H3);13C-NMR(CD3OD,125MHz)δ:166.1(C-1a),159.2(C-4),153.8(C-7),144.4(C-2),143.2(C-2),142.0(C-8),141.6(C-8a),119.6(C-5),115.9(C-4a),113.5(C-6),106.3(C-3),105.7(C-4a),103.4(C-3a),60.3(C8-O C—H3),58.7(C4-O C—H3),55.8(C7-O C—H3).其波谱数据与文献报道的茵芋碱[5-6]一致,故鉴定该化合物为茵芋碱.
化合物Ⅳ浅黄色晶体.1H-NMR(DMSO-d6,500MHz)δ:8.83(1H,d,J=5.0Hz,H-2),8.51(1H,d,J=8.0Hz,H-8),8.38(1H,br.d,J=7.5Hz,H-11),8.30(1H,d,J=5.0Hz,H-1),8.14(1H,d,J=9.5Hz,H-5),7.77(1H,br.dd,J=7.5,8.0Hz,H-9),7.60(1H,br.t,J=7.5Hz,H-10),7.00(1H,d,J=9.5Hz,H-4);13C-NMR(DMSO-d6,125MHz)δ:159.5(C-6),146.4(C-2),140.4(C-4),139.2(C-7a),136.2(C-3a),131.9(C-11c),131.4(C-9),129.9(C-11b),129.1(C-5),126.2(C-10),124.6(C-11a),124.1(C-11),117.8(C-8),116.7(C-1)其波谱数据与文献报道的铁屎米酮[7]一致,故鉴定该化合物为铁屎米酮.
化合物Ⅴ白色粉末状晶体.1H-NMR(CD3OD,500MHz)δ:7.58(1H,d,J=15.5Hz,H-7),7.16(1H,d,J=2.0Hz,H-2),7.06(1H,dd,J=2.0,8.0Hz,H-6),6.81(1H,d,J=8.0Hz,H-5),6.30(1H,d,J=15.5Hz,H-8),3.88(3H,s,3-O C—H3);13C-NMR(CD3OD,125MHz)δ:170.9(C-9),150.4(C-3),149.3(C-4),146.9(C-7),127.8(C-1),123.9(C-6),116.4(C-5),115.9(C-8),111.7(C-2),56.5(-O C—H3)),其波谱数据与文献报道的阿魏酸[8]一致,故鉴定该化合物为阿魏酸.
化合物Ⅵ黄色晶体.1H-NMR (CD3OD,500MHz)δ:7.59(1H,d,J=15.9Hz,H-7),7.12(1H,d,J=1.6Hz,H-2),7.03(1H,dd,J=1.6,8.2Hz,H-6),6.82(1H,d,J=8.2Hz,H-5),6.36(1H,d,J=15.9Hz,H-8),5.38(1H,m,H-10),4.16(1H,m,H-14),3.84(3H,s,3-O C—H3),3.73(1H,dd,J=3.0,9.8Hz,H-15),1.95~2.05(4H,m,H-11,13);13C-NMR(CD3OD,125MHz)δ:180.3(C12-C—OOH),168.8(C-9),150.3(C-3),149.1(C-4),146.5(C-7),127.5(C-1),123.9(C-6),116.5(C-5),115.7(C-8),111.7(C-2),77.5(C-12),74.7(C-15),72.7(C-14),72.5(C-10),56.6(C3-O C—H3),40.3(C-11),38.8(C-13).其波谱数据与文献报道的5-O-阿魏酰基奎宁酸[9]一致,故鉴定该化合物为5-O-阿魏酰基奎宁酸.
3 结 论
研究了黄柏乙醇提取物中的化学成分,采用硅胶柱色谱,结合反相中压色谱和制备液相从提取物中分离得到了6个化合物,通过NMR光谱数据鉴定其结构,这6个化合物分别为异阔果芸香碱,γ-花椒碱,茵芋碱,铁屎米酮,阿魏酸,5-O-阿魏酰基奎宁酸,其中异阔果芸香碱是首次从该属植物中分离得到,为完善黄柏化学组分信息库和药效研究提供物质基础.
[1]国家药典委员会.中国药典:一部[M].北京:中国医药科技出版社,2010.
[2]王浴生,邓文龙,薛春生.中药药理与应用[M].北京:北京人民卫生出版社,2002.
[3]BROW N,GRUNDON M,HARRISON D,et al.The13CNMR spectra of hemiterpenoid quinoline alkaloids and related prenylquinolines[J].Tetrahedron,1980,36(25):3579-3584.
[4]冯熙,王鸣,董云发,等.臭常山喹啉生物碱成分[J].中草药,2004,35(12):1336-1338.
[5]祝丹,陈玉,郑桐,等.野花椒化学成分研究[J].华中师范大学学报,2009,43 (3):424-427.
[6]韦瑀龙,张翠仙,林朝展,等.蚬壳花椒中生物碱成分的研究[J].中药新药与临床药理,2009,20(5):471-474.
[7]YONG D M,HAK C K,MIN C Y,et al.Isolation of limonoids and alkaloids fromPhellodendronamurenseand their multidrug resistance(MDR)reversal activity[J].Arch Pharm Res,2007,30(1):58-63.
[8]王希,张焜,陈优生.仙鹤草降糖活性成分的提取分离[J].中国实验方剂学杂志,2010,16(6):85-87.
[9]SMARRITO C,MUNARI C,ROBERT F,et al.A novel efficient and versatile route to the synthesis of 5-O-feruloylquinic acids[J].Org Biomol Chem,2008,6 (6):986-987.

